文档内容
第一章 化学反应的热效应
第2节 反应热的计算
课题:1.2.2 反应热的计算 课时 1 授课年级 高二
1、用盖斯定律计算反应热
2、用键能计算反应热
教学内容
3、用反应物和生成物的总能量计算反应热
上一节内容介绍了盖斯定律。通过实例使学生感受盖斯定律的应用,并以此说明盖
教材 斯定律在科学研究中的重要意义。本节课是第二部分,利用反应热的概念、盖斯定律和热
分析 化学方程式进行有关反应热的计算,通过不同类型的例题加以展示。帮助学生进步巩固概
念 、应用定律、理解热化学方程式的意义。
[能力目标]
①掌握运用盖斯定律解决具体问题
②学会化学反应热的有关计算。
教学目标
[素养目标]
通过实例感受盖斯定律,并以此说明盖斯定律在科学研究中的重要作用。体会化学对生活
的贡献。
教学重、 重点:反应热的计算
难点:反应热的计算
难点
前面学生已经学习盖斯定律,并从定量的角度来进一步认识物质发生化学反应伴随的
热效应。注意引导学生准确理解反应热、燃烧热、盖斯定律等理论概念,熟悉热化学方程
式的书写,重视概念和热化学方程式的应用。处于高中学习阶段的学生,已经具备了逆向
思维和举一反三的能力,而且在他们的脑海中,已经构建起化学反应与能量在宏观和微观
学情分析
上的联系以及其能相互转化的知识。有关反应热的计算与有关物质的量的计算联系很紧
密,在计算过程中要注意培养学生综合运用知识的能力。可适当补充一些不同类型的习题
作为课堂练习,发现问题并及时解决。不仅巩固、落实了知识和计算技能,还能通过计算
的结果说明有些物质燃烧时,其∆H的数值都很大。
教学方法 自主学习、合作交流、探究与验证
教学环节一:温故知新引出课题。
教师活动 学生活动 设计意图
1、温故知新:
学生思考回答。
复习盖斯定律内容:
2.已知下列热化学方程式: 复习巩固
一个化学反应,不管是一步完成的还是分几步完成
反应Ⅰ.Hg(l)+O(g)=HgO(s) ΔH; 盖斯定律内
的,其反应热是相同的。也就是说,化学反应的反 2 1
容
应热与体系的始态和终态有关,而与反应的途径无 反应Ⅱ.Zn(s)+O(g)=ZnO(s) ΔH;
2 2
关,这就是盖斯定律。
则反应ⅢZn(s)+HgO(s)= Hg(l)+ZnO(s) ΔH 值为( )
3
A.ΔH-ΔH
2 1
B.ΔH+ΔH
2 1
C.ΔH-ΔH
1 2
D.-ΔH-ΔH
1 2
【答案】A
【解析】根据盖斯定律:Ⅲ=Ⅱ-Ⅰ,
则ΔH=ΔH-ΔH,故选A。
3 2 1
教学环节二:用盖斯定律计算反应热
教师活动 学生活动 设计意图
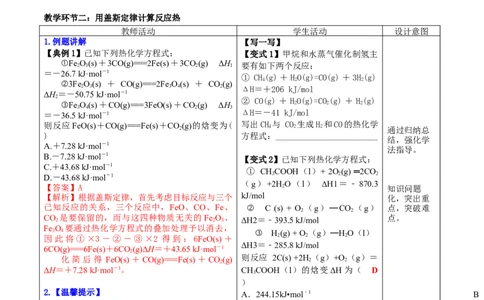
1.例题讲解 【写一写】
【典例1】已知下列热化学方程式: 【变式1】甲烷和水蒸气催化制氢主
①Fe 2 O 3 (s)+3CO(g)===2Fe(s)+3CO 2 (g) ΔH 1 要有如下两个反应:
=-26.7 kJ·mol-1
① CH(g)+HO(g)=CO(g)+3H(g)
4 2 2
②3Fe O(s) + CO(g)===2Fe O(s) + CO(g)
2 3 3 4 2 ΔH=+206 kJ/mol
ΔH=-50.75 kJ·mol-1
2 ② CO(g) + HO(g)=CO(g) + H(g)
③Fe O(s)+CO(g)===3FeO(s)+CO(g) ΔH 2 2 2
3 4 2 3
=-36.5 kJ·mol-1 ΔH=-41 kJ/mol
则反应FeO(s)+CO(g)===Fe(s)+CO 2 (g)的焓变为( 写出CH 4 与 CO 2 生成H 2 和CO的热化学 通过归纳总
) 方程式:________________________
结,强化学
A.+7.28 kJ·mol-1
法指导。
B.-7.28 kJ·mol-1
【变式2】已知下列热化学方程式:
C.+43.68 kJ·mol-1
① CHCOOH(l)+ 2O (g) ═2CO
D.-43.68 kJ·mol-1 3 2 2
(g)+2H O(l) ΔH1=﹣870.3
【答案】A 2 知识问题
【解析】根据盖斯定律,首先考虑目标反应与三个 kJ/mol 化,突出重
已知反应的关系,三个反应中,FeO、CO、Fe、 ② C (s) + O (g)═CO (g) 点,突破难
2 2
CO 2 是要保留的,而与这四种物质无关的 Fe 2 O 3 、 ΔH2=﹣393.5 kJ/mol 点。
Fe O 要通过热化学方程式的叠加处理予以消去,
3 4 ③ H (g) + O (g)═HO(l)
因此将①×3-②-③×2 得到:6FeO(s)+ 2 2 2
ΔH3=﹣285.8 kJ/mol
6CO(g)===6Fe(s)+6CO(g)ΔH=+43.65 kJ·mol-1
2
化简后得 FeO(s)+CO(g)===Fe(s)+CO 2 (g) 则反应 2C(s) +2H 2 (g)+O 2 (g)=
ΔH=+7.28 kJ·mol-1。 CHCOOH(l)的焓变ΔH为( D
3
)
2.【温馨提示】 A.244.15kJ•mol﹣1 B
B.﹣224.15kJ•mol﹣1 巩固所学,
(1)运用热化学方程式进行反应热的计算,可以
检测目标达
C.488.3kJ•mol﹣1
从反应式中各物质的物质的量、质量、标准状况下 成度。
D.﹣488.3kJ•mol﹣1
气体体积、反应热等对应关系,列式进行简单计 【变式3】CH-CO 催化重整不仅可以
4 2
得到合成气(CO和H ),还对温室
算。 2
气体的减排具有重要意义。回答下列
(2)注意热化学方程式中化学计量数只表示物质 问题:CH 4 -CO 2 催化重整反应为:
CH(g)+ CO (g)=2CO(g)+2H(g)。
4 2 2
的物质的量,必须与ΔH相对应,如果化学计量数 ①C(s)+2H(g)=CH (g)
2 4
ΔH=-75 kJ·mol−1
加倍,则ΔH也要加倍。尤其是利用盖斯定律计算
②C(s)+O (g)=CO (g)
2 2
反应热时,热化学方程式可以直接相加减,化学计 ΔH=-394 kJ·mol−1③C(s)+ (g)=CO(g)
ΔH=-111 kJ·mol−1 该催化重整反应
的ΔH=______ kJ·mol−1,
【答案】 +247
【解析】催化重整反应可以由如
量数必须与ΔH相对应。
下过程的到:1/2[③×2-(①+②)。
(3)热化学方程式中的反应热是指按所给形式反
应完全时的反应热。
【技巧指导】
(4)正、逆反应的反应热数值相等,符号相反。 ①目标方程中找唯一
目标方程式中的物质:在给出的各个
(5)热化学方程式相加减时,同种物质之间可相加
已知方程式中只出现一次的物质
减,反应热也随之相加减,所求之和为其代数和。 ②化系数
(6)将一个热化学方程式颠倒时,ΔH的“+”、
把已知方程式中的系数化成与目标方
“-”号必须随之改变。
程式中物质的系数一致。
③同加异减
目标方程式中的物质:与已知方程式
中物质在方程式的同侧,则相加;
与已知方程式
中物质在方程式的异侧,则相减;
教学环节三:用键能计算反应热
教师活动 学生活动 设计意图
1.例题讲解
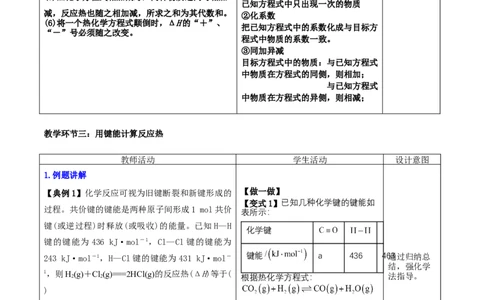
【典例1】化学反应可视为旧键断裂和新键形成的 【做一做】
【变式1】已知几种化学键的键能如
过程。共价键的键能是两种原子间形成1 mol共价
表所示:
键(或逆过程)时释放(或吸收)的能量。已知H—H
化学键
键的键能为436 kJ·mol-1,Cl—Cl键的键能为
243 kJ·mol-1,H—Cl键的键能为431 kJ·mol- 键能 a 436 46通3过归纳总
结,强化学
1,则H 2 (g)+Cl 2 (g)===2HCl(g)的反应热(ΔH)等于( 根据热化学方程式: 法指导。
)
A.183 kJ·mol-1 ,计算表中的a为
巩固所学,
B.-183 kJ·mol-1 A.484.5 B.969 检测目标达
C.779 D.538 成度。
C.-862 kJ·mol-1
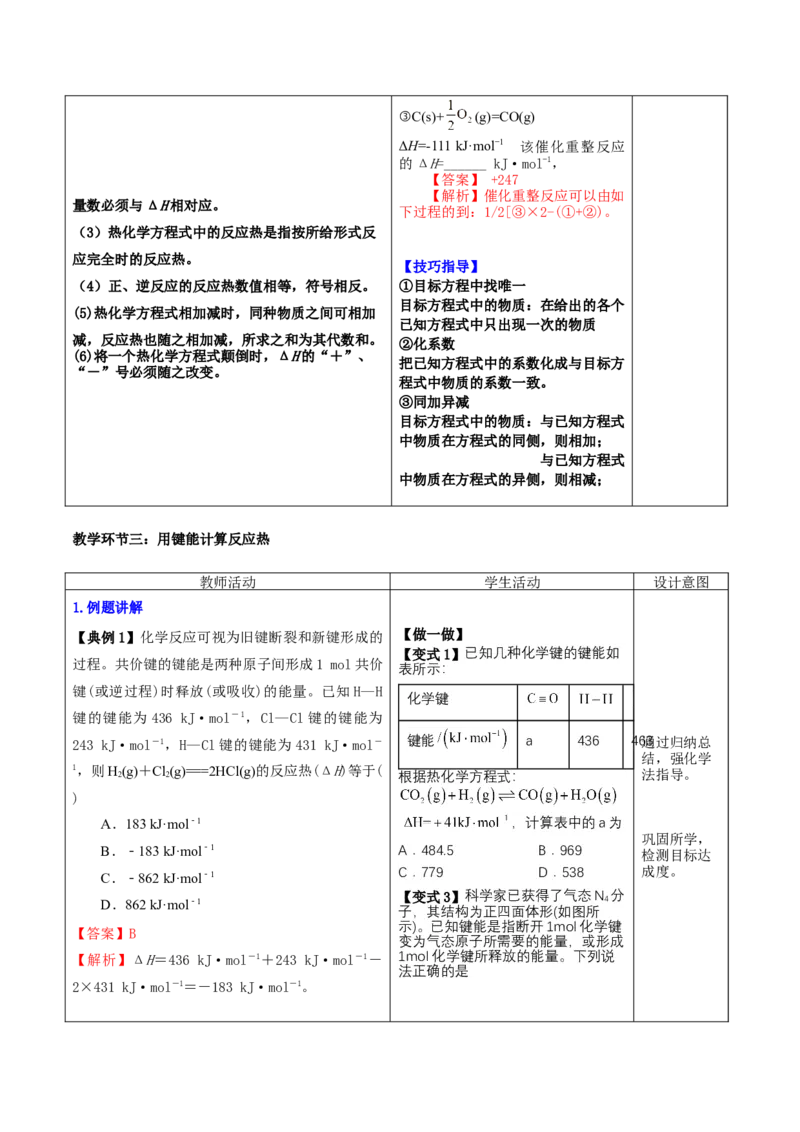
【变式3】科学家已获得了气态N 分
D.862 kJ·mol-1 4
子,其结构为正四面体形(如图所
示)。已知键能是指断开1mol化学键
【答案】B
变为气态原子所需要的能量,或形成
【解析】ΔH=436 kJ·mol-1+243 kJ·mol-1- 1mol化学键所释放的能量。下列说
法正确的是
2×431 kJ·mol-1=-183 kJ·mol-1。2.【技巧指导】
关键:利用键能计算反应热的关键,就是要算清
物质中化学键的种类和数目。
注意特殊物质中键数的判断 N≡ N−
化学键
N N
键能/ kJ∙mol−1 946 193
A.N 属于一种新型的化合物
4
反应热ΔH的计算公式:ΔH=E(反应物的总键能
B.N (g)比N (g)稳定
4 2
之和)-E(生成物的总键能之和) C.56 g N (g)转化为N (g)时要释
4 2
放734 kJ能量
D.N (g)和N (g)互为同位素,N
4 2 4
转化为N 属于化学变化
2
教学环节四:用反应物和生成物的总能量计算反应热
教师活动 学生活动 设计意图
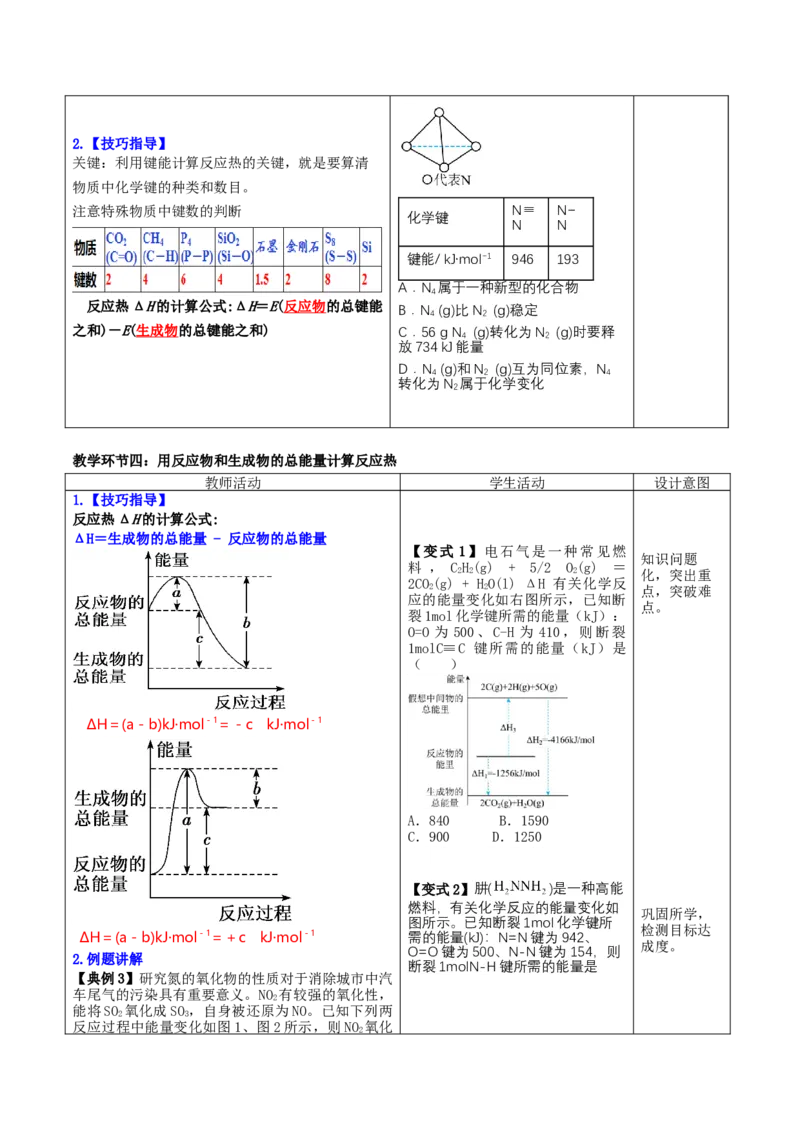
1.【技巧指导】
反应热ΔH的计算公式:
ΔH=生成物的总能量 - 反应物的总能量
【变式 1】电石气是一种常见燃
知识问题
料 , CH(g) + 5/2 O(g) =
2 2 2 化,突出重
2CO(g) + HO(l) ΔH 有关化学反
2 2 点,突破难
应的能量变化如右图所示,已知断
点。
裂1mol化学键所需的能量(kJ):
O=O 为 500、C-H 为 410,则断裂
1molC≡C 键所需的能量(kJ)是
( )
ΔH=(a-b)kJ·mol-1=-c kJ·mol-1
A.840 B.1590
C.900 D.1250
【变式2】肼( )是一种高能
燃料,有关化学反应的能量变化如
巩固所学,
图所示。已知断裂1mol化学键所
检测目标达
ΔH=(a-b)kJ·mol-1=+c kJ·mol-1 需的能量(kJ):N=N键为942、
成度。
O=O键为500、N-N键为154,则
2.例题讲解
断裂1molN-H键所需的能量是
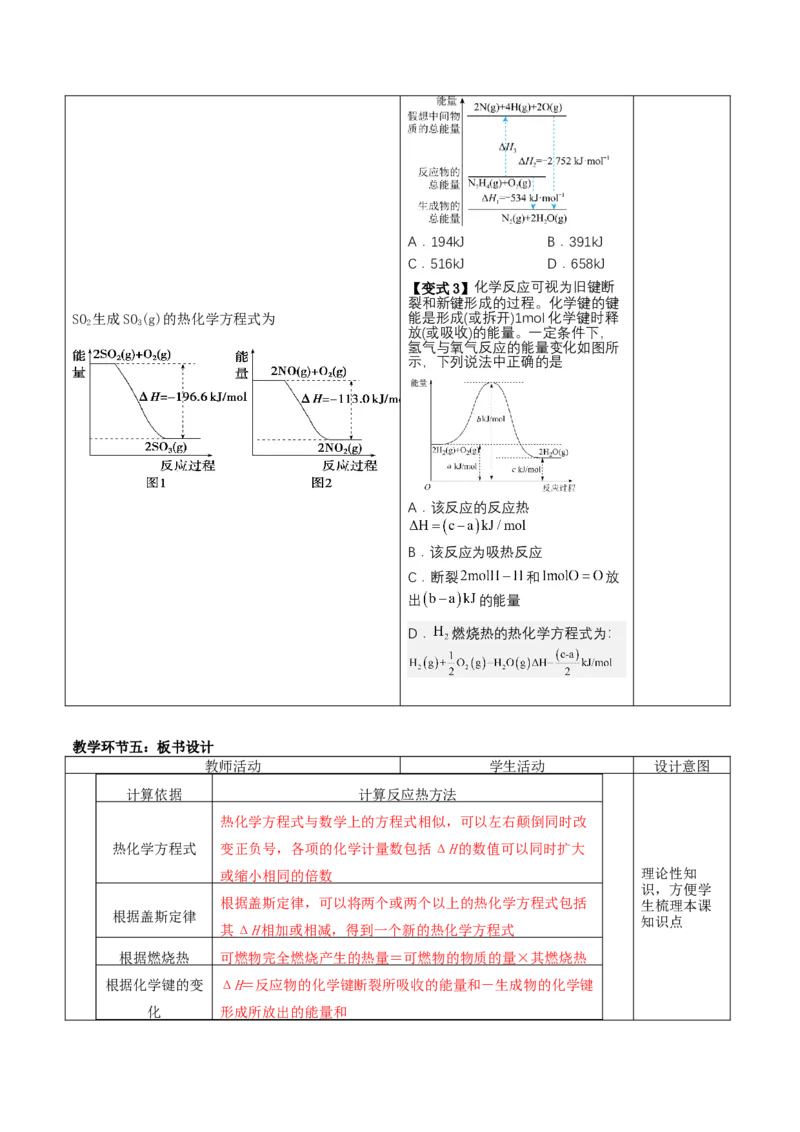
【典例3】研究氮的氧化物的性质对于消除城市中汽
车尾气的污染具有重要意义。NO 有较强的氧化性,
2
能将SO 氧化成SO ,自身被还原为NO。已知下列两
2 3
反应过程中能量变化如图1、图2所示,则NO 氧化
2A.194kJ B.391kJ
C.516kJ D.658kJ
【变式3】化学反应可视为旧键断
裂和新键形成的过程。化学键的键
SO 生成SO(g)的热化学方程式为 能是形成(或拆开)1mol化学键时释
2 3
放(或吸收)的能量。一定条件下,
氢气与氧气反应的能量变化如图所
示,下列说法中正确的是
A.该反应的反应热
B.该反应为吸热反应
C.断裂 和 放
出 的能量
D. 燃烧热的热化学方程式为:
教学环节五:板书设计
教师活动 学生活动 设计意图
计算依据 计算反应热方法
热化学方程式与数学上的方程式相似,可以左右颠倒同时改
热化学方程式 变正负号,各项的化学计量数包括ΔH的数值可以同时扩大
或缩小相同的倍数 理论性知
识,方便学
根据盖斯定律,可以将两个或两个以上的热化学方程式包括 生梳理本课
根据盖斯定律
知识点
其ΔH相加或相减,得到一个新的热化学方程式
根据燃烧热 可燃物完全燃烧产生的热量=可燃物的物质的量×其燃烧热
根据化学键的变 ΔH=反应物的化学键断裂所吸收的能量和-生成物的化学键
化 形成所放出的能量和根据反应物和生
ΔH=E(生成物)-E(反应物)
成物的总能量
教学环节六:教学评价与反馈
教师活动 教学评价 设计意图
教学反思:本课的设计采取课前下发预习学案,学
生预习本节内容,找出自己疑惑的地方。课堂上师
评价任务一:学生能用盖斯定律计
生主要解决重点、难点、疑点、考点、探究点以及
算反应热
学生学习过程中易混点等,并进行当堂检测,课后 对学生掌握
进行延伸拓展,达到提高课堂效率的目的。本节课 知识、形成
的授课时间为45分钟,其中情景导人、展示目标、 评价任务二:学生能用键能计算反 能力的状况
检查预习5分钟,合作探究、精讲点拨10分钟左 应热 作出准确及
右,反思总结、当堂检测10分钟左右,其余环节20 评价任务三:用反应物和生成物的 时的评价和
分钟,能够完成教学内容。在下面的教学过程中会 总能量计算反应热 反馈
继续研究本节课,争取设计得更科学,更有利于学
生的学习。