文档内容
1.3.1 氧化还原反应
【题组一 氧化还原反应的判断】
1.(2019·仙游县度尾中学高一期中)下列变化是氧化还原反应的是( )
A.NH HCO NH ↑+H O+CO↑ B.2FeSO Fe O+SO↑+SO↑
4 3 3 2 2 4 2 3 2 3
C.2O 3O D.CaO+CO = CaCO
3 2 2 3
2.(2020·东莞市东莞中学松山湖学校期中)歌曲《青花瓷》,唱道“帘外芭蕉惹骤雨,门环惹铜绿”,其中
的“铜绿”即是铜锈,它的化学成分是Cu (OH) CO(碱式碳酸铜)。铜在潮湿的空气中生锈的化学反应为
2 2 3
2Cu+O +CO +H O=Cu (OH) CO。下列有关该反应的说法正确的是( )
2 2 2 2 2 3
A.该反应不属于氧化还原反应
B.该反应中氧元素和碳元素化合价发生变化,所以是氧化还原反应
C.该反应中铜得电子,O 失电子,所以是氧化还原反应
2
D.该反应是氧化还原反应,化合价发生改变的只有两种元素
3.(2020·全国课时练习)下列反应中,属于非氧化还原反应的是( )
A.3CuS+8HNO =3Cu(NO)+2NO↑+3S↓+4H O
3 3 2 2
B.3Cl+6KOH=5KCl+KClO +3H O
2 3 2
C.3HO+2KCrO+2KOH=2K CrO+4H O
2 2 2 2 4 2
D.3CCl +K Cr O=2CrO Cl+3COCl +2KCl
4 2 2 7 2 2 2
4.(2020·全国课时练习)下列变化过程发生还原反应的是
A. B.
C. D.
5.(2020·全国课时练习)下列关于氧化还原反应的叙述中,正确的是( )
A.一种元素被氧化,肯定有另一种元素被还原
B.氧化还原反应的实质是电子的转移
C.某元素由化合态变为游离态,则该元素一定被还原
D.氧化还原反应中,得电子越多,氧化性越强
6.(2020·重庆高一期末)下列反应属于氧化还原反应的是
A.CaCO CaO+CO ↑ B.Fe O+3CO 2Fe+3CO
3 2 2 3 2
C.CaO+H O=Ca(OH) D.NaO+2HCl= 2NaCl+H O
2 2 2 2【题组二 氧化还原反应与基本反应】
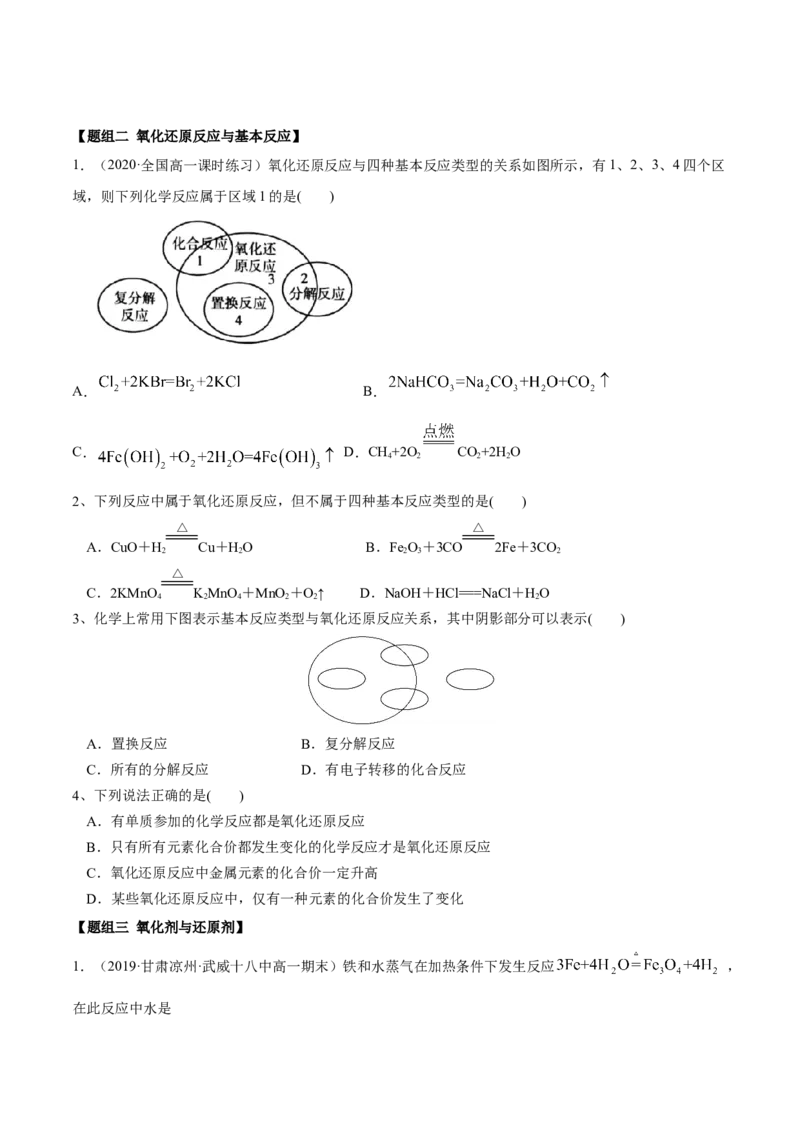
1.(2020·全国高一课时练习)氧化还原反应与四种基本反应类型的关系如图所示,有1、2、3、4四个区
域,则下列化学反应属于区域1的是( )
A. B.
C. D.CH+2O CO+2H O
4 2 2 2
2、下列反应中属于氧化还原反应,但不属于四种基本反应类型的是( )
△ △
A.CuO+H Cu+HO B.Fe O+3CO 2Fe+3CO
2 2 2 3 2
△
C.2KMnO KMnO +MnO +O↑ D.NaOH+HCl===NaCl+HO
4 2 4 2 2 2
3、化学上常用下图表示基本反应类型与氧化还原反应关系,其中阴影部分可以表示( )
A.置换反应 B.复分解反应
C.所有的分解反应 D.有电子转移的化合反应
4、下列说法正确的是( )
A.有单质参加的化学反应都是氧化还原反应
B.只有所有元素化合价都发生变化的化学反应才是氧化还原反应
C.氧化还原反应中金属元素的化合价一定升高
D.某些氧化还原反应中,仅有一种元素的化合价发生了变化
【题组三 氧化剂与还原剂】
1.(2019·甘肃凉州·武威十八中高一期末)铁和水蒸气在加热条件下发生反应 ,
在此反应中水是A.氧化剂 B.还原剂
C.既是氧化剂又是还原剂 D.既不是氧化剂又不是还原剂
2.(2020·全国课时练习)下列变化过程中,加入氧化剂才能实现的是( )
A.Cl→Cl- B.I-→I C.SO → D.CuO→Cu
2 2 2
3.(2020·全国高一课时练习)下列反应表示二氧化硫被还原的是( )
A. B.
C. D.
4.(2020·渝中·重庆巴蜀中学高一期末)下列反应中,硫元素被氧化的是
A.Zn+H SO =ZnSO +H ↑
2 4 4 2
B.C+2H SO (浓) CO↑+2SO↑+2H O
2 4 2 2 2
C.Cu+2H SO (浓)=CuSO+SO↑+2H O
2 4 4 2 2
D.S+O SO
2 2
【题组四 氧化剂还原剂强弱】
1.(2020·全国课时练习)已知 、 、 、 四种物质的氧化能力为 ,下列氧
化还原反应能发生的是( )
A. B.
C. D.
2.(2020·全国课时练习)已知在相同的条件下,下列几种微粒的还原性强弱顺序为Mn2+<Cl-<Br-<
Fe2+<I-<SO ,由此判断下列反应不能发生的是( )
2
A.2 +5SO+2H O=5 +2Mn2++4H+
2 2
B.2Fe3++SO+2H O= +4H++2Fe2+
2 2
C.I+2Fe2+=2Fe3++2I-
2D.2Fe2++2Br-+2Cl=2Fe3++Br +4Cl-
2 2
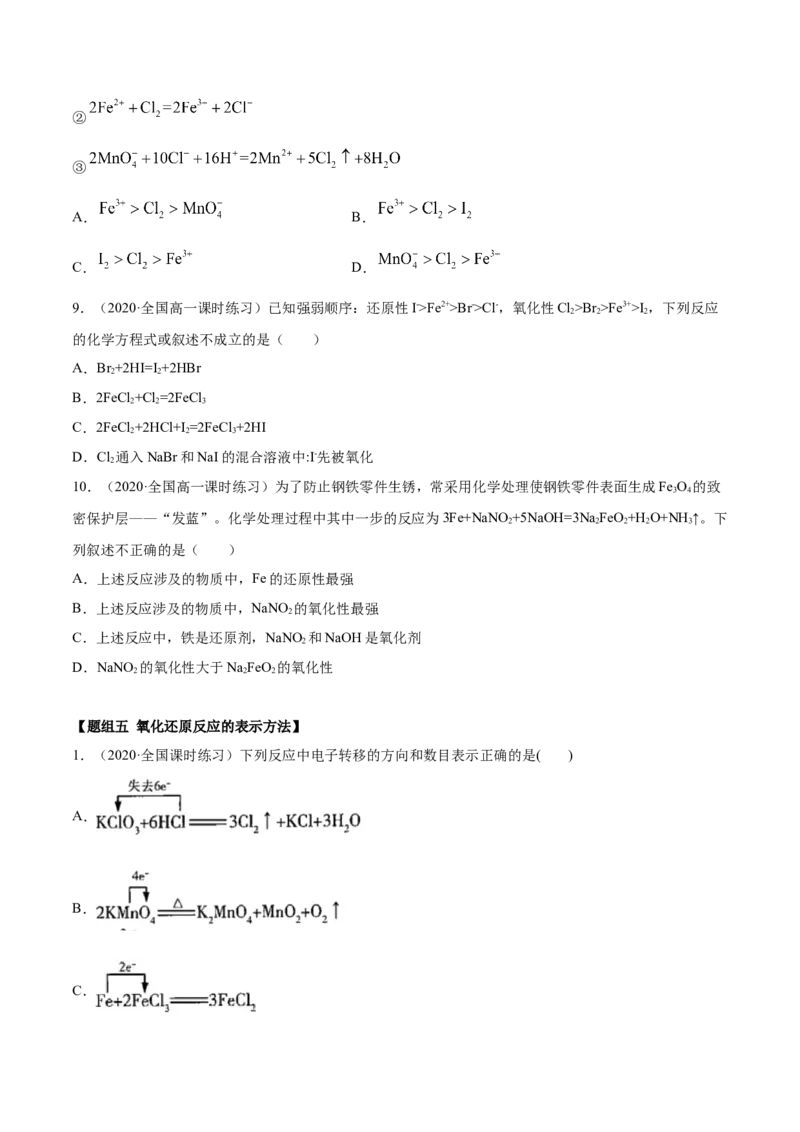
3.(2019·全国高一)已知有如下反应:①2BrO + Cl = Br + 2ClO ,②ClO + 5Cl- + 6H+ = 3Cl +
2 2 2
3HO,③2FeCl + 2KI = 2FeCl + 2KCl + I ,④2FeCl + Cl = 2FeCl 。
2 3 2 2 2 2 3
下列各微粒氧化能力由强到弱的顺序正确的是( )
A.ClO > BrO > Cl > Fe3+ > I B.BrO > Cl > ClO > I > Fe3+
2 2 2 2
C.BrO > ClO > Cl > Fe3+ > I D.BrO > ClO > Fe3+ > Cl > I
2 2 2 2
4.(2020·全国高一课时练习)根据下列反应判断有关物质还原性由强到弱的顺序是( )
①HSO +I +H O═2HI+H SO
2 3 2 2 2 4
②2FeCl +2HI═2FeCl +2HCl+I
3 2 2
③3FeCl +4HNO ═2FeCl +NO↑+2HO+Fe(NO )
2 3 3 2 3 3
A.HSO >I﹣>Fe2+>NO B.I﹣>Fe2+>HSO >NO
2 3 2 3
C.Fe2+>I﹣>HSO >NO D.NO>Fe2+>HSO >I﹣
2 3 2 3
5.(2020·福建省泰宁第一中学高一月考)根据化学方程式:(1)2Fe3++2I-=2Fe2++I ;(2)Br +2Fe2+=2Br-
2 2
+2Fe3+,可判断离子的还原性从强到弱的顺序是( )
A.Br-、Fe2+、I- B.I-、Fe2+、Br-
C.Br 、Fe3+、I D.Br-、I-、Fe2+
2 2
6.(2020·福建省泰宁第一中学高一月考)已知有如下反应:① 2BrO-+ Cl ═ Br + 2ClO -,② 2FeCl +
3 2 2 3 3
2KI ═ 2FeCl + 2KCl + I ,③ ClO -+ 5Cl-+ 6H+ ═ 3Cl + 3H O,④ 2FeCl + Cl ═ 2FeCl ,下列各微粒氧
2 2 3 2 2 2 2 3
化能力由强到弱的顺序正确的是
A.ClO - > BrO- > Cl > Fe3+ > I B.BrO- > Cl > ClO - > I > Fe3+
3 3 2 2 3 2 3 2
C.BrO- > ClO - > Fe3+ > Cl > I D.BrO- > ClO - > Cl > Fe3+ > I
3 3 2 2 3 3 2 2
7.(2020·全国高一单元测试)根据下列三个反应,判断物质的还原性由强到弱的顺序正确的是
2FeCl + 2HI === 2FeCl + 2HCl + I
3 2 2
HSO + I + H O ===2HI + H SO
2 3 2 2 2 4
3FeCl + 4HNO === 2FeCl + NO↑ + 2H O + Fe(NO )
2 3 3 2 3 3
A.NO>Fe2+>H SO >I- B.I->Fe2+>H SO >NO
2 3 2 3
C.Fe2+>I->H SO >NO D.HSO >I->Fe2+>NO
2 3 2 3
8.(2020·全国高一课时练习)根据下列反应判断物质的氧化性强弱,其中排序正确的是( )
①②
③
A. B.
C. D.
9.(2020·全国高一课时练习)已知强弱顺序:还原性I->Fe2+>Br->Cl-,氧化性Cl>Br >Fe3+>I ,下列反应
2 2 2
的化学方程式或叙述不成立的是( )
A.Br +2HI=I +2HBr
2 2
B.2FeCl +Cl=2FeCl
2 2 3
C.2FeCl +2HCl+I =2FeCl +2HI
2 2 3
D.Cl 通入NaBr和NaI的混合溶液中:I-先被氧化
2
10.(2020·全国高一课时练习)为了防止钢铁零件生锈,常采用化学处理使钢铁零件表面生成Fe O 的致
3 4
密保护层——“发蓝”。化学处理过程中其中一步的反应为3Fe+NaNO +5NaOH=3Na FeO+H O+NH ↑。下
2 2 2 2 3
列叙述不正确的是( )
A.上述反应涉及的物质中,Fe的还原性最强
B.上述反应涉及的物质中,NaNO 的氧化性最强
2
C.上述反应中,铁是还原剂,NaNO 和NaOH是氧化剂
2
D.NaNO 的氧化性大于NaFeO 的氧化性
2 2 2
【题组五 氧化还原反应的表示方法】
1.(2020·全国课时练习)下列反应中电子转移的方向和数目表示正确的是( )
A.
B.
C.D.
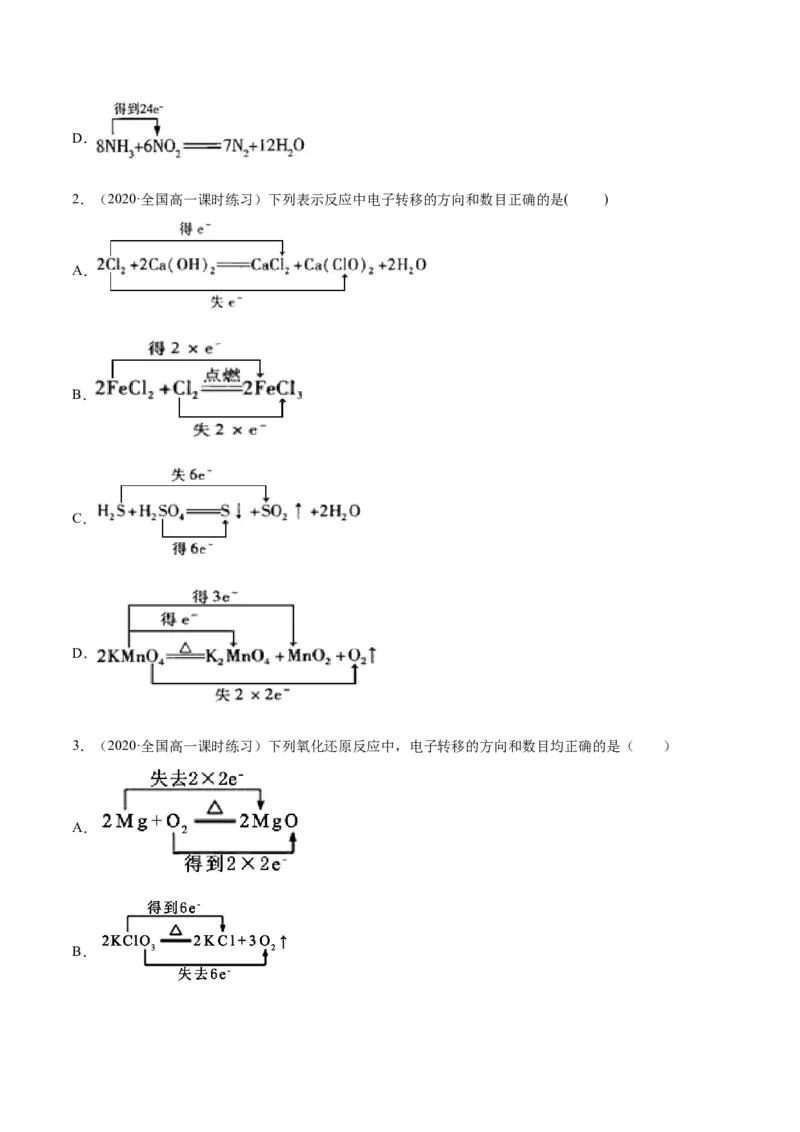
2.(2020·全国高一课时练习)下列表示反应中电子转移的方向和数目正确的是( )
A.
B.
C.
D.
3.(2020·全国高一课时练习)下列氧化还原反应中,电子转移的方向和数目均正确的是( )
A.
B.C.
D.