文档内容
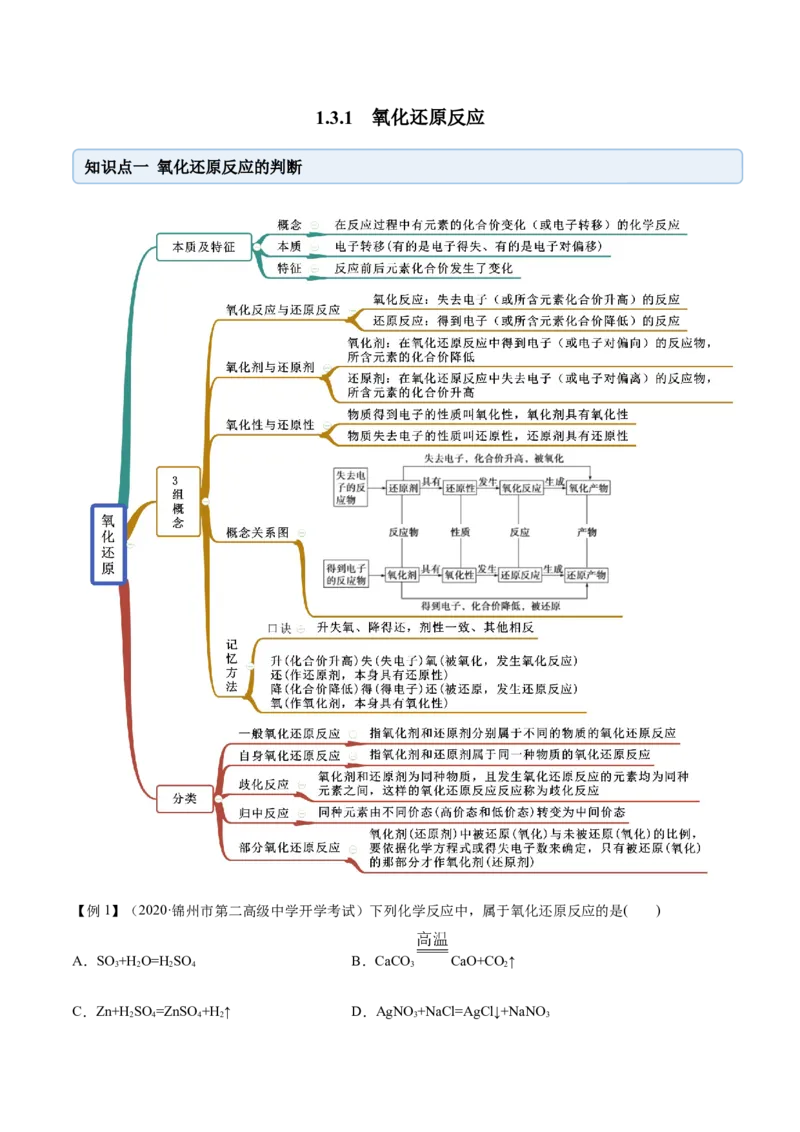
1.3.1 氧化还原反应
知识点一 氧化还原反应的判断
【例1】(2020·锦州市第二高级中学开学考试)下列化学反应中,属于氧化还原反应的是( )
A.SO +H O=HSO B.CaCO CaO+CO ↑
3 2 2 4 3 2
C.Zn+H SO =ZnSO +H ↑ D.AgNO+NaCl=AgCl↓+NaNO
2 4 4 2 3 3【答案】C
【解析】A.SO +H O═H SO ,不存在元素化合价的变化,不属于氧化还原反应,故A不选;
3 2 2 4
B.CaCO CaO+CO ↑,不存在元素化合价的变化,不属于氧化还原反应,故B不选;
3 2
C.Zn+H SO ═ZnSO +H ↑,Zn、H元素的化合价发生变化,属于氧化还原反应,故C选;
2 4 4 2
D.AgNO+NaCl=AgCl↓+NaNO ,不存在元素化合价的变化,不属于氧化还原反应,故D不选;故选C。
3 3
【一隅三反】
1.(2020·全国课时练习)下列属于氧化还原反应的是( )
A. B.
C. D.
【答案】C
【解析】A.反应中无元素化合价发生变化,不是氧化还原反应,A错误;
B.反应中无元素化合价发生变化,不是氧化还原反应,B错误;
C.反应中Ⅰ和Br元素在反应前后化合价发生变化,该反应为氧化还原反应,C正确;
D.反应中无元素化合价发生变化,不是氧化还原反应,D错误;故选C。
2.(2020·全国高一课时练习)下列氧化还原反应发生在同种元素之间的是( )
A.Zn+2HCl===ZnCl +H↑ B.2HS+SO ===3S↓+2HO
2 2 2 2 2
C.H+CuO Cu+HO D.2HO 2H↑+O↑
2 2 2 2 2
【答案】B
【解析】A.Zn、H元素的化合价变化,故A不选;
B.只有S元素的化合价变化,则氧化还原反应发生在同种元素之间,故B选;
C.Cu、H元素的化合价变化,故C不选;
D.H、O元素的化合价变化,故D不选;故选B。
3.(2020·全国课时练习)下列属于氧化还原反应的是( )
①
②③
④
⑤
A.①④⑤ B.②④⑤ C.①②③④ D.①②④⑤
【答案】D
【解析】元素化合价变化分析如下:
①中Cu元素化合价降低(+2→0),H元素化合价升高(0→+1);②中Cl元素的化合价既有升高(0→+1)又有
降低(0→-1);③中各元素的化合价均未变化;④中H元素的化合价降低(+1→0),Na元素的化合价升高
(0→+1);⑤中O元素的化合价升高(-2→0),Mn元素的化合价降低(+7→+6、+4);正确的是D;
答案选D。
知识点二 氧化还原反应与4大基本反应类型关系【例2】(2020·全国高一课时练习)化学反应按照不同的分类方法,可以分为化合反应,分解反应、置换
反应、复分解反应,也可分为氧化还原反应和非氧化还原反应。有下列反应:
① ②
③ ④
⑤ ⑥
⑦ ⑧
(1)其中属于化合反应的是____________(填序号,下同),属于置换反应的是_______。
(2)在化学反应前后元素的化合价没有变化的是_____________。
(3)上述反应中,既是分解反应,又是氧化还原反应的是_______。
(4)上述反应中,既是溶液中的离子反应,又是氧化还原反应的是_______。
【答案】①④⑧ ⑤ ②⑧ ⑦ ③
【解析】① 属于化合反应,有元素的化合价变化,属于氧化还原反应;
② 属于分解反应,反应中无元素发生化合价变化,不属于氧化还原
反应;
③ 中有元素的化合价变化,属于氧化还原反应;
④ 属于化合反应,有元素的化合价变化,属于氧化还原反应;
⑤ 属于置换反应,有元素的化合价变化,属于氧化还原反应;⑥ 中有元素的化合价变化,属于氧化还原反应;
⑦ 属于分解反应,有元素的化合价变化,属于氧化还原反应;
⑧ 属于化合反应,无元素的化合价变化,不属于氧化还原反应;
(1)其中属于化合反应的是①④⑧,属于置换反应的是⑤;
(2)在化学反应前后元素的化合价没有变化的是②⑧;
(3)上述反应中,既是分解反应,又是氧化还原反应的是⑦;
(4)上述反应中,既是溶液中的离子反应,又是氧化还原反应的是③。
【一隅三反】
1.(2019·广东东莞·期中)下列关于氧化还原反应的叙述正确的是
A.H 还原CuO的反应只属于还原反应
2
B.置换反应都是氧化还原反应,所以3CO+Fe O 2Fe+3CO 既是置换反应又是氧化还原反应
2 3 2
C.3O===2O 是氧化还原反应
2 3
D.复分解反应一定不是氧化还原反应
【答案】D
【解析】A.氧化还原反应是同时发生的,氢气还原氧化铜的反应是氧化还原反应,A错误;
B.氧化还原反应的本质是有电子转移,特征是有元素化合价升降。一种化合物和一种单质反应生成另外
的单质和化合物的反应是置换反应,该反应中Fe元素化合价由+3价变为0价、C元素化合价由+2价变为
+4价,所以属于氧化还原反应,但不是置换反应,B错误;
C.该反应为单质生成单质,化合价没有变化,即没有电子转移,所以不是氧化还原反应,C错误;
D.有电子转移的化学反应是氧化还原反应,复分解反应中没有电子转移,所以复分解反应一定不是氧化
还原反应,D正确;故选D。
2.(2020·全国课时练习)氧化还原反应与四种基本反应类型的关系如图所示,则下列化学反应属于阴影
3区域的是( )A.
B.
C.
D.
【答案】D
【解析】A.该反应属于分解反应,又属于氧化还原反应,属于2区域,A错误;
B.该反应属于分解反应,不属于氧化还原反应,B错误;
C.该反应属于化合反应,又属于氧化还原反应,属于1区域,C错误;
D.该反应属于氧化还原反应,且不属于化合、分解、置换反应中的任意一种,故属于阴影3区域,D正
确;
答案选D。
3.下列反应中属于氧化还原反应,但不属于四种基本反应类型的是( )
△ △
A.CuO+H Cu+HO B.Fe O+3CO 2Fe+3CO
2 2 2 3 2
△
C.2KMnO KMnO +MnO +O↑ D.NaOH+HCl===NaCl+HO
4 2 4 2 2 2
【答案】 B
【解析】D没有化合价的变化,排除;A是置换反应,C是分解反应。
知识点三 氧化剂还原剂的判断【例3】(1)(2020·大安市第一中学校月考)下列变化中,需要加入还原剂的是( )
A.H→HCl B.NaCO→NaHCO
2 2 3 3
C.FeCl →FeCl D.SO →SO
3 2 2 3
(2)(2020·大安市第一中学校月考)氢化钙可以作为生氢剂(其中CaH 中氢元素为-1价),反应方程式如
2
下:CaH+2H O=Ca(OH) +2H ↑,其中水的作用是( )
2 2 2 2
A.既不是氧化剂也不是还原剂 B.是氧化剂
C.是还原剂 D.既是氧化剂又是还原剂
【答案】(1)C(2)B
【解析】(1)A. H →HCl,H元素化合价升高,失去电子,需要加入氧化剂才能实现,A错误;
2
B. Na CO→NaHCO ,各元素化合价均无发生变化,不是氧化还原反应,NaCO 溶液中通入CO 即可变为
2 3 3 2 3 2
NaHCO ,B错误;
3
C. FeCl →FeCl ,Fe元素化合价降低,得到电子,需要加入还原剂才能实现,C正确;
3 2
D. SO →SO ,S元素化合价升高,失去电子,需要加入氧化剂才能实现,D错误;故答案为:C。
2 3
(2)根据反应前后元素的化合价变化来看,Ca和O的化合价均没有变化,其中CaH 中H的化合价由-1
2
价升高到0价,被氧化,作还原剂;HO中H的化合价由+1价降低到0价,被还原,作氧化剂;氢气既是
2
氧化产物,又是还原产物;答案选B 。元素化合价角度分析,元素化合价升高,失去电子,被氧化,作还原剂,变为氧化产物;
元素化合价降低,获得电子,被还原,作氧化剂,变为还原产物
【一隅三反】
1.(2017·上海高一期末)在下列氧化还原反应中,水作氧化剂的是
A.Cl+HO→HCl+HClO B.2F+2HO→4HF+O↑
2 2 2 2 2
C.Cl+2NaOH→NaCl+NaClO+HO D.2Na+2HO→2NaOH+H↑
2 2 2 2
【答案】D
【解析】A.在反应Cl+H O→HCl+HClO中,只有Cl元素化合价的变化,所以该反应Cl 既是氧化剂,又是
2 2 2
还原剂;HO的组成元素化合价不变,因此HO不是氧化剂,也不是还原剂,A错误;
2 2
B.在反应2F+2H O→4HF+O ↑中,HO中的O化合价为-2价,反应后变为O 中的0价,化合价升高,失去
2 2 2 2 2
电子,所以水作还原剂,B错误;
C.在反应Cl+2NaOH→NaCl+NaClO+H O中,水是生成物,不是氧化剂,也不是还原剂,C错误;
2 2
D.在反应2Na+2HO→2NaOH+H↑中,HO中的H元素化合价为+1价,反应后变为H 中的0价,化合价降
2 2 2 2
低,获得电子,所以HO是氧化剂,D正确;故合理选项是D。
2
2.(2019·新疆生产建设兵团第五师高级中学高一期中)下列反应中必须加入还原剂才能进行的是( )
A.CuO → Cu B.H → H O
2 2
C.CaO → Ca(OH) D.Zn → Zn2+
2
【答案】A
【解析】A.Cu元素的化合价降低,必须加入还原剂才能进行,A符合题意;
B.H元素的化合价升高,需要加氧化剂发生,B不符合题意;
C.元素化合价没有发生变化,不需要加入还原剂就可以实现,C不符合题意;
C.Zn元素的化合价升高,需要加氧化剂发生,D不符合题意;故合理选项是A。
3.(2020·吐鲁番市高昌区第二中学高一期末)下列反应中水起还原剂作用的是( )
A.CaO + H O = Ca(OH) B.C+H O(g) CO+H
2 2 2 2
C.2F + 2H O = 4HF + O D.3NO + H O = 2HNO + NO
2 2 2 2 2 3
【答案】C
【解析】A、氧化钙与水反应是非氧化还原反应,A错误;
B、反应中氢元素化合价降低,水是氧化剂,B错误;C、反应中氧元素化合价升高,水是还原剂,C正确;
D、反应中只有氮元素化合价变化,NO 是氧化剂,又是还原剂,D错误;答案选C。
2
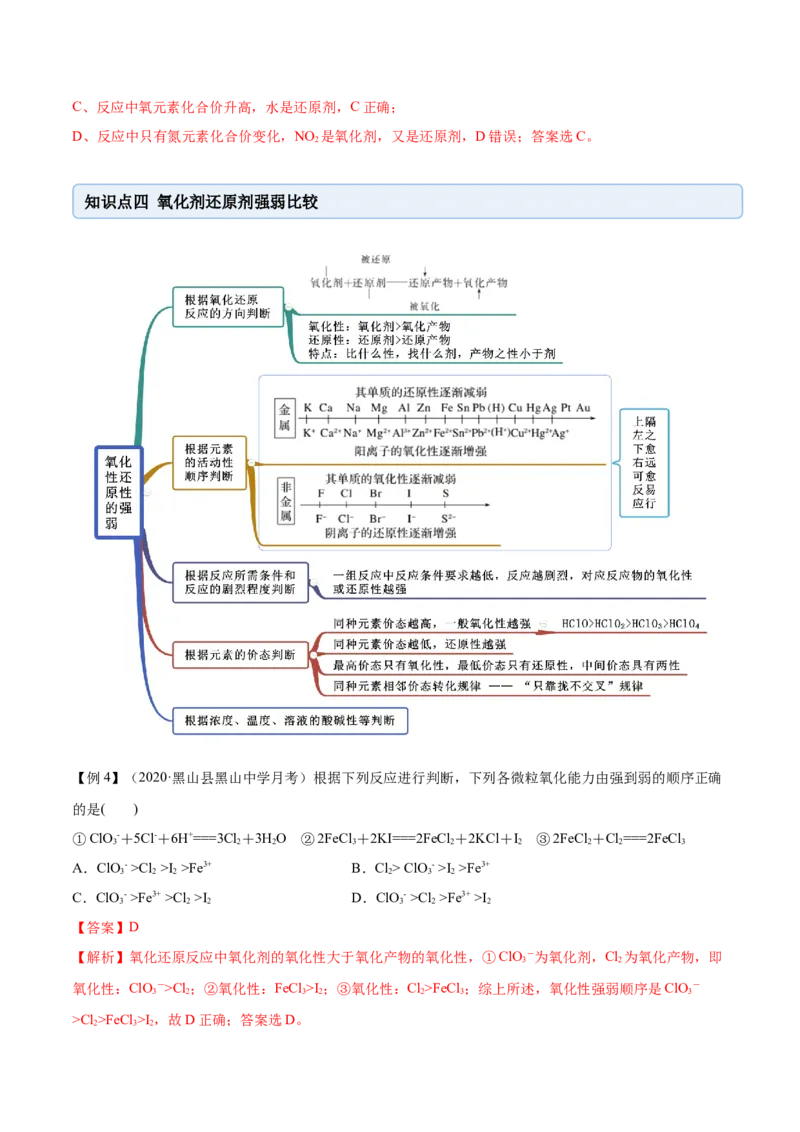
知识点四 氧化剂还原剂强弱比较
【例4】(2020·黑山县黑山中学月考)根据下列反应进行判断,下列各微粒氧化能力由强到弱的顺序正确
的是( )
①ClO -+5Cl-+6H+===3Cl +3HO ②2FeCl +2KI===2FeCl +2KCl+I ③2FeCl +Cl===2FeCl
3 2 2 3 2 2 2 2 3
A.ClO - >Cl >I >Fe3+ B.Cl> ClO - >I >Fe3+
3 2 2 2 3 2
C.ClO - >Fe3+ >Cl >I D.ClO - >Cl >Fe3+ >I
3 2 2 3 2 2
【答案】D
【解析】氧化还原反应中氧化剂的氧化性大于氧化产物的氧化性,①ClO -为氧化剂,Cl 为氧化产物,即
3 2
氧化性:ClO ->Cl;②氧化性:FeCl >I ;③氧化性:Cl>FeCl ;综上所述,氧化性强弱顺序是ClO -
3 2 3 2 2 3 3
>Cl>FeCl >I ,故D正确;答案选D。
2 3 2【一隅三反】
1.(2020·陕西榆阳·榆林十二中月考)已知常温下在溶液中可发生如下两个离子反应:①Ge4++Fe2+=Fe3+
+Ge3+ ②Sn2++2Fe3+=2Fe2++Sn4+。由此可以确定Fe2+、Ge3+、Sn2+三种离子的还原性由强到弱的顺序
是( )
A.Sn2+、Fe2+、Ge3+ B.Sn2+、Ge3+、Fe2+
C.Ge3+、Fe2+、Sn2+ D.Fe2+、Sn2+、Ge3+
【答案】A
【解析】在反应①Ge4++Fe2+=Fe3++Ge3+中,Fe的化合价从+2升高到+3价,Fe2+是还原剂,Ge3+是还原产
物,所以还原性:Fe2+>Ge3+;在反应②Sn2++2Fe3+=2Fe2++Sn4+中,Sn的化合价从+2价升高到+4价,
Sn2+是还原剂,Fe2+是还原产物,所以还原性:Sn2+>Fe2+,所以Fe2+、Ge3+、Sn2+三种离子的还原性由
强到弱的顺序是Sn2+、Fe2+、Ge3+,故选A。
2.(2020·南昌县莲塘第二中学期末)已知Co O 在酸性溶液中易被还原成Co2+,Co O、Cl、FeCl 、I 的
2 3 2 3 2 3 2
氧化性依次减弱。下列反应在水溶液中不可能发生的是( )
A.3Cl+6FeI =2FeCl +4FeI B.Cl+FeI =FeCl +I
2 2 3 3 2 2 2 2
C.Co O+6HCl=2CoCl +Cl↑+3H O D.2Fe3++2I-=2Fe2++I
2 3 2 2 2 2
【答案】A
【解析】A.根据反应:3Cl+6FeI =2FeCl +4FeI ,得出氧化性是:Cl>FeCl ,但是氧化性是FeCl >I,
2 2 3 3 2 3 3 2
还原性是碘离子强于亚铁离子,碘离子会先被氯气氧化,和题意不相符合,不可能发生,故A符合题意;
B.因为氧化性FeCl >I,所以氯气先氧化碘离子后氧化铁离子,故B不符合题意;
3 2
C.根据反应:Co O+6HCl=2CoCl +Cl↑+3H O,得出氧化性是:Co O>Cl,和题意相符合,反应可能发
2 3 2 2 2 2 3 2
生,故C不符合题意;D.因为氧化性FeCl >I,所以2Fe3++2I-=2Fe2++I 能发生,故D不符合题意。
3 2 2
答案选A。
3.(2020·大安市第一中学校月考)根据下列反应的化学方程式:①I+SO+2H O = HSO +2HI;
2 2 2 2 4
②2FeCl +Cl = 2FeCl ;③2FeCl +2HI = 2FeCl +2HCl+I 判断有关物质的还原性强弱顺序是
2 2 3 3 2 2
A.I->Fe2+>Cl->SO B.Cl->Fe2+>SO>I-
2 2
C.Fe2+>I->Cl->SO D.SO >I->Fe2+>Cl-
2 2
【答案】D
【解析】在①I+SO+2H O=2HI+HSO 中还原剂是SO 、还原产物是HI,所以还原性SO >HI;
2 2 2 2 4 2 2
在②2FeCl +Cl=2FeCl 中还原剂是FeCl 、还原产物是FeCl ,所以还原性FeCl >FeCl ;
2 2 3 2 3 2 3③2FeCl +2HI=I +2FeCl +2HCl中还原剂是HI、还原产物是FeCl ,所以还原性KI>FeCl ;
3 2 2 2 2
通过以上分析知,物质的还原性有强到弱的顺序是SO >I->Fe2+>Cl-,故合理选项是D。
2
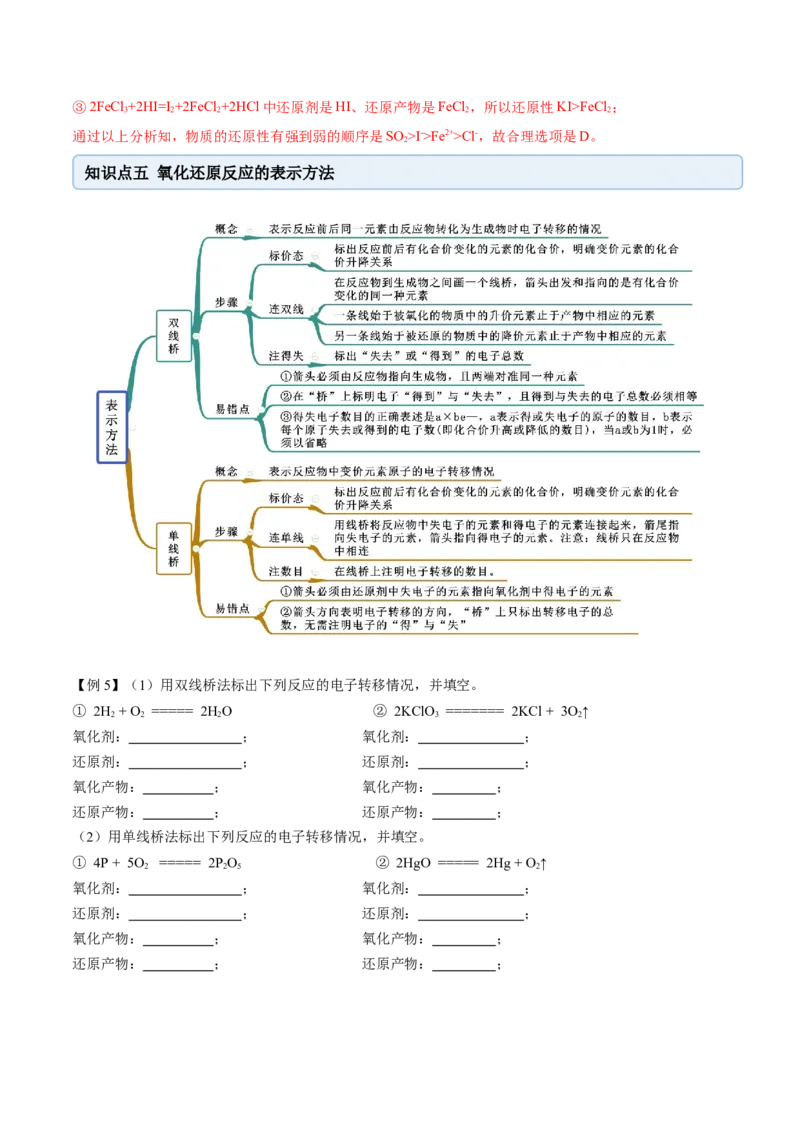
知识点五 氧化还原反应的表示方法
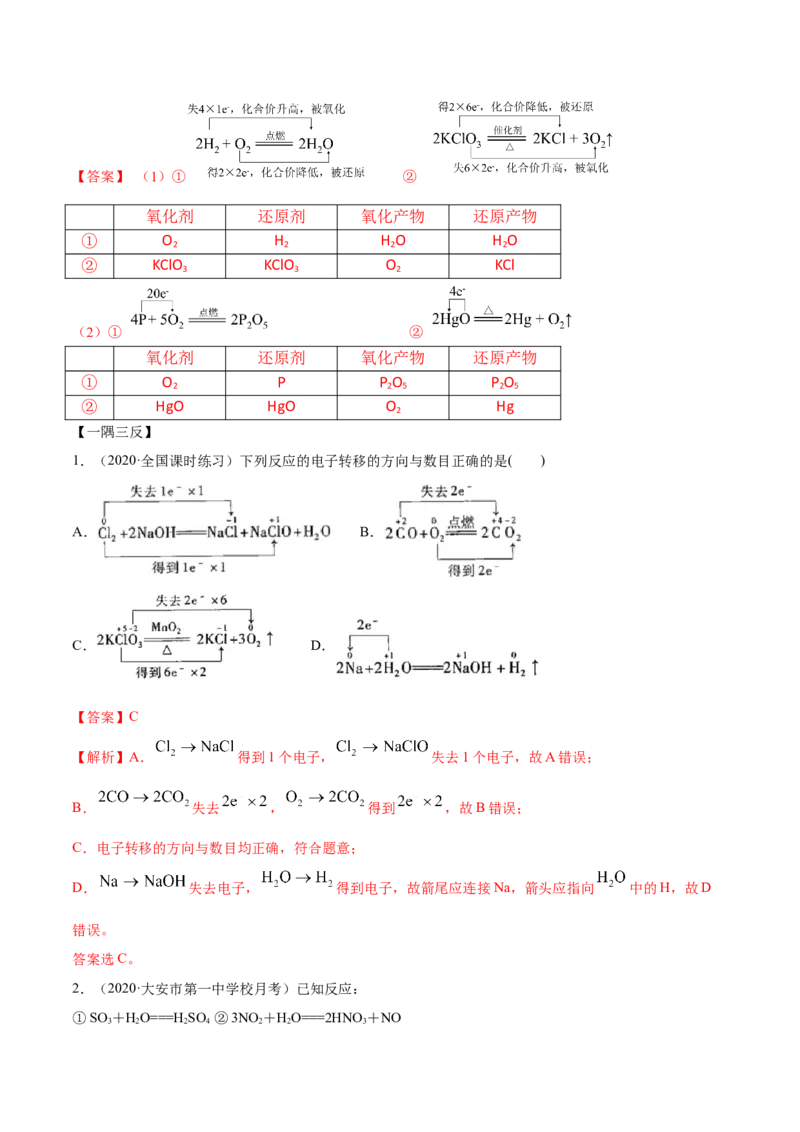
【例5】(1)用双线桥法标出下列反应的电子转移情况,并填空。
① 2H + O ===== 2HO ② 2KClO ======= 2KCl + 3O↑
2 2 2 3 2
氧化剂: ; 氧化剂: ;
还原剂: ; 还原剂: ;
氧化产物: ; 氧化产物: ;
还原产物: ; 还原产物: ;
(2)用单线桥法标出下列反应的电子转移情况,并填空。
① 4P+ 5O ===== 2PO ② 2HgO ===== 2Hg + O ↑
2 2 5 2
氧化剂: ; 氧化剂: ;
还原剂: ; 还原剂: ;
氧化产物: ; 氧化产物: ;
还原产物: ; 还原产物: ;【答案】 (1)① ②
氧化剂 还原剂 氧化产物 还原产物
① O H H O H O
2 2 2 2
② KClO KClO O KCl
3 3 2
(2)① ②
氧化剂 还原剂 氧化产物 还原产物
① O P P O P O
2 2 5 2 5
② HgO HgO O Hg
2
【一隅三反】
1.(2020·全国课时练习)下列反应的电子转移的方向与数目正确的是( )
A. B.
C. D.
【答案】C
【解析】A. 得到1个电子, 失去1个电子,故A错误;
B. 失去 , 得到 ,故B错误;
C.电子转移的方向与数目均正确,符合题意;
D. 失去电子, 得到电子,故箭尾应连接Na,箭头应指向 中的H,故D
错误。
答案选C。
2.(2020·大安市第一中学校月考)已知反应:
①SO +HO===H SO ②3NO +HO===2HNO+NO
3 2 2 4 2 2 3③2F+2HO===4HF+O ④2Na+2HO===2NaOH+H↑
2 2 2 2 2
⑤NaO+2HCl===2NaCl+HO ⑥SiO+2NaOH===Na SiO+HO
2 2 2 2 3 2
(1)上述反应中,不属于氧化还原反应的是________(填序号,下同)。HO被氧化的是________;HO被还
2 2
原的是________;属于氧化还原反应,但其中的HO既不被氧化又不被还原的是_____________。
2
(2)用双线桥法标出反应②中电子转移的方向和数目:________________________。
(3)用单线桥法标出反应③中电子转移的方向和数目:____________________________。
(4)写出反应⑥的离子方程式:______________________________________________。
【答案】①⑤⑥ ③ ④ ② SiO
2
+2OH-= +HO
2
【解析】(1)只有①⑤⑥反应中没有元素的化合价变化,不属于氧化还原反应;只有③水中O元素的化
合价升高,水被氧化;只有④水中H元素的化合价降低,水被还原;只有②中属于氧化还原反应,但水中
H、O元素的化合价不变,则HO既不被氧化,又不被还原;
2
(2)该反应中,只有氮原子化合价变化,电子转移的方向和数目为 ;
(3)2F+2H O═4HF+O 反应中O失电子,F得电子,所以用单线桥表示电子转移的方向和数目为
2 2 2
;
(4)SiO+2NaOH===Na SiO+HO的离子方程式为SiO+2OH-= +HO。
2 2 3 2 2 2
3.(2020·全国高一课时练习)(1)写出 与 在高温下反应的化学方程式,并用双线桥标出电子转
移的方向和数目____。
(2)写出 和 溶液反应的离子方程式,并用单线桥标出电子转移的方向和数目_____。
【答案】【解析】(1) 与 反应的反应中,1mol 得到6mol电子,被还原为单质铁,1molCO被氧化
为CO 只能得到2mol电子,1mol 需消耗3molCO,故答案为: ;
2
(2) 和 反应中,Cu为还原剂,Ag+为氧化剂,1molAg+等得到1mol电子,1molCu失去2mol
电子,故答案为: 。