文档内容
第一章 第三节 氧化还原反应(第一课时)
教学目标:
1.通过对不同化学反应分类依据的评价,体会以元素化合价有无变化为依据
对反应进行分类的价值;
2.认识有化合价变化的反应是氧化还原反应;
3.利用氯化钠和氯化氢电子转移模型,认识氧化还原反应的本质是电子的转
移.渗透和培养证据推理与模型认知,宏观辨识与微观探析的核心素养。
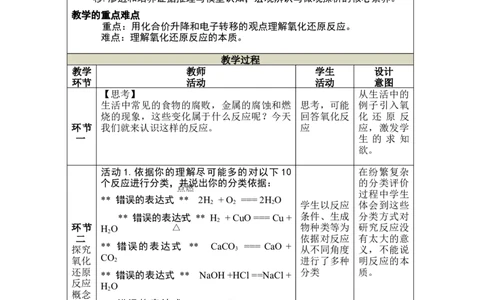
教学的重点难点
重点:用化合价升降和电子转移的观点理解氧化还原反应。
难点:理解氧化还原反应的本质。
教学过程
教学 教师 学生 设计
环节 活动 活动 意图
【思考】 从生活中的
生活中常见的食物的腐败,金属的腐蚀和燃 思考,可能 例子引入氧
烧的现象,这些变化属于什么反应呢?今天 回答氧化反 化 还 原 反
环节 我们就来认识这样的反应。 应 应,激发学
一 生 的 求 知
欲。
活动 1.依据你的理解尽可能多的对以下 10 在纷繁复杂
个反应进行分类,并说出你的分类依据: 的分类评价
点燃
过程中学生
** 错误的表达式 ** 2H + O === 2H O
2 2 2 学生以反应 体会到这些
** 错误的表达△式 ** H + CuO === Cu + 条件、生成 分类方式对
2
环节 H O △ 物种类等为 研究反应没
2
二 依据对反应 有太大的意
** 错误的表达式 ** CaCO === CaO +
探究 3 从不同角度 义,不能说
CO
氧化 2 进行了多种 明反应的本
还原 分类 质。
** 错误的表达式 ** NaOH +HCl ==NaCl +
反应
H O
2
概念
特征 ** 错误的表达式 ** 2FeCl +Cl ===
2 2
2FeCl
3
** 错误的表达式 ** 2Na +2H O === 2NaOH
2
+ H
2 △
** 错误的表达式 ** Fe O +3CO === 2Fe + 思考交流
2 3
3CO 通过同组间
2
找共性,不
** 错误的表达式 ** Na SO + 2HCl ===
2 3 同组之间找
2NaCl + SO + H O
2 2 光 差异,寻找
** 错误的表达式 ** 2HClO === 2HCl + 到了以元素
O 化合价有无
2
变化作为反** 错误的表达式 ** 3NO + H O ==2HNO 应分类的依
2 2 3
+ NO 据,体会氧
化还原反应
活动2. 某同学认真观察、思考后,将上述
的特征
反应分为如下两组:
第** 错误的表达式 **组 第** 错误的表达式 **组 对比,思考 探查并培养
找到分类的 了学生归纳
依据 共性,感悟
* = * = = 错 误 2H 的 2 O 表达式 点 ** 燃 2H 2 + O 2 * C * a O 错 + 误 CO 的 2 表达式 △ **CaCO 3 == 新的分类依
** 错误的表达式 *△*H 2 + CuO ** 错误的表达式 **NaOH + HCl 据的能力,
=== Cu + H 2 O = NaCl + H 2 O 初步建立氧
** 错误的表达式 **2FeCl 2 + ** 错误的表达式 **Na 2 SO 3 +2HCl 化还原反应
Cl 2 = 2FeCl 3 = 2NaCl +SO 2 + H 2 O
概念模型
** 错误的表达式 **2Na +
2HO =2NaOH + H
2 2
** 错误的表达式 **F△eO +
2 3
3CO === 2Fe + 3CO
2
光
** 错误的表达式 **2HClO
=== 2HCl + O
2
** 错误的表达式 **3NO +
2
HO = 2HNO + NO
2 3
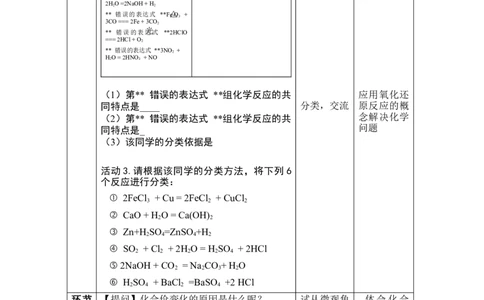
(1)第** 错误的表达式 **组化学反应的共 应用氧化还
同特点是____ 分类,交流 原反应的概
(2)第** 错误的表达式 **组化学反应的共 念解决化学
同特点是_ 问题
(3)该同学的分类依据是
活动3.请根据该同学的分类方法,将下列 6
个反应进行分类:
2FeCl + Cu = 2FeCl + CuCl
3 2 2
CaO + H O = Ca(OH)
2 2
Zn+H SO =ZnSO +H
2 4 4 2
SO + Cl + 2H O = H SO + 2HCl
2 2 2 2 4
⑤ 2NaOH + CO = Na CO + H O
2 2 3 2
H SO + BaCl =BaSO +2 HCl
2 4 2 4
环节 【提问】化合价变化的原因是什么呢? 试从微观角 体会化合
三 度分析,总 价变化的本
探究 【引导分析】2Na+Cl ====2NaCl 结氧化还原 质是电子的
2
氧化 H +Cl 2HCl 反应中化合 得失
2 2===
还原 两个反应,从微观角度分析化合价变化的原 价变化的本 培养学生的
反应 因。 质原因。 自学能力,
本质 【提问】 根据我们今天所学的知识,化学反 思考回答 及解决问题
应还可以怎么分? 的能力
掌握氧化还
【提问】 氧化还原反应与四种基本反应有什 分析 PPT 反 原反应的本
么关系呢? 应,思考 质
学以致用。
到PPT 上画 理解氧化还关系图 原反应和四
【图示】氧化还原反应与四种基本反应关系 大基本反应
图 及它们之间
关系
环节 有化合价升 梳理本节课
氧化还原反应
四 降的反应 所学内容,
小结 本质 特征
升升
化合价的变 加深记忆和
化合价 升电降子转移化 理解
电子的转移
相等
相等失失
氧氧
降降
得得
还还
板书设计
氧化还原反应(第一课时)
一、氧化还原反应
1. 概念:有元素化合价升降的化学反应
2. 本质:电子的转移(得失或偏移)
3.化学反应分类
4、氧化还原反应与四大基本反应的关系