文档内容
第三节 氧化还原反应 第2课时氧化剂还原剂(教学设计)
教学目标:
1. 通过用双线桥表示电子转移过程,明确电子转移代数和为 0,提炼氧化还原反应的一般
认识思路,初步形成“氧化还原”的概念网络。
2. 通过对具体氧化还原反应的判断和分析,归纳常见的氧化剂和还原剂,找到化合价与
氧化性、还原性的关联规律,初步形成氧化还原认识思路的结构化。
3. 通过分析汽车尾气系统中催化转化器中的反应,感受氧化还原反应的价值,初步形成
绿色应用的意识,增强社会责任感。
教学过程
教学环节 教师活动 学生活动 设计意图
【课前任务】 通过【课前
分析氧化还原反应1-6,用双线桥表示 思考 任务】,复
习巩固双线
电子转移的过程,指出被氧化和被还 比对,
桥表示电子
原的元素。
改正自己的学案 转移的方法
和过程
【讲述】
在任何一个氧化还原反应中,有
电子的“得”就一定同时存在电子的
“失”。化合价升高的原子,失电
子,该元素被氧化,反应物发生氧化
环节一
反应;被另一种反应物(对方)氧 理解、记忆,有关 通过聆听和
复习巩固
化,对方具有氧化性,作氧化剂;相 氧化还原的概念, 理解,将氧
双线桥,
反,失电子物质作还原剂,具有还原 重点是氧化剂、还 化还原概念
引出氧化
性。 原剂;氧化产物、 初步形成网
剂还原剂
还原产物。 络
概念 还原剂,反应物,具有还原性,
其中某元素在反应过程中化合价升
高,失电子,该元素被氧化,发生氧
化反应,生成氧化产物。
【梳理】
梳理氧化还原的相关概念
【任务1】指出反应1-6的氧化剂、还
原剂;氧化产物、还原产物
完成【任务1】
【思考】
在Fe元素家庭中,不同价态的Fe 通过分析氧
在氧化还原反应中,充当哪个角色? 化 还 原 反
为什么? 应,发现化
环节二 思考,讨论 合价与氧化
【追问】能否从化合价角度出发,举
发现化合 分析元素原子结 性、还原性
出几种含有其他元素的氧化剂、还原
价与氧化 构,利用最高价、 的关系
剂?
剂、还原
最低价和中间价的
剂之间的
氧化还原规律,梳
关系
理常见氧化剂和还梳理常见氧化剂和还原剂,并适当补 原剂
充反应,为学生的分析结果提供证
据。
环节三 课本,第24页 自主阅读,思考, 简单应用氧
学以致用 完成本题 化还原反应
汽车尾气系统中催化转化器的反应
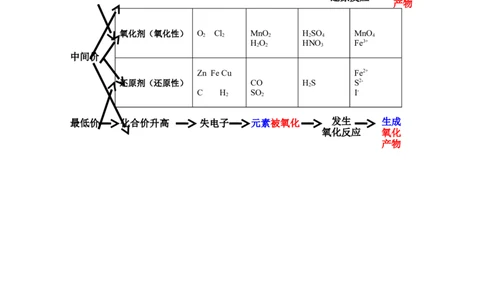
【板书设计】
生成
发生
最高价 化合价降低 得电子 元素被还原 还原反应 还原
产物
氧化剂(氧化性) O Cl MnO HSO MnO
2 2 2 2 4 4
HO HNO Fe3+
2 2 3
中间价
Zn Fe Cu Fe2+
还原剂(还原性) CO HS S2-
2
C H SO I-
2 2
最低价 化合价升高 失电子 元素被氧化 发生 生成
氧化反应 氧化
产物