文档内容
第二章 分子结构与性质
第一节 共价键
2.1.1 共价键
1.认识共价键的本质,原子间通过原子轨道重叠形成共价键。
2.熟知共价键的概念与形成,知道共价键的特征——具有饱和性和方向性。
3.能够从不同的角度对共价键分类,会分析σ键和π键的形成及特点。
教学重点:σ键和π键的形成及特点
教学难点:σ键和π键的形成及特点
一、温故知新
1.化学反应的本质: 的断裂和 的形成的过程。
2.化学键:相邻的原子之间强烈的相互作用。化学键分为 、 、金属键。
3.离子化合物:由 构成的化合物,离子化合物中一定含有离子键,可能含有
。
4.共价化合物:以 形成分子的化合物叫做共价化合物。共价化合物中只含有共价键,但
只含共价键的物质不一定是共价化合物。
二、新知学习
【学生活动一】
钠、氯通过得失电子形成电子对,为什么这对电子不被钠原子和氯原子共用形成共价键而形成离子
键?你能从元素的电负性差别来理解吗?填写下表。8uo-【=
元素 Na Cl H Cl C O
电负性
电负性差值 0.9 1
元素的电负性差值很大,化学反应形成的电子对不会被共用,形成 ,而 是电
负性差值不大的原子间形成的共价键。
1、共价键的定义及本质
(1).含义:原子间通过共用电子对所形成的相互作用叫做共价键。
(2).本质:在原子间形成的共用电子对,原子间通过共用电子对(即电子云重叠)产生的强烈作用。(3).形成条件: 的原子之间形成共价键,大多数电负性之差小于 的金属与非
金属原子之间形成共价键。
2、共价键的特征
(1).饱和性
按照定义,一个原子有几个未成对电子,便可和几个 相反的电子配对成键,这就是共价键
的饱和性。
(2).方向性
共价键形成的过程中,两个参与成键的原子轨道沿着 的方向进行重叠,且原子轨
道重叠越 ,电子在两核间出现的概率越 ,形成的共价键越 。因此共价
键将尽可能沿着电子出现概率最大的方向形成。
【学生活动二】
书写H、HCl、Cl 的电子式。思考为什么难以形成H、HCl、Cl 等分子?
2 2 3 2 3
3、共价键的类型
(1).σ键
①概念:两原子在成键时,原子轨道以“ ”的方式重叠形成的共价键。
②σ键的类型与形成过程
σ键的类型 、 、
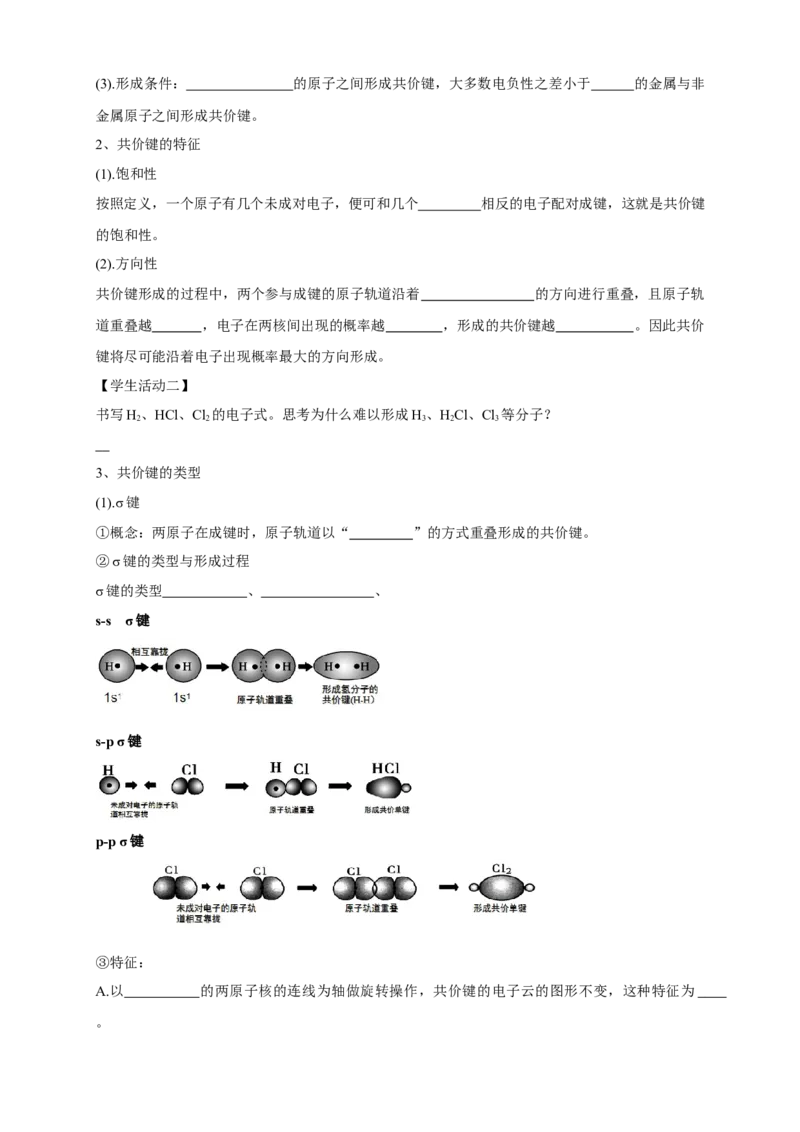
s-s σ键
s-p σ键
p-p σ键
③特征:
A.以 的两原子核的连线为轴做旋转操作,共价键的电子云的图形不变,这种特征为
。B.以 的两个原子核的连线为轴,任意一个原子可以 旋转,并不会破坏σ键
C.形成σ键的原子轨道的重叠程度较 ,故σ键具有较强的 。
(2).π键
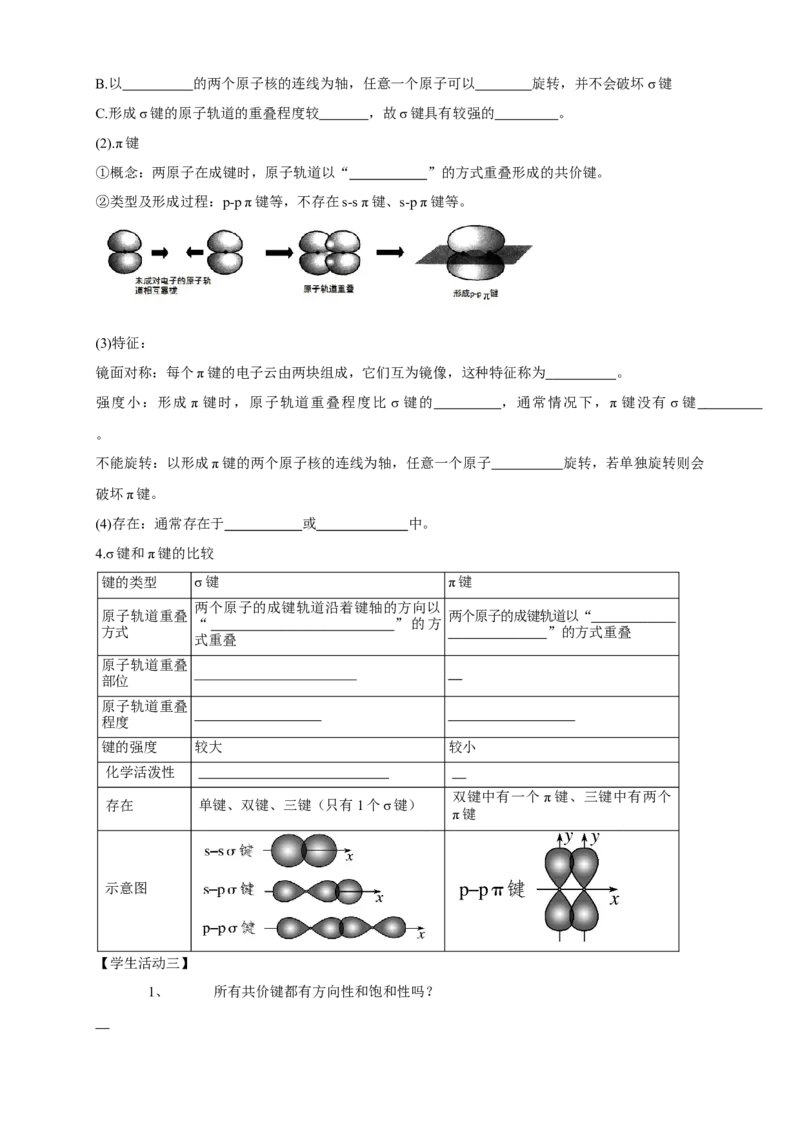
①概念:两原子在成键时,原子轨道以“ ”的方式重叠形成的共价键。
②类型及形成过程:p-p π键等,不存在s-s π键、s-p π键等。
(3)特征:
镜面对称:每个π键的电子云由两块组成,它们互为镜像,这种特征称为 。
强度小:形成 π 键时,原子轨道重叠程度比 σ 键的 ,通常情况下,π 键没有 σ 键
。
不能旋转:以形成π键的两个原子核的连线为轴,任意一个原子 旋转,若单独旋转则会
破坏π键。
(4)存在:通常存在于 或 中。
4.σ键和π键的比较
键的类型 σ键 π键
两个原子的成键轨道沿着键轴的方向以
原子轨道重叠 两个原子的成键轨道以“
“ ”的方
方式 ”的方式重叠
式重叠
原子轨道重叠
_______________________
部位
原子轨道重叠
程度
键的强度 较大 较小
化学活泼性
双键中有一个π键、三键中有两个
存在 单键、双键、三键(只有1个σ键)
π键
示意图
【学生活动三】
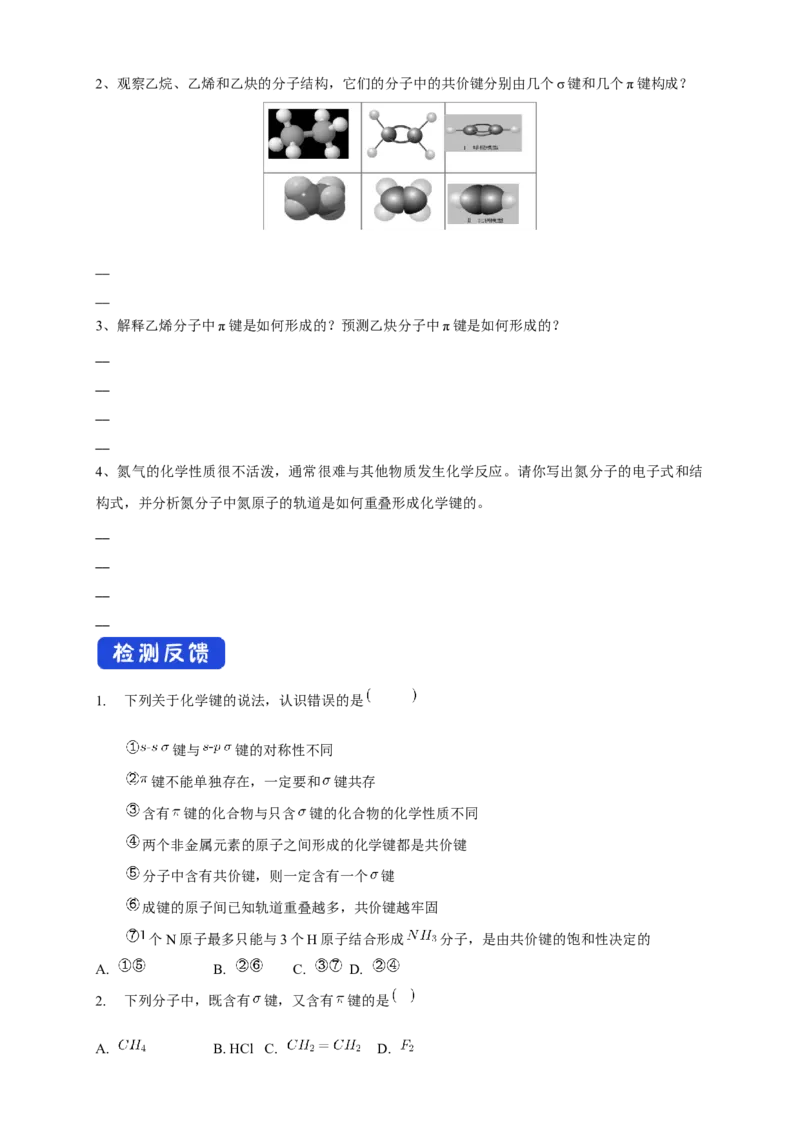
1、 所有共价键都有方向性和饱和性吗?2、观察乙烷、乙烯和乙炔的分子结构,它们的分子中的共价键分别由几个σ键和几个π键构成?
3、解释乙烯分子中π键是如何形成的?预测乙炔分子中π键是如何形成的?
4、氮气的化学性质很不活泼,通常很难与其他物质发生化学反应。请你写出氮分子的电子式和结
构式,并分析氮分子中氮原子的轨道是如何重叠形成化学键的。
1. 下列关于化学键的说法,认识错误的是
键与 键的对称性不同
键不能单独存在,一定要和 键共存
含有 键的化合物与只含 键的化合物的化学性质不同
两个非金属元素的原子之间形成的化学键都是共价键
分子中含有共价键,则一定含有一个 键
成键的原子间已知轨道重叠越多,共价键越牢固
个N原子最多只能与3个H原子结合形成 分子,是由共价键的饱和性决定的
A. B. C. D.
2. 下列分子中,既含有 键,又含有 键的是
A. B. HCl C. D.3. 已知 呈粉红色, 呈蓝色, 为无色。现将 溶于水,加入
浓盐酸后,溶液由粉红色变为蓝色,存在以下平衡:
用该溶液做实验,溶液的颜色变化如图:
以下结论和解释正确的是
A. 等物质的量的 和 中 键数之比为3:2
B. 由实验 可推知
C. 实验 是由于 增大,导致平衡逆向移动
D. 由实验 可知配离子的稳定性:
4. 氰气的分子式为 ,结构式为 ,性质与卤素相似。下列叙述正确的是
A. 分子中原子的最外层均满足8电子结构
B. 分子中 键的键长大于 键的键长
C. 分子中含有2个 键和4个 键
D. 不能和氢氧化钠溶液发生反应
5. 由短周期前10号元素组成的物质T和X,有如图所示的转化。X不稳定,易分解。有关说法
正确的是A. T分子中只含有极性键,X分子中既含有极性键又含有非极性键
B. 等物质的量的T、X分子中含有 键的数目均为
C. X分子中含有的 键个数是T分子中含有的 键个数的2倍
D. 为使该转化成功进行,Y可以是酸性 溶液