文档内容
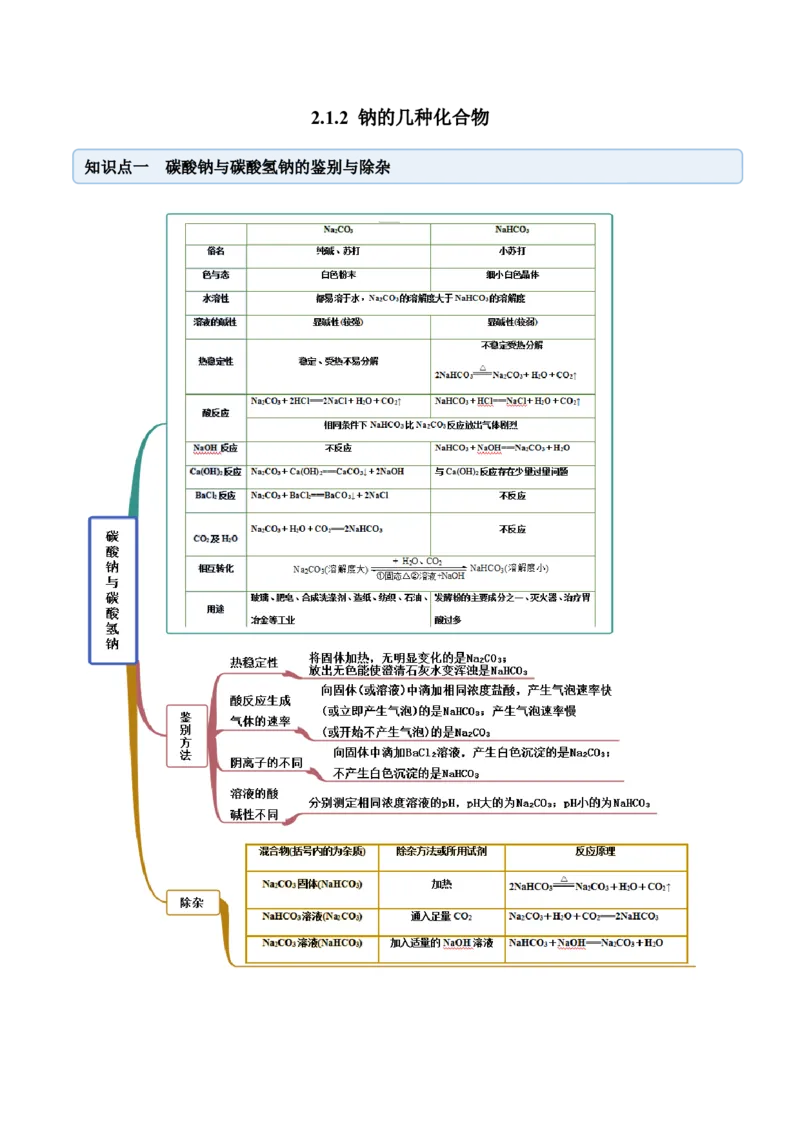
2.1.2 钠的几种化合物
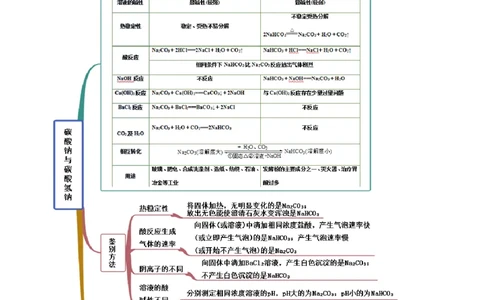
知识点一 碳酸钠与碳酸氢钠的鉴别与除杂【例1】(2020·全国课时练习)某校化学兴趣小组的同学在进行课外调查时得知:制作糕点常用
或 做膨松剂。于是同学们对 和 的性质进行了探究。利用图所示装置进行实验
测定某 和 混合物中 的质量分数(装置气密性良好,各装置中气体吸收剂足
量)。
(实验步骤)
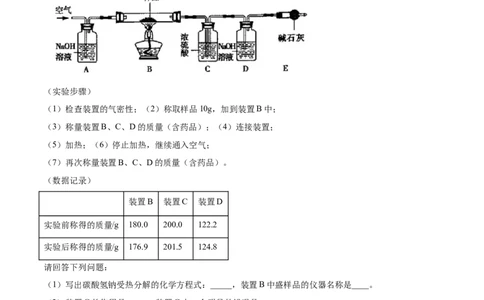
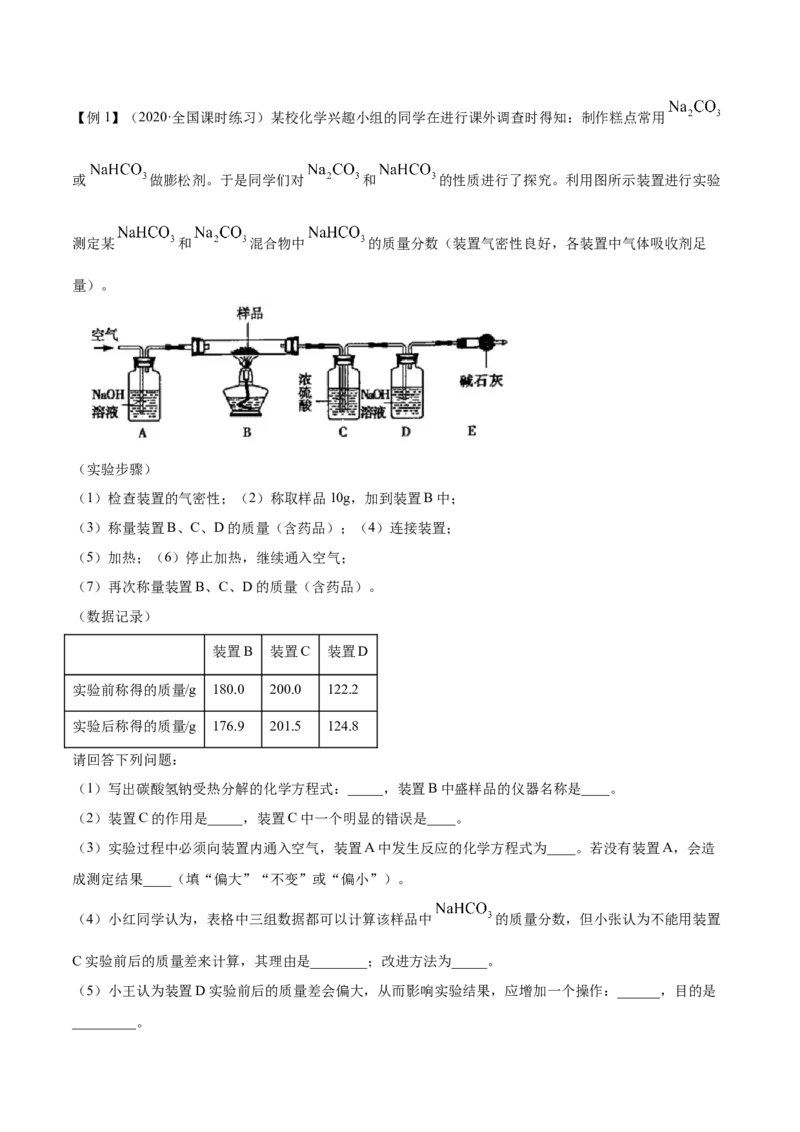
(1)检查装置的气密性;(2)称取样品10g,加到装置B中;
(3)称量装置B、C、D的质量(含药品);(4)连接装置;
(5)加热;(6)停止加热,继续通入空气;
(7)再次称量装置B、C、D的质量(含药品)。
(数据记录)
装置B 装置C 装置D
实验前称得的质量/g 180.0 200.0 122.2
实验后称得的质量/g 176.9 201.5 124.8
请回答下列问题:
(1)写出碳酸氢钠受热分解的化学方程式:_____,装置B中盛样品的仪器名称是____。
(2)装置C的作用是_____,装置C中一个明显的错误是____。
(3)实验过程中必须向装置内通入空气,装置A中发生反应的化学方程式为____。若没有装置A,会造
成测定结果____(填“偏大”“不变”或“偏小”)。
(4)小红同学认为,表格中三组数据都可以计算该样品中 的质量分数,但小张认为不能用装置
C实验前后的质量差来计算,其理由是________;改进方法为_____。
(5)小王认为装置D实验前后的质量差会偏大,从而影响实验结果,应增加一个操作:______,目的是
_________。【答案】(1) 硬质玻璃管
(2)吸收水蒸气 右侧导管伸入液面以下
(3) 偏大
(4)装置A中逸出的水蒸气会进入装置C中 在装置A、B之间增加一个盛有浓硫酸的干燥装置
(5)连接装置D前,缓缓鼓入空气 排尽装置内的二氧化碳气体
【解析】(1)碳酸氢钠受热分解为碳酸钠、水和二氧化碳,化学方程式为:
,根据仪器结构可知,装置B中盛样品的仪器名称为硬质玻璃管;
(2)浓硫酸具有吸水性,可以做干燥剂,除去水蒸气,洗气时应该是长导管进气,短导管出气,所以右侧导
管不能伸入液面以下。
(3)空气经过装置A时,其中的二氧化碳与足量氢氧化钠反应生成碳酸钠和水,反应方程式为
CO+2NaOH=Na CO+H O,若没有此装置,则装置D实验后称得的质量会偏大,测得生成的二氧化碳质量
2 2 3 2
偏大,造成测定结果偏大。
(4)小张认为不能用装置C实验前后的质量差来计算,其理由是装置A中逸出的水蒸气会进入装置C中;改
进方法为在装置A、B之间增加一个盛有浓硫酸的干燥装置。
(5)小王认为装置D实验前后的质量差会偏大,应在连接装置D前缓缓鼓入空气,目的是排尽装置内的二氧
化碳气体。
【一隅三反】
1.(2020·全国高一单元测试)下列实验方案鉴别NaCO 和NaHCO 两种白色粉末,不能达到预期目的的
2 3 3
是( )
A.分别向等量的白色粉末中加等体积、等浓度的稀盐酸,比较生成气体的快慢
B.分别向等量的白色粉末中加等体积适量的水,比较固体溶解量的多少
C.分别将等量的白色粉末配成溶液,然后加入澄清石灰水,比较是否有沉淀生成
D.分别将等量的白色粉末用如图装置进行实验,比较澄清石灰水是否变浑浊【答案】C
【解析】A.分别向等量的白色粉末中加等体积、等物质的量浓度的稀盐酸,碳酸氢钠立即和盐酸反应生
成二氧化碳,碳酸钠和盐酸反应先生成碳酸氢钠,碳酸氢钠再和盐酸反应生成二氧化碳,所以生成二氧化
碳速率不同,能达到实验目的,故A不选;
B.相同温度下,碳酸氢钠的溶解度小于碳酸钠,所以分别向等量的白色粉末中加等体积适量的水,比较
固体溶解量的多少来鉴别,能达到实验目的,故B不选;
C.碳酸氢钠和碳酸钠都和氢氧化钙反应生成白色沉淀,反应现象相同,无法鉴别,所以不能达到实验目
的,故C选;
D.碳酸钠比碳酸氢钠稳定,加热时,碳酸钠不分解,碳酸氢钠分解生成二氧化碳,用澄清石灰水检验是
否生成二氧化碳,所以能达到实验目的,故D不选;
故选C。
2.(2019·全国高一课时练习)某校化学课外小组为了鉴别碳酸钠和碳酸氢钠两种白色固体,做了如图所
示的实验。
(1)图甲、乙所示实验,能够达到实验目的的是__________(填序号)。
(2)图丙、丁所示实验均能鉴别这两种物质,其反应的化学方程式为__________;与丙相比,丁所示实验的
优点是________(填序号)。A.丁比丙复杂
B.丁比丙安全
C.丁可以做到用一套装置同时进行两个实验对比,而丙不行
(3)若用丁所示实验验证碳酸钠和碳酸氢钠的稳定性,则试管B中装入的固体最好是________(填化学式)。
【答案】(1)乙 (2)2NaHCO Na CO+CO ↑+H O C (3) NaHCO
3 2 3 2 2 3
【解析】(1) Na CO、NaHCO 均能与盐酸反应生成使澄清石灰水变浑浊的CO 气体,但等质量的NaCO
2 3 3 2 2 3
与NaHCO 跟过量盐酸反应时,NaHCO 与盐酸反应更剧烈且产生气体的量多,故图甲所示实验不能鉴别
3 3
NaCO 与NaHCO ,而图乙所示实验可以。
2 3 3
(2) NaHCO 受热易分解:2NaHCO Na CO+CO ↑+H O,NaCO 受热不易分解,可用加热方法鉴别。
3 3 2 3 2 2 2 3
与图丙所示实验相比,丁可以同时进行两个实验对比,现象明显。
(3)将NaHCO 置于小试管B中,NaCO 置于大试管A中,加热时碳酸钠直接受热,D中澄清石灰水不变浑
3 2 3
浊,而碳酸氢钠间接受热也能分解,C中澄清石灰水变浑浊,说明NaCO 比NaHCO 稳定。
2 3 3
3.(2020·河北定州一中高一期末)碳酸钠(NaCO)和碳酸氢钠(NaHCO )都可作为食用碱。
2 3 3
(1)用上图装置分别加热上述两种固体,当观察到澄清石灰水变浑浊时,则试管中受热的固体是
_________。通过本实验证明,这两种固体对热的稳定性是NaCO ________于(选填“强”或“弱”)
2 3
NaHCO 。
3
(2)若分别向碳酸钠溶液和碳酸氢钠溶液中滴加足量稀盐酸,都能观察到的现象是__________________,
其中碳酸氢钠和稀盐酸反应的化学方程式为_______________________________。
(3)钠的化合物中,除了碳酸钠和碳酸氢钠外,还有 _________ 、_________ 等。
【答案】(1)碳酸氢钠(NaHCO ) 强
3
(2)产生气泡 NaHCO + HCl =NaCl+ H O + CO ↑
3 2 2
(3) NaNO Na SO
3 2 4
【解析】(1)NaHCO 受热易分解,NaCO 受热不分解,碳酸钠较碳酸氢钠稳定,则观察到澄清石灰水变
3 2 3
浑浊时,则试管中加热的固体是NaHCO ,故答案为NaHCO ;强;
3 3(2)二者均与盐酸反应生成二氧化碳,观察到的现象为有气泡冒出,碳酸氢钠与盐酸反应生成氯化钠、
水、二氧化碳,其化学反应为NaHCO +HCl=NaCl+H O+CO↑,故答案为有气泡冒出;
3 2 2
NaHCO +HCl=NaCl+H O+CO↑;
3 2 2
(3)氧化钠、氯化钠、过氧化钠、硫酸钠等均为常见的钠的化合物,故答案为氧化钠;氯化钠;NaNO ;
3
NaSO (任选2个即可)
2 4
知识点二 碳酸钠、碳酸氢钠与盐酸反应
【例2】(2020·遵义县育新高级中学高一月考)碳酸钠、碳酸氢钠与盐酸反应的比较。(1)按上图要求完成实验:在两支试管中分别加入3 mL稀盐酸,将两个各装有少量等质量的碳酸钠、碳酸
氢钠粉末的小气球套在两支试管的管口。将气球内的碳酸钠和碳酸氢钠同时倒入试管中,观察到的实验现
象是_________。
(2)实验结论是_____________________。
(3)碳酸钠与盐酸反应的化学方程式是____________,离子方程式是_________________。
(4)碳酸氢钠与盐酸反应的化学方程式是____________,离子方程式是__________。
【答案】(1)两个气球均膨胀;碳酸氢钠与盐酸混合比碳酸钠与盐酸混合气体膨胀得快且大
(2)碳酸氢钠与盐酸反应产生气体比碳酸钠与盐酸反应产生气体多且剧烈
(3) Na CO+2HCl===2NaCl+HO+CO↑ CO 2—+2H+=CO ↑+HO
2 3 2 2 3 2 2
(4)NaHCO +HCl===NaCl+HO+CO↑ HCO —+H+===CO ↑+HO
3 2 2 3 2 2
【解析】(1)与相同浓度的盐酸反应时,碳酸氢钠反应速率快,等质量的碳酸钠、碳酸氢钠,碳酸氢钠的物
质的量大于碳酸钠,根据方程式NaCO + 2HCl = 2NaCl + H O + CO ↑、NaHCO + HCl=NaCl+H O+CO↑
2 3 2 2 3 2 2
可知碳酸氢钠放出的二氧化碳多,因此看到的现象为两个气球均膨胀;碳酸氢钠与盐酸混合比碳酸钠与盐
酸混合气体膨胀得快且大,故答案为:两个气球均膨胀;碳酸氢钠与盐酸混合比碳酸钠与盐酸混合气体膨
胀得快且大;
(2)根据(1)的分析,实验结论为碳酸氢钠与盐酸反应产生气体比碳酸钠与盐酸反应产生气体多且剧烈,故答
案为:碳酸氢钠与盐酸反应产生气体比碳酸钠与盐酸反应产生气体多且剧烈;
(3)碳酸钠与盐酸反应的化学方程式为NaCO+2HCl=2NaCl+HO+CO↑,离子方程式为CO2-+2H+
2 3 2 2 3
=CO ↑+HO,故答案为:NaCO+2HCl=2NaCl+HO+CO↑;CO2-+2H+=CO ↑+HO;
2 2 2 3 2 2 3 2 2
(4)碳酸氢钠与盐酸反应的化学方程式为NaHCO +HCl=NaCl+HO+CO↑,离子方程式为HCO -+H+
3 2 2 3
=CO ↑+HO,故答案为:NaHCO +HCl=NaCl+HO+CO↑;HCO -+H+=CO ↑+HO。
2 2 3 2 2 3 2 2
【一隅三反】
1.(2019·武宣县第二中学高一期末)下列反应的离子方程式正确的是( )
A.少量的碳酸氢钠溶液与澄清石灰水混合:2 +2OH-+Ca2+=CaCO ↓+ +2HO
3 2B.过量的碳酸氢钠溶液与澄清石灰水混合: +OH-+Ca2+=CaCO ↓+HO
3 2
C.碳酸氢钠溶液与少量的盐酸溶液混合: +H+=CO ↑+HO
2 2
D.碳酸钠溶液与过量的盐酸溶液混合:NaCO+2H+=2Na++CO↑+HO
2 3 2 2
【答案】C
【解析】A. 少量的碳酸氢钠溶液与澄清石灰水混合离子方程式为HCO -+OH-+Ca2+=CaCO ↓+HO,故
3 3 2
A错误;
B. 澄清石灰水与过量碳酸氢钠溶液,反应生成碳酸钙沉淀、碳酸钠和水,正确的离子方程式为:2HCO -
3
+Ca2++2OH-═CO2-+CaCO ↓+H O,故B错误;
3 3 2
C. 碳酸氢钠溶液与少量的盐酸溶液混合生成二氧化碳和水,离子方程式为HCO -+H+=CO ↑+HO,故C
3 2 2
正确;
D. 碳酸钠为强电解质应写成离子,离子方程式为CO2-+2H+=CO ↑+HO,故D错误;
3 2 2
故答案为C。
2.(2020·镇远县第二初级中学校高一期末)向等量的NaOH溶液中分别通入CO 气体。因CO 的通入量
2 2
不同,得到组分不同的溶液M。若向M中逐滴加入盐酸,产生的气体体积V(CO )与加入盐酸的体积
2
V(HCl)关系如图,(注:①假设CO 全部逸出;②图中Oaab)。其中M中
2
只有1种溶质的是( )
A.只有① B.只有③ C.②④ D.①③
【答案】D
【解析】加入盐酸可能发生的反应为NaOH+HCl=NaCl+H O,NaCO+HCl=NaCl+NaHCO ,
2 2 3 3
NaHCO +HCl=NaCl+CO +H O,由方程式可知碳酸钠转化为碳酸氢钠消耗盐酸与该碳酸氢钠反应消耗盐酸
3 2 2
体积相等;图①中加入盐酸即有CO 生成,说明溶质只有一种为NaHCO ;图②中Oa<ab,说明溶液M中
2 3
含有NaCO 和NaHCO 两种溶质;图③中Oa=ab,说明溶质只有NaCO;图④中Oa>ab,说明溶液M中
2 3 3 2 3
含有NaOH和NaCO 两种溶质;所以①③符合,答案选D。
2 3
3.(2019·邵东县第一中学高一月考)向四瓶盛有相同物质的量的NaOH溶液中通入体积不同的CO 气体,
2
得到①②③④四瓶溶液。分别向四瓶溶液中逐滴加入等体积、等浓度的盐酸,产生的气体体积V(CO )与所
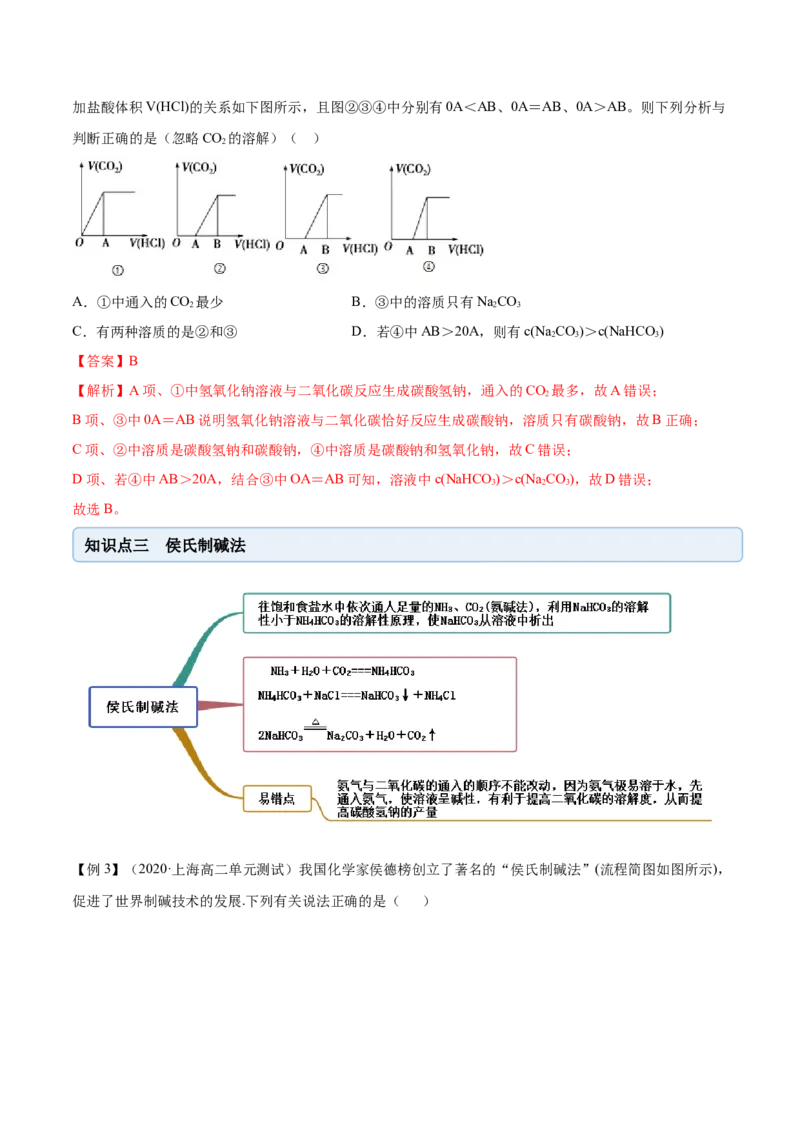
2加盐酸体积V(HCl)的关系如下图所示,且图②③④中分别有0A<AB、0A=AB、0A>AB。则下列分析与
判断正确的是(忽略CO 的溶解)( )
2
A.①中通入的CO 最少 B.③中的溶质只有NaCO
2 2 3
C.有两种溶质的是②和③ D.若④中AB>20A,则有c(Na CO)>c(NaHCO )
2 3 3
【答案】B
【解析】A项、①中氢氧化钠溶液与二氧化碳反应生成碳酸氢钠,通入的CO 最多,故A错误;
2
B项、③中0A=AB说明氢氧化钠溶液与二氧化碳恰好反应生成碳酸钠,溶质只有碳酸钠,故B正确;
C项、②中溶质是碳酸氢钠和碳酸钠,④中溶质是碳酸钠和氢氧化钠,故C错误;
D项、若④中AB>20A,结合③中OA=AB可知,溶液中c(NaHCO )>c(Na CO),故D错误;
3 2 3
故选B。
知识点三 侯氏制碱法
【例3】(2020·上海高二单元测试)我国化学家侯德榜创立了著名的“侯氏制碱法”(流程简图如图所示),
促进了世界制碱技术的发展.下列有关说法正确的是( )A.沉淀池中的反应物共含有五种元素
B.过滤得到的“母液”中一定只含有两种溶质
C.图中X可能是氨气
D.通入氨气的作用是使溶液呈碱性,促进二氧化碳的吸收,更多地析出沉淀
【答案】D
【解析】A.沉淀池中发生的反应的反应物是氯化钠、氨气、二氧化碳和水,所以含有钠、氯、氮、氢、
碳、氧六种元素,故A错误;
B.过滤得到的“母液”中含有的溶质有碳酸氢钠、氯化铵,还有可能含有过量的氯化钠,故B错误;
C.碳酸氢钠分解生成碳酸钠、水、二氧化碳,所以X是二氧化碳,故C错误;
D.氨气的水溶液显碱性,能更好的吸收二氧化碳,使反应物浓度大,反应速度快,故D正确;
故答案为D。
氨碱法:以食盐(氯化钠)、石灰石(经煅烧生成生石灰和二氧化碳)、氨气为原料来制取纯碱.先使氨
气通入饱和食盐水中而成氨盐水,再通入二氧化碳生成溶解度较小的碳酸氢钠沉淀和氯化铵溶液;化学反
应原理为:NH +CO+H O+NaCl(饱和)=NaHCO ↓+NHCl,将经过过滤、洗涤得到NaHCO 微小晶体,
3 2 2 3 4 3
再加热煅烧制得纯碱产品:2NaHCO =Na CO +CO↑+H O,放出的二氧化碳气体可回收循环使用,含有氯
3 2 3 2 2
化铵的滤液与石灰乳(Ca(OH))混合加热,所放出的氨气可回收循环使用,CaO+H O=Ca(OH),
2 2 2
2NH Cl+Ca(OH)=CaCl +2NH↑+2H O;
4 2 2 3 2
联合制碱法:以食盐、氨和二氧化碳(其中二氧化碳来自合成氨厂用水煤气制取氢气时的废气)为原料来
制取纯碱,联合制碱法包括两个过程:第一个过程与氨碱法相同,将氨通入饱和食盐水而成氨盐水,再通
入二氧化碳生成碳酸氢钠沉淀,经过滤、洗涤得NaHCO 微小晶体,再煅烧制得纯碱产品,其滤液是含有
3
氯化铵和氯化钠的溶液;第二个过程是从含有氯化铵和氯化钠的滤液中结晶沉淀出氯化铵晶体,由于氯化
铵在常温下的溶解度比氯化钠要大,低温时的溶解度则比氯化钠小,而且氯化铵在氯化钠的浓溶液里的溶
解度要比在水里的溶解度小得多,所以在低温条件下,向滤液中加入细粉状的氯化钠,并通入氨气,可以
使氯化铵单独结晶沉淀析出,经过滤、洗涤和干燥即得氯化铵产品,此时滤出氯化铵沉淀后所得的滤液,
已基本上被氯化钠饱和,可回收循环使用。【一隅三反】
1.(2020·陕西榆阳·榆林十二中月考)如图是模拟“侯氏制碱法”制取NaHCO 的部分装置。下列操作正
3
确的是( )
A.a通入CO,然后b通入NH ,c中放碱石灰
2 3
B.b通入NH ,然后a通入CO,c中放碱石灰
3 2
C.a通入NH ,然后b通入CO,c中放蘸稀硫酸的脱脂棉
3 2
D.b通入CO,然后a通入NH ,c中放蘸稀硫酸的脱脂棉
2 3
【答案】C
【解析】由于CO 在水中的溶解度比较小,而NH 极易溶于水,所以在实验中要先通入溶解度较大的
2 3
NH ,再通入CO;由于NH 极易溶于水,在溶于水时极易发生倒吸现象,所以通入NH 的导气管的末端
3 2 3 3
不能伸入到溶液中,即a先通入NH ,然后b通入CO,A、B、D选项均错误;因为NH 是碱性气体,所
3 2 3
以过量的NH 要用稀硫酸来吸收,选项C合理;故合理答案是C。
3
2.(2020·上海浦东新·高三二模)纯碱是一种重要的化工原料,对于“氨碱法”和“联合制碱法”的分析
中,错误的是( )
A.主反应的原理相同 B.二氧化碳来源不同
C.都有氨的循环利用 D.都具有一定局限性
【答案】C
【解析】①氨碱法:以食盐(氯化钠)、石灰石(经煅烧生成生石灰和二氧化碳)、氨气为原料来制取纯碱,向
饱和食盐水中先通入氨气,再通入二氧化碳气体NH +CO +H O+NaCl(饱和)=NaHCO ↓+NHCl、2NaHCO
3 2 2 3 4 3
NaCO+CO ↑+H O,得到碳酸钠,然后在氯化铵溶液中加入氧化钙回收氨气;②联合制碱法:以食盐、
2 3 2 2
氨和二氧化碳(其中二氧化碳来自合成氨厂用水煤气制取氢气时的废气)为原料来制取纯碱,原理为:
NH +CO +H O+NaCl(饱和)=NaHCO ↓+NHCl、2NaHCO NaCO+CO ↑+H O,在氯化铵溶液中加入氯
3 2 2 3 4 3 2 3 2 2
化钠,使氯化铵析出,得到碳酸钠和氯化铵两种主要产品。
A.两种方法的主反应的原理相同,均为NH +CO +H O+NaCl(饱和)=NaHCO ↓+NHCl、2NaHCO
3 2 2 3 4 3
NaCO+CO ↑+H O,故A正确;
2 3 2 2
B.氨碱法中的二氧化碳来自于生石灰的煅烧,联合制碱法中中的二氧化碳来自于合成氨厂制取氢气时的废气,二氧化碳来源不同,故B正确;
C.氨碱法中有氨的循环利用,“联合制碱法”得到的产品为碳酸钠和氯化铵,循环利用的物质是NaCl和
CO,故C错误;
2
D.氨碱法的原料食盐的利用率只有72%~74%,其余的食盐都随着氯化钙溶液作为废液被抛弃了。较氨
碱法而言,联合制碱法中用氨量较大,在有些情况下不适用,产品的纯度略低于索尔维法即氨碱法,二者
都具有一定局限性,故D正确;
故选C。
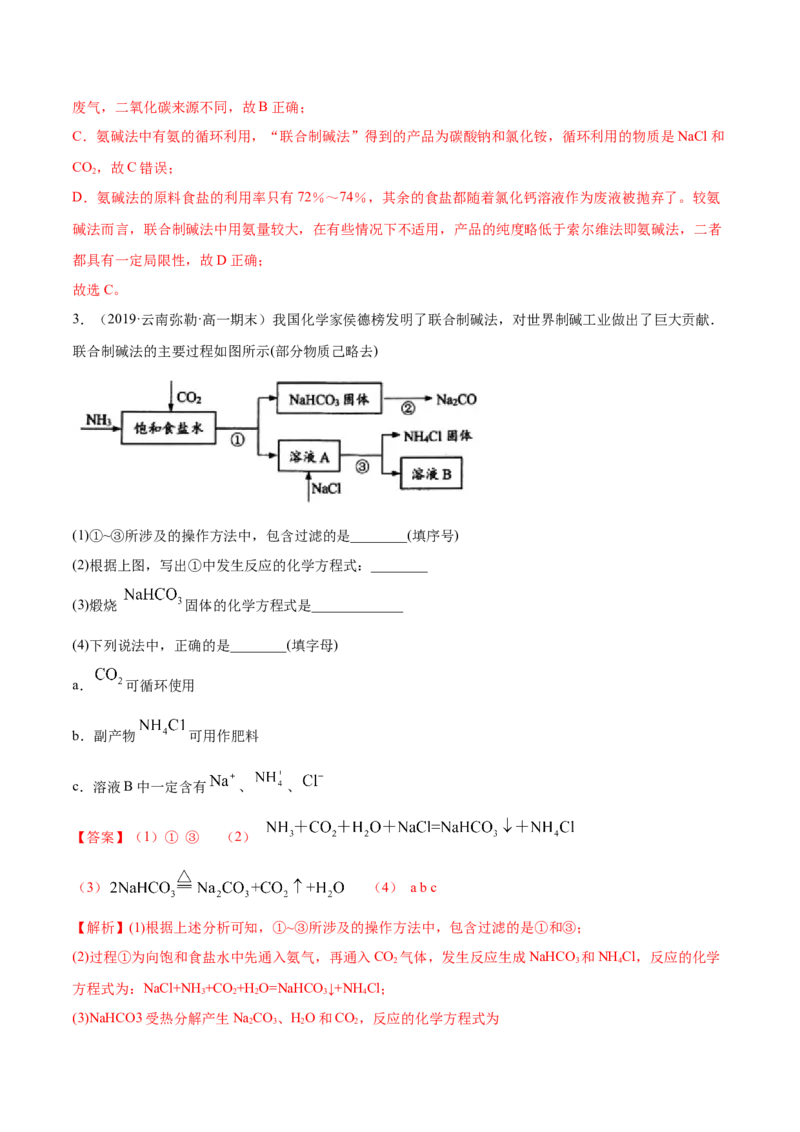
3.(2019·云南弥勒·高一期末)我国化学家侯德榜发明了联合制碱法,对世界制碱工业做出了巨大贡献.
联合制碱法的主要过程如图所示(部分物质己略去)
(1)①~③所涉及的操作方法中,包含过滤的是________(填序号)
(2)根据上图,写出①中发生反应的化学方程式:________
(3)煅烧 固体的化学方程式是_____________
(4)下列说法中,正确的是________(填字母)
a. 可循环使用
b.副产物 可用作肥料
c.溶液B中一定含有 、 、
【答案】(1)① ③ (2)
(3) (4) a b c
【解析】(1)根据上述分析可知,①~③所涉及的操作方法中,包含过滤的是①和③;
(2)过程①为向饱和食盐水中先通入氨气,再通入CO 气体,发生反应生成NaHCO 和NH Cl,反应的化学
2 3 4
方程式为:NaCl+NH +CO +H O=NaHCO ↓+NHCl;
3 2 2 3 4
(3)NaHCO3受热分解产生NaCO、HO和CO,反应的化学方程式为
2 3 2 2;
(4)a.开始通入二氧化碳反应,最后碳酸氢钠受热分解生成的CO 可循环使用,a正确;
2
b.副产物NH Cl是氮肥,可用作植物生长所需的肥料,b正确;
4
c.溶液B中主要是氯化钠、氯化铵饱和溶液,一定含有Na+、 、Cl-,c正确;故合理选项是abc。
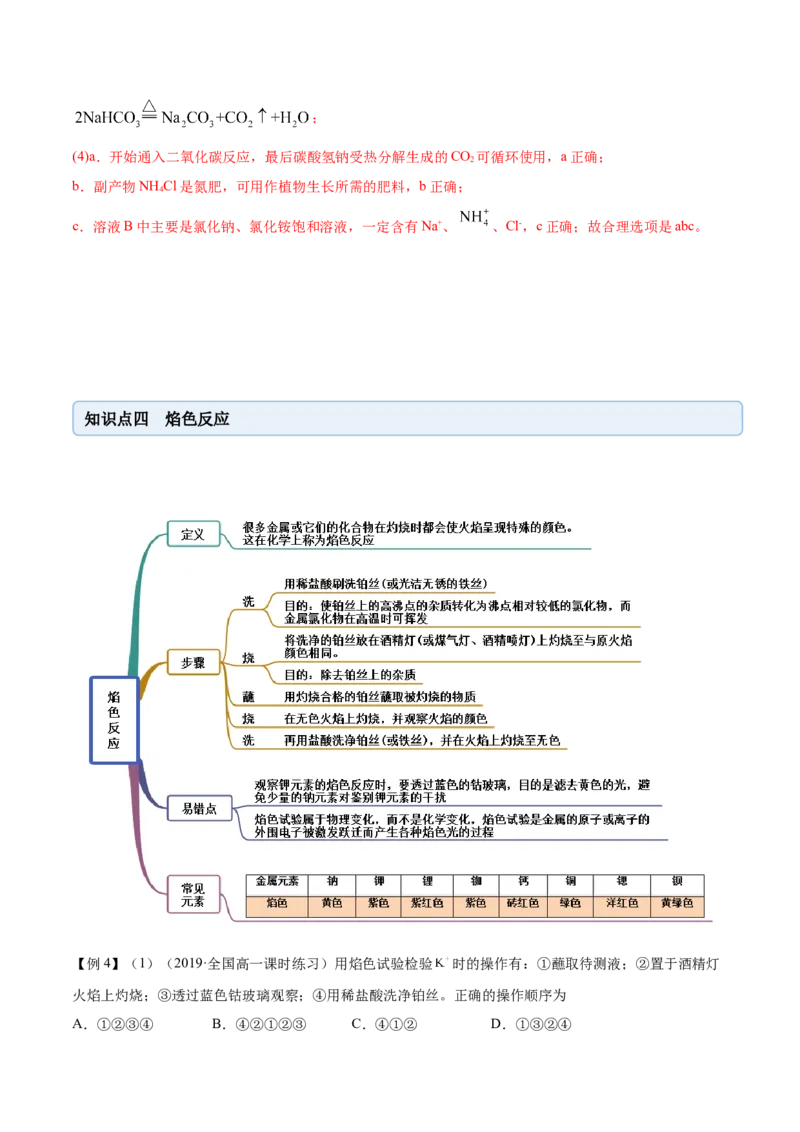
知识点四 焰色反应
【例4】(1)(2019·全国高一课时练习)用焰色试验检验 时的操作有:①蘸取待测液;②置于酒精灯
火焰上灼烧;③透过蓝色钴玻璃观察;④用稀盐酸洗净铂丝。正确的操作顺序为
A.①②③④ B.④②①②③ C.④①② D.①③②④(2)(2020·全国高一课时练习)焰色反应实验过程中铂丝的清洗和灼烧与钾焰色反应的观察两项操作如
图所示:
下列叙述中不正确的是
A.每次实验中都要先将铂丝灼烧到火焰无色,再蘸取被检验物质
B.钾的焰色反应要透过蓝色钴玻璃观察
C.实验时最好选择本身颜色较深的火焰
D.没有铂丝可用无锈铁丝代替进行实验
【答案】(1)B(2)C
【解析】(1)根据焰色试验的操作步骤:洗、烧、蘸、烧、观,所以正确的操作顺序为:用稀盐酸洗净
铂丝,置于酒精灯火焰上灼烧,蘸取待测液,置于酒精灯火焰上灼烧,过蓝色钴玻璃观察,故选B。
(2)A.取一根的铂丝,用盐酸洗净后,放在酒精灯上灼烧至无色,再蘸取被检验物质,进行焰色反应,
故A正确;
B.在观测钾的焰色反应时要透过蓝色钴玻璃片,滤去钠的黄光的干扰,故B正确;
C.为了能够更加突出被检验试剂的颜色,选用本身颜色较浅的火焰,最大限度的减少火焰本身颜色的干
扰,故C错误;
D.洁净的细铁丝,放在酒精灯上灼烧至无色,本身无颜色,故可用铁丝进行焰色反应,故D正确;
故选C。
【一隅三反】
1.(2020·全国课时练习)下列关于KCO 焰色试验的操作不正确的是( )
2 3
A.用稀盐酸冲洗铂丝
B.把稀盐酸冲洗过的铂丝在酒精灯火焰上灼烧至无色
C.用红热的铂丝蘸取KCO 固体,在火焰上灼烧
2 3
D.直接观察KCO 的焰色是否呈浅紫色
2 3
【答案】D
【解析】A.焰色反应第一步,用稀盐酸冲洗铂丝,A正确;
B.焰色反应第二步,把稀盐酸冲洗过的铂丝在酒精灯火焰上灼烧至无色,B正确;
C.用红热的铂丝蘸取KCO 固体,在火焰上灼烧,C正确;
2 3D.观察K的焰色时,应透过蓝色钴玻璃,以滤去黄光,排除Na的干扰,D错误;答案选D。
2.(2020·全国高一课时练习)下列关于焰色反应的说法不正确的是
A.金属单质无焰色反应
B.很多金属或它们的化合物灼烧时有焰色反应
C.透过蓝色钴玻璃观察钾元素焰色反应的颜色为紫色
D.每次焰色反应实验后都要将铂丝用稀盐酸洗净并灼烧
【答案】A
【解析】很多金属或它们的化合物在灼烧时都会使火焰呈现特殊的颜色,这在化学上叫做焰色反应;
A.根据定义可知,无论某金属元素的单质还是化合物在灼烧时都呈现相同的特殊颜色,体现的是元素的性
质,故A错误;
B.根据定义可知,某些金属或它们的化合物灼烧时有焰色反应,故B正确;
C.钾元素的焰色反应的颜色为紫色,但要透过蓝色钴玻璃滤去火焰的黄光才能观察到,故C正确;
D.铂丝要用盐酸来洗涤,更容易将铂丝上的物质洗去,且盐酸易挥发不会干扰实验,故D正确;
综上所述,本题选A。
3.(2020·全国高一课时练习)人们利用焰色反应制造了绚丽多彩的烟花,下列物质的焰色为黄色的是
A.NaCO B.KCl C.CaCl D.CuSO
2 3 2 4
【答案】A
【解析】A.含有钠元素的物质的焰色反应为黄色,A正确;
B.含有钾元素的物质的焰色反应为紫色(透过蓝色钴玻璃),B错误;
C.含有钙元素的物质的焰色反应为砖红色,C错误;
D.含有铜元素的物质的焰色反应为绿色,D错误;答案选A。