文档内容
第一节 化学反应速率
一、化学反应速率
(一)定义:通常用单位时间内反应物浓度的减少或生成物浓度的增加来表示
(二)表示方法: Δc:反应物浓度或生成物浓度的变化,常用单位:mol/L
(或mol•L-1)
Δt:反应时间的变化,常用单位:s或min
v : 化 学 反 应 速 率 , 常 用 单 位 : mol/(L• s) 或
(mol•L-1•s-1)、
mol/(L• min) 或
(mol•L-1•min -1)
(三)意义:衡量化学反应进行快慢的物理量
(四)注意事项:
1、同一反应,用不同物质表示的反应速率其数值可能不同,但表示的意义相同,即表示整
个化学反应的快慢,故表、示一个化学反应的反应速率时,必须指明是用哪种物质来表
示
2、化学反应速率没有负值,均取正值
3、化学反应速率是一段时间内的平均反应速率,而不是某一时刻的瞬时反应速率
4、反应方程式中各物质的化学计量数之比等于各物质的化学反应速率之比,等于变化的浓
度 之 比 , 等 于 变 化 的 物 质 的 量 之 比 。 例 如 : aA+bB=cC+dD
a:b:c:d=v :v :v :v =Δc :Δc :Δc :Δc =Δn :Δn :Δn :Δn
A B C D A B C D A B C D
5、固体或纯液体(不是溶液),其浓度可视为常数,因此一般不用固体或纯液体表示反应
速率
(五)比较大小:
1、比较大小时,要先转化为同一物质的化学反应速率,再进行比较,同时要注意时间单位
的转化
2、比较大小时,可以比较速率与计量数的比值。例如:比较 aA+bB=cC+dD中A与B
的速率大小,可比较与 的大小,若 > ,则A的速率大于B的速率
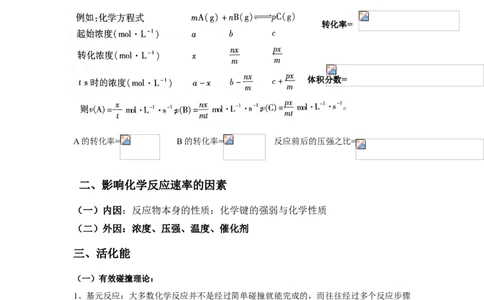
(六)计算——“三段式”
1、写出有关反应的化学方程式
2、设未知数,列出各物质的起始量、转化量、某时刻(或平衡)量
3、根据已知条件得出各物质的转化浓度(Δc)
4、根据速率的计算公式计算反应速率
转化率=
体积分数=
A的转化率= B的转化率= 反应前后的压强之比=
二、影响化学反应速率的因素
(一)内因:反应物本身的性质:化学键的强弱与化学性质
(二)外因:浓度、压强、温度、催化剂
三、活化能
(一)有效碰撞理论:
1、基元反应:大多数化学反应并不是经过简单碰撞就能完成的,而往往经过多个反应步骤
才能实现,这其中的每一步反应都称为基元反应。基元反应反应了反应历程,反应历程
又称反应机理。
2、基元反应发生的先决条件:反应物的分子必须发生碰撞
3、有效碰撞:
(1)定义:能够发生化学反应的碰撞叫做有效碰撞。
(2)条件:第一,分子必须具有一定的能量,即活化分子(能够发生有
效碰撞的分子)第二,有合适的取向
4、活化能:活化分子具有的平均能量与反应物分子具有的平均能量之差,叫做反应的
活化能
5、有效碰撞理论与化学反应的关系:普通分子 活化分子 有效碰撞→
新物质+能量
(二)浓度:
1、影响规律:其他条件相同时,增大反应物浓度,化学反应速率增大;减小反应物浓度,
反应速率减小
2、理论解释:单位体积内活化分子的数目与反应物分子的总数成正比,即与反应物的浓度
成正比。当其他条件相同时,反应物浓度增大,单位体积内活化分子的数目
增多,单位时间内有效碰撞的次数增多,化学反应速率增大
注:(1)改变固体或纯液体的量,对化学反应速率无影响
(2)增加固体接触面积(将固体研碎)或加快液体扩散速率(对反应物进行搅拌),
均可以提高化学反应速率
(三)压强:
1、影响规律:对于有气体参加的反应,其他条件相同时,压强越大,化学反应速率越快
(1)恒温恒容时,①充入反应物气体→浓度增大→速率增大
I ②充入“惰性气体”→总的压强增大,但各气体分压不变,即浓
度不变→速率不变
(2)恒温恒压时,充入惰性气体→体积增大→浓度减小→速率减慢
注:压强的改变实际上是体积的改变引起浓度的改变,从而对化学反应速率产生影响,如
果压强的改变不能引起浓度变化,则不会对速率产生影响
2、理论解释:增大压强,单位体积内活化分子的数目增多,单位时间内有效碰撞的次数增
多,化学反应速率增大
(四)温度:
1、影响规律:在其他条件不变时,升高温度,化学反应速率越快;温度每升高 10℃,化学
反应速率增大到原来的2-4倍。
2、理论解释:在其他条件不变时,升高温度,反应物分子的能量增加,使一部分原来能量
较低的分子变成活化分子,从而增大了反应物分子中活化分子的百分数,使
得单位时间内有效碰撞次数增多,因而使反应速率加快。(五)催化剂:
1、影响规律:一般是加快反应速率。使用时要注意温度及防止催化剂中毒
2、理论解释:在其他条件不变时,使用催化剂,改变了反应的历程,使发生的每一次反应
所需的活化能降低,这就使更多的反应物分子成为活化分子,增大了单位体
积内反应物分子中活化分子的数目,化学反应速率加快
特点:(1)催化剂在化学变化中能改变化学反应速率,但不能改变反应物的转化率,也
不能使本来不发生的反应发生
(2)催化剂本身在反应前后自身的组成、化学性质和质量不变,但物理性质可以发
生改变
(3)催化剂对一个反应由催化作用,对另一个反应不一定由催化作用,即催化剂具
有专一性,没有万能催化剂
(4)催化剂分正催化剂和负催化剂。正催化剂能加快化学反应速率,负催化剂能减
慢化学反应速率。若无特别说明,催化剂是指正催化剂
小结:浓度、压强、温度、催化剂的改变影响单位体积内的活化分子数,温度和催化剂的
改变也同时影响活化分子的
百分数
(六)其他因素:光辐射、放射线辐照、超声波、电弧、强磁场、高速研磨等。总之,
向反应体系输入能量,都有
可能影响化学反应速率