文档内容
2.1化学反应速率(分层作业)
1.下列判断正确的是
A.0.1 mol·L-1的硫酸和0.1 mol·L-1的盐酸分别与0.2 mol·L-1 的NaOH溶液反应的速率相同
B.0.1 mol·L-1的盐酸和0.1 mol·L-1的硝酸分别与大小相同的大理石反应的速率相同
C.Mg和Fe分别与0.1 mol·L-1的硫酸反应的速率相同
D.大理石块与大理石粉分别与0.1 mol·L-1的盐酸反应的速率相同
2.下列说法不正确的是
A.反应 在低温下能自发进行,则该反应的ΔH﹥0
B.对于2A(g)+B(g) 2C(g) ΔH﹥0,当温度升高时,平衡向正反应方向移动,v 和v 均增大
正 逆
C.对于2A(g)+B(g) 2C(g) ΔH﹥0,增大C的浓度,平衡向逆反应方向移动,v 和v 均增大
正 逆
D.升高温度或加入催化剂能使单位体积内活化分子的百分数增大,但原因不同
3.为应对日益加剧的温室效应,“碳中和”是当前工业生产必须考虑的问题,以 为原料进行生产是一个
重要途径,反应原理: 。下列措施能加快该
反应速率的是
A.使用合适的催化剂 B.恒温恒容下充入He
C.及时移出产物甲醇 D.降低温度
4.反应4A(s)+3B(g)= 2C(g)+D(g),经2 min,B的浓度减少0.6 mol·L-1对此反应速率的表示正确的是
A.用A表示的反应速率是0.4 mol·L-1·min-1
B.分别用B、C、D表示的反应速率之比是3∶2∶1
C.在2 min末的反应速率,用B表示是0.3 mol·L-1·min-1
D.在2 min内的反应速率,用C表示是0.3 mol·L-1·min-1
5.化学在生活中的应用随处可见。下列有关化学反应速率的描述正确的是
A.将食物存放在冰箱中,可降低食物腐败速率
B.冶炼铁时将铁矿石粉碎可增大浓度,加快反应速率
C.食品抽真空包装是为了减小包装袋内压强,减缓食物变质速率
D.烘培糕点使用小苏打作催化剂,加快烘焙速率
6.把下列四种 溶液分别加入四只均盛有20mL3mol/L稀硫酸的烧杯中(稀硫酸的初始温度相同),然后均加入蒸馏水稀释到60mL,溶液中最先出现浑浊的是
A.20℃,10mL,5mol/L的 溶液
B.20℃,20mL,3mol/L的 溶液
C.30℃,10mL,4mol/L的 溶液
D.30℃,30mL,2mol/L的 溶液
7.下列说法正确的是
A.亚硝酸钠是一种防腐剂和护色剂,不可用于肉制品的生产
B.能够发生化学反应的碰撞叫做有效碰撞
C.常温下,实验室制氢气(锌与稀硫酸反应)时,若用98.6%的浓硫酸代替稀硫酸进行反应,则可加快氢气
的生成速率
D.氧化还原反应一定为吸热反应
8.某化学小组利用传感器、数据采集器和计算机等设备,探究外界条件对化学反应速率和限度的影响。回答
下列问题:
(1)在某温度下,探究影响 分解的因素的实验方案如下:
实验序号 实验方案
I 25℃,10mL5% 溶液
Ⅱ 50℃,10mL5% 溶液
Ⅲ 25℃,10mL30% 溶液
Ⅳ 25℃,少量 ,10mL5% 溶液
①实验I、Ⅱ探究目的是 ;实验I、Ⅲ相比反应速率大的是 。
②实验I、Ⅳ得出的结论是 。
(2)为进一步研究催化剂对 分解反应速率的影响,化学小组同学又做了下列实验:①定性研究:小组同学用图1装置进行实验,在注射器中分别加入相同体积的1mol/L 溶液和1mol/L
溶液,可通过观察 ,定性确定反应速率的大小。
②定量研究:为了更精确地研究催化剂对反应速率的影响,小组同学利用图2装置进行定量实验,向大试管中
加入10mL2mol/L的 溶液,向注射器中分别加入1mL1mol/L 溶液和1mL1mol/L 溶液,测定的
数据是 ,比较催化剂对反应速率的影响。
9.下列说法中正确的是
A.增加水的量,可以加快镁与水反应的反应速率
B.增大硫酸的浓度,一定可以加快锌与硫酸反应制取氢气的速率
C.在反应2H++SO =S↓+SO ↑+HO中,增大压强,可以加快硫析出的速率
2 2 2
D.煅烧硫铁矿时,把硫铁矿粉碎或通入纯O 可加快反应的速率
2
10.依据图示判断,下列说法不正确的是
A.图甲中曲线Ⅱ可以表示催化剂降低了反应的活化能
B.图乙中HI分子发生了有效碰撞
C.盐酸和氢氧化钠溶液的反应活化能很小
D.图甲所示反应:ΔH<0
11.将4molA气体和2molB气体在2L的容器中混合并在一定条件下发生如下反应:2A(g)+B(g)⇌2C(g)。若经
2s后测得C的浓度为0.6mol·L-1,现有下列几种说法:①用物质A表示的反应平均速率为0.6mol·L-1·s-1
②用物质B表示的反应的平均速率为0.15mol·L-1·s-1
③2s时物质A的浓度为1.4mol·L-1
④2s时物质B的浓度为0.3mol·L-1
其中正确的是
A.①③ B.①④ C.②③ D.③④
12.下列关于化学反应速率的说法错误的是
A.恒容时, ,向密闭容器内充入He,化学反应速率不变
B.锌与稀硫酸反应时,加入氯化钠溶液,化学反应速率减小
C.制氯气时,增加二氧化锰的用量,能加快反应速率,浓盐酸被完全消耗
D.恒容时,2NO(g)+O
2
(g)≜2NO2(g),升高温度,正逆反应速率都增大
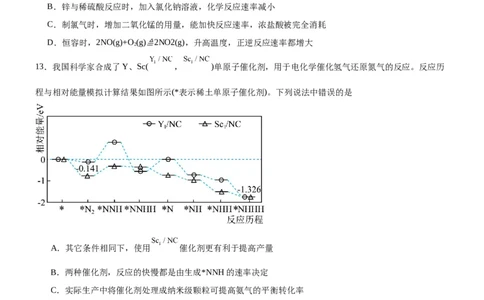
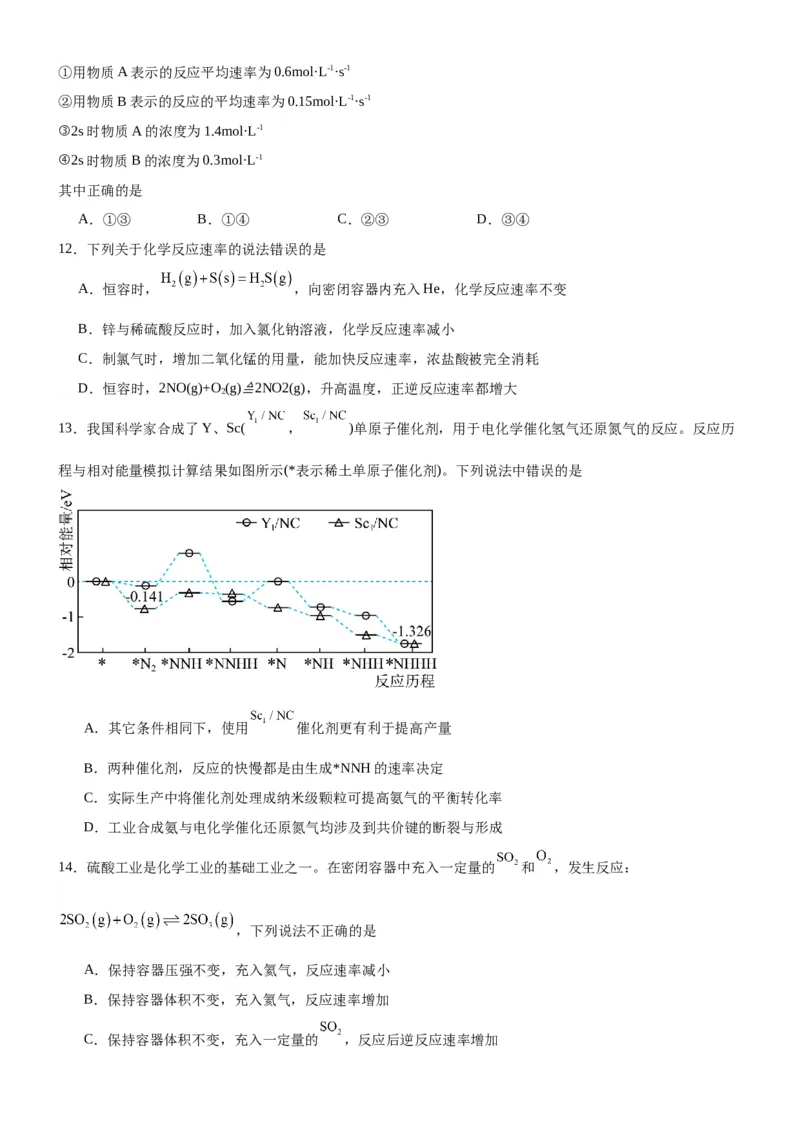
13.我国科学家合成了Y、Sc( , )单原子催化剂,用于电化学催化氢气还原氮气的反应。反应历
程与相对能量模拟计算结果如图所示(*表示稀土单原子催化剂)。下列说法中错误的是
A.其它条件相同下,使用 催化剂更有利于提高产量
B.两种催化剂,反应的快慢都是由生成*NNH的速率决定
C.实际生产中将催化剂处理成纳米级颗粒可提高氨气的平衡转化率
D.工业合成氨与电化学催化还原氮气均涉及到共价键的断裂与形成
14.硫酸工业是化学工业的基础工业之一。在密闭容器中充入一定量的 和 ,发生反应:
,下列说法不正确的是
A.保持容器压强不变,充入氦气,反应速率减小
B.保持容器体积不变,充入氦气,反应速率增加
C.保持容器体积不变,充入一定量的 ,反应后逆反应速率增加D.升高温度,反应的正逆速率均增加
15.“科学态度”是科学研究的基本要求,“社会责任”是化学人人生观和价值观的基本体现,“科学态度与
社会责任”是化学的核心素养。
Ⅰ.Fenton法常用于处理含难降解有机物的工业废水,在加入Fe2+并调好pH后再加入HO,所产生的羟基自
2 2
由基(·OH)能氧化降解污染物。现运用该法降解某有机污染物(p-CP),探究有关因素对该降解反应速率的影响。
实验数据:(表中时间,是p-CP浓度降低1.50mol/L所需时间)
实 蒸馏
HO 溶液 Fe2+溶液 温度 时间
验 2 2 水
pH
编
号 cmol·L-1 V/mL cmol·L-1 V/mL V/mL T/K t/s
① 6.0×10-3 1.50 3.0×10-2 3.50 10.00 3 298 200
② 6.0×10-3 1.50 3.0×10-2 3.50 10.00 3 313 60
③ 6.0×10-3 3.50 3.0×10-2 3.50 V 3 298 140
1
④ 6.0×10-3 1.50 3.0×10-2 4.50 9.00 3 298 170
⑤ 6.0×10-3 1.50 3.0×10-2 3.50 V 12 298 0
2
请回答:
(1)V mL,V mL。
1 2
(2)实验①条件下,p-CP的降解速率为: 。
(3)设置实验①②的目的是: 。设置实验①③的目的是: 。由实验①④
可得到的结论是: 。
(4)实验⑤在200s时没有检测到p-CP浓度的变化。其原因可能是: 。
Ⅱ.
(5)在NO催化下,丙烷与氧气反应制备丙烯的部分反应机理如图所示。下列说法错误的是 。
A.如图所示反应机理中共有4种自由基
B.由NO生成HONO的反应历程有2种
C.改变NO的浓度,总反应的反应热不变
D.当主要发生包含②的历程时,最终生成的水减少
E.含N分子参与的反应一定有电子转移
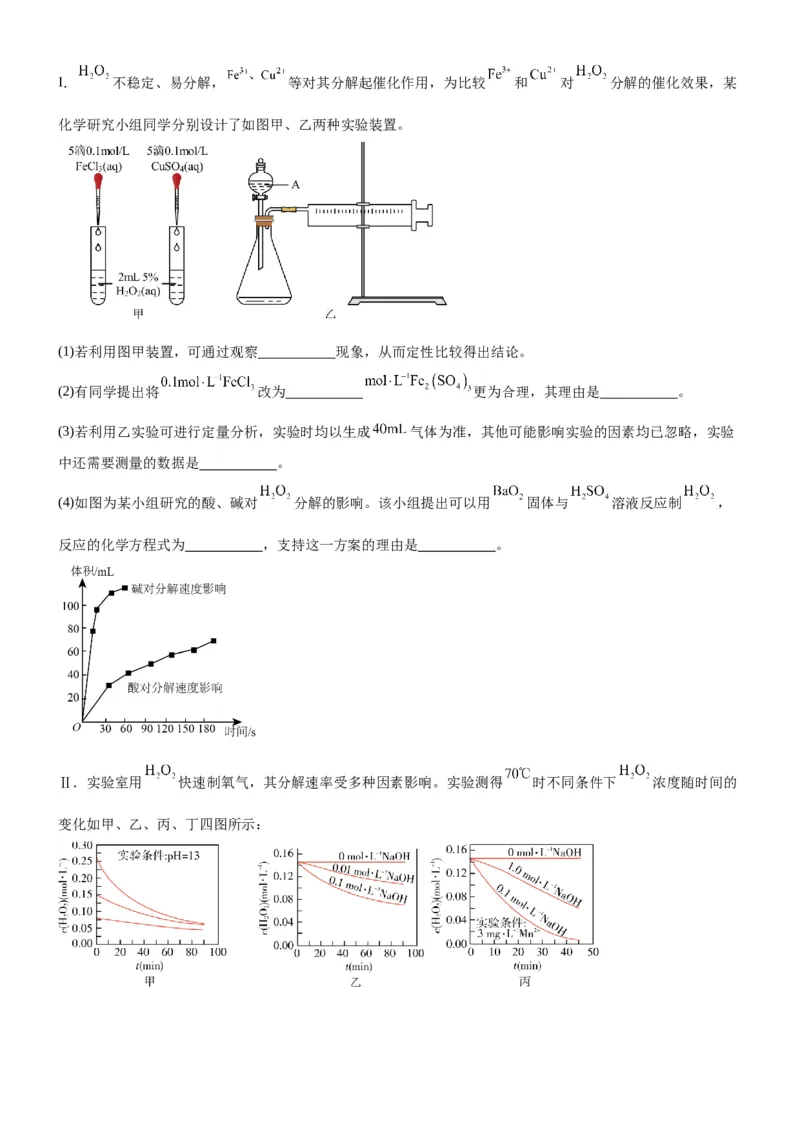
16. 是一种常见试剂,在实验室、工业生产上有广泛用途。I. 不稳定、易分解, 等对其分解起催化作用,为比较 和 对 分解的催化效果,某
化学研究小组同学分别设计了如图甲、乙两种实验装置。
(1)若利用图甲装置,可通过观察 现象,从而定性比较得出结论。
(2)有同学提出将 改为 更为合理,其理由是 。
(3)若利用乙实验可进行定量分析,实验时均以生成 气体为准,其他可能影响实验的因素均已忽略,实验
中还需要测量的数据是 。
(4)如图为某小组研究的酸、碱对 分解的影响。该小组提出可以用 固体与 溶液反应制 ,
反应的化学方程式为 ,支持这一方案的理由是 。
Ⅱ.实验室用 快速制氧气,其分解速率受多种因素影响。实验测得 时不同条件下 浓度随时间的
变化如甲、乙、丙、丁四图所示:(5)下列说法正确的是:___________(填字母序号)
A.图甲表明,其他条件相同时, 浓度越小,其分解越慢
B.图乙表明,其他条件相同时,溶液碱性越弱, 分解越快
C.图丙表明,少量 存在时,溶液碱性越强, 分解越快
D.图丁表明,碱性溶液中, 浓度越大,对 分解速率的影响越大
(6)催化剂 在反应中,改变了 (填字母序号)