文档内容
《分子的空间结构》第一课时 教学设计
课题 《分分子的空间 单元 2 学科 化学 年级 高二
结构》
本章内容比较系统地介绍了分子的结构与性质,内容比较丰富。首先,在第一章有
关电子云和原子轨道等概念的基础上,介绍了共价键的主要类型δ键和π键,以及键参数
——键能、键长、键角;接着,在共价键概念的基础上,介绍了分子的立体结构,并根
据价层电子对互斥理论和杂化轨道理论对简单共价分子结构的多样性和复杂性进行了解
释;最后,介绍了极性分子和非极性分子、分子间作用力、氢键等概念,以及它们对物
质性质的影响,并从分子结构的角度说明了“相似相溶“规则、无机含氧酸分子的酸性
等。本节教学内容是人教版高中化学选择性必修第二册第二章《分子结构与性质》第二
教材
节《分子的空间结构》第一课时。这一课时的教学内容主要是分子结构的测定方法以及
分析 典型分子空间结构。
本节安排了“分子结构的测定方法、多样的分子空间结构”这部分内容。学生通过
学习这部分知识,了解分子结构的测定方法,了解红外光谱和质谱工作原理及应用;通
过对典型分子空间结构的学习,认识微观结构对分子空间结构的影响,了解共价分子结
构的多样性和复杂性。学生能够在分子水平上,从分子结构的视角认识物质的性质,进
一步形成有关物质结构的基本观念;学生的学习兴趣能得到有效保持,学生的科学素养
能得到进一步提高。
宏观辨识与微观探析:通过对典型分子空间结构的学习,认识微观结构对分子空间
教学目 结构的影响,了解共价分子结构的多样性和复杂性。
标与核
心素养 科学精神与社会责任:通过了解分子结构的测定方法,认识到科学是在不断发展
的,培养求真务实、不断进步的科学精神与社会责任感。
重点 分子结构的测定方法、多样的分子空间结构
难点
教学过程
教学环节 教师活动 学生活动 设计意图
导入新课 【思考】肉眼不能看到分子,科学家是怎样知道分子的 思考问题 通 过 问
结构的呢? 题,引发
学 生 思
考,提高
学生学习
积极性。
讲授新课 第二节 分子的空间结构
第一课时 分子结构的测定
一、分子结构的测定
早年的科学家主要靠对物质的化学性质进行系统总结得
出规律后推测分子的结构。如今,科学家应用了许多测定分 了解分子
子结构的现代仪器和方法,如红外光谱、晶体X射线衍射 结构的测
等。 定方法。
下面先介绍红外光谱,下一章还将介绍晶体X射线衍
射。
1.测定分子结构的现代仪器和方法红外光谱:分子中的原子不是固定不动的,而是处于不
断振动着的。红外线透过分子时,分子会吸收跟它的某些化
学键的振动频率相同的红外线,再记录到谱图上呈现吸收
峰。
通过和已有谱图库比对,或通过量子化学计算,可以得
知分子中含有何种化学键或官能团的信息。 了解红外
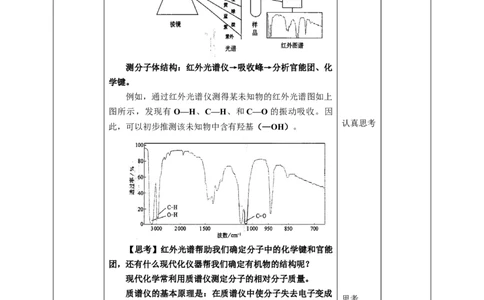
红外光谱仪原理示意图 光谱和质
谱工作原
理 及 应
用。
测分子体结构:红外光谱仪→吸收峰→分析官能团、化
学键。
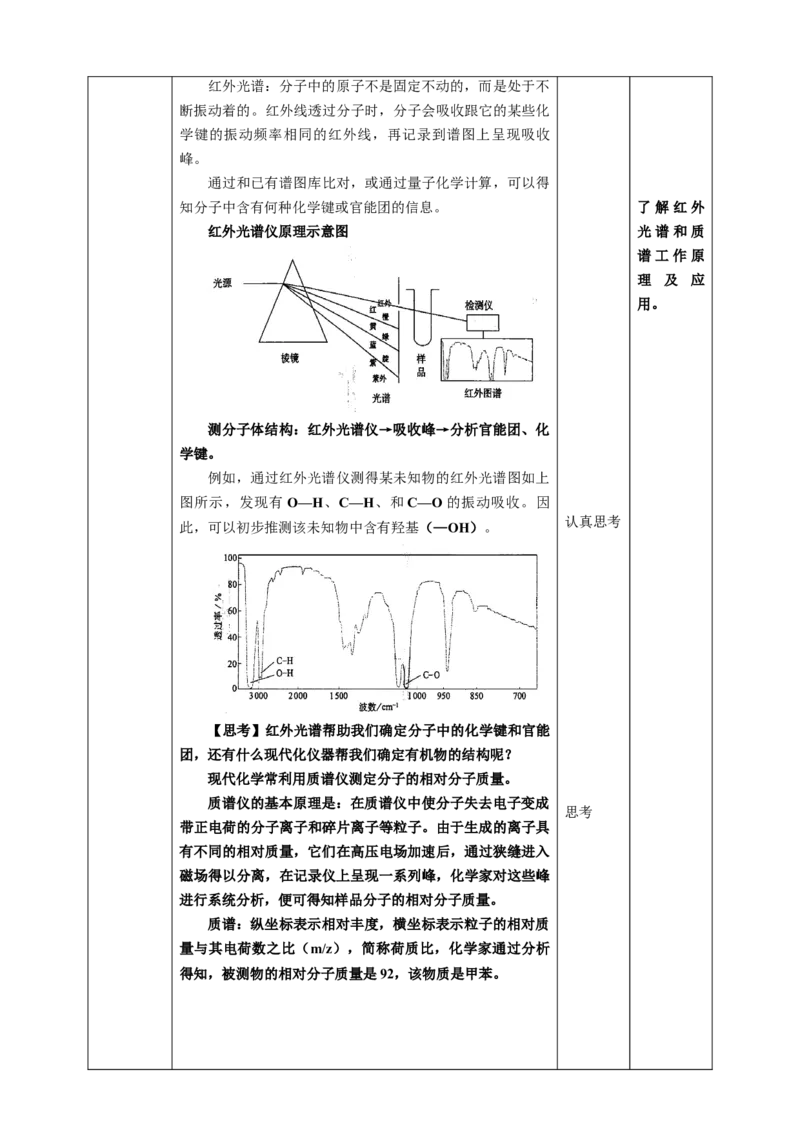
例如,通过红外光谱仪测得某未知物的红外光谱图如上
图所示,发现有O—H、C—H、和C—O的振动吸收。因
认真思考
此,可以初步推测该未知物中含有羟基(—OH)。
【思考】红外光谱帮助我们确定分子中的化学键和官能
团,还有什么现代化仪器帮我们确定有机物的结构呢?
现代化学常利用质谱仪测定分子的相对分子质量。
质谱仪的基本原理是:在质谱仪中使分子失去电子变成
思考
带正电荷的分子离子和碎片离子等粒子。由于生成的离子具
有不同的相对质量,它们在高压电场加速后,通过狭缝进入
磁场得以分离,在记录仪上呈现一系列峰,化学家对这些峰
进行系统分析,便可得知样品分子的相对分子质量。
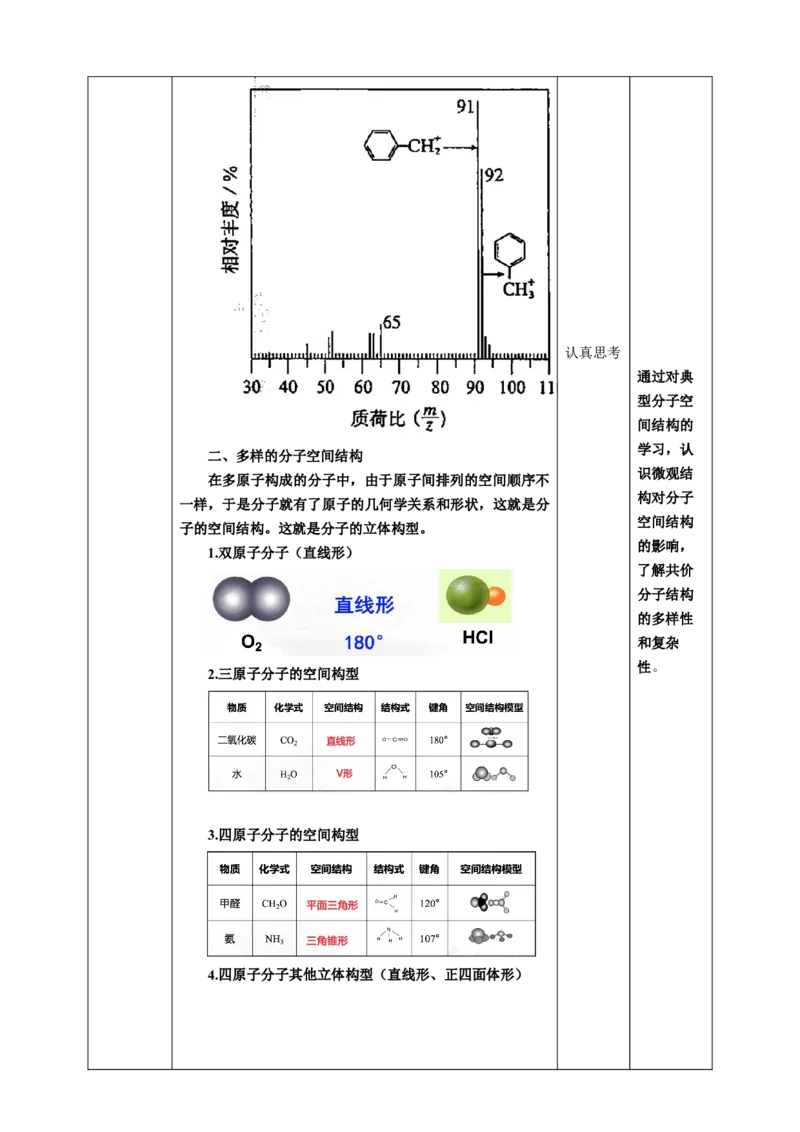
质谱:纵坐标表示相对丰度,横坐标表示粒子的相对质
量与其电荷数之比(m/z),简称荷质比,化学家通过分析
得知,被测物的相对分子质量是92,该物质是甲苯。认真思考
通过对典
型分子空
间结构的
学习,认
二、多样的分子空间结构
识微观结
在多原子构成的分子中,由于原子间排列的空间顺序不
构对分子
一样,于是分子就有了原子的几何学关系和形状,这就是分
空间结构
子的空间结构。这就是分子的立体构型。
的影响,
1.双原子分子(直线形)
了解共价
分子结构
的多样性
和复杂
性。
2.三原子分子的空间构型
3.四原子分子的空间构型
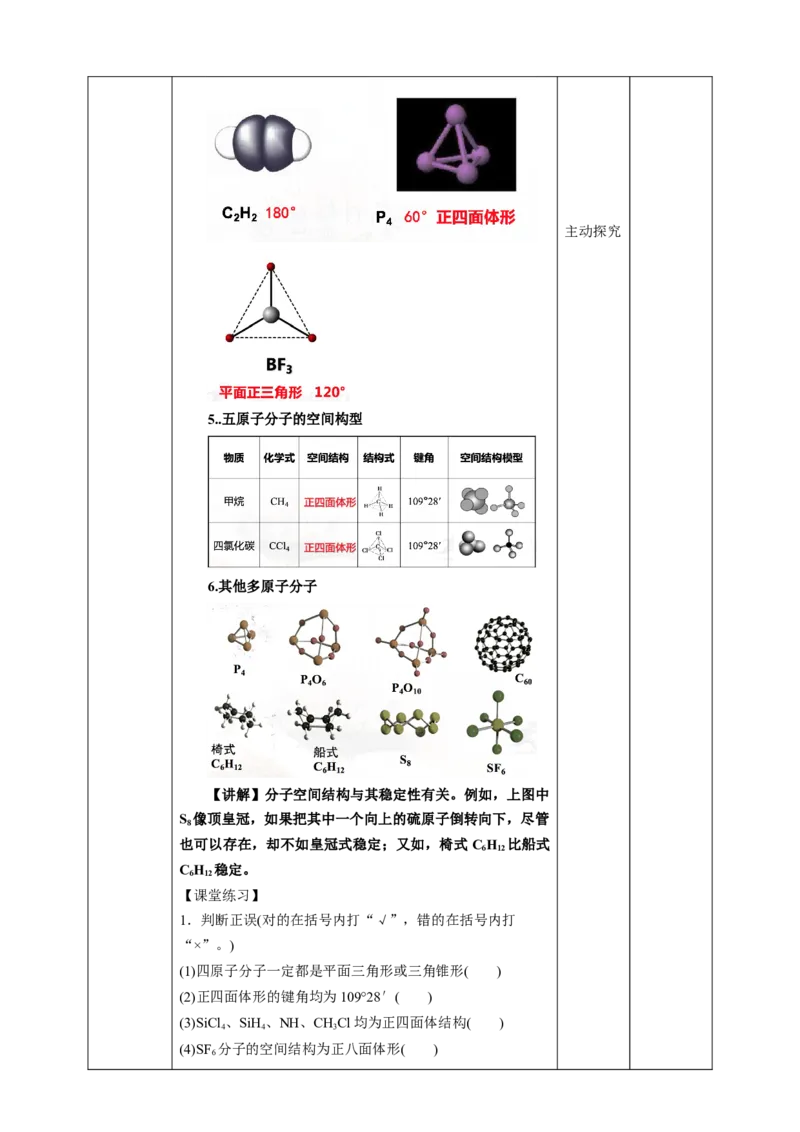
4.四原子分子其他立体构型(直线形、正四面体形)主动探究
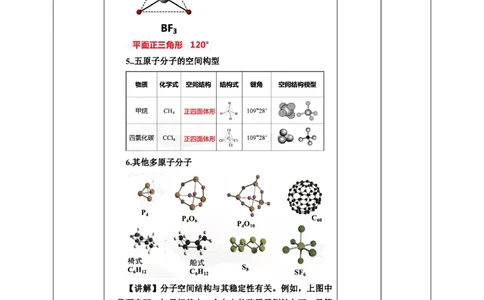
5..五原子分子的空间构型
6.其他多原子分子
【讲解】分子空间结构与其稳定性有关。例如,上图中
S 像顶皇冠,如果把其中一个向上的硫原子倒转向下,尽管
8
也可以存在,却不如皇冠式稳定;又如,椅式CH 比船式
6 12
CH 稳定。
6 12
【课堂练习】
1.判断正误(对的在括号内打“√”,错的在括号内打
“×”。)
(1)四原子分子一定都是平面三角形或三角锥形( )
(2)正四面体形的键角均为109°28′( )
(3)SiCl 、SiH、NH、CHCl均为正四面体结构( )
4 4 3
(4)SF 分子的空间结构为正八面体形( )
6(5)椅式C H 比船式C H 稳定( )
6 12 6 12
答案: (1)× (2)× (3)× (4)√ (5)√
2.可以准确判断有机物分子中含有哪些官能团的分析方法是(
)
A.核磁共振氢谱 B.质谱
C.红外光谱 D.紫外光谱
答案:C
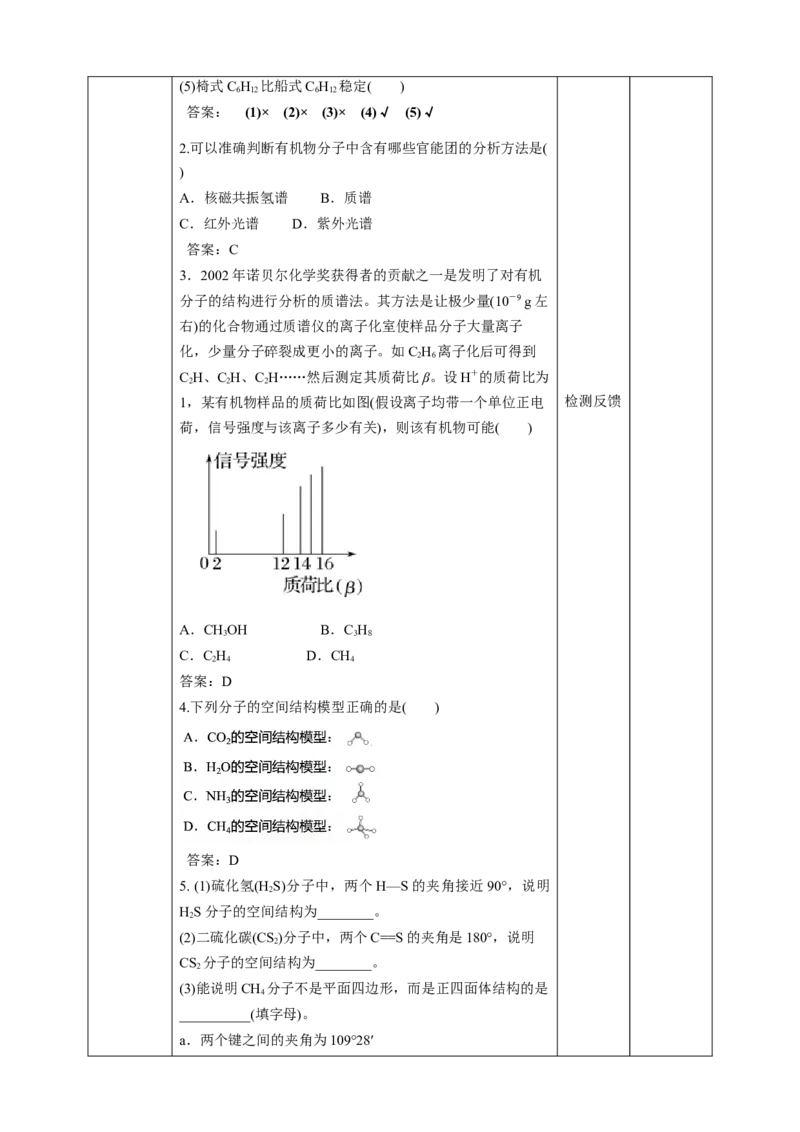
3.2002年诺贝尔化学奖获得者的贡献之一是发明了对有机
分子的结构进行分析的质谱法。其方法是让极少量(10-9 g左
右)的化合物通过质谱仪的离子化室使样品分子大量离子
化,少量分子碎裂成更小的离子。如C H 离子化后可得到
2 6
C H、C H、C H……然后测定其质荷比β。设H+的质荷比为
2 2 2
1,某有机物样品的质荷比如图(假设离子均带一个单位正电 检测反馈
荷,信号强度与该离子多少有关),则该有机物可能( )
A.CHOH B.C H
3 3 8
C.C H D.CH
2 4 4
答案:D
4.下列分子的空间结构模型正确的是( )
答案:D
5. (1)硫化氢(H S)分子中,两个H—S的夹角接近90°,说明
2
HS分子的空间结构为________。
2
(2)二硫化碳(CS)分子中,两个C==S的夹角是180°,说明
2
CS 分子的空间结构为________。
2
(3)能说明CH 分子不是平面四边形,而是正四面体结构的是
4
__________(填字母)。
a.两个键之间的夹角为109°28′b.C—H为极性共价键
c.4个C—H的键能、键长都相等
d.二氯甲烷(CHCl)只有一种(不存在同分异构体)
2 2
答案:(1) V形
(2)直线形
(3) ad
课堂小结
一、分子结构的测定
红外光谱——化学键或官能团
质谱——相对分子质量
二、多样的分子空间结构
1.三原子分子的空间结构有直线形和V形(又称角形)两
种。
CO 直线形 HO V形
2 2
2.大多数四原子分子采取平面三角形和三角锥两种空间结
构。
3.五原子分子的形状更多,最常见的是四面体形,如甲烷,
键角109°28´
板书
一、分子结构的测定
红外光谱——化学键或官能团
质谱——相对分子质量
二、多样的分子空间结构
1.三原子分子的空间结构有直线形和V形(又称角形)两
种。
CO 直线形 HO V形
2 2
2.大多数四原子分子采取平面三角形和三角锥两种空间结
构。
3.五原子分子的形状更多,最常见的是四面体形,如甲
烷,键角109°28´