文档内容
第 1 讲 化学反应速率
1.知道化学反应速率的表示方法,了解测定化学反应速率的方法
2.通过实验探究,学习运用变量控制的方法研究化学反应速率;速率影响的一般规律,
能运用规律解释生产、生活和科学实验中的实际问题。
3.知道化学反应是有历程的,认识基元反应活化能对化学反应速率的影响;知道催化
剂可以改变反应历程,能从调控化学反应速率的角度分析和选择反应条件。
4.能用简单碰撞理论说明反应条件对化学反应速率的影响,体会理论模型的建构过程,
强化模型认知意识。
重点:化学反应速率的简单计算;反应条件对化学反应速率的影响。
难点:用简单碰撞理论说明反应条件对化学反应速率的影响。
一、化学反应速率
1.化学反应速率可以用单位 、单位、 中反应物或生成物的 的变化来表示。
2.如果反应体系的体积是恒定的,则化学反应速率通常用
来表示,公式为 。式中, Δc表示 ,其
常用单位是 等。Δt表示 ,其常用单位是
等。v表示 (取正值),其常用单位是 等。
3.对于一个化学反应:mA+nB===pC+qD,可以用任一种物质的物质的量浓度随时间的
变化来表示该化学反应的速率 v(A)= ,v(B)= ,v(C)= ,v(D)=
。且有===。即v(A)∶v(B)∶v(C)∶v(D)= m ∶ n ∶ p ∶ q 。
4.化学反应速率是可以通过实验测定的。根据化学反应速率的表达式,实验中需要测定
。实际上任何一种与物质浓度有关的可观测量都可以
加以利用,如 、 、 、 、 等。
二、影响化学反应速率的因素
1.相同条件下,不同的化学反应会有不同的速率,这表明反应速率首先是由 、
等因素决定的。
2.在一般情况下,当其他条件相同时,增大反应物的浓度,化学反应速率 ,降低反应
物的浓度,化学反应速率 ,升高温度,化学反应速率 ,降低温度,化学反应速率。
3.催化剂可以改变化学反应的速率。
4.对于 化学反应,改变压强同样可以改变化学反应速率。
三、活化能
1.大多数化学反应并不是经过简单碰撞就能完成的,而往往经过 才能实现。
例如:2HI===H +I,经过以下两步反应完成:
2 2
2HI―→H+2I
2
2I―→I
2
这两个先后进行的每一步反应都称为 ,反映了2HI===H +I 的反应历程,反
2 2
应历程又称为 。
2.基元反应发生的先决条件是反应物分子必须发生 。并不是反应物分子的每一次碰撞
都能发生化学反应。我们把 叫做有效碰撞。
3.发生有效碰撞的分子必须具有 ,这种分子叫做活化分子,
,叫做反应的活化能。
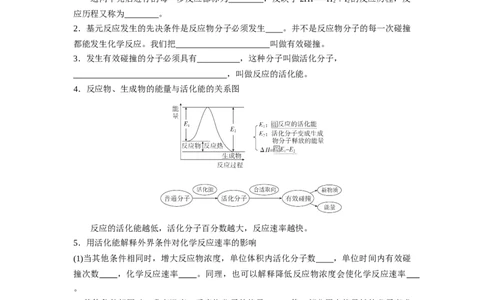
4.反应物、生成物的能量与活化能的关系图
反应的活化能越低,活化分子百分数越大,反应速率越快。
5.用活化能解释外界条件对化学反应速率的影响
(1)当其他条件相同时,增大反应物浓度,单位体积内活化分子数 ,单位时间内有效碰
撞次数 ,化学反应速率 。同理,也可以解释降低反应物浓度会使化学反应速率
。
(2)其他条件相同时,升高温度,反应物分子的能量 ,使一部分原来能量低的分子变成
活化分子,从而增加了 ,使得单位时间内有效碰撞次数
,因而化学反应速率 。同理,降低温度会使化学反应速率 。
(3)催化剂能改变反应的历程,改变反应的 。有催化剂时反应的活化能比无催化剂时
反应的活化能 了很多,这就使更多的反应物分子成为活化分子,增大了单位体积内反
应物分子中活化分子的数目,从而 了化学反应速率。
1.判断正误,正确的打“√”,错误的打“×”。(1)对于任何化学反应来说,反应速率越快,反应现象就越明显。( )
(2)甲、乙两容器中分别充入2 mol NO 和4 mol NO ,5分钟后两者各反应掉NO 1 mol和
2 2 2
2 mol,则说明乙中反应速率大。( )
(3)化学反应速率一定随着时间的延长而减小。( )
(4)由v=计算平均速率,用反应物表示为正值,用生成物表示为负值。( )
(5)决定化学反应速率快慢的根本因素是温度、浓度和催化剂。( )
(6)二氧化锰能加快所有化学反应的速率。( )
(7)锌与硫酸反应时,硫酸的浓度越大,产生H 的速度越快。( )
2
(8)恒压时,增加惰性气体的量,使有气体物质参加的反应的化学反应速率减慢。( )
(9)增大反应物的浓度,能够增大活化分子的百分含量,所以反应速率增大。( )
考点1化学反应速率的计算和比较
1.化学反应速率的计算方法
(1)定义式法
利用公式v==计算化学反应速率。
注意:①用公式v==计算得到的化学反应速率是平均速率,不是瞬时速率,化学反
应速率均取正值。
②浓度的变化量Δc=c(某时刻)-c(初始)
所以一般Δc(反应物)为负值,Δc(生成物)为正值,但是计算出的反应速率都为正值。
③同一化学反应,用不同物质表示的化学反应速率其数值可能不同,但表示意义相同,
故表示化学反应速率时,必须指明具体物质。
④固体或纯液体物质的浓度视为常数,不能用固体或纯液体物质的浓度变化来表示化
学反应速率。
(2)关系式法
利用“化学反应速率之比=物质的量浓度变化量之比=化学计量数之比”计算化学反
应速率。
(3)“三段式”法
①求解化学反应速率计算题的一般步骤:
a.写出有关反应的化学方程式。
b.找出各物质的起始量、转化量、某时刻量。
c.根据已知条件列方程计算。
例如 mA + nB pC
\s\up11(起始浓度) a b c
\s\up11(转化浓度) x\s\up11(某时刻浓度) a-x b- c+
v(B)==
②计算中注意以下量的关系:
a.对反应物:c(起始)-c(转化)=c(某时刻)
b.对生成物:c(起始)+c(转化)=c(某时刻)
c.转化率=×100%
2.化学反应速率快慢的比较方法——比值法
(1)转化为同一单位表示,其转化公式为1 mol·L-1·s-1=60 mol·L-1·min-1。
(2)比较化学反应速率与化学计量数的比值。
如反应aA+bB===cC,要比较v(A)与v(B)的相对大小,即比较与,若>,则A表示的
反应速率比B表示的大。
将等物质的量的A、B混合于2L的密闭容器中,发生下列反应:3A(g)+B(g)=xC(g)
+2D(g),经2min后测得D的浓度为0.5mol/L,c(A) ∶ c(B)=3∶5,以C表示的平均速率为
下列说法正确的是
A.该反应方程式中,x=2
B.反应速率:
C.2min时,B的物质的量为1.5mol
D.2min时,A的转化率为60%
2molA与2molB混合于2L的密闭容器中,发生反应:2A(g)+3B(g) 2C(g)+
zD(g);若2s后,A的转化率为50%,测得v(D)=0.25mol·L-1·s-1,下列推断正确的是
A.v(C)=0.2mol·L-1·s-1 B.z=3
C.B的转化率为75% D.反应前与2s后容器的压强比为4:3
将等物质的量A、B混合于2L的密闭容器中,发生反应:3A(g)+B(g) xC(g)+
2D(g),经5min后测得D的浓度为0.5mol·L-1,c(A)∶c(B)=3∶5,C的平均反应速率是
0.1mol·L-1·min-1。
(1)经5min后A的浓度为 。
(2)反应开始前充入容器中B的物质的量为 。
(3)B的平均反应速率为 。(4)x的值为 。
(5)对于反应A(g)+3B(g)=2C(g)+2D(g),下列分别表示不同条件下的反应速率,则反应速率
大小关系是 。
①v(A)=0.01mol·L-1·s-1
②v(B)=1.20mol·L-1·min-1
③v(C)=2.40mol·L-1·min-1
④v(D)=0.02mol·L-1·s-1
考点2化学反应速率的测定
1.基本原理与思路
化学反应的速率是通过实验测定的。因为化学反应中发生变化的是体系中的化学物质
(包括反应物和生成物),所以与其中任何一种化学物质的浓度(或质量)相关的性质在测量反
应速率时都可以加以利用。
2.化学反应速率的测量
(1)可直接通过实验测定某些物理量,如释放出气体的体积等。
(2)依靠科学仪器才能测量的性质,如光的吸收、光的发射、导电能力等。
(3)在溶液中,当反应物或生成物本身有比较明显的颜色时,常常利用颜色深浅和显色
物质浓度间的正比关系来跟踪反应的过程和测量反应速率。
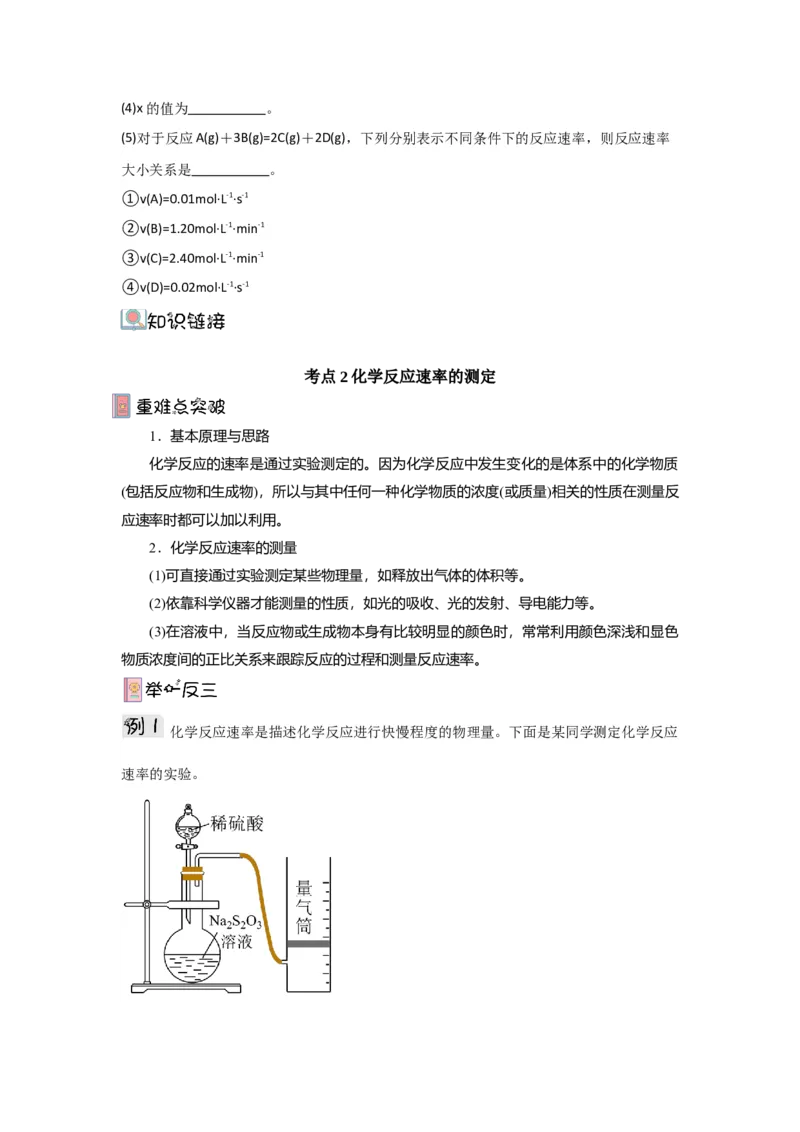
化学反应速率是描述化学反应进行快慢程度的物理量。下面是某同学测定化学反应
速率的实验。该同学利用如图装置测定化学反应速率。(已知:S O +2H+ = H O+S↓+SO ↑)
2 2 2
(1)除如图装置所示的实验用品外,还需要的一件实验用品是 。
(2)若在2 min时收集到224 mL(已折算成标准状况)气体,可计算出该2 min内H+的反应速率,
而该测定值比实际值偏小,其原因可能是 。
(3)利用该化学反应,试简述测定反应速率的其他方法: (写一种)。
小李同学采用如图所示的实验装置测定锌与稀硫酸反应的速率,取1g锌粒与
20mL0.5mol·L-1的硫酸进行反应,测得不同时刻反应生成的H 的体积(已折算为标准状况)如
2
表。下列说法正确的是
t/s 0 5 10 15 20 25
V(H )/mL 0.0 14.6 34.5 44.8 52.2 56.9
2
A.反应结束时锌粒无剩余
B.锌与稀硫酸反应初期速率逐渐加快,后又变慢
C.应用锌粉代替锌粒进行实验,以节约实验时间
D.假设溶液的体积不变,10~25s内的平均反应速率v(H SO )=0.02mol·L-1·min-1
2 4
某校化学活动社团为测定1mol/L的H SO 溶液与锌粒和锌粉反应的速率,设计如图
2 4
1装置。(1)图1中盛有H SO 溶液的仪器名称是 。
2 4
(2)按照图1装置实验时,限定了两次实验时间均为10min,还需要测定的另一个数据是
。
(3)若将图1装置中的气体收集装置改为图2装置,实验完毕待冷却后,该学生准备读取量
气管上液面所在处的刻度,发现量气管中液面高于干燥管中液面,应首先采取的操作是
。
考点3 定性与定量研究影响化学反应速率的因素
1.温度对反应速率的影响
反应
NaSO+HSO ===Na SO +SO ↑+S↓+HO
2 2 3 2 4 2 4 2 2
原理
实验
操作
实验 冷水和热水中的两组实验均出现浑浊,但热水中的一组实验先
现象 出现浑浊
实验
升高温度,NaSO 与HSO 的反应速率增大
2 2 3 2 4
结论
结论:其他条件不变时,升高温度,反应速率增大;降低温度,反应速率减小。
2.浓度对反应速率的影响(1)按照图示安装两套装置。
(2)在两个锥形瓶中各加入2 g锌粒(颗粒大小基本相同)。
(3)通过分液漏斗分别加入40 mL 1 mol/L和40 mL 4 mol/L的HSO 溶液。
2 4
(4)观察并记录收集10 mL H 所用的时间,发现4 mol/L的HSO 溶液所用时间比1
2 2 4
mol/L的HSO 溶液所用时间短。
2 4
结论:其他条件不变时,增大反应物浓度,反应速率增大;减小反应物浓度,反应速率减
小。
注意:(1)固体和纯液体的浓度可视为常数,改变其物质的量,对反应速率无影响。
(2)若某物质的浓度变化改变了其性质,反应实质可能发生改变,要具体分析反应速率
的变化(如铁与稀硫酸反应,在一定浓度范围内反应速率与浓度有关,但 Fe与浓硫酸反应
不产生H,且常温下铁遇浓硫酸发生钝化)。
2
(3)固体物质的反应速率与表面积有关,颗粒越小,表面积越大,反应速率就越快,故
块状固体可通过研磨来增大表面积,从而加快反应速率。
(4)对于离子反应,只有实际参加反应的各离子浓度发生变化,才会引起化学反应速率
的改变。
(5)改变压强,对化学反应速率的影响的根本原因是引起浓度改变。所以在讨论压强对
反应速率的影响时,应区分引起压强改变的原因。
①对于没有气体参与的化学反应,改变压强,对化学反应速率无影响。
②对于有气体参与的化学反应,有以下几种情况
Ⅰ.恒温恒容时:
a.充入气体反应物→总压强增大→浓度增大→反应速率加快。
b.充入“无关气体(如He、Ne、Ar、N 等不参与本反应也不干扰本反应的气体,下
2
同)”→总压强增大,但各反应物浓度不变,则反应速率不变。
Ⅱ.恒温恒压时:
a.同等程度地充入相应的气体反应物→体积增大,但各反应物浓度不变,则反应速率
不变。
b.充入“无关气体”→体积增大→各反应物浓度减小→反应速率减慢。
某小组探究实验条件对反应速率的影响,设计如下实验,并记录结果如下:编
温度 HSO 溶液 KI溶液 1%淀粉溶液体积 出现蓝色时间
号 2 4
① 20°C 0.10mol·L-110mL 0.40mol·L-15mL 1mL 40s
② 20°C 0.10mol·L-110mL 0.80mol·L-15mL 1mL 21s
③ 50°C 0.10mol·L-110mL 0.40mol·L-15mL 1mL 5s
④ 80°C 0.10mol·L-110mL 0.40mol·L-15mL 1mL 未见蓝色
下列说法正确的是
A.实验①~④中,应将KI溶液与淀粉溶液先混合
B.实验①~④中,应将HSO 溶液与淀粉溶液先混合
2 4
C.在I-被O 氧化过程中,H+只是降低活化能
2
D.由④实验可知,温度越高,反应速率越慢
课外实验小组以KI参与的某些反应来对反应过程和化学反应原理进行探究。
(1)KI中的 促进 分解的反应机理如下
① (慢)
② (快)
则此过程的决速步骤为 (填序号), 在此过程中的作用是 。
(2)KI中的 在经酸化的溶液中易被空气氧化:
实验小组探究外界条件对反应速率的影响,部分实验数据如下表。
编 温 硫酸 KI溶 体 淀粉溶液 出现蓝色
号 度/℃ 体积/mL 液体积/mL 积/mL 体积/mL 的时间/s
A 39 10.0 5.0 5.0 1.0 5
B 5 10.0 5.0 V 1.0 39
C 39 15.0 5.0 0.0 1.0 t
①为确保A组实验在39℃下进行,应采用的控温方法为 。
②B组实验中V= ,C组是探究 对反应速率的影响,t的取值范围为 。(3)若将C组实验反应后溶液充分放置一段时间,检验其吸收 的体积,可用 标准
溶液滴定吸收液( ),实验时应将 标准溶液放在
滴定管中,滴定终点时实验现象为 ,若消耗0.2mol/L 标准溶液为15.00mL,
则吸收氧气在标准状况下的体积为 。
考点4 活化能与化学反应历程
1.基元反应、过渡态理论及活化能
(1)基元反应:研究发现,大多数化学反应并不是经过简单碰撞就能完成,往往要经过
多个反应步骤才能实现。每一步反应都称为基元反应。
(2)过渡态理论:过渡态理论认为,反应物分子并不只是通过简单碰撞直接形成产物,
而是必须经过一个形成活化络合物的过渡状态,并且达到这个过渡状态需要一定的活化能。
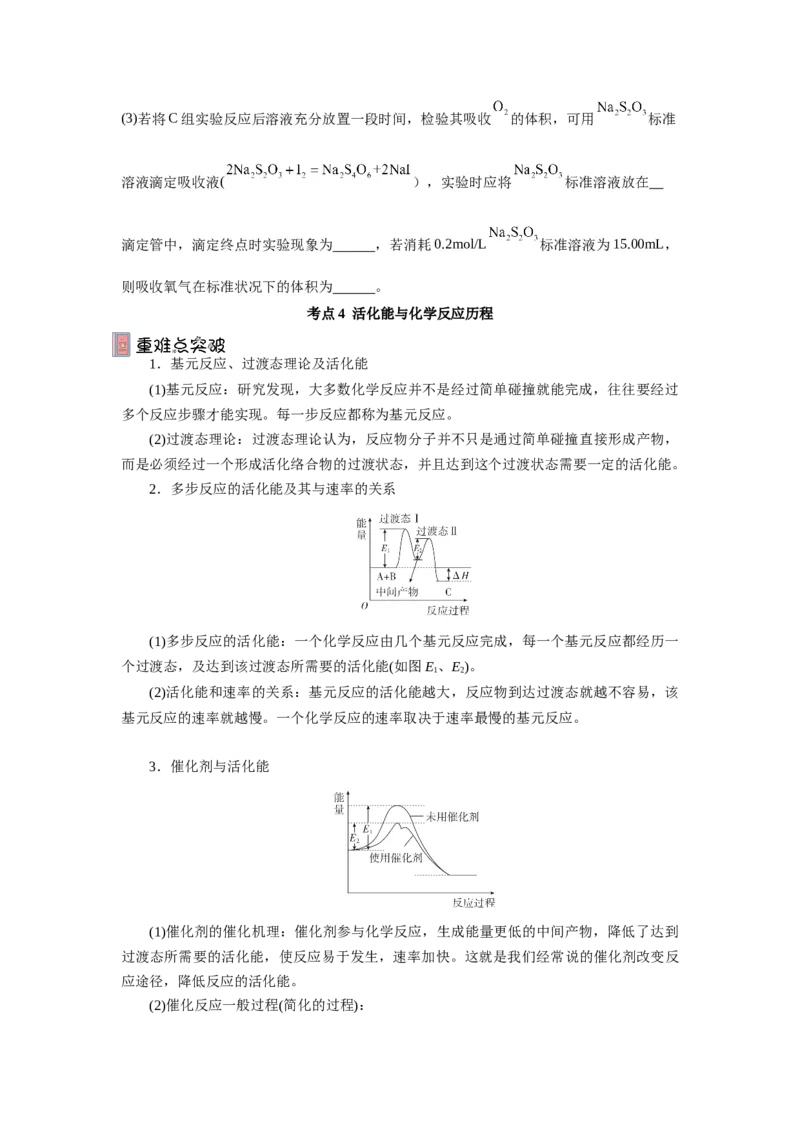
2.多步反应的活化能及其与速率的关系
(1)多步反应的活化能:一个化学反应由几个基元反应完成,每一个基元反应都经历一
个过渡态,及达到该过渡态所需要的活化能(如图E、E)。
1 2
(2)活化能和速率的关系:基元反应的活化能越大,反应物到达过渡态就越不容易,该
基元反应的速率就越慢。一个化学反应的速率取决于速率最慢的基元反应。
3.催化剂与活化能
(1)催化剂的催化机理:催化剂参与化学反应,生成能量更低的中间产物,降低了达到
过渡态所需要的活化能,使反应易于发生,速率加快。这就是我们经常说的催化剂改变反
应途径,降低反应的活化能。
(2)催化反应一般过程(简化的过程):①反应物扩散到催化剂表面;
②反应物被吸附在催化剂表面;
③被吸附的反应物发生化学反应生成产物;
④产物的解吸。
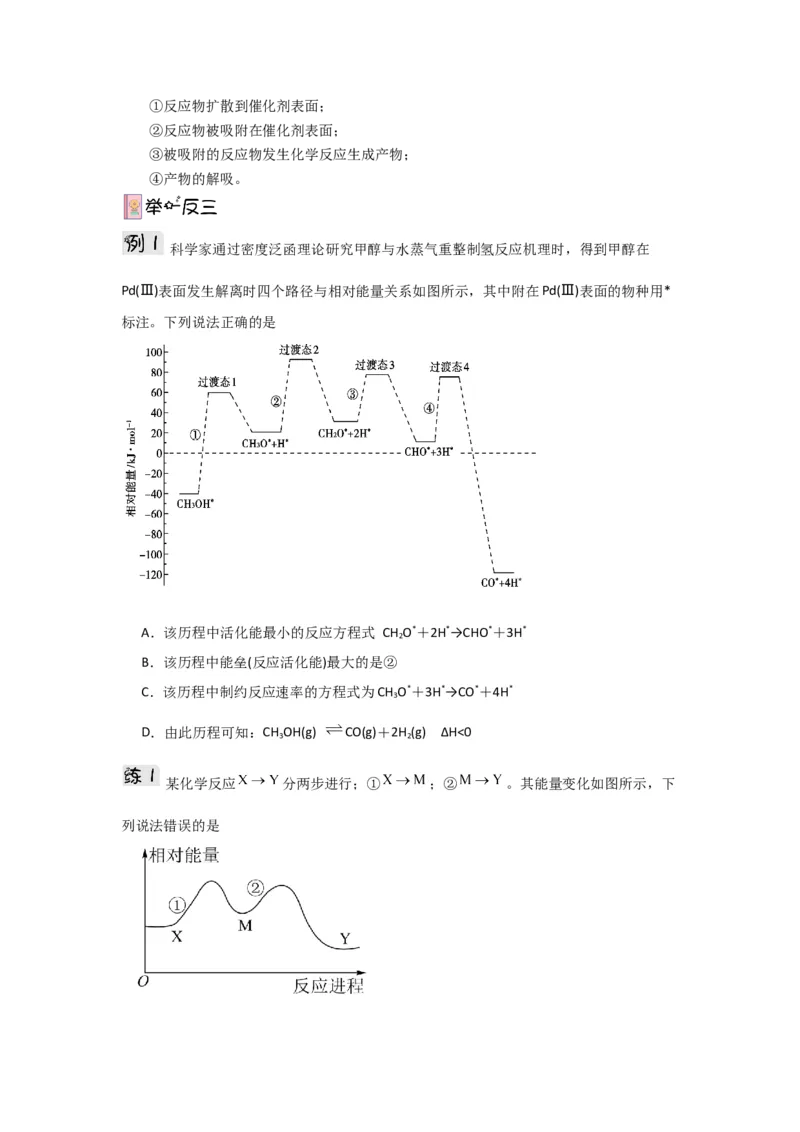
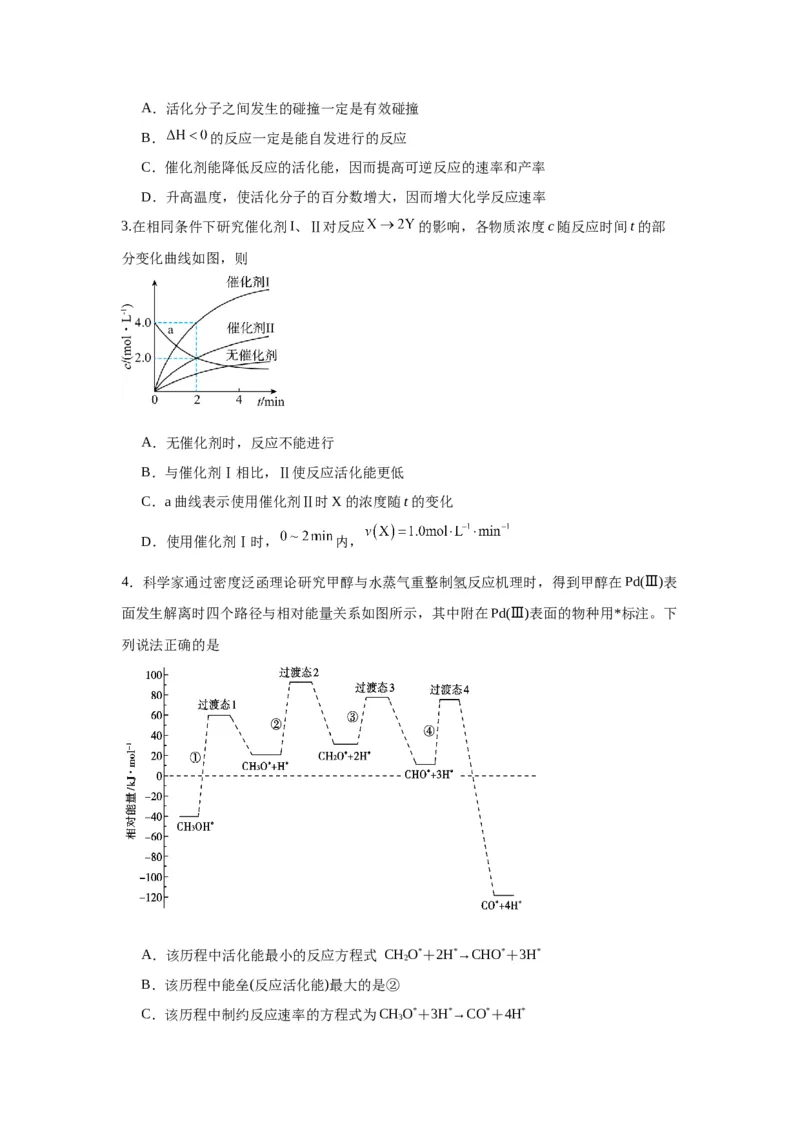
科学家通过密度泛函理论研究甲醇与水蒸气重整制氢反应机理时,得到甲醇在
Pd(Ⅲ)表面发生解离时四个路径与相对能量关系如图所示,其中附在Pd(Ⅲ)表面的物种用*
标注。下列说法正确的是
A.该历程中活化能最小的反应方程式 CH O*+2H*→CHO*+3H*
2
B.该历程中能垒(反应活化能)最大的是②
C.该历程中制约反应速率的方程式为CH O*+3H*→CO*+4H*
3
D.由此历程可知:CH OH(g) CO(g)+2H (g) ΔH<0
3 2
某化学反应 分两步进行;① ;② 。其能量变化如图所示,下
列说法错误的是A.该反应是放热反应
B.反应①是总反应的决速步骤
C.X、Y、M三种物质中Y最稳定
D.M是该反应的催化剂,可降低该反应的焓变,提高该反应的速率
合成氨是目前最有效工业固氮的方法,可解决数亿人口生存问题。科学家研究利用
铁触媒催化合成氨的反应历程如图所示,其中吸附在催化剂表面的物种用“ad”表示。下列
说法错误的是
A.合成氨总反应 正反应的活化能高于逆反应的活化能
B.该历程的决速步为
C.合成氨总反应 的反应热为
D.铁触媒能使反应物活化分子百分数增大,有效碰撞次数增多
1.合成气转变为甲醇的反应为:CO(g)+2H(g) CHOH(g) ΔH=-90.8kJ·mol−1。一定条件
2 3
下,将1mol CO和3mol H 通入2L的恒容密闭容器中,5min时测得H 的物质的量为
2 2
2.4mol。下列说法正确的是
A.0~5min,反应放出的热量为27.24kJ
B.第5min时,H 的反应速率为0.06mol·L−1min−1
2
C.其他条件不变,增大CO浓度可以增加体系中活化分子百分数
D.反应到5min时,生成0.6mol CH OH
3
2.下列说法中正确的是A.活化分子之间发生的碰撞一定是有效碰撞
B. 的反应一定是能自发进行的反应
C.催化剂能降低反应的活化能,因而提高可逆反应的速率和产率
D.升高温度,使活化分子的百分数增大,因而增大化学反应速率
3.在相同条件下研究催化剂I、Ⅱ对反应 的影响,各物质浓度c随反应时间t的部
分变化曲线如图,则
A.无催化剂时,反应不能进行
B.与催化剂Ⅰ相比,Ⅱ使反应活化能更低
C.a曲线表示使用催化剂Ⅱ时X的浓度随t的变化
D.使用催化剂Ⅰ时, 内,
4.科学家通过密度泛函理论研究甲醇与水蒸气重整制氢反应机理时,得到甲醇在Pd(Ⅲ)表
面发生解离时四个路径与相对能量关系如图所示,其中附在Pd(Ⅲ)表面的物种用*标注。下
列说法正确的是
A.该历程中活化能最小的反应方程式 CHO*+2H*→CHO*+3H*
2
B.该历程中能垒(反应活化能)最大的是②
C.该历程中制约反应速率的方程式为CHO*+3H*→CO*+4H*
3D.由此历程可知:CHOH(g) CO(g)+2H(g) ΔH<0
3 2
5.某小组利用 溶液和酸性 溶液反应来探究“条件对化学反应速率的影响”。
实验时,先分别量取两种溶液,然后倒入试管中迅速振荡混合均匀,开始计时,通过测定
褪色所需时间来判断反应的快慢。该小组设计了如下的方案。
酸性 溶液 溶液
编
溶液/℃
号
浓度/ 体积/ 浓度/ 体积/
① 0.010 4.0 0.20 2.0 25
② 4.0 2.0 25
③ 0.010 4.0 0.20 2.0 50
(1)已知反应后 转化为 逸出, 转化为 。为了观察到紫色褪去,
与 初始的物质的量需要满足的关系为:
。
(2)实验编号①②可探究反应物浓度对化学反应速率影响,其中 ,探究温度
时化学反应速率影响的实验编号是 (填编号)。
(3)实验①测得 溶液的褪色时间为 ,忽略混合前后溶液体积的微小变化,
这段时间内平均反应速率 。
(4)请在答题卡坐标图中,画出25℃和50℃两种温度下, 的变化曲线图
。
(5)该小组的同学实验时发现开始时反应产生气泡非常慢,一段时间后反应产生气泡速率明显加快。其原因可能是___________。
A.反应放热导致温度升高 B.压强增大
C.生成物的催化作用 D.反应物接触面积增大
(6)该小组对实验①测定反应过程中溶液不同时间的温度,结果如表:
时间/ 0 5 10 15 20 25 35 40 50
温度/℃ 25 26 26 26 26 26 26.5 27 27
结合实验目的和表中数据,实验①明显加快的主要原因是: 。
6.某学习小组用酸性KMnO 溶液和HC O(草酸)溶液之间的反应来研究“影响反应速率的
4 2 2 4
因素”,设计实验方案如下:(假设溶液混合时体积可以加和)
室温下,试管中所加试剂及其用量/mL
实验 溶液褪色至无色所
编号 0.6mol/L 0.1mol/L 3mol/L 需时间/min
溶液 溶液 溶液
1 3.0 13.0 2.0 2.0 10.0
2 1.0 2.0 12.8
(1)该实验探究的是 因素对化学反应速率的影响,上述实验设计表: ,
。
(2)利用实验1中数据计算,平均反应速率: 。
(3)该小组同学查阅已有的实验资料发现,该实验过程中Mn2+对反应有催化作用,并继续进
行实验探究。请你帮助该小组同学完成实验方案。所加试剂X最好选用___________
室温下,试管中所加试剂及其用量/mL
实验 少 溶液褪色至无色
编号 0.6mol/L 0.1mol/L 3mol/L 量 所需时间/min
溶液 溶液 溶液
3 3.0 13.0 2.0 2.0 X t
A.0.1mol/L B.0.1mo1/L