文档内容
第 4 讲 化学平衡图像
1.学会分析化学反应速率与化学平衡图像
2.由定性和定量结合的方式揭示化学平衡及移动的本质特征。
3.能运用相关的图像解答化学反应原理的相关问题。
重点:化学平衡图像
难点:分析化学平衡图像
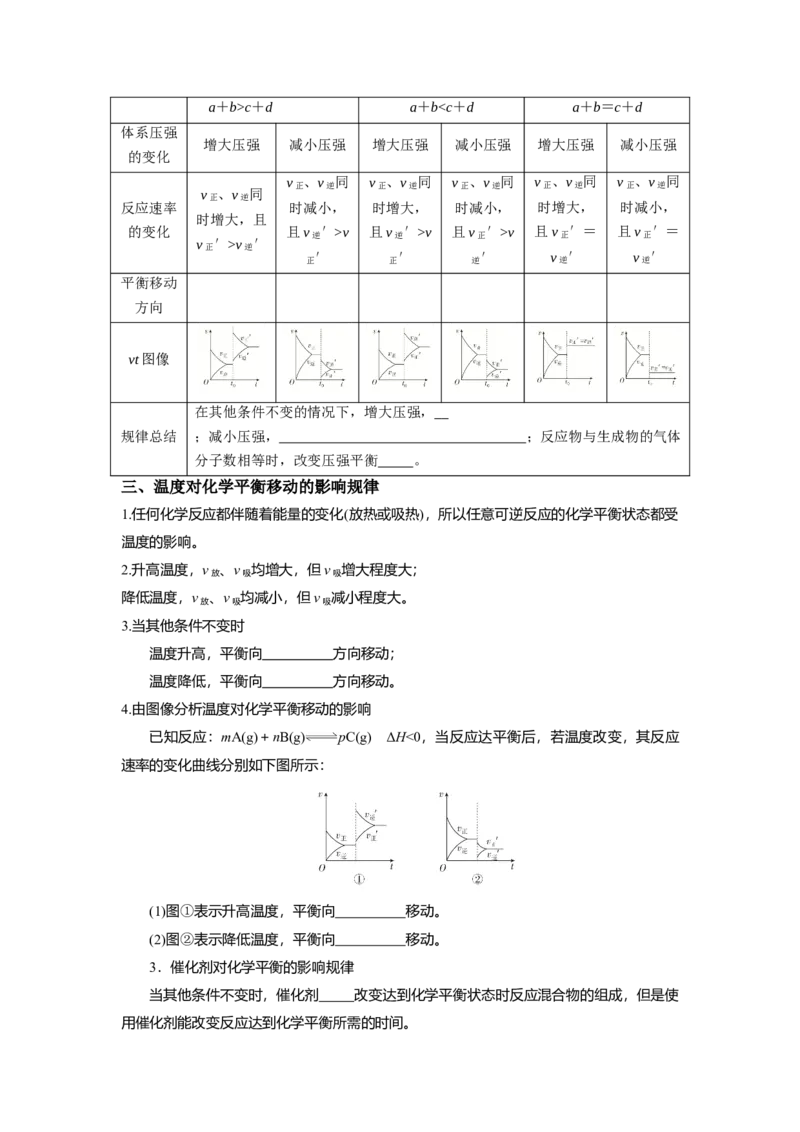
一、浓度变化对化学平衡的影响规律
化学反应 aA+bB cC+dD(A、B、C、D均不是固体或纯液体)
增大反应 减小反应 增大生成 减小生成
浓度的变化
物浓度 物浓度 物浓度 物浓度
v 瞬间增大,v v 瞬间减小,v v 瞬间增大,v v 瞬间减小,v
正 正 逆 逆
反应速率变化 瞬间不变,v 瞬间不变,v 瞬间不变,v 瞬间不变,v
逆 逆 正 正
′>v ′ ′>v ′ ′>v ′ ′>v ′
正 逆 逆 正 逆 正 正 逆
平衡移动方向 方向 方向 方向 方向
vt图像
在其他条件不变的情况下,增大反应物的浓度或减小生成物的浓度,都
规律总结 可以使平衡向 方向移动;增大生成物的浓度或减小反应物的浓度,
都可以使平衡向 方向移动
二、压强变化(改变容器容积)对化学平衡的影响规律
aA(g)+bB(g) aA(g)+bB(g) aA(g)+bB(g)
化学反应
cC(g)+dD(g) cC(g)+dD(g) cC(g)+dD(g)a+b>c+d a+bv 且v ′>v 且v ′>v 且v ′= 且v ′=
逆 逆 正 正 正
v ′>v ′
正 逆
′ ′ ′ v ′ v ′
正 正 逆 逆 逆
平衡移动
方向
vt图像
在其他条件不变的情况下,增大压强,
规律总结 ;减小压强, ;反应物与生成物的气体
分子数相等时,改变压强平衡 。
三、温度对化学平衡移动的影响规律
1.任何化学反应都伴随着能量的变化(放热或吸热),所以任意可逆反应的化学平衡状态都受
温度的影响。
2.升高温度,v 、v 均增大,但v 增大程度大;
放 吸 吸
降低温度,v 、v 均减小,但v 减小程度大。
放 吸 吸
3.当其他条件不变时
温度升高,平衡向 方向移动;
温度降低,平衡向 方向移动。
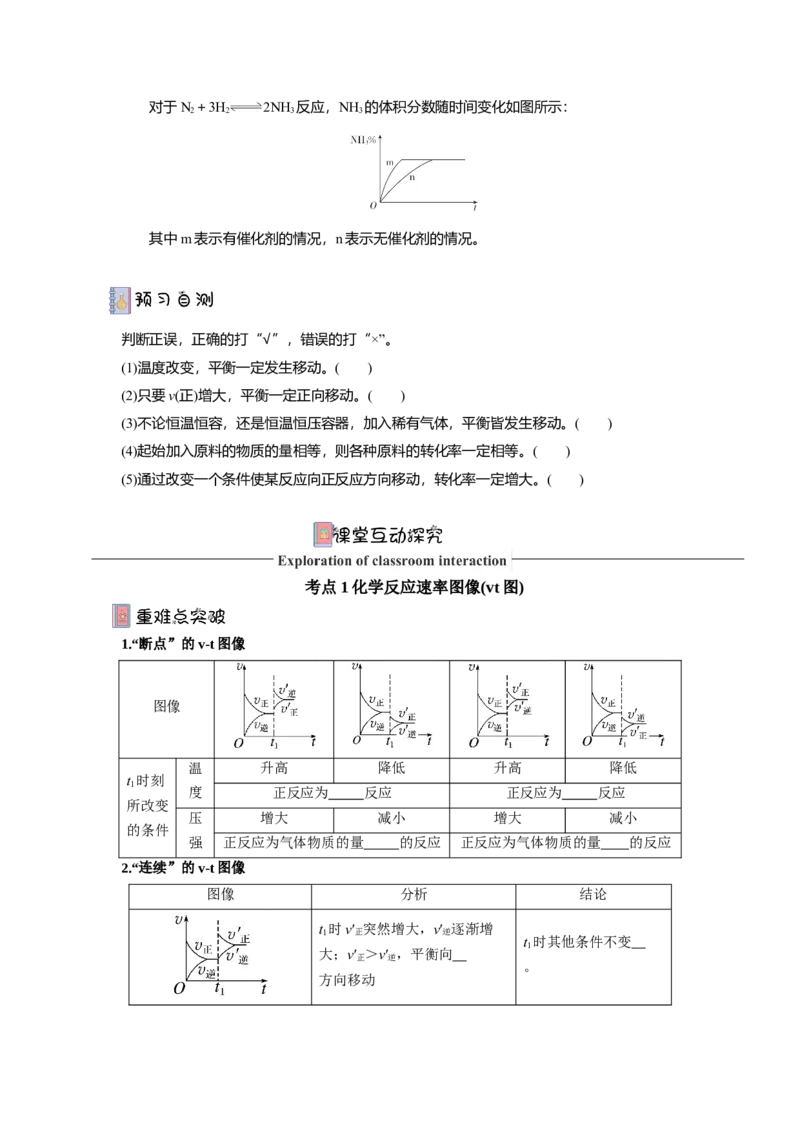
4.由图像分析温度对化学平衡移动的影响
已知反应:mA(g)+nB(g) pC(g) ΔH<0,当反应达平衡后,若温度改变,其反应
速率的变化曲线分别如下图所示:
(1)图①表示升高温度,平衡向 移动。
(2)图②表示降低温度,平衡向 移动。
3.催化剂对化学平衡的影响规律
当其他条件不变时,催化剂 改变达到化学平衡状态时反应混合物的组成,但是使
用催化剂能改变反应达到化学平衡所需的时间。对于N+3H 2NH 反应,NH 的体积分数随时间变化如图所示:
2 2 3 3
其中m表示有催化剂的情况,n表示无催化剂的情况。
判断正误,正确的打“√”,错误的打“×”。
(1)温度改变,平衡一定发生移动。( )
(2)只要v(正)增大,平衡一定正向移动。( )
(3)不论恒温恒容,还是恒温恒压容器,加入稀有气体,平衡皆发生移动。( )
(4)起始加入原料的物质的量相等,则各种原料的转化率一定相等。( )
(5)通过改变一个条件使某反应向正反应方向移动,转化率一定增大。( )
考点1化学反应速率图像(vt图)
1.“断点”的v-t图像
图像
温 升高 降低 升高 降低
t 时刻
1
度 正反应为 反应 正反应为 反应
所改变
压 增大 减小 增大 减小
的条件
强 正反应为气体物质的量 的反应 正反应为气体物质的量 的反应
2.“连续”的v-t图像
图像 分析 结论
t 时v′ 突然增大,v′ 逐渐增
1 正 逆
t 时其他条件不变
1
大;v′ >v′ ,平衡向
正 逆
。
方向移动t 时v′ 突然减小,v′ 逐渐减
1 正 逆
t 时其他条件不变,
1
小;v′ >v′ ,平衡向
逆 正
。
方向移动
t 时v′ 突然增大,v′ 逐渐增
1 逆 正
t 时其他条件不变,
1
大;v′ >v′ ,平衡向
逆 正
。
方向移动
t 时v′ 突然减小,v′ 逐渐减
1 逆 正
t 时其他条件不变,
1
小;v′ >v′ ,平衡向
正 逆
。
方向移动
3.“平台”的v-t图像
图像 分析 结论
t 时其他条件不变使用 。
1
t 时v′正、v′逆均突然
1 t 时其他条件不变增大反应体系的
1
增大且v′正=v′逆,平
压强且 (反应前后气
衡 。
体体积无变化)
t 时v′正、v′逆均突然 t 时其他条件不变,减小反应体系
1 1
减小且v′正=v′逆,平 的压强且 (反应前后
衡 。 气体体积无变化)
4.全程速率—时间图像
例如:Zn与足量盐酸的反应,化学反应速率随时间的变化出现如图所示情况。
原因:
(1)AB段(v增大), 。
(2)BC段(v减小), 。
(3)B (是或否)平衡点
根据v-t图分析外界条件改变对可逆反应A(g)+3B(g) 2C(g) ΔH<0的影响。
该反应的反应速率与时间的关系如图所示:可见在t 、t 、t 、t 时反应都处于平衡状态,如果t 、t 、t 、t 时都只改变了一个反应条件,
1 3 5 7 2 4 6 8
则下列对t、t、t、t 时改变条件的判断正确的是( )
2 4 6 8
A.使用了催化剂、增大压强、减小反应物浓度、降低温度
B.升高温度、减小压强、增大生成物浓度、使用了催化剂
C.增大反应物浓度、使用了催化剂、减小压强、升高温度
D.升高温度、减小压强、增大反应物浓度、使用了催化剂
乙酸甲酯转化为乙醇的反应原理为 CHCOOCH (g)+2H(g) C HOH(g)+
3 3 2 2 5
CHOH(g) ΔH<0。该反应中反应速率随时间变化的关系如图所示,t、t、t 时刻分别改变
3 1 3 4
某一外界条件。下列说法错误的是( )
A.t 时升高温度
1
B.t 时加入催化剂
3
C.t 时增大反应容器的容积,使体系压强减小
4
D.在反应保持化学平衡的时间段中,C HOH的体积分数最小的时间段是t~t
2 5 2 3
一定条件下,A(g)+B(g) C(g) ΔH<0,达到平衡后根据下列图像判断:
(1)升高温度,达到新平衡的是 (填“A”“B”“C”“D”或“E”,下同),新平衡中C的体
积分数 (填“增大”“减小”或“不变”,下同)。
(2)增大容器容积,达到新平衡的是 ,A的转化率 。
(3)减少C的量,达到新平衡的是 。(4)增加A的量,达到新平衡的是 ,此时B的转化率 ,A的转化率 。
(5)使用催化剂,达到新平衡的是 ,C的质量分数 。
考点2 某物质的转化率(或百分含量)-时间-温度(或压强)图像
看图要领:
(1)先从拐点向横轴作垂线:先拐先平,温度、压强均高
(2)再从拐点向纵轴作垂线:
①分析温度、压强升高时,转化率或含量的变化,
② 判断平衡移动的方向,从而确定反应的热效应或物质计量数
1.含量—时间—温度(压强)图像
C%指生成物的质量分数,B%指反应物的质量分数。
【方法技巧】 “先拐先平,数值大”,即曲线先出现拐点的首先达到平衡,反应速
率快,以此判断温度或压强的高低。再依据外界条件对平衡的影响分析判断反应的热效应
及反应前后气体体积的变化。2.转化率(或浓度)—压强—温度图像
α表示某反应物的转化率,c表示某反应物的平衡浓度。
图①,若p>p>p,则正反应为气体体积减小的反应,ΔH 0 ;
1 2 3
图②,若T>T,则正反应为放热反应。
1 2
[技法解读] “定一议二”,即把自变量(温度、压强)之一设为恒量,讨论另外两个变
量的关系。
有一化学平衡mA(g)+nB(g) pC(g)+qD(g),如图所示的是A的转化率与压
强、温度的关系。下列叙述正确的是( )
A.正反应是放热反应;m+n>p+q
B.正反应是吸热反应;m+np+q
反应mA(g)+nB(g) pC(g)的速率和平衡图像如下,下列判断正确的是( )
A.由图1可知,Tv逆 的是点3
D.图4中,若m+n=p,则a曲线一定使用了催化剂
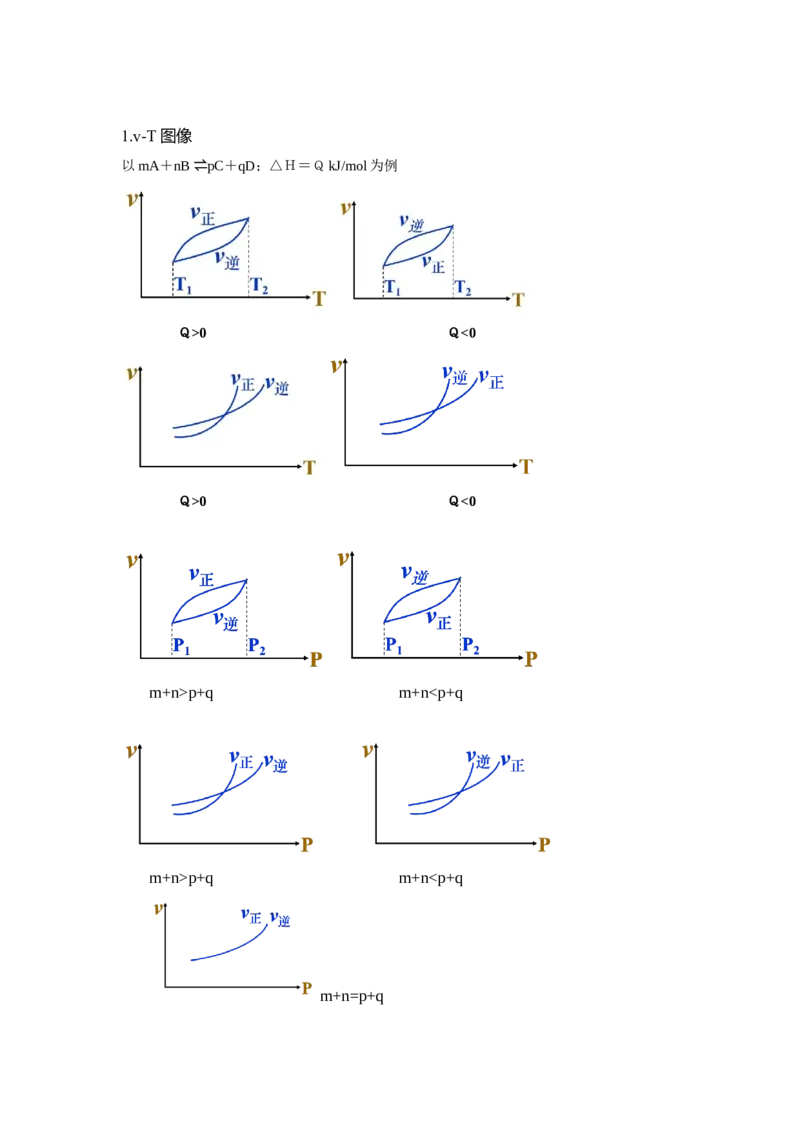
考点3速率-压强(或温度)(v-T/P)图像1.v-T图像
以mA+nB ⇌pC+qD;△H=QkJ/mol为例
Q>0 Q<0
Q>0 Q<0
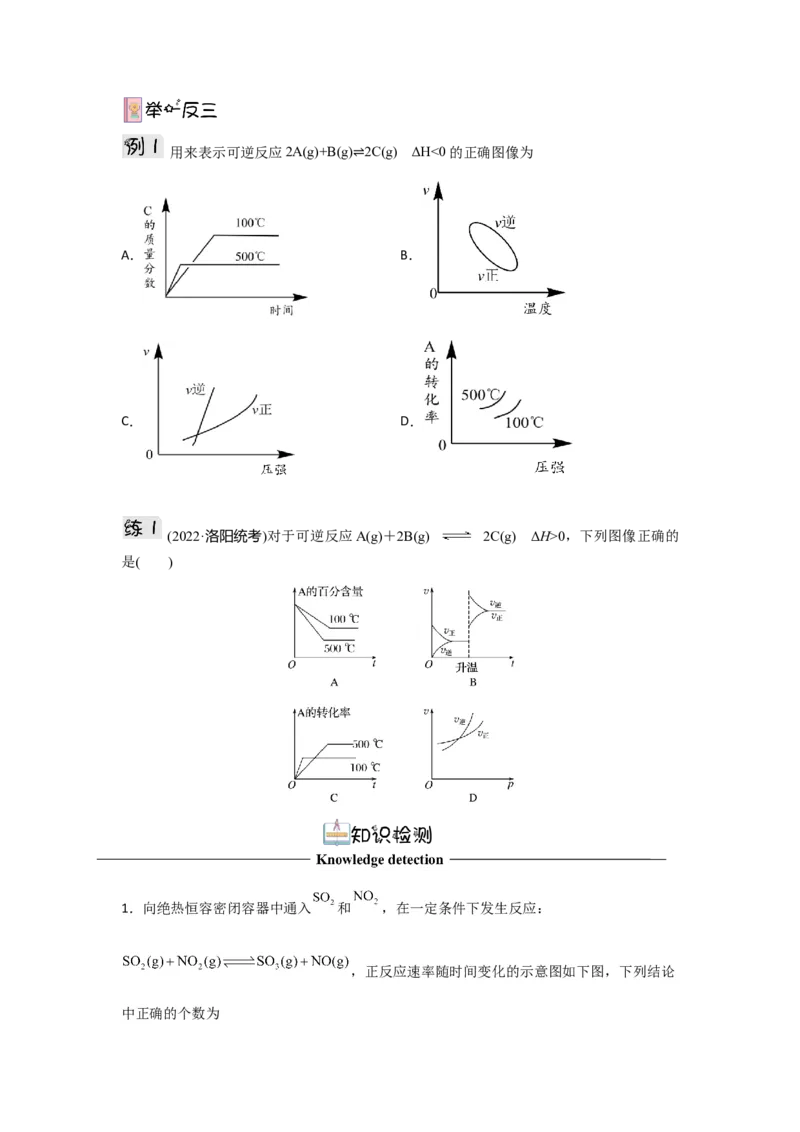
m+n>p+q m+np+q m+n0,下列图像正确的
是( )
1.向绝热恒容密闭容器中通入 和 ,在一定条件下发生反应:
,正反应速率随时间变化的示意图如下图,下列结论
中正确的个数为①反应在c点到达平衡
② 浓度:a点小于c点
③反应物的总能量高于生成物的总能量
④ , 段 的消耗量小于 段 的消耗量
⑤混合物颜色不再变化,说明反应达到平衡
⑥体系压强不再变化,说明反应达到平衡
⑦逆反应速率图像在此时间段内和上图趋势相同
⑧混合气体的平均摩尔质量不再变化,说明反应达到平衡
A.3个 B.4个 C.5个 D.6个
2.向绝热恒容密闭容器中通入SO 和NO ,在一定条件下发生反应:SO (g)+NO (g)
2 2 2 2
SO (g)+NO(g),正反应速率随时间变化的示意图如下图,下列结论中正确的个数为
3
①反应在c点到达平衡
②SO 浓度:a点小于c点
2
③反应物的总能量高于生成物的总能量
④Δt =Δt ,ab段NO 的消耗量小于bc段NO 的消耗量
1 2 2 2
⑤混合物颜色不再变化,说明反应达到平衡
⑥体系压强不再变化,说明反应达到平衡
⑦逆反应速率图像在此时间段内和上图趋势相同
⑧混合物气体的平均摩尔质量不再变化,说明反应达到平衡A.4个 B.5个 C.6个 D.7个
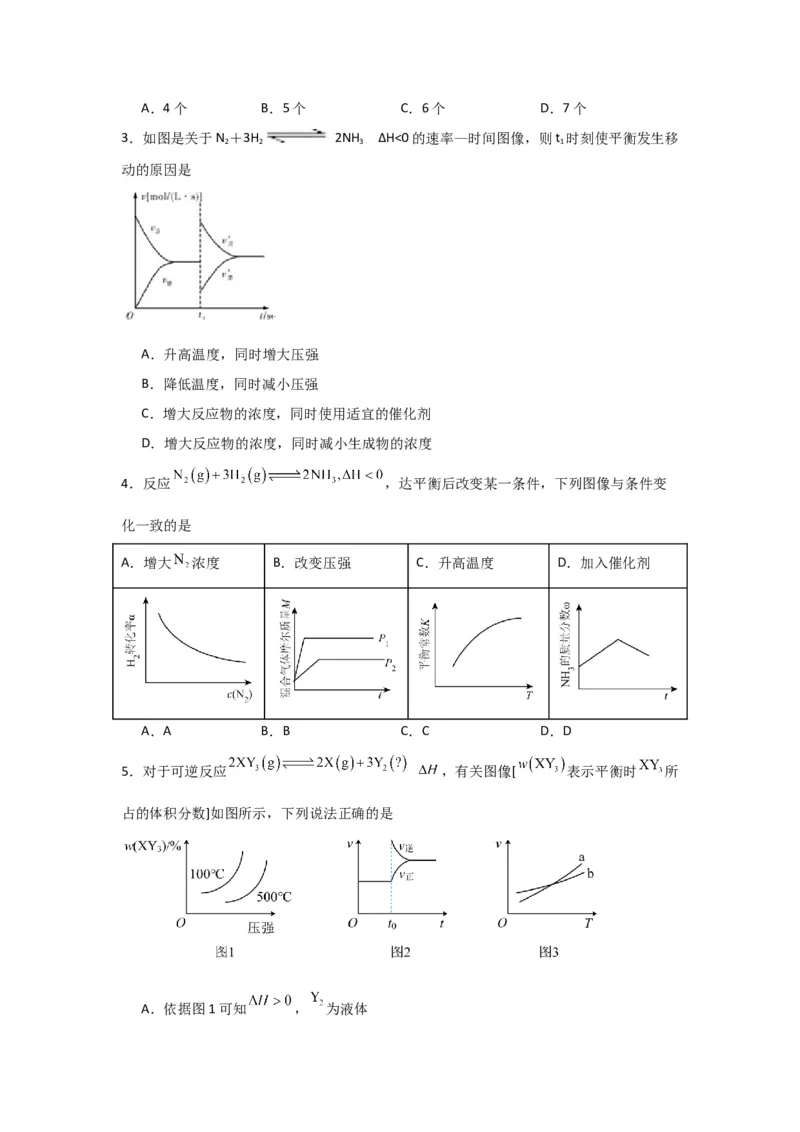
3.如图是关于N +3H 2NH ΔH<0的速率—时间图像,则t 时刻使平衡发生移
2 2 3 1
动的原因是
A.升高温度,同时增大压强
B.降低温度,同时减小压强
C.增大反应物的浓度,同时使用适宜的催化剂
D.增大反应物的浓度,同时减小生成物的浓度
4.反应 ,达平衡后改变某一条件,下列图像与条件变
化一致的是
A.增大 浓度 B.改变压强 C.升高温度 D.加入催化剂
A.A B.B C.C D.D
5.对于可逆反应 ,有关图像[ 表示平衡时 所
占的体积分数]如图所示,下列说法正确的是
A.依据图1可知 , 为液体B.图2中 时改变的条件可能为压缩容器体积
C.图3中曲线b表示的是该反应的逆反应速率
D.已知 时,平衡常数 。若在此温度下,测得某密闭容器中某时刻
, ,则此时
6.对于可逆反应 (?) ,有关图像 表示平衡时 所
占的体积分数]如图所示,下列说法正确的是
A.依据图1可知 , 为液体
B.图2中 时改变的条件不可能为压缩容器体积
C.图3中曲线b表示的是该反应的正反应速率
D.已知100℃时,平衡常数 。若在此温度下,测得某密闭容器中某时刻
mol⋅L , mol⋅L ,则此时
7.将一定量的 固体置于一初始体积为 且充有稀有气体的体积可变密闭容器中,
在 ℃下,发生反应 ,一段时间后
反应达到平衡,下列有关反应过程中的图像表示正确的是
A. B. C.D.
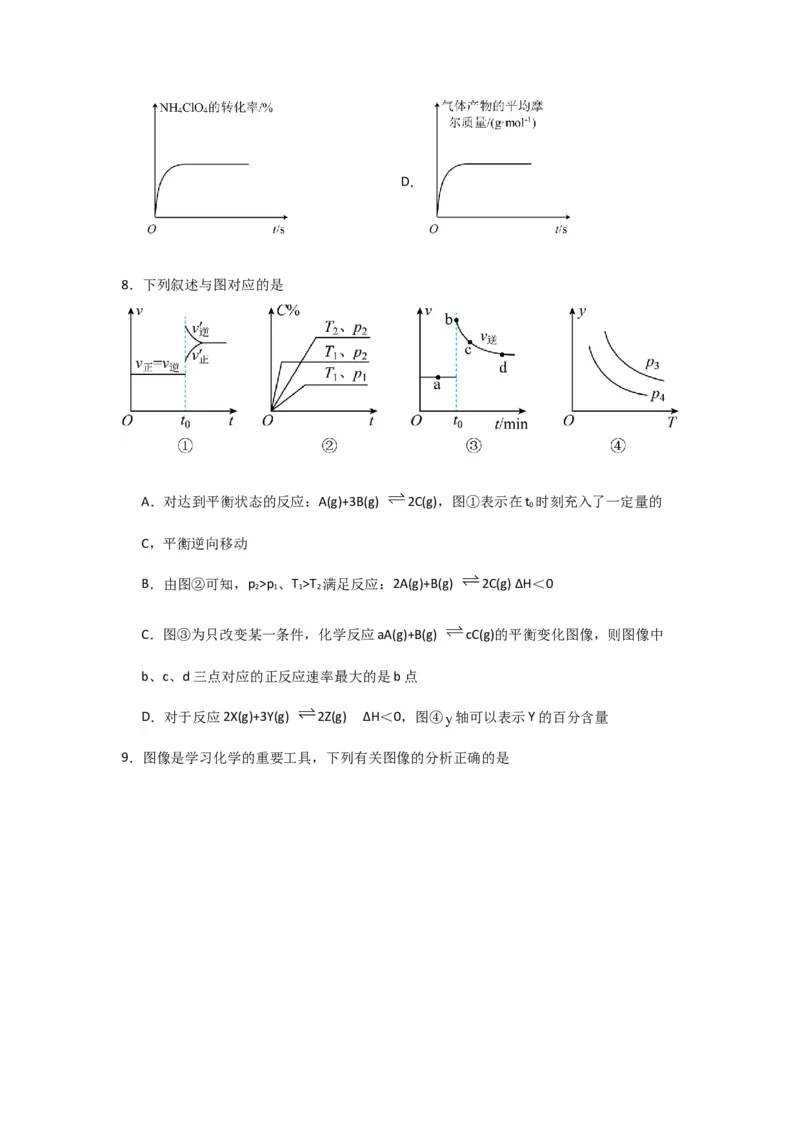
8.下列叙述与图对应的是
A.对达到平衡状态的反应:A(g)+3B(g) 2C(g),图①表示在t 时刻充入了一定量的
0
C,平衡逆向移动
B.由图②可知,p >p 、T >T 满足反应:2A(g)+B(g) 2C(g) ΔH<0
2 1 1 2
C.图③为只改变某一条件,化学反应aA(g)+B(g) cC(g)的平衡变化图像,则图像中
b、c、d三点对应的正反应速率最大的是b点
D.对于反应2X(g)+3Y(g) 2Z(g) ΔH<0,图④ 轴可以表示Y的百分含量
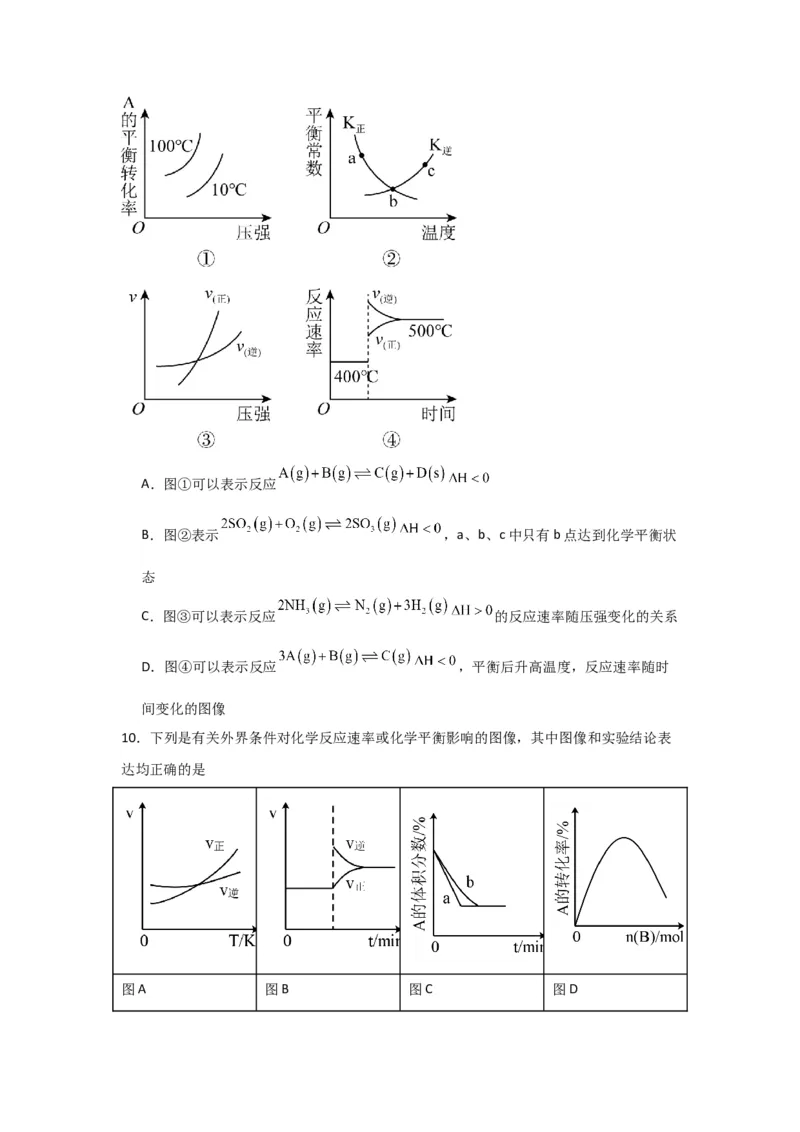
9.图像是学习化学的重要工具,下列有关图像的分析正确的是A.图①可以表示反应
B.图②表示 ,a、b、c中只有b点达到化学平衡状
态
C.图③可以表示反应 的反应速率随压强变化的关系
D.图④可以表示反应 ,平衡后升高温度,反应速率随时
间变化的图像
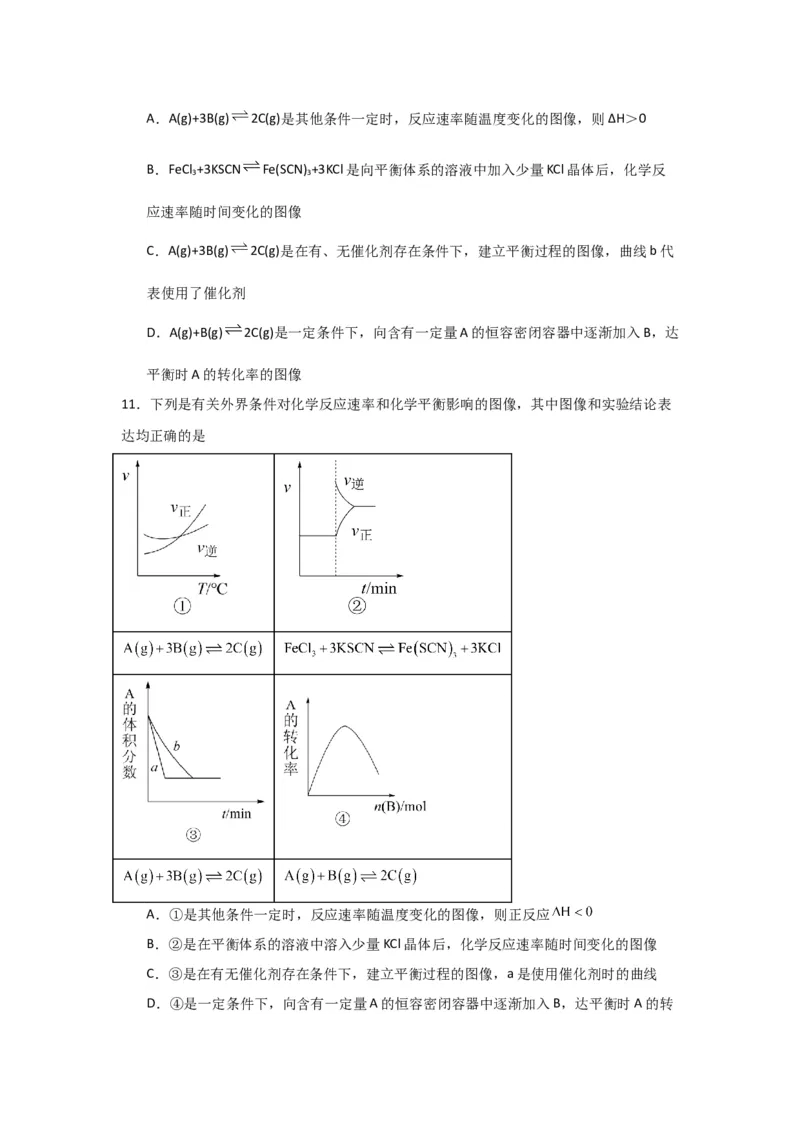
10.下列是有关外界条件对化学反应速率或化学平衡影响的图像,其中图像和实验结论表
达均正确的是
图A 图B 图C 图DA.A(g)+3B(g) 2C(g)是其他条件一定时,反应速率随温度变化的图像,则ΔH>0
B.FeCl +3KSCN Fe(SCN) +3KCl是向平衡体系的溶液中加入少量KCl晶体后,化学反
3 3
应速率随时间变化的图像
C.A(g)+3B(g) 2C(g)是在有、无催化剂存在条件下,建立平衡过程的图像,曲线b代
表使用了催化剂
D.A(g)+B(g) 2C(g)是一定条件下,向含有一定量A的恒容密闭容器中逐渐加入B,达
平衡时A的转化率的图像
11.下列是有关外界条件对化学反应速率和化学平衡影响的图像,其中图像和实验结论表
达均正确的是
A.①是其他条件一定时,反应速率随温度变化的图像,则正反应
B.②是在平衡体系的溶液中溶入少量KCl晶体后,化学反应速率随时间变化的图像
C.③是在有无催化剂存在条件下,建立平衡过程的图像,a是使用催化剂时的曲线
D.④是一定条件下,向含有一定量A的恒容密闭容器中逐渐加入B,达平衡时A的转化率的图像
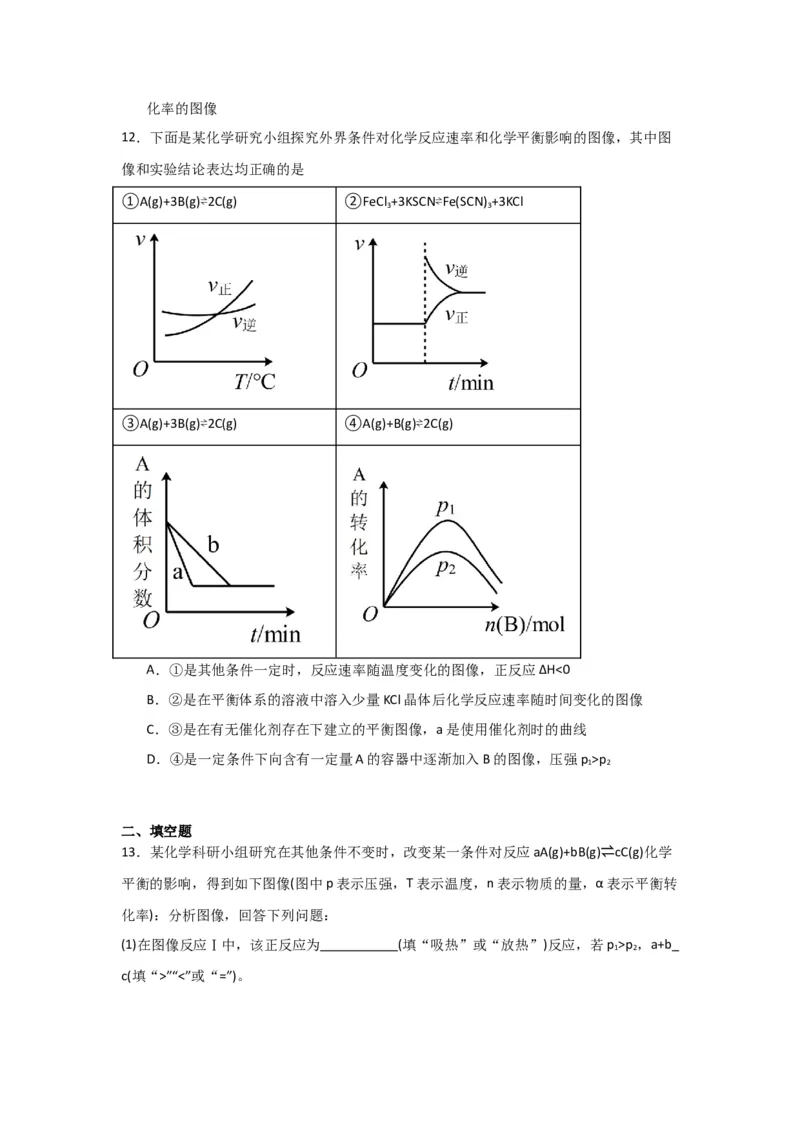
12.下面是某化学研究小组探究外界条件对化学反应速率和化学平衡影响的图像,其中图
像和实验结论表达均正确的是
①A(g)+3B(g)⇌2C(g) ②FeCl +3KSCN⇌Fe(SCN) +3KCl
3 3
③A(g)+3B(g)⇌2C(g) ④A(g)+B(g)⇌2C(g)
A.①是其他条件一定时,反应速率随温度变化的图像,正反应ΔH<0
B.②是在平衡体系的溶液中溶入少量KCl晶体后化学反应速率随时间变化的图像
C.③是在有无催化剂存在下建立的平衡图像,a是使用催化剂时的曲线
D.④是一定条件下向含有一定量A的容器中逐渐加入B的图像,压强p >p
1 2
二、填空题
13.某化学科研小组研究在其他条件不变时,改变某一条件对反应aA(g)+bB(g)⇌cC(g)化学
平衡的影响,得到如下图像(图中p表示压强,T表示温度,n表示物质的量,α表示平衡转
化率):分析图像,回答下列问题:
(1)在图像反应Ⅰ中,该正反应为 (填“吸热”或“放热”)反应,若p >p ,a+b
1 2
c(填“>”“<”或“=”)。(2)在图像反应Ⅱ中,T T (填“>”“<”或“=”),该正反应为 (填“吸
1 2
热”或“放热”)反应。
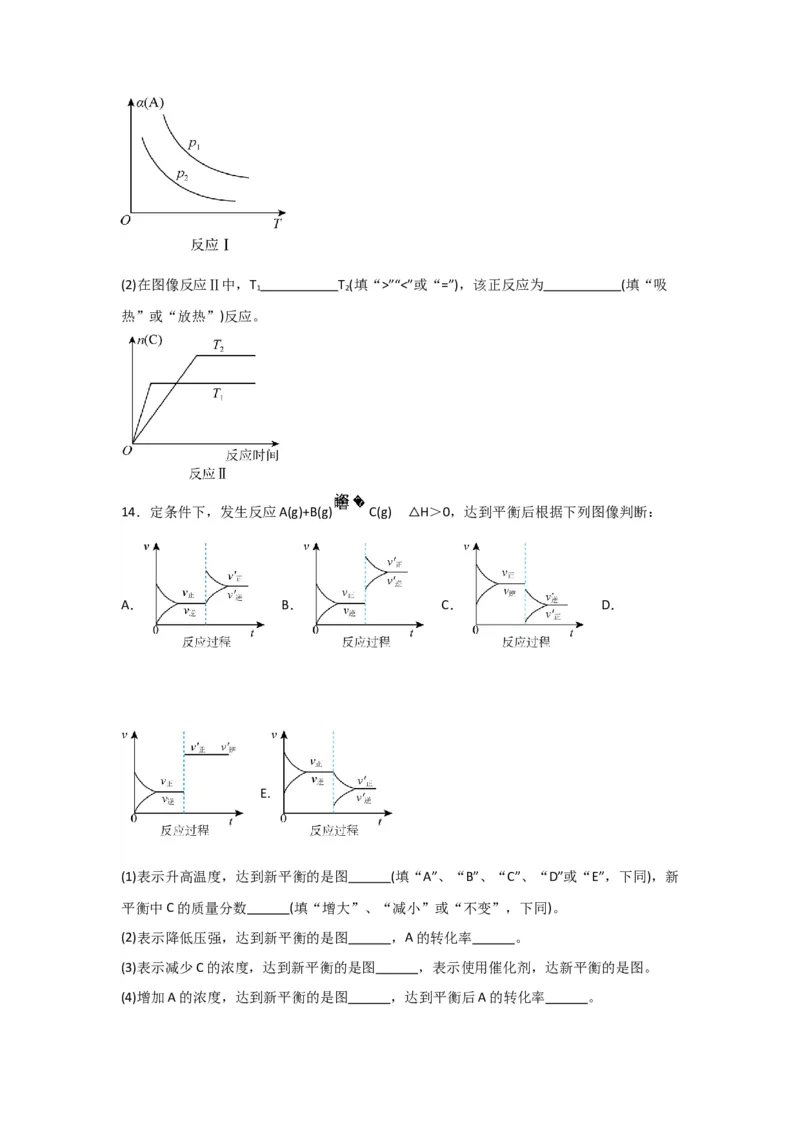
14.定条件下,发生反应A(g)+B(g) C(g) H>0,达到平衡后根据下列图像判断:
△
A. B. C. D.
E.
(1)表示升高温度,达到新平衡的是图 (填“A”、“B”、“C”、“D”或“E”,下同),新
平衡中C的质量分数 (填“增大”、“减小”或“不变”,下同)。
(2)表示降低压强,达到新平衡的是图 ,A的转化率 。
(3)表示减少C的浓度,达到新平衡的是图 ,表示使用催化剂,达新平衡的是图。
(4)增加A的浓度,达到新平衡的是图 ,达到平衡后A的转化率 。