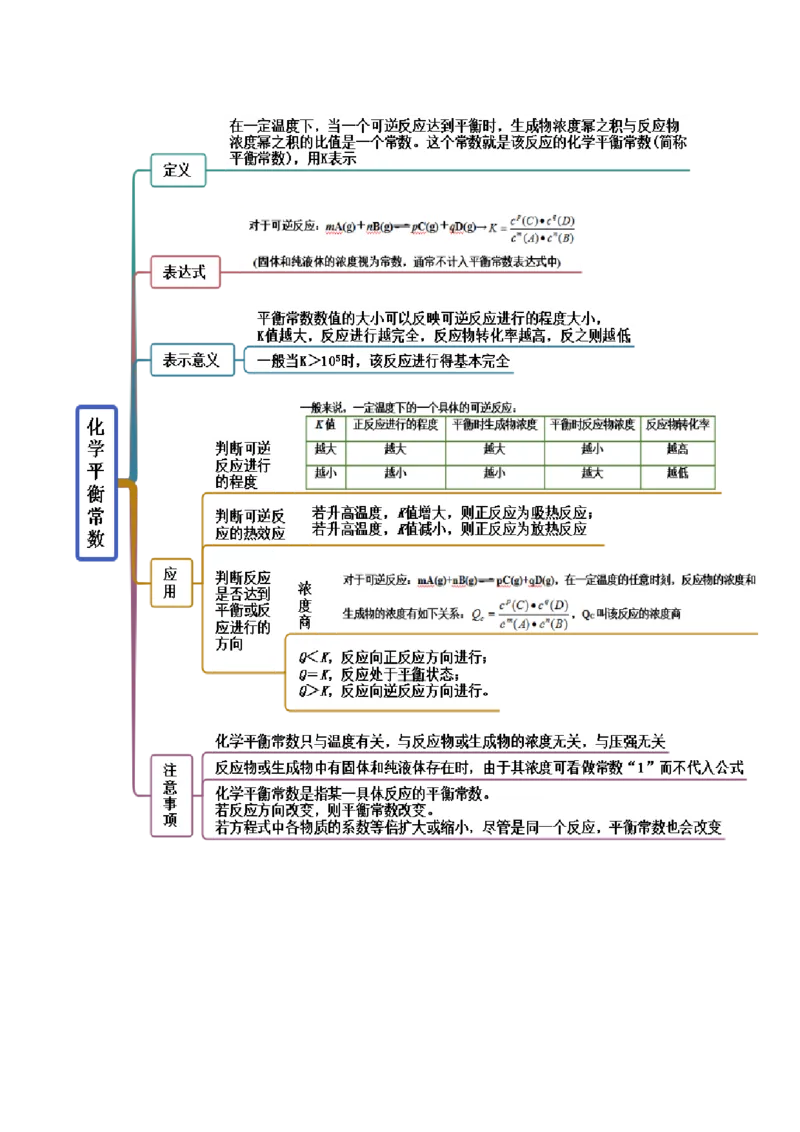
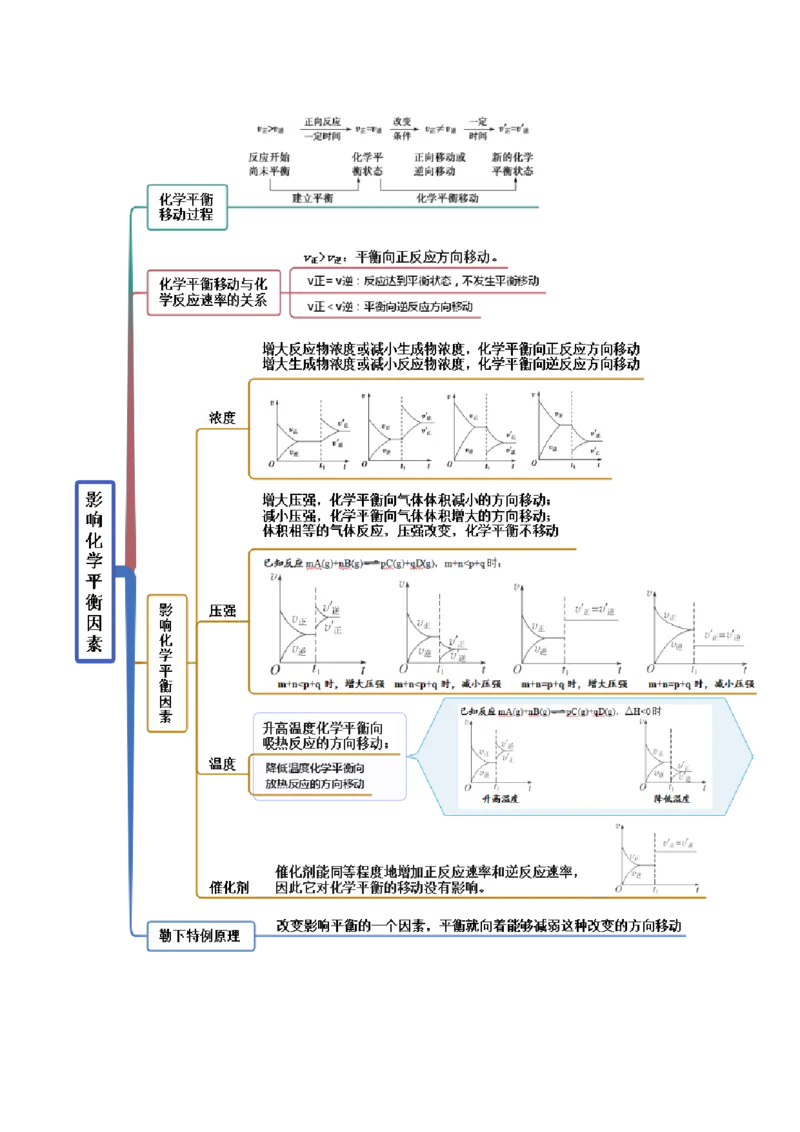
文档内容
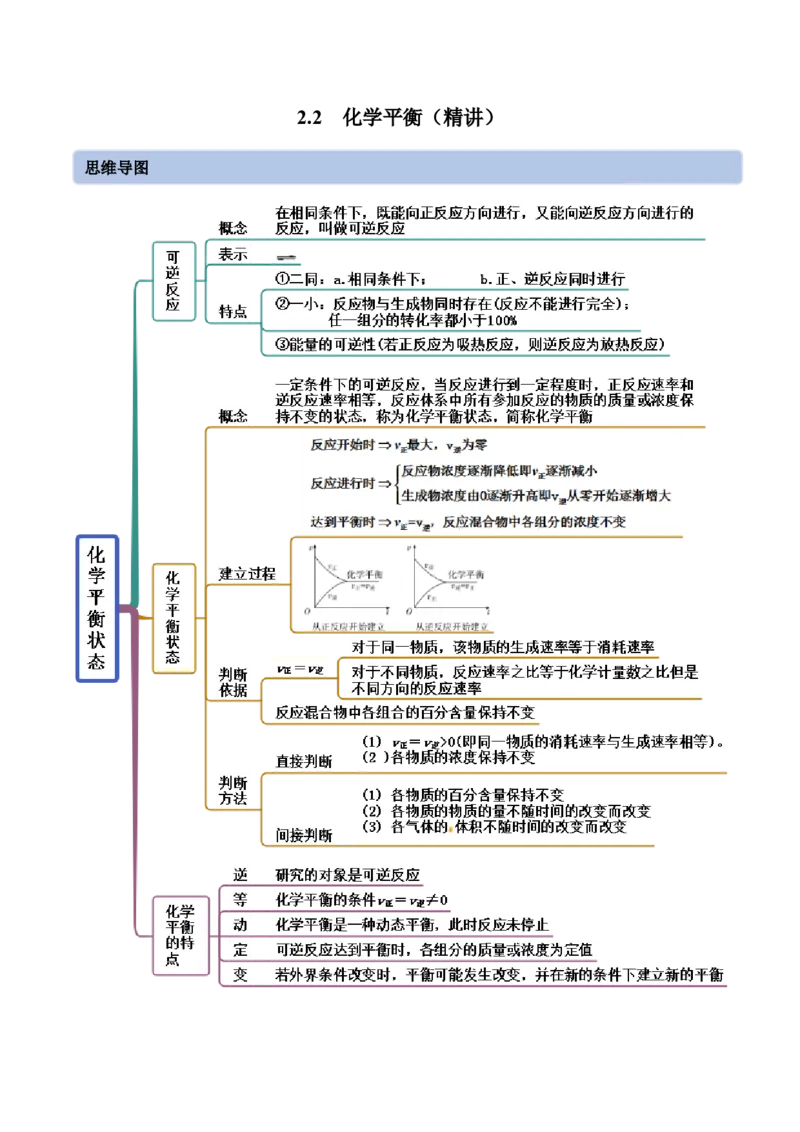
2.2 化学平衡(精讲)
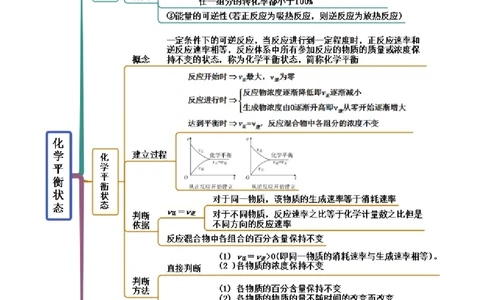
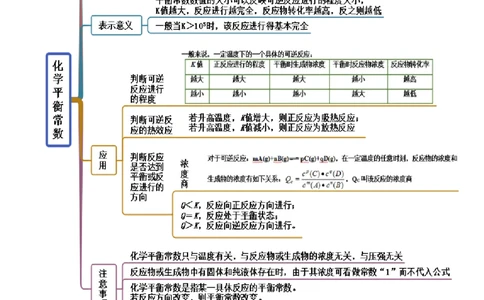
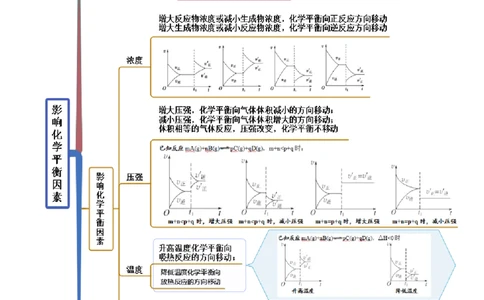
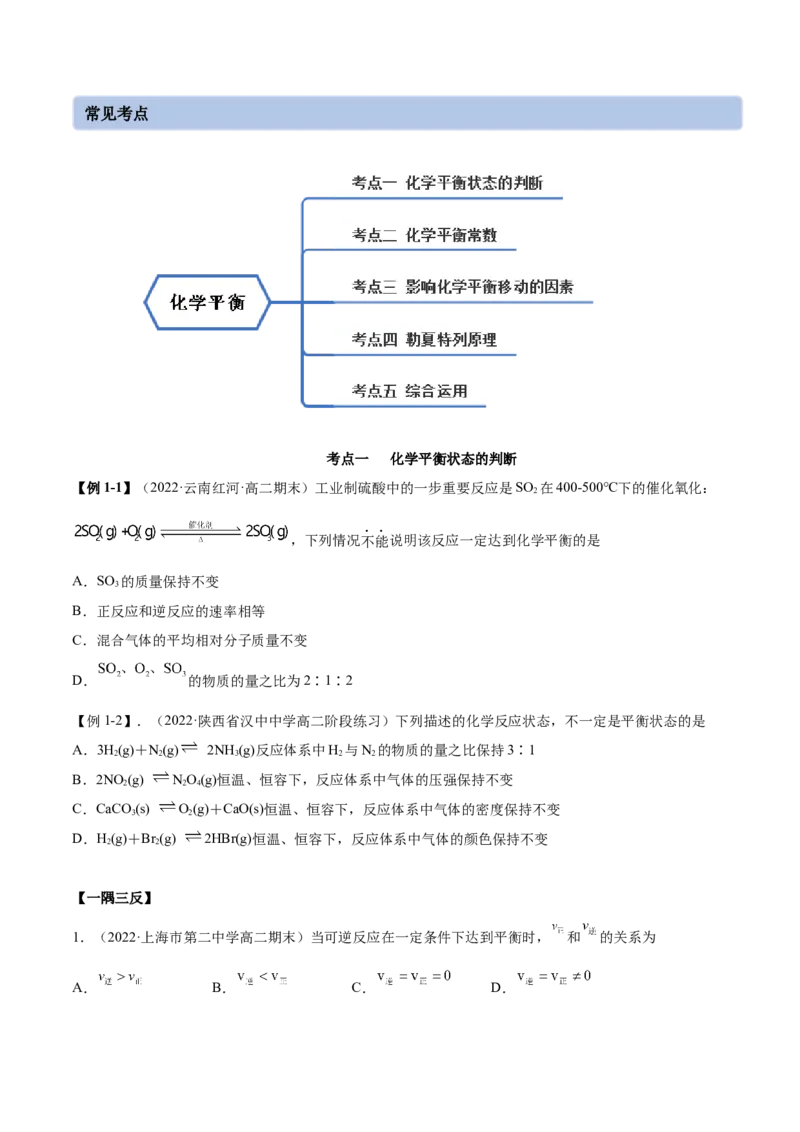
思维导图常见考点
考点一 化学平衡状态的判断
【例1-1】(2022·云南红河·高二期末)工业制硫酸中的一步重要反应是SO 在400-500℃下的催化氧化:
2
,下列情况不能说明该反应一定达到化学平衡的是
A.SO 的质量保持不变
3
B.正反应和逆反应的速率相等
C.混合气体的平均相对分子质量不变
D. 的物质的量之比为2∶1∶2
【例1-2】.(2022·陕西省汉中中学高二阶段练习)下列描述的化学反应状态,不一定是平衡状态的是
A.3H(g)+N(g) 2NH (g)反应体系中H 与N 的物质的量之比保持3∶1
2 2 3 2 2
B.2NO (g) NO(g)恒温、恒容下,反应体系中气体的压强保持不变
2 2 4
C.CaCO (s) O(g)+CaO(s)恒温、恒容下,反应体系中气体的密度保持不变
3 2
D.H(g)+Br (g) 2HBr(g)恒温、恒容下,反应体系中气体的颜色保持不变
2 2
【一隅三反】
1.(2022·上海市第二中学高二期末)当可逆反应在一定条件下达到平衡时, 和 的关系为
A. B. C. D.2.(2022·江西省信丰中学高二阶段练习)在一恒温、恒容密闭容器中,发生反应:
,下列描述中能表明反应已达到平衡状态的是
①混合气体的密度不变
②单位时间内生成1molD,同时消耗了2molA
③混合气体的平均相对分子质量不变
④C的物质的量浓度不变
⑤混合气体的压强不变
A.①②③ B.①③④ C.②③④ D.①②⑤
3.(2022·四川·射洪中学高二阶段练习)一定温度下,向恒容容器中充入1molA和2molB发生反应A(g)
+2B(g) 3C(g)+D(s)。下列能判断该反应达到平衡状态的是
A.混合⇌气体的平均相对分子质量不变
B.单位时间内消耗B的物质的量与生成C的物质的量之比为2:3
C.混合气体总的压强不再变化
D.反应物A和B的转化率相等
4.(2021·四川省内江市第六中学高二阶段练习)恒温条件下,可逆反应: 在
体积固定的密闭容器中进行,下列可作为判断反应达到平衡状态的标志的是
①单位时间内生成nmolO 的同时生成nmolNO
2 2
②单位时间内生成nmolNO的同时生成nmolNO
2
③用NO 、NO、O 表示的反应速率的比为2:2:1的状态
2 2
④混合气体的颜色不再改变的状态
⑤混合气体的密度不再改变的状态
⑥混合气体的压强不再改变的状态
⑦混合气体的平均相对分子质量不再改变的状态
A.①④⑥⑦ B.②③⑤⑦ C.②④⑥⑦ D.②④⑤⑦
考点二 化学平衡常数
【例2-1】下列关于平衡常数的说法正确的是:
A.K不变,平衡可能移动
B.同一个反应的化学计量数增大2倍,K值也增大两倍
C.K值越大,反应速率也越快D.对于合成氨反应,压强增大,平衡右移,K增大
【例2-2】在一定体积的密闭容器中,进行如下化学反应:CO (g)+H (g) CO(g)+H O(g),
2 2 2
K为化学平衡常数,其中K和温度的关系如下表:
t/℃ 700 800 830 1 000 1 200
K 0.6 0.9 1.0 1.7 2.6
根据以上信息推断以下说法正确的是
A.此反应为放热反应
B.此反应只有达到平衡时,密闭容器中的压强才不会变化
C.此反应达到1 000℃时的反应速率比700℃时大
D.该反应的化学平衡常数越大,反应物的转化率越低
【一隅三反】
1.关于化学平衡常数,下列说法不正确的是( )
A.化学平衡常数不随反应物或生成物的浓度的改变而改变
B.对于一定温度下的同一个反应,其正反应和逆反应的化学平衡常数的乘积等于1
C.温度越高,K值越大
D.化学平衡常数随温度的改变而改变
2.对于反应3Fe(s)+4HO(g) Fe O(s)+4H(g)的平衡常数,下列说法正确的是
2 3 4 2
A.增大HO(g)的浓度或减小H 的浓度,会使平衡常数减小
2 2
B.改变反应的温度,平衡常数不一定变化
C.K=
D.K=
3.可逆反应:2SO +O 2SO 达到平衡状态时,保持恒温恒容向容器中加入一定量的O。下列说法
2 2 3 2
正确的是(K为平衡常数,Q为浓度商)( )
A.Q不变,K变大,O 转化率增大
2
B.Q不变,K变大,SO 转化率减小
2
C.Q变小,K不变,O 转化率减小
2
D.Q增大,K不变,SO 转化率增大
2考点三 影响化学平衡移动的因素
【例3】(2022·贵州·毕节市第一中学高二阶段练习)有一处于平衡状态的反应:3A(s)+2B(g)
3C(g),ΔH>0。为了使平衡向生成C的方向移动,应选择的条件是
①高温 ②低温 ③高压 ④低压 ⑤加催化剂
A.①③ B.①③⑤ C.①④ D.②④⑤
【一隅三反】
1.(2022·广西桂林·高二期末)在一定条件下的密闭容器中,反应 达到
平衡,下列操作能使气体颜色加深的是
A.增大 B.降低温度 C.减小容器体积 D.加入催化剂
2.(2022·湖南·益阳平高学校高二期末)一定条件下,反应 在恒容密闭容器
中进行,关于该反应的说法错误的是
A.生成2molNO的同时生成2mol ,则反应达到平衡状态
B.反应平衡后升高温度如果气体颜色变浅,则反应是吸热反应
C.减小容器的体积增大压强,则NO气体的浓度一定减小
D.平衡后不改变其他条件,向容器中再充入一定量的 ,再次平衡后 的体积分数比原平衡大
3.(2022·上海市第二中学高二期末)对于平衡体系 ,增大压强时(其他条
件不变),C的含量减少,则下列关系中正确的是
A. B. C. D.
考点四 勒夏特列原理
【例4】下列事实不能用勒夏特列原理解释的是
A.对CO(g)+NO (g) CO(g)+NO(g)平衡体系,增大压强可使颜色变深
2 2
B.氯水中存在下列平衡:Cl+H O HCl+HClO,当加入AgNO 溶液后,溶液颜色变浅
2 2 3
C.对2NO (g) NO(g),升高温度平衡体系颜色变深
2 2 4D.夏天从冰箱拿出的啤酒刚一开启即涌出大量泡沫。
【一隅三反】
1(2022·上海中学东校高二期末)合成氨反应为 ,在合成氨工业
中常采取的下列措施不能用勒夏特列原理来解释的是
A.及时补充氮气和氢气 B.使用铁触媒做催化剂
C.将氨液化及时分离出反应器 D.压强增至20MPa~50MPa
2.(2022·四川成都·高二期末)下列操作或事实不能用勒夏特列原理解释的是
A. ,把 球浸泡在冰水中,气体颜色变浅
B.用饱和食盐水除去 中的 ,可减少 的损失
C.对 、 和 组成的平衡体系加压后颜色变深
D.向含有 的红色溶液中加入铁粉,振荡,溶液颜色变浅或褪去
3.(2022·浙江宁波·高二阶段练习)化学和生活密切相关,下列生产生活实例中不能用勒夏特列原理解释
的是
A.摇晃后的可乐开启后有大量气泡
B.二氧化氮与四氧化二氮的平衡体系,加压缩小体积后颜色加深
C.酸遇紫色石蕊试剂变红
D.生产硫酸的过程中用过量的空气和二氧化硫反应
考点五 综合运用
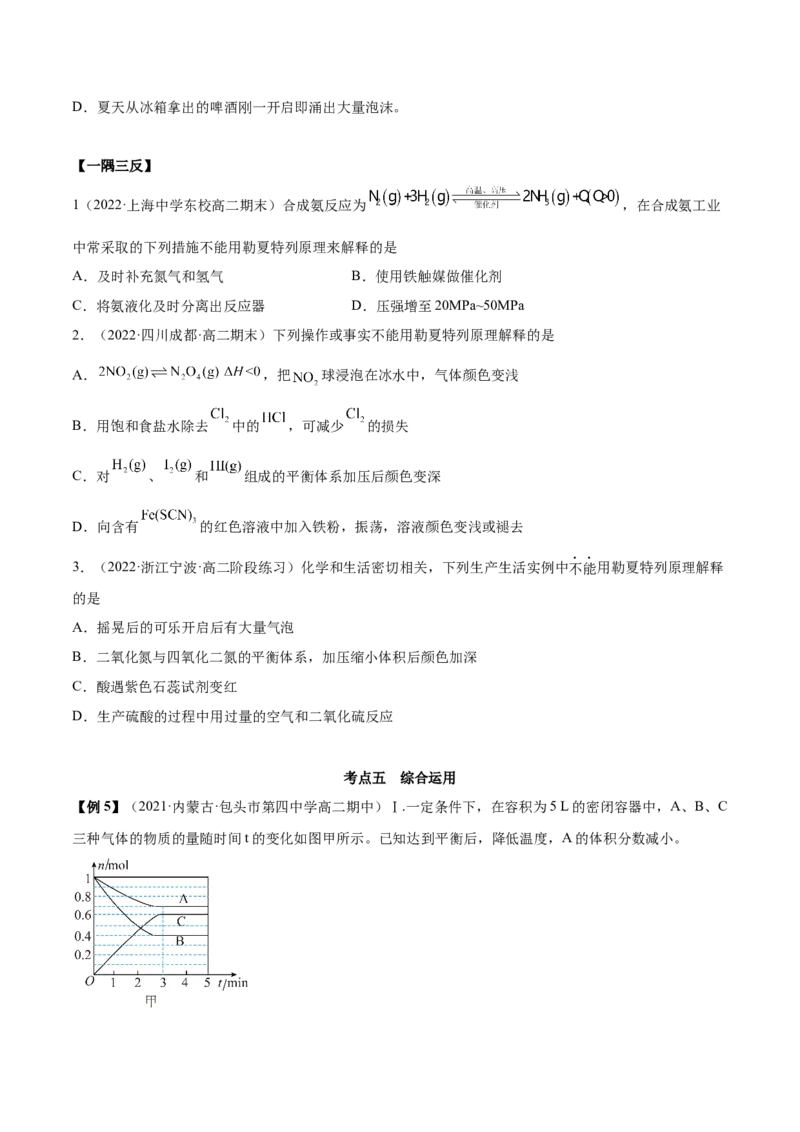
【例5】(2021·内蒙古·包头市第四中学高二期中)Ⅰ.一定条件下,在容积为5 L的密闭容器中,A、B、C
三种气体的物质的量随时间t的变化如图甲所示。已知达到平衡后,降低温度,A的体积分数减小。(1)该反应的化学方程式为_______。
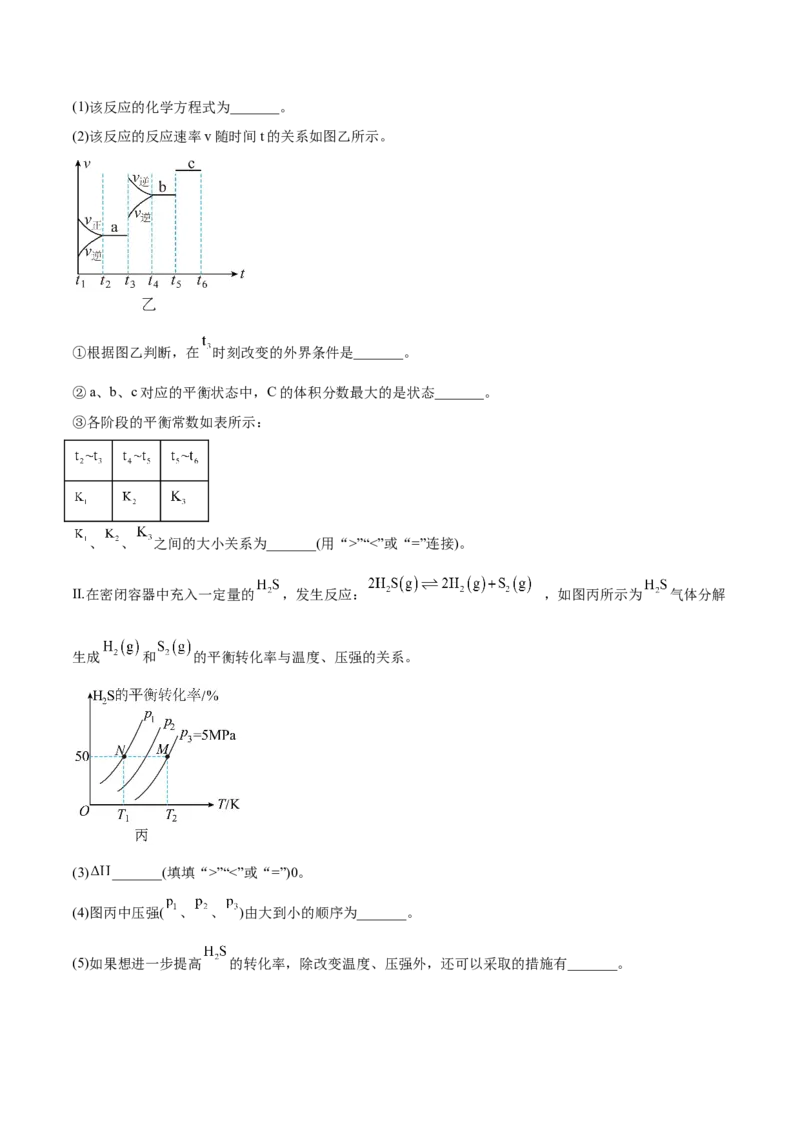
(2)该反应的反应速率v随时间t的关系如图乙所示。
①根据图乙判断,在 时刻改变的外界条件是_______。
②a、b、c对应的平衡状态中,C的体积分数最大的是状态_______。
③各阶段的平衡常数如表所示:
、 、 之间的大小关系为_______(用“>”“<”或“=”连接)。
Ⅱ.在密闭容器中充入一定量的 ,发生反应: ,如图丙所示为 气体分解
生成 和 的平衡转化率与温度、压强的关系。
(3) _______(填填“>”“<”或“=”)0。
(4)图丙中压强( 、 、 )由大到小的顺序为_______。
(5)如果想进一步提高 的转化率,除改变温度、压强外,还可以采取的措施有_______。【一隅三反】
1.(2021·陕西·渭南市华州区咸林中学高二阶段练习)在一定体积的密闭容器中,进行如下化学反应:
。其化学平衡常数K和温度t的关系如下表所示:
83
t/℃ 700 800 1000 1200
0
K 0.6 0.9 1.0 1.7 2.6
回答下列问题:
(1)该反应的化学平衡常数表达式为K=___________。
(2)该反应为___________(填“吸热”或“放热”)反应。
(3)下列几种状态可判断为化学平衡状态的是___________(多选扣分)。
a.容器中压强不再改变 b.混合气体中c(CO)不变c. v (H )=v (H O) d. c(CO)=c(CO)e. 700℃时,
正 2 逆 2 2
某时刻测得CO、HO、CO、H 的浓度分别为0.01 、0.03 、0.01 、0.05
2 2 2
(4)某温度下,平衡浓度符合下式: ,判断此时的温度为___________℃。
2.(2022·广西河池·高二期末)NH 是一种重要的化工产品,可用于生产尿素[CO(NH)]、处理烟气等。
3 2 2
(1)工业上合成尿素的反应:2NH (g)+CO (g) CO(NH)(s)+HO(g) H
3 2 2 2 2
△
已知合成尿素的反应分两步进行:
2NH (g)+CO (g) NH COONH(s) H=—159.47kJ·mol-1
3 2 2 4 1
△
NH COONH(s) CO(NH)(s)+HO(g) H=+72.49kJ·mol-1
2 4 2 2 2 2
△
则 H=____。
(2)△某实验小组为了模拟工业上合成尿素,在恒温恒容的真空密闭容器中充入一定量的CO
2
和NH
3
发生反应:
2NH (g)+CO (g) CO(NH)(s)+HO(g),反应过程中混合气体中NH 的体积分数如图所示。
3 2 2 2 2 3①点的正反应速率v (CO)____B点的逆反应速率v (CO)(填“>”“<”或“=”)。
正 2 逆 2
②下列能说明该反应达到平衡状态的是____(填字母)。
a.NH 、CO、HO的体积之比为2:1:1
3 2 2
b.体系的压强保持不变
c.单位时间内消耗1molH O同时生成2molNH
2 3
d.v (NH )=2v (CO)
正 3 逆 2
③对于有气体参与的反应,平衡常数K 可用气体组分(B)的平衡分压p(B)代替该气体的物质的量浓度
p
c(B)。实验测得体系平衡时的压强为10MPa,列式计算该反应的平衡常数K =____(提示:写出K 的表达式
p p
再代入数据进行计算,分压=总压×体积分数)。
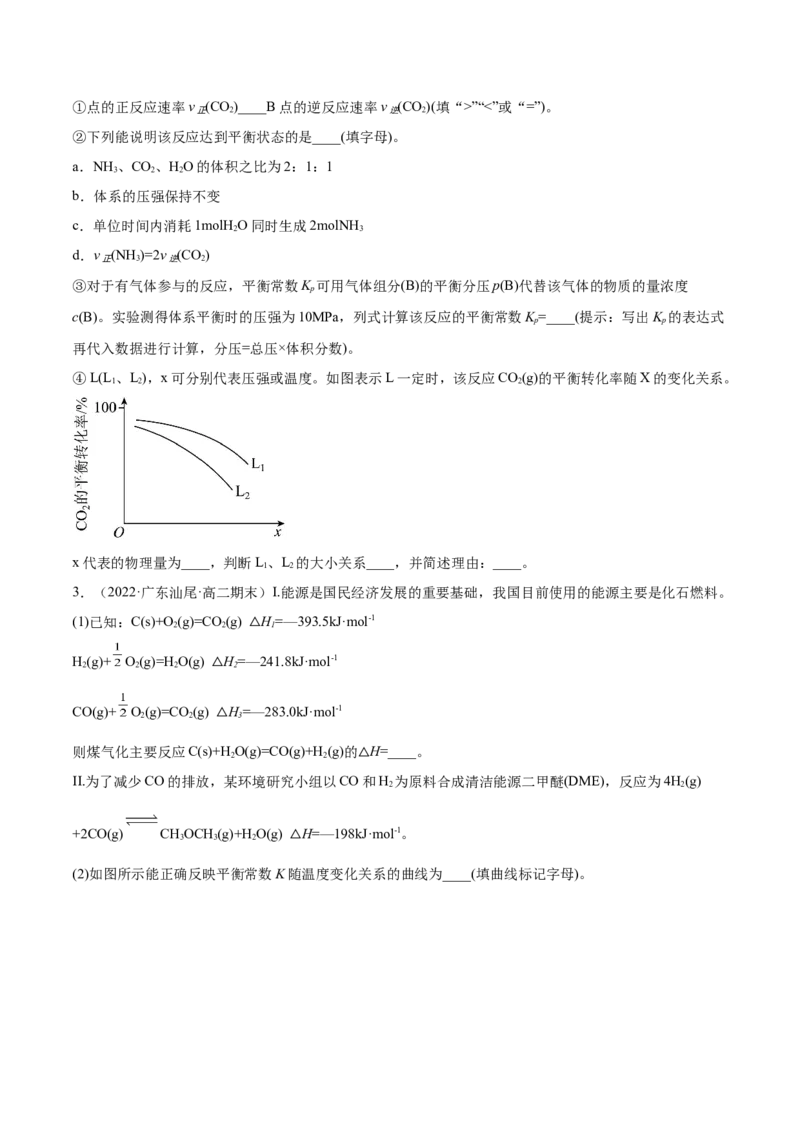
④L(L、L),x可分别代表压强或温度。如图表示L一定时,该反应CO(g)的平衡转化率随X的变化关系。
1 2 2
x代表的物理量为____,判断L、L 的大小关系____,并简述理由:____。
1 2
3.(2022·广东汕尾·高二期末)I.能源是国民经济发展的重要基础,我国目前使用的能源主要是化石燃料。
(1)已知:C(s)+O(g)=CO (g) H=—393.5kJ·mol-1
2 2 1
△
H(g)+ O(g)=HO(g) H=—241.8kJ·mol-1
2 2 2 2
△
CO(g)+ O(g)=CO (g) H=—283.0kJ·mol-1
2 2 3
△
则煤气化主要反应C(s)+HO(g)=CO(g)+H (g)的 H=____。
2 2
II.为了减少CO的排放,某环境研究小组以CO△和H
2
为原料合成清洁能源二甲醚(DME),反应为4H
2
(g)
+2CO(g) CHOCH (g)+HO(g) H=—198kJ·mol-1。
3 3 2
△
(2)如图所示能正确反映平衡常数K随温度变化关系的曲线为____(填曲线标记字母)。(3)在一定温度下,向2.0L固定容积的密闭容器中充入2molH 和1molCO,经过一段时间后,反应4H(g)
2 2
+2CO(g) CHOCH (g)+HO(g)达到平衡。反应过程中测得的部分数据见表:
3 3 2
时间/min 0 20 40 80 100
n(H )/mol 2.0 1.4 0.85 0.4 —
2
n(CO)/mol 1.0 — 0.425 0.2 0.2
n(CHOCH )/mol 0 0.15 — — 0.4
3 3
n(H O)/mol 0 0.15 0.2875 0.4 0.4
2
①0~20min的平均反应速率v(CO)=____mol·L-1·min-1。
②达到平衡时,H 的转化率为____。
2
③在上述温度下,该反应的平衡常数K=____。
④能表明该反应达到平衡状态的是____(填字母)。
A.CO的转化率等于HO的产率 B.混合气体的平均相对分子质量不变
2
C.v(CO)与v(H )的比值不变 D.混合气体的密度不变
2
⑤在上述温度下,向平衡后的2L容器中再充入0.4molH 和0.4molCHOCH (g),则化学平衡____(填“向
2 3 3
左”“向右”或“不”)移动。倒卖拉黑,关注更新免费领取,淘宝唯一每月更新店铺:知二教育