文档内容
第二章 分子结构与性质
第二节 分子的空间结构
2.3.1共价键的极性
1.能从共用电子对是否发生偏移的角度认识键的极性的实质是成键原子分别带正电和负电。
2.知道分子可以分为极性分子和非极性分子。
3.知道分子极性和分子中键的极性、分子的空间结构密切相关。
教学重点:极性分子与非极性分子的判断
教学难点:极性分子与非极性分子的判断
一、共价键的分类
分类标准 类型
共用电子对数
电子云重叠方式
共用电子对是否偏移
【学生活动】
写出H、O、N、HCl、CO、HO、CH、NH 的电子式和结构式。
2 2 2 2 2 4 3
二、键的极性
极性共价键 非极性共价键
实例
成键原子 ________元素的原子 _________元素的原子电子对 ______________ ____________
成键原子的 一个原子呈正电性(δ+),一个原子呈
电中性
电性 负电性(δ-)
存在 _____________________________ __________________________
三、分子的极性
分子有 分子和 分子。分子的极性与分子的空间结构及分子中键的极性有关。
1.极性分子和非极性分子的定义
(1)极性分子:分子的正电中心和负电中心 ,使分子的某一部分呈正电性,另一部分
呈负电性,这样的分子是极性分子。如HCl、HO等。
2
(2)非极性分子:分子的正电中心和负电中性 ,使分子没有带正电和带负电的两部分,这
样的分子是非极性分子。如P、CO 等。
4 2
【学生活动2】
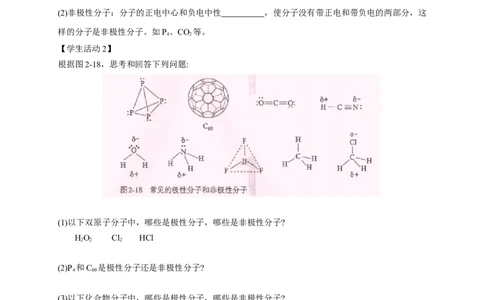
根据图2-18,思考和回答下列问题:
(1)以下双原子分子中,哪些是极性分子,哪些是非极性分子?
HO Cl HCl
2 2 2
(2)P 和C 是极性分子还是非极性分子?
4 60
(3)以下化合物分子中,哪些是极性分子,哪些是非极性分子?
CO HCN HO NH BF CH CHCl
2 2 3 3 4 3
2.从向量的角度理解分子的极性
(1)若分子中共价键的极性的向量和等于 0,则分子中没有带正电和带负电的两部分,为非极性分
子,如BF、CH 等。
3 4实例
解释
(2)若分子中共价键的极性的向量和不等于 0,则分子中存在带正电和带负电的两部分,为极性分
子,如HO、NH 等。
2 3
实例
解释
四、键的极性与分子的极性关系
(1)只含有非极性键的双原子分子或多原子分子大多是 ,如O、H、P、C 。
2 2 4 60
(2)含有极性键的双原子分子都是 ,如HCl、HF、HBr。
(3)含有极性键的多原子分子,立体构型对称的是 ;立体构型不对称的是
。
【学生活动】
1.常见ABn型分子的极性
类型 实例 键的极性 立体异构 分子的极性
X H、N
2 2 2
XY HCl、NO
CO、CS
2 2
XY
2
SO
2
(X Y)
2
HO、HS
2 2
XY BF
3 3
NH
3
XY CH、CCl
4 4 4
2.O 是V形分子,其空间结构不对称,故O 为 分子。
3 3
HO 分子不是直线形,两个H原子犹如在半展开的书的两面上,即结构不对称,为 分
2 2
子。【结论】
若中心原子有孤电子对,则为极性分子;若无孤电子对,则为非极性分子。如 CS 、BF 、SO 、
2 3 3
CH 为非极性分子;HS、SO 、NH 、PCl 为极性分子。
4 2 2 3 3
五、键的极性对化学性质的影响
键的极性对物质的化学性质有重要的影响。例如,羧酸是一大类含羧基(—COOH)的有机酸,羧基
可电离出H+而呈酸性。羧酸的酸性可用 的大小来衡量,pK ,酸性 。
a
【学生活动】
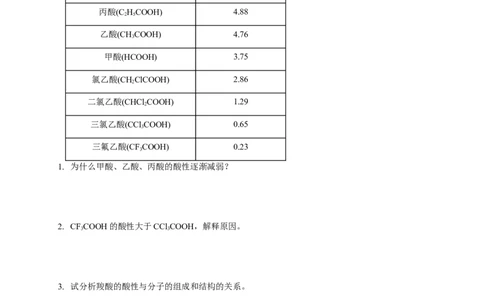
有机酸的酸性
羧酸 pKa
丙酸(C HCOOH) 4.88
2 5
乙酸(CHCOOH) 4.76
3
甲酸(HCOOH) 3.75
氯乙酸(CHClCOOH) 2.86
2
二氯乙酸(CHCl COOH) 1.29
2
三氯乙酸(CCl COOH) 0.65
3
三氟乙酸(CFCOOH) 0.23
3
1. 为什么甲酸、乙酸、丙酸的酸性逐渐减弱?
2. CFCOOH的酸性大于CCl COOH,解释原因。
3 3
3. 试分析羧酸的酸性与分子的组成和结构的关系。
1. 用VSEPR模型预测下列分子或离子的立体结构,其中正确的是()
A. H O与BeCl 为角形(V形) B. CS 与SO 为直线形
2 2 2 2
C. BF 与PCl 为三角锥形 D. SO 与CO2− 为平面三角形
3 3 3 32. 下列说法中正确的是()
A. CH 、C H 、HCN都是含有极性键的非极性分子
4 2 2
B. CO 与SO 的立体构型相似,都是非极性分子
2 2
C. 分子中含有1个手性碳原子
D. 含氧酸可用通式(HO) RO 表示,若m值越大,则含氧酸的酸性越强
m n
3. 已知H O 分子的空间结构可在二面角中如图所示,下列有关H O 结构的说法正确的是()
2 2 2 2
A. H O 中有3个σ键、1个π键
2 2
B. H O 为非极性分子
2 2
C. H O 中氧原子为sp杂化
2 2
D. H O 沸点高达158℃,可推测H O 分子间可形成氢键
2 2 2 2
4. 关于CS 、SO 、N H 三种物质的说法中正确的是( )
2 2 3
A. CS 在水中的溶解度很小,是由于其属于极性分子
2
B. SO 和N H 均易溶于水,原因之一是它们都是极性分子
2 3
C. CS 和SO 的分子结构相似,均为非极性分子
2 2
D. N H 在水中溶解度很大只是由于N H 分子有极性
3 3
5. 下列有关物质结构与性质的说法正确的是( )
A. CH OH能形成分子内氢键,则CH OH与水以任意比例互溶
3 3
B. C H 、N H 分子组成相同,则它们的分子所有原子共平面
2 4 2 4
C. C 溶于CS 形成红色溶液,则C 是非极性分子
60 2 60
D. 间二甲苯只有一种结构,则苯环不存在单键和双键交替