文档内容
第二章 海水中的重要元素—钠和氯
第三节 物质的量
第二课时 气体摩尔体积
【学习目标】1.联系宏观物质的体积特点,通过对比探究,能从宏观和微观相结合的角度理解影响
宏观物质体积大小的主要因素和外部条件对气体体积大小的影响,培养宏观辨识与微观探析的化学核心素
养。
2.通过讨论交流、对比归纳,增强理解和掌握气体摩尔体积的概念,初步理解阿伏加德罗定律的内
容,培养证据推理与模型认知的化学核心素养。
3.通过练习巩固、归纳小结,能基于物质的量认识物质的组成及变化,建立物质的量、质量、摩尔
体积之间计算的模型,熟悉阿伏加德罗定律的应用。
【学习重点】气体摩尔体积的理解及应用、阿伏加德罗定律。
【学习难点】阿伏加德罗定律及其推论的理解。
【课前预习】
旧知回顾:1.物质的量(n)、质量(m)、摩尔质量(M)三者之间的关系为 。其中摩尔质量
的定义为 ,具有的三性为
。
2.气体 容易 被压缩(填“容易”或“难”,下同),说明气体分子间距离比较 ,(填“大”或
“小”,下同);温度越高,气体分子间距离 ;压强越大,气体分子间距离 ;而固体和液
体的体积 被压缩,这说明固体和液体分子间距离非常 。
新知预习:1.气体摩尔体积是 ,符号 ,单位 。定义
式为 。气体摩尔体积的数值取决于气体所处的 和 。标准状况下
(温度为 ,压强为 )V =_ _。
m
2.根据表中数据计算(00C、101KPa时):
物质名称 密度(g/L) 1mol气体的质量(g) 1mol气体体积(L)
二氧化碳 1.977
空气 1.293
【课中探究】
情景导入:在科学研究或实际生产中,涉及气态物质时,测量体积往往比称量质量更方便。所以,气体一
般都是测量体积,而不是称量质量。我们在前面的学习中已经知道了两个计算物质的量的公式:n=N/N 和
A
n=m/M,如果已知某气体的体积,能否直接应用上面的公式计算出某气体的物质的量呢?显然不能,因为
既不知道气体的分子数,也不知道气体的质量。那么,气体体积与物质的量之间有什么关系呢?本节课我们就来解决这个问题。
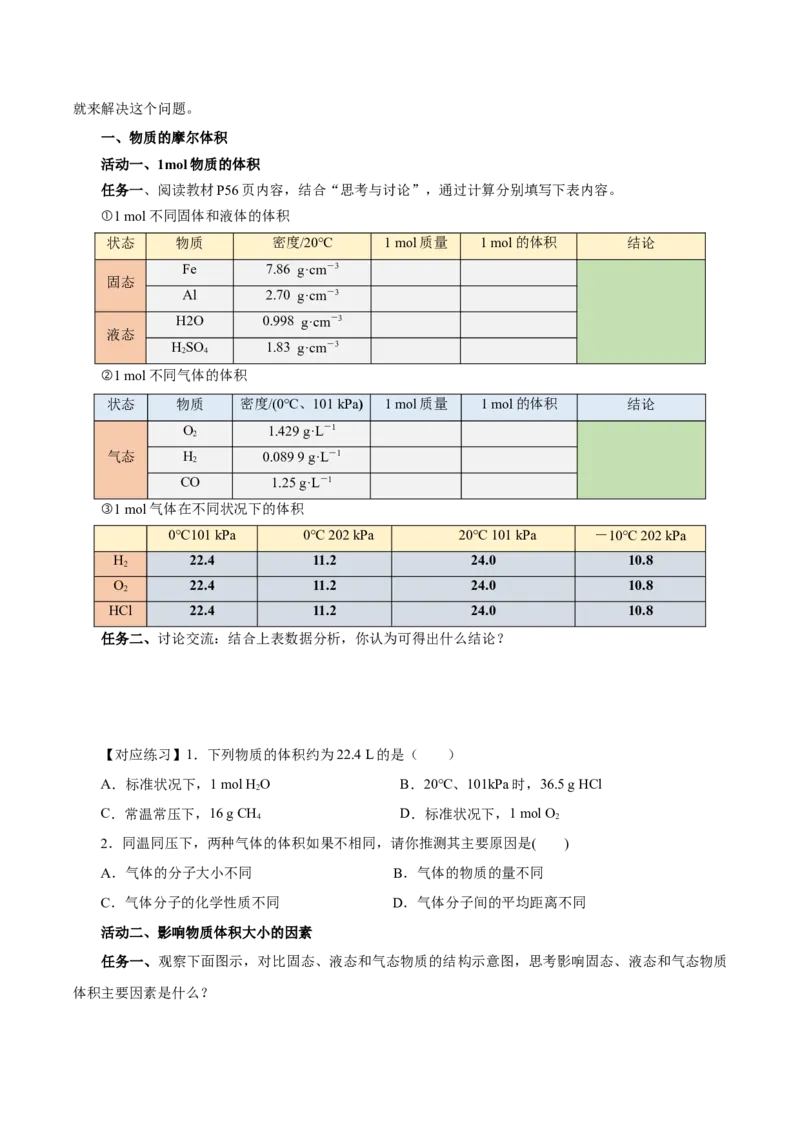
一、物质的摩尔体积
活动一、1mol物质的体积
任务一、阅读教材P56页内容,结合“思考与讨论”,通过计算分别填写下表内容。
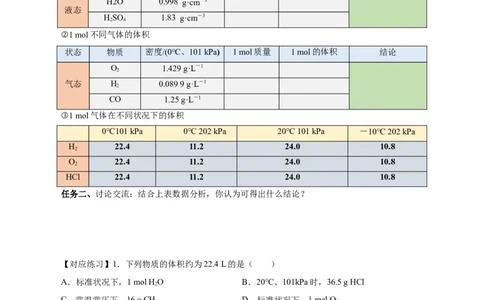
①1 mol不同固体和液体的体积
状态 物质 密度/20℃ 1 mol质量 1 mol的体积 结论
Fe 7.86 g·cm-3
固态
Al 2.70 g·cm-3
H2O 0.998 g·cm-3
液态
HSO 1.83 g·cm-3
2 4
②1 mol不同气体的体积
状态 物质 密度/(0℃、101 kPa) 1 mol质量 1 mol的体积 结论
O 1.429 g·L-1
2
气态 H 0.089 9 g·L-1
2
CO 1.25 g·L-1
③1 mol气体在不同状况下的体积
0℃101 kPa 0℃ 202 kPa 20℃ 101 kPa -10℃ 202 kPa
H 22.4 11.2 24.0 10.8
2
O 22.4 11.2 24.0 10.8
2
HCl 22.4 11.2 24.0 10.8
任务二、讨论交流:结合上表数据分析,你认为可得出什么结论?
【对应练习】1.下列物质的体积约为22.4 L的是( )
A.标准状况下,1 mol H O B.20℃、101kPa时,36.5 g HCl
2
C.常温常压下,16 g CH D.标准状况下,1 mol O
4 2
2.同温同压下,两种气体的体积如果不相同,请你推测其主要原因是( )
A.气体的分子大小不同 B.气体的物质的量不同
C.气体分子的化学性质不同 D.气体分子间的平均距离不同
活动二、影响物质体积大小的因素
任务一、观察下面图示,对比固态、液态和气态物质的结构示意图,思考影响固态、液态和气态物质
体积主要因素是什么?①影响物质体积的大小因素:
②影响1 mol任何物质体积的大小的因素:
任务二、问题探究:为什么相同条件下,1mol不同固体和液体的体积不同,而1mol不同气体的体积
几乎相同?物质的体积与什么因素有关?
【对应练习】1.关于物质的体积的说法正确的是( )
A.1mol固体或液体的体积主要决定于微粒间的距离
B.固体和液体的微粒间的空隙很小,因此不能被压缩
C.气态物质微粒间的距离较大,因此气体的体积决定于气体分子间的距离
D.气体的体积受温度和压强的影响较大,固体或液体的体积受温度和压强的影响较小
2.下列关于决定物质体积的因素的说法不正确的是( )
A.物质的体积取决于粒子数目、粒子大小和粒子间距
B.相同条件下,粒子数相同的任何气体都具有相同体积
C.同温同压下,1 mol任何物质所占有的体积均相同
D.等质量的H,压强越小、温度越高,气体所占体积越大
2
二、气体的摩尔体积
活动一、气体的摩尔体积
任务一、阅读教材P56-57页内容,观察图2-22,思考什么是气体的摩尔体积?影响气体摩尔体积的因
素是什么?①气体摩尔体积定义:
②影响气体摩尔体积的因素:
③标准状况是指:
任务二、讨论交流:气体摩尔体积适用范围是否必须为纯净气体?气体在非标准状况下的气体摩尔体
积,一定不是22.4 L·mol-1吗?
【对应练习】1.下列有关气体摩尔体积的描述正确的是( )
A.在一定温度和压强下,单位物质的量的气体所占的体积就是气体摩尔体积
B.只有在0℃,101kPa下的1mol气体所占体积是22.4L
C.标准状况下,1mol乙醇的体积约为22.4L
D.相同物质的量的两种气体,其体积也相同
2.下列关于气体摩尔体积的几种说法正确的是( )
A.22.4 L任何气体的物质的量均为1 mol
B.非标准状况下,1 mol气体的体积不可能是22.4 L
C.0.1 mol H、0.2 mol O、0.3 mol N 和0.4 mol CO 组成的混合气体在标准状况下的体积约为22.4 L
2 2 2 2
D.在同温同压下,相同体积的任何气体单质所含分子数和原子数都相同
活动二、阿伏伽德罗定律
任务一、讨论交流:温度、压强、物质的量和气体的体积有何关系?
①关系:
②阿伏加德罗定律:
任务二、问题探究:根据阿伏加德罗定律,根据下表条件,你还可以得到哪些结论?填写表格内容。
相同条件 结论公式 语言叙述
同温同压
同温同体积
同温同压
同温同压同
体积
任务三、请谈谈你对阿伏伽德罗定律还有哪些理解?
【对应练习】1.下列叙述正确的是( )
A.同温同压下,相同体积的物质,其物质的量必然相等
B.任何条件下,等物质的量的氧气和一氧化碳所含的分子数必然相等
C.1 L一氧化碳气体一定比1 L氧气的质量小
D.同温同压下,等体积的物质所含的分子数一定相等
2.在体积相同的两个密闭容器中分别充满C H、C H 气体,当这两个容器内温度和气体密度相等时,
2 4 3 6
下列说法正确的是( )
A.两种气体的压强是P(C H)<P(C H) B.C H 比C H 的质量小
2 4 3 6 2 4 3 6
C.两种气体的分子数目相等 D.两种气体的氢原子数目相等
【课后巩固】1.(易)教材作业:P61页练习1、2、7
2.(易)现有下列四种因素:①温度和压强、②所含微粒数、③微粒本身大小、④微粒间的距离,其
中对气体物质体积有显著影响的是( )
A.②③④ B.①②④ C.①③④ D.①②③④
3.(易)下列叙述正确的是( )
A.一定温度、压强下,气体体积由其分子的大小决定
B.一定温度、压强下,气体体积由气体的物质的量的多少决定
C.气体摩尔体积是指1 mol 任何气体所占的体积为22.4 L
D.不同的气体,若体积不等,则它们所含的分子数一定不相等
4.(中)下列有关气体所占体积的说法中正确的是( )A.1mol任何气体的体积都是22.4L
B.1molH 的质量是1g,它所占的体积是22.4L
2
C.在标准状况下,1mol任何气体所占的体积都约为22.4L/mol
D.在标准状况下,1mol任何气体所占的体积都约为22.4L
5.(中)标准状况下,下列物质所占体积最大的是( )
A.36 g HO B.1.5 mol H
2 2
C.48 g O D.3.01×1023个N
3 2
6.(中)下列说法正确的是( )
A.硫酸、磷酸的摩尔质量均为98g
B.20℃、1.0×10 5Pa时,同体积的O 与CO 含有相同的分子数
2 2
C.标准状况下,16gO 与24g Mg所占的体积相同
2
D.当1mol气态物质的体积为22.4L时,该气体一定处于标准状况
7.(中)下列说法不正确的是( )
A.在常温常压下,1gCO和1gN 所含分子数目相同
2
B.体积相同的N 与O 拥有相同的原子数
2 2
C.在0℃、101kPa下等体积的CO和H 所含分子数目相同
2
D.在同温同压下,气体的密度之比等于摩尔质量之比
8.(难)已知N 为阿伏加德罗常数的值。回答下列问题:
A
(1)质量相同的H、NH 、SO 、O 四种气体中,含有分子数目最少的是________(填化学式,下
2 3 2 3
同),在相同温度和相同压强条件下,体积最大的是_______。
(2)73.0 g HCl气体中含有的分子数为_____________,标准状况下的体积为_________L。
(3)18.6 g Na R含0.6 mol Na+,则NaR的摩尔质量为________,R的相对原子质量为________。
2 2
(4)已知CO、CO 的混合气体质量共16.0 g,标准状况下体积为8.96 L,则该混合气体中CO与CO
2 2
的体积比为_________。