文档内容
第四节 化学反应的调控
一、合成氨反应的特点
(一)反应:N+3H 2NH
2 2 3
(二)特点:1、可逆反应
2、放热反应:ΔH<0
3、熵减小的反应:ΔS<0
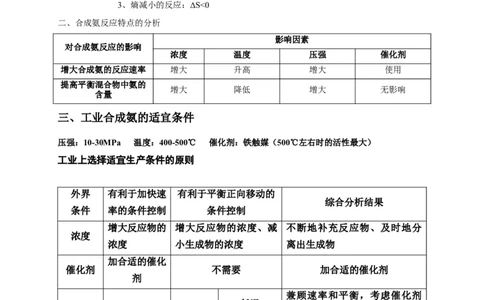
二、合成氨反应特点的分析
影响因素
对合成氨反应的影响
浓度 温度 压强 催化剂
增大合成氨的反应速率 增大 升高 增大 使用
提高平衡混合物中氨的
增大 降低 增大 无影响
含量
三、工业合成氨的适宜条件
压强:10-30MPa 温度:400-500℃ 催化剂:铁触媒(500℃左右时的活性最大)
工业上选择适宜生产条件的原则
外界 有利于加快速 有利于平衡正向移动的
综合分析结果
条件 率的条件控制 条件控制
增大反应物的 增大反应物的浓度、减 不断地补充反应物、及时地分
浓度
浓度 小生成物的浓度 离出生成物
加合适的催化
催化剂 不需要 加合适的催化剂
剂
兼顾速率和平衡,考虑催化剂
ΔH<0 低温
的适宜温度
温度 高温 在设备条件允许的前提下,尽
ΔH>0 高温 量采取高温并考虑催化剂的活
性
在设备条件允许的前提下,尽
高压(有气体 Δν <0 高压
g
压强 量采取高压
参加)
Δν g >0 低压 兼顾速率和平衡,选取适宜的压强
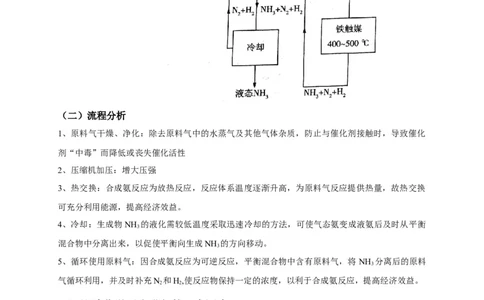
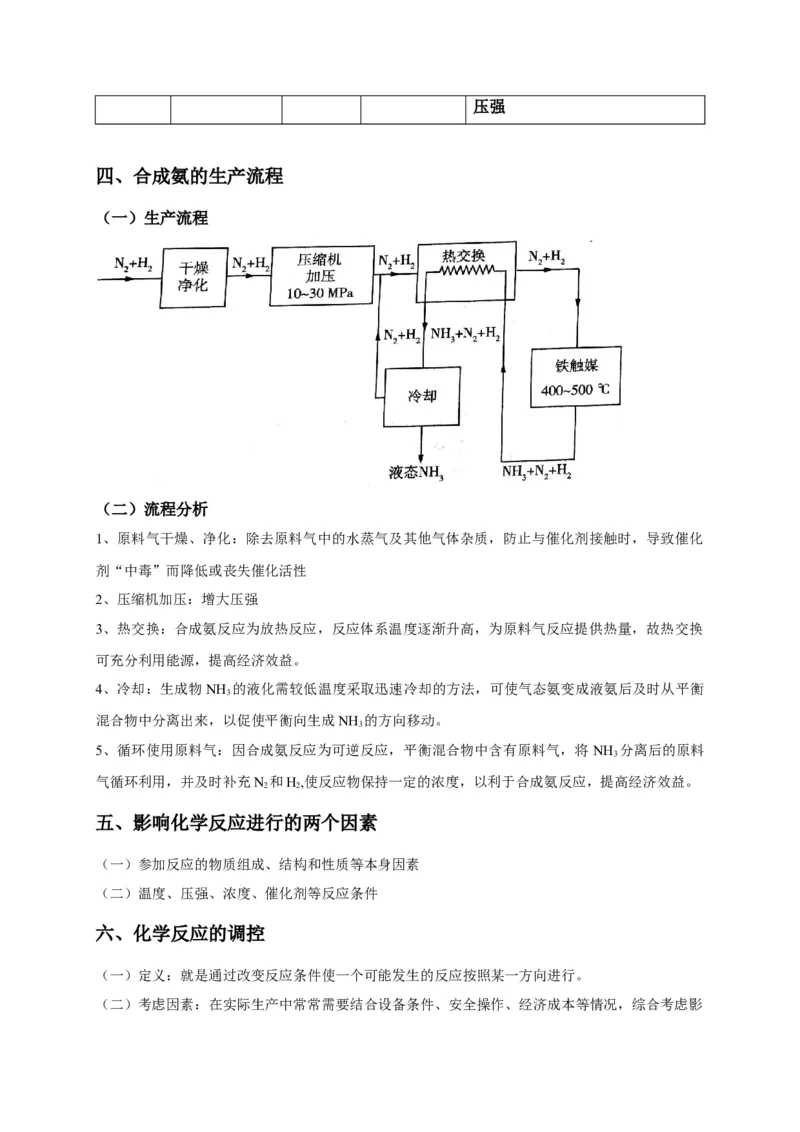
四、合成氨的生产流程
(一)生产流程
(二)流程分析
1、原料气干燥、净化:除去原料气中的水蒸气及其他气体杂质,防止与催化剂接触时,导致催化
剂“中毒”而降低或丧失催化活性
2、压缩机加压:增大压强
3、热交换:合成氨反应为放热反应,反应体系温度逐渐升高,为原料气反应提供热量,故热交换
可充分利用能源,提高经济效益。
4、冷却:生成物NH 的液化需较低温度采取迅速冷却的方法,可使气态氨变成液氨后及时从平衡
3
混合物中分离出来,以促使平衡向生成NH 的方向移动。
3
5、循环使用原料气:因合成氨反应为可逆反应,平衡混合物中含有原料气,将 NH 分离后的原料
3
气循环利用,并及时补充N 和H,使反应物保持一定的浓度,以利于合成氨反应,提高经济效益。
2 2
五、影响化学反应进行的两个因素
(一)参加反应的物质组成、结构和性质等本身因素
(二)温度、压强、浓度、催化剂等反应条件
六、化学反应的调控
(一)定义:就是通过改变反应条件使一个可能发生的反应按照某一方向进行。
(二)考虑因素:在实际生产中常常需要结合设备条件、安全操作、经济成本等情况,综合考虑影响化学反应速率和化学平衡的因素,寻找适宜的生产条件。此外,还要根据环境保护及社会效益等
方面的规定和要求做出分析,权衡利弊,才能实施生产。