文档内容
期末备考试卷(一)
时间:90分钟 满分:100分
一、选择题(本题共15小题,每小题3分,共45分,每小题仅有一个选项符合
题意)
1.化学与资源、环境、生活关系密切,下列说法错误的是( )
A.对“地沟油”蒸馏可以得到汽油
B.新型氢动力计程车可以降低PM2.5的排放,减少大气污染
C.低碳生活注重节能减排,尽量使用太阳能等代替化石燃料,减小温室气体
的排放
D.针对病毒性流感的扩散情况,要加强环境、个人等消毒预防,其中消毒剂
常选用含氯消毒剂、过氧化氢溶液、酒精等适宜的物质
答案 A
解析 地沟油的主要成分是油脂,属于酯类,汽油是烃的混合物,A错误。
2.下列物质中,不属于合成材料的是( )
A.塑料 B.天然橡胶
C.合成纤维 D.合成橡胶
答案 B
解析 天然橡胶是天然的高分子化合物,不是合成材料,故选B。
3.下列有关化学用语表示正确的是( )
A.乙酸的结构简式:C H O
2 4 2
B.离子结构示意图 可以表示32S2-,又可以表示34S2-
C.空间充填模型 可以表示甲烷分子,也可以表示四氯化碳分子
D.NH 的电子式:
3
答案 B
解析 乙酸的结构简式是CH COOH,A错误;模型中白球比黑球小,故该模
3
型可以表示甲烷,而不能表示四氯化碳,C错误;氨气中的氮原子少一个电子对,D
错误。
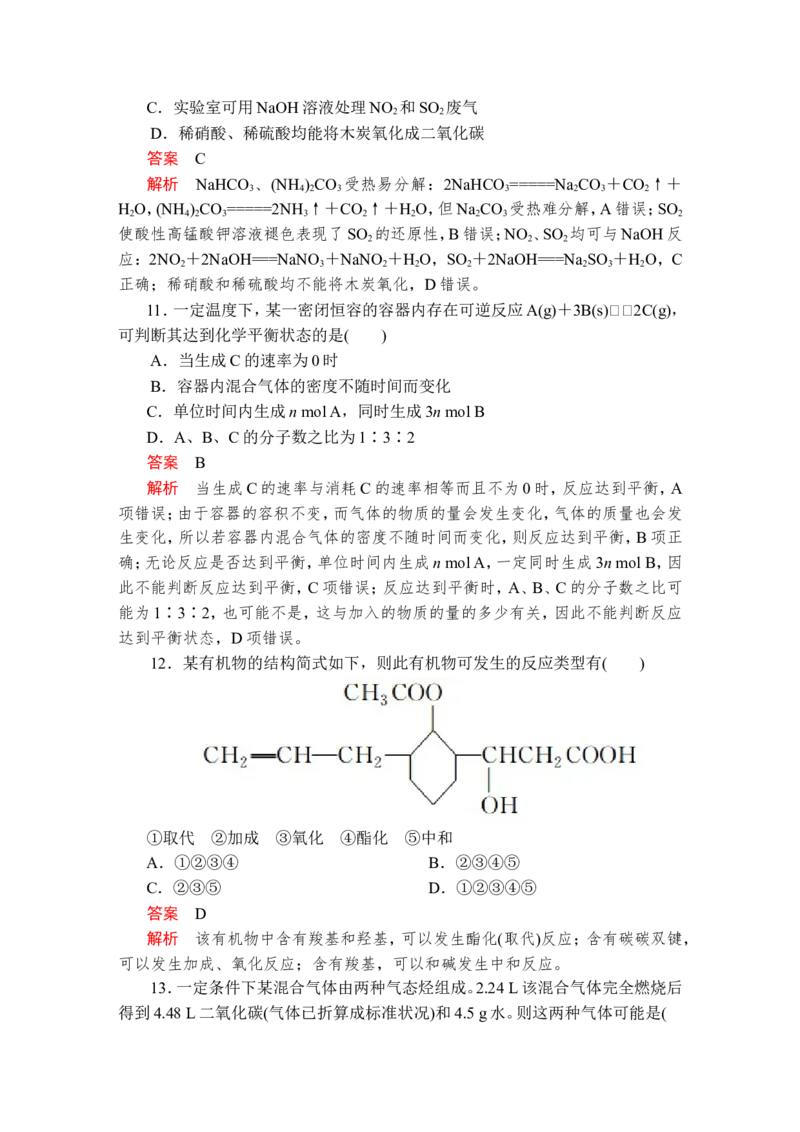
4.如图为一原电池示意图,在原电池两极之间设有隔膜,离子可以自由通过。
则下列说法不正确的是( )A.Zn2+通过隔膜从负极区向正极区移动
B.电子由Cu极通过导线流向Zn极
C.一段时间后,ZnSO 溶液浓度增大,CuSO 溶液浓度减小
4 4
D.Cu2+与Zn2+物质的量之和保持不变
答案 B
解析 该原电池总反应为Zn+CuSO ===Cu+ZnSO ,故CuSO 浓度减小,
4 4 4
ZnSO 浓度增大;Zn失去电子被氧化,电子沿导线从Zn极流向Cu极,在原电池内
4
部,负极产生Zn2+,Zn2+通过隔膜向正极区移动;由方程式可以看出,每消耗1 mol
Cu2+则生成1 mol Zn2+。
5.物质的量相同的下列各物质分别在足量的O 中完全燃烧,其中耗氧量相同
2
的一组是( )
A.CH OH和C H
3 3 6
B.C H COOH和
3 7
C.C H CHO和C H
2 5 3 4
D.C H 和C H
3 8 4 6
答案 C
解析 CH OH(CH ·H O)的耗氧量实际等于 CH 的耗氧量,等物质的量的
3 2 2 2
CH OH和C H 的耗氧量不相同,A不正确;C H COOH可写成
3 3 6 3 7
C H CCH O可写成C H (H O),等物质的量的C H 和C H 的耗氧量不相同,即等
2 5 3 4 6 2 4 4 4 6
物质的量的 C H COOH 和 的耗氧量不相同,B 不正确;
3 7
C H CHO可写成C H (H O),故等物质的量的C H CHO和C H 的耗氧量相同,C
2 5 3 4 2 2 5 3 4
正确;1 mol C H 的耗氧量为3+=5(mol),1 mol C H 的耗氧量为4+=5.5(mol),
3 8 4 6D不正确。
6.某化学反应中,反应物B的物质的量浓度在20 s内,从2.0 mol/L变成了
1.0 mol/L,则这20 s内B的反应速率为( )
A.0.05 mol/(L·s) B.0.05 mol/L·s
C.0.5 mol/(L·s) D.0.05 mol/L
答案 A
解析 v(B)=Δc(B)÷Δt=(2.0 mol/L-1.0 mol/L)÷20 s=0.05 mol/(L·s),因此选
A。
7.下列反应中,属于加成反应的是( )
A.CH +Cl ――→CH Cl+HCl
4 2 3
B.CH ===CH +Br ―→CH BrCH Br
2 2 2 2 2
C.2C H OH+2Na―→2C H ONa+H ↑
2 5 2 5 2
D.C H OH+3O ――→2CO +3H O
2 5 2 2 2
答案 B
解析 A发生的是取代反应,错误;B发生的是加成反应,正确;C发生的是置
换反应,错误;D发生的是氧化反应,错误。
8.物质氧化性、还原性的强弱,不仅与物质的结构有关,还与物质的浓度和反
应温度有关。下列各组物质:
①Cu与HNO 溶液 ②Cu与FeCl 溶液 ③Zn与H SO 溶液 ④Fe与HCl
3 3 2 4
溶液,其中由于浓度不同而能发生不同氧化还原反应的是( )
A.①③ B.③④
C.①② D.①③④
答案 A
解析 一般而言,同种氧化剂:浓度大者氧化性强。Cu与稀HNO 反应,还原
3
产物是NO,Cu与浓HNO 反应,还原产物是NO ;Zn与稀H SO 反应,还原产物
3 2 2 4
是H ,Zn与浓H SO 反应,还原产物是SO 。
2 2 4 2
9.下列实验或实验过程符合化学实验“绿色化”原则的是( )
A.用过氧化氢溶液代替高锰酸钾制取氧气
B.用铜粉代替铜丝进行铜和浓硝酸反应的实验
C.用溴水代替碘水进行萃取实验
D.用较多量的氯气进行性质实验
答案 A
解析 氯气、溴均为有毒物质,C、D错误;铜与浓硝酸反应生成有毒的NO 气
2
体,B错误,故选A。
10.下列有关C、N、S等非金属元素化合物的说法正确的是( )
A.NaHCO 、Na CO 、(NH ) CO 三种固体受热后均能生成气体
3 2 3 4 2 3
B.SO 具有漂白性可以使酸性高锰酸钾溶液褪色
2C.实验室可用NaOH溶液处理NO 和SO 废气
2 2
D.稀硝酸、稀硫酸均能将木炭氧化成二氧化碳
答案 C
解析 NaHCO 、(NH ) CO 受热易分解:2NaHCO =====Na CO +CO ↑+
3 4 2 3 3 2 3 2
H O,(NH ) CO =====2NH ↑+CO ↑+H O,但Na CO 受热难分解,A错误;SO
2 4 2 3 3 2 2 2 3 2
使酸性高锰酸钾溶液褪色表现了SO 的还原性,B错误;NO 、SO 均可与NaOH反
2 2 2
应:2NO +2NaOH===NaNO +NaNO +H O,SO +2NaOH===Na SO +H O,C
2 3 2 2 2 2 3 2
正确;稀硝酸和稀硫酸均不能将木炭氧化,D错误。
11.一定温度下,某一密闭恒容的容器内存在可逆反应A(g)+3B(s)2C(g),
可判断其达到化学平衡状态的是( )
A.当生成C的速率为0时
B.容器内混合气体的密度不随时间而变化
C.单位时间内生成n mol A,同时生成3n mol B
D.A、B、C的分子数之比为1∶3∶2
答案 B
解析 当生成C的速率与消耗C的速率相等而且不为0时,反应达到平衡,A
项错误;由于容器的容积不变,而气体的物质的量会发生变化,气体的质量也会发
生变化,所以若容器内混合气体的密度不随时间而变化,则反应达到平衡,B项正
确;无论反应是否达到平衡,单位时间内生成n mol A,一定同时生成3n mol B,因
此不能判断反应达到平衡,C项错误;反应达到平衡时,A、B、C的分子数之比可
能为1∶3∶2,也可能不是,这与加入的物质的量的多少有关,因此不能判断反应
达到平衡状态,D项错误。
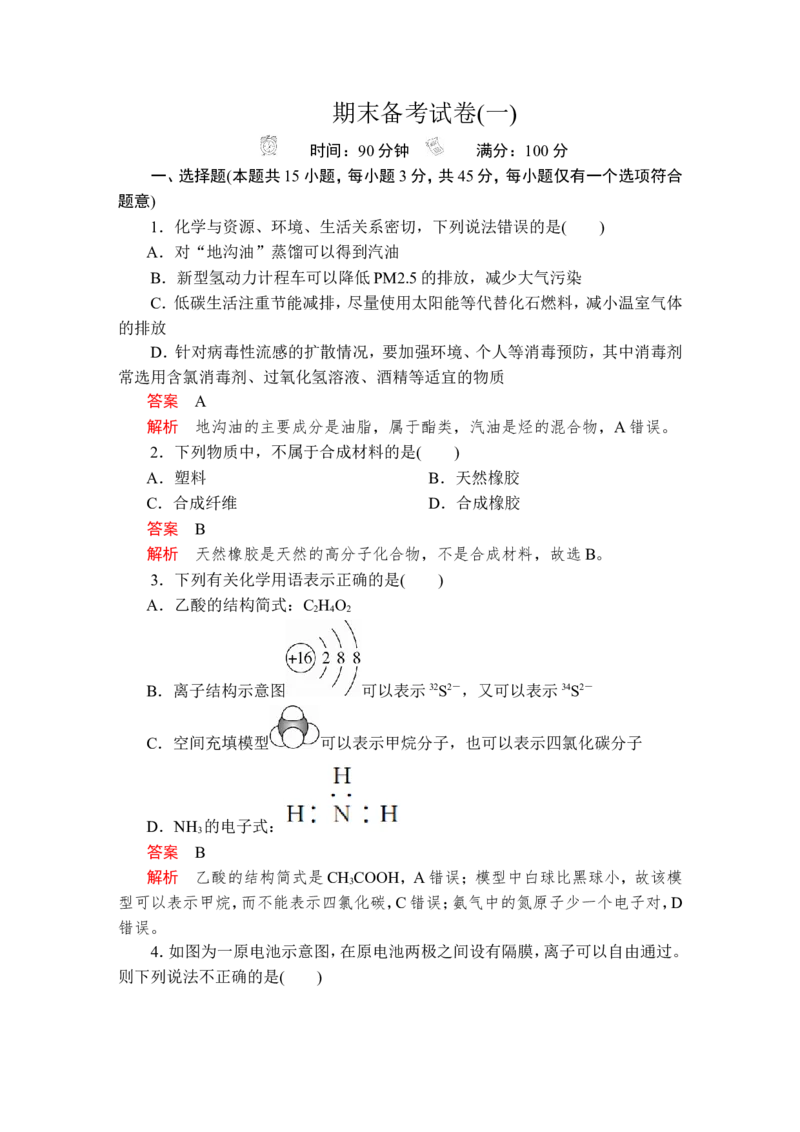
12.某有机物的结构简式如下,则此有机物可发生的反应类型有( )
①取代 ②加成 ③氧化 ④酯化 ⑤中和
A.①②③④ B.②③④⑤
C.②③⑤ D.①②③④⑤
答案 D
解析 该有机物中含有羧基和羟基,可以发生酯化(取代)反应;含有碳碳双键,
可以发生加成、氧化反应;含有羧基,可以和碱发生中和反应。
13.一定条件下某混合气体由两种气态烃组成。2.24 L该混合气体完全燃烧后
得到4.48 L二氧化碳(气体已折算成标准状况)和4.5 g水。则这两种气体可能是()
A.CH 和C H B.C H 和C H
4 2 4 2 4 5 8
C.C H 和C H D.C H 和C H
2 4 3 4 2 4 2 6
答案 D
解析 根据题意可得1 mol该混合气体中含有2 mol碳原子和5 mol氢原子,
即其“平均分子式”为C H ,只有D项组合中的两种物质符合条件。
2 5
14.按图所示装置进行实验,将液体A逐滴加入到固体B中,下列叙述正确的
是( )
A.若A为浓盐酸,B为MnO ,C中盛品红溶液,则C中溶液褪色
2
B.若A为醋酸,B为贝壳,C中盛澄清石灰水,则C中溶液无变化
C.若A为浓氨水,B为生石灰,C中盛AlCl 溶液,则C中先产生白色沉淀后
3
沉淀又溶解
D.实验仪器D可以起到防止溶液倒吸的作用
答案 D
解析 用MnO 与浓盐酸反应制取Cl ,反应需要加热,A错误;贝壳的主要成
2 2
分为CaCO ,与醋酸反应生成的CO 会使澄清石灰水变浑浊,B错误;氨水不能溶
3 2
解Al(OH) ,C错误;D有较大的容积,可起防止倒吸的作用,D正确。
3
15.在100 mL混合液中,HNO 和H SO 的物质的量浓度分别是0.4 mol/L和
3 2 4
0.1 mol/L,向该混合液中加入1.92 g铜粉,加热充分反应后,所得溶液中Cu2+的物
质的量浓度是(假设反应前后溶液的体积不变)( )
A.0.15 mol/L B.0.225 mol/L
C.0.35 mol/L D.0.45 mol/L
答案 B
解析 反应的离子方程式为3Cu+8H++2NO===3Cu2++2NO↑+4H O,由
2
题可知,n(NO)=0.04 mol,n(H+)=0.06 mol,n(Cu)=0.03 mol,H+不足,则生成的
n(Cu2+)=×0.06 mol=0.0225 mol,c(Cu2+)==0.225 mol/L。
二、非选择题(本题共4小题,共55分)
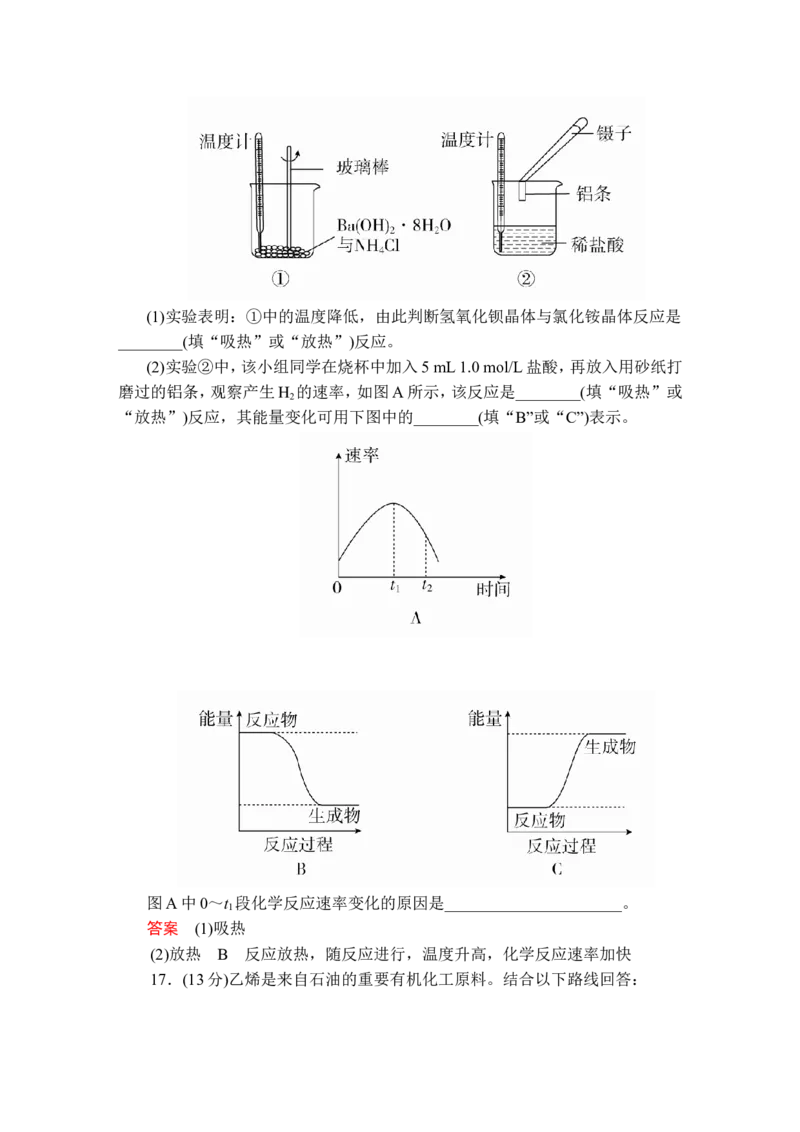
16.(11分)某实验小组同学进行如下实验,以探究化学反应中的能量变化。(1)实验表明:①中的温度降低,由此判断氢氧化钡晶体与氯化铵晶体反应是
________(填“吸热”或“放热”)反应。
(2)实验②中,该小组同学在烧杯中加入5 mL 1.0 mol/L盐酸,再放入用砂纸打
磨过的铝条,观察产生H 的速率,如图A所示,该反应是________(填“吸热”或
2
“放热”)反应,其能量变化可用下图中的________(填“B”或“C”)表示。
图A中0~t 段化学反应速率变化的原因是______________________。
1
答案 (1)吸热
(2)放热 B 反应放热,随反应进行,温度升高,化学反应速率加快
17.(13分)乙烯是来自石油的重要有机化工原料。结合以下路线回答:已知:2CH CHO+O ――→2CH COOH
3 2 3
(1)D为高分子化合物,可以用来制造多种包装材料,其结构简式是________。
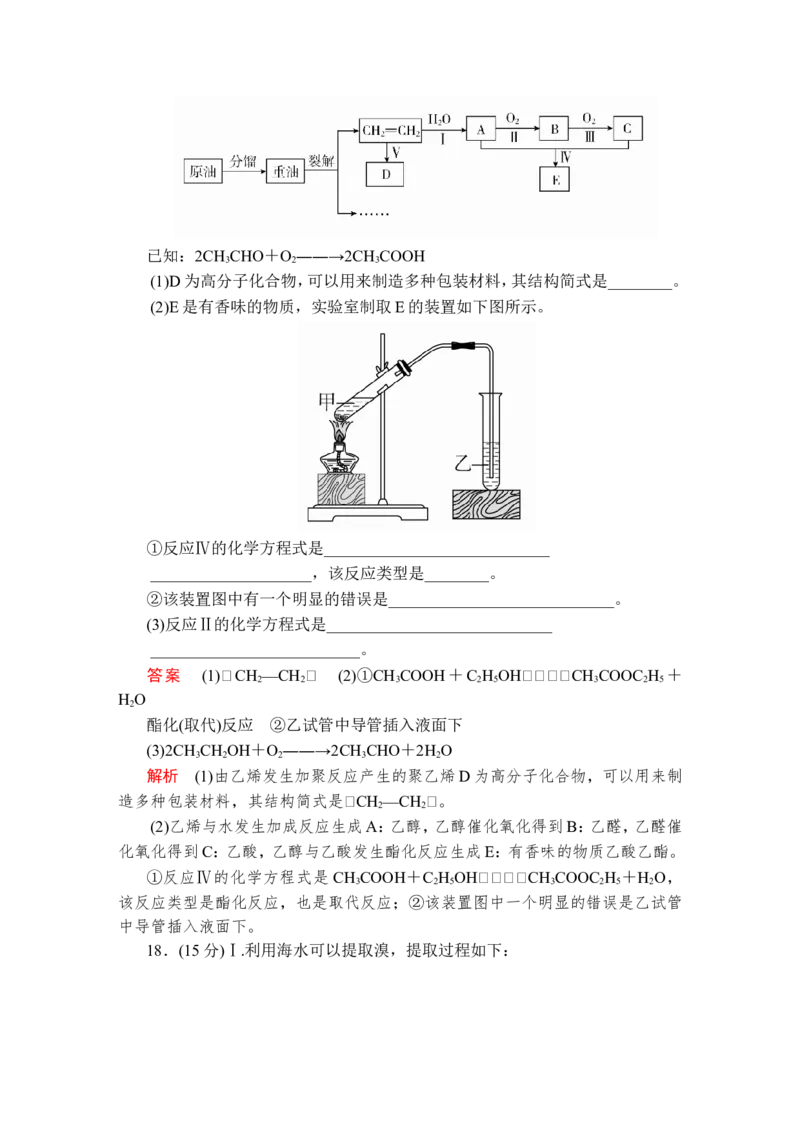
(2)E是有香味的物质,实验室制取E的装置如下图所示。
①反应Ⅳ的化学方程式是____________________________
____________________,该反应类型是________。
②该装置图中有一个明显的错误是____________________________。
(3)反应Ⅱ的化学方程式是____________________________
__________________________。
答案 (1)CH —CH (2)①CH COOH+C H OHCH COOC H +
2 2 3 2 5 3 2 5
H O
2
酯化(取代)反应 ②乙试管中导管插入液面下
(3)2CH CH OH+O ――→2CH CHO+2H O
3 2 2 3 2
解析 (1)由乙烯发生加聚反应产生的聚乙烯D为高分子化合物,可以用来制
造多种包装材料,其结构简式是CH —CH 。
2 2
(2)乙烯与水发生加成反应生成A:乙醇,乙醇催化氧化得到B:乙醛,乙醛催
化氧化得到C:乙酸,乙醇与乙酸发生酯化反应生成E:有香味的物质乙酸乙酯。
①反应Ⅳ的化学方程式是CH COOH+C H OHCH COOC H +H O,
3 2 5 3 2 5 2
该反应类型是酯化反应,也是取代反应;②该装置图中一个明显的错误是乙试管
中导管插入液面下。
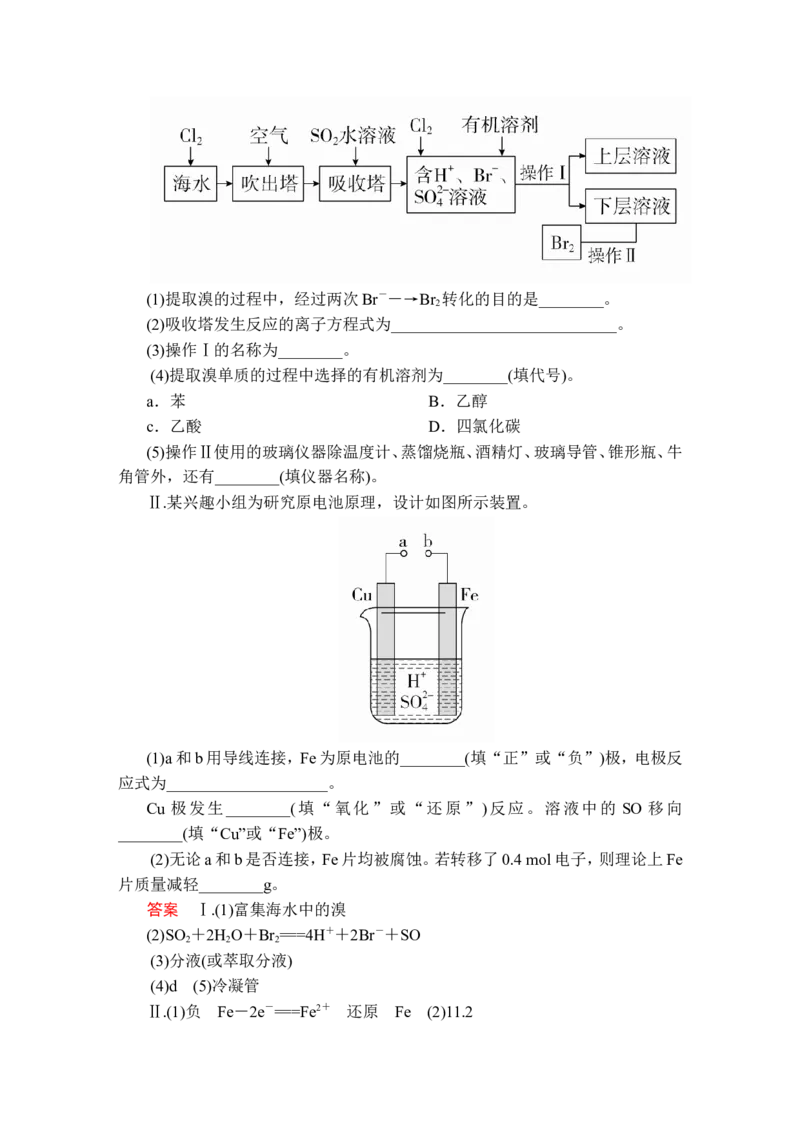
18.(15分)Ⅰ.利用海水可以提取溴,提取过程如下:(1)提取溴的过程中,经过两次Br-―→Br 转化的目的是________。
2
(2)吸收塔发生反应的离子方程式为____________________________。
(3)操作Ⅰ的名称为________。
(4)提取溴单质的过程中选择的有机溶剂为________(填代号)。
a.苯 B.乙醇
c.乙酸 D.四氯化碳
(5)操作Ⅱ使用的玻璃仪器除温度计、蒸馏烧瓶、酒精灯、玻璃导管、锥形瓶、牛
角管外,还有________(填仪器名称)。
Ⅱ.某兴趣小组为研究原电池原理,设计如图所示装置。
(1)a和b用导线连接,Fe为原电池的________(填“正”或“负”)极,电极反
应式为____________________。
Cu 极发生________(填“氧化”或“还原”)反应。溶液中的 SO 移向
________(填“Cu”或“Fe”)极。
(2)无论a和b是否连接,Fe片均被腐蚀。若转移了0.4 mol电子,则理论上Fe
片质量减轻________g。
答案 Ⅰ.(1)富集海水中的溴
(2)SO +2H O+Br ===4H++2Br-+SO
2 2 2
(3)分液(或萃取分液)
(4)d (5)冷凝管
Ⅱ.(1)负 Fe-2e-===Fe2+ 还原 Fe (2)11.219.(16分)为研究铁质材料与热浓硫酸的反应,某学习小组用碳素钢(即铁和
碳的合金)进行了以下探究活动:
【探究一】
(1) 常 温 下 , 工 业 上 用 铁 质 容 器 盛 放 冷 的 浓 硫 酸 , 其 原 因 是
____________________________。
(2)称取碳素钢6.0 g放入15.0 mL浓硫酸中,加热,充分反应后得到溶液X并
收集到混合气体Y。
①甲同学认为X中除Fe3+之外还可能含有Fe2+。若要确认其中的Fe2+,应选
用________(填序号)。
a.KSCN溶液和氯水 B.铁粉和KSCN溶液
c.浓氨水 D.酸性KMnO 溶液
4
②乙同学取 560 mL(标准状况)气体 Y 通入足量溴水中,发生 SO +Br +
2 2
2H O===2HBr+H SO 反应,然后加入足量BaCl 溶液,经适当操作后得干燥固体
2 2 4 2
4.66 g。由此推知气体Y中SO 的体积分数为________。
2
【探究二】
根据上述实验中SO 体积分数的分析,丙同学认为气体Y中还可能含有Q 和
2 1
Q 两种气体,其中Q 气体在标准状况下密度为0.0893 g·L-1。为此设计了下列探
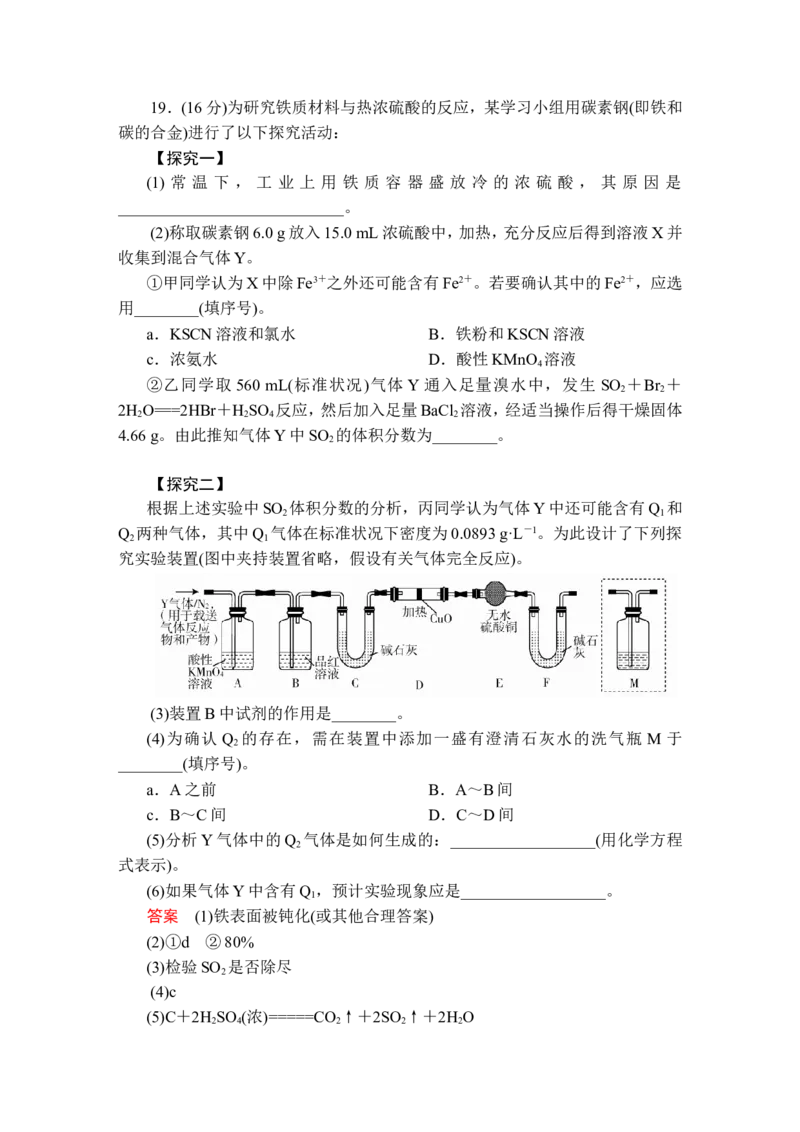
2 1
究实验装置(图中夹持装置省略,假设有关气体完全反应)。
(3)装置B中试剂的作用是________。
(4)为确认 Q 的存在,需在装置中添加一盛有澄清石灰水的洗气瓶 M 于
2
________(填序号)。
a.A之前 B.A~B间
c.B~C间 D.C~D间
(5)分析Y气体中的Q 气体是如何生成的:__________________(用化学方程
2
式表示)。
(6)如果气体Y中含有Q ,预计实验现象应是__________________。
1
答案 (1)铁表面被钝化(或其他合理答案)
(2)①d ②80%
(3)检验SO 是否除尽
2
(4)c
(5)C+2H SO (浓)=====CO ↑+2SO ↑+2H O
2 4 2 2 2(6)D中固体由黑色变红色和E中固体由白色变蓝色
解析 (2)①Fe2+具有还原性,能使酸性KMnO 溶液褪色。
4
②n(SO )=n(H SO )=n(BaSO )==0.02 mol,V(SO )=0.02 mol×22.4 L·mol-1
2 2 4 4 2
=448 mL,所以SO 的体积分数为 ×100%=80%。
2
(3)碳素钢中含有一定量的碳,在加热条件下也能与浓硫酸发生反应生成CO ,
2
同时随着反应的进行,浓硫酸逐渐变稀,再根据密度可知Q 是H ,则Q 是CO 。
1 2 2 2
SO 的存在对CO 的检验有干扰,所以A中酸性高锰酸钾溶液的作用是除去SO ,
2 2 2
B中品红溶液是检验SO 是否除净,若品红溶液不褪色说明SO 除尽。
2 2
(4)装置C的作用是干燥,CO 、SO 均能使澄清石灰水变浑浊,为了确认CO
2 2 2
的存在,必须排除SO 的干扰,所以CO 的检验应放在装置B和装置C之间。
2 2
(6)若有H 存在,则在装置D中H 与CuO反应生成Cu和H O。
2 2 2