文档内容
第五章 化工生产中的重要非金属元素
(时间:90分钟 分值:100分)
一、选择题(本题包括16小题,每小题3分,共48分)
1.(2019全国Ⅲ)化学与生活密切相关。下列叙述错误的是( )
A.高纯硅可用于制作光感电池
B.铝合金大量用于高铁建设
C.活性炭具有除异味和杀菌作用
D.碘酒可用于皮肤外用消毒
答案C
解析本题考查了化学与STSE的关系,特别注重了化学物质在生产、生活中的应用。晶体硅中的
电子吸收光能,电子发生跃迁,可将光能转换为电能,A项正确;铝合金具有密度小、硬度大等优
点,可大量用于高铁的建设,B项正确;活性炭具有疏松多孔结构,有较强的吸附性,可用于除异味,
但不具有杀菌作用,C项错误;碘酒中的碘单质具有强氧化性,可杀菌消毒,故可用于皮肤外用消
毒,D项正确。
2.下列关于硫酸和硝酸的说法中,不正确的是( )
A.稀硫酸和稀硝酸都具有氧化性
B.浓硝酸在光照条件下变黄,说明浓硝酸不稳定,分解生成的有色产物溶于浓硝酸
C.在铜分别与浓硫酸和浓硝酸的反应中,两种酸都表现了强氧化性和酸性
D.浓硫酸和浓硝酸都具有很强的腐蚀性、脱水性
答案D
解析浓硝酸显黄色是因为HNO 分解产生的NO 溶解在其中,B正确;浓硝酸不具有脱水性,D错
3 2
误。
3.下列有关化学反应的叙述正确的是( )
A.Fe在稀硝酸中发生钝化
B.MnO 和稀盐酸反应制取Cl
2 2
C.SO 与过量氨水反应生成(NH )SO
2 4 2 3
D.室温下Na与空气中O 反应制取NaO
2 2 2
答案C
解析常温下,Fe在稀硝酸中剧烈反应,不会发生钝化,A项错误;MnO 和稀盐酸不反应,制取氯气
2
应用浓盐酸,B项错误;室温下,钠与氧气反应生成氧化钠,在加热条件下才生成过氧化钠,D项错
误。
4.下列有关物质性质与用途具有对应关系的是( )
A.NaO 吸收CO 产生O,可用作呼吸面具供氧剂
2 2 2 2
B.ClO 具有还原性,可用于自来水的杀菌消毒
2
C.SiO 硬度大,可用于制造光导纤维
2
D.NH 易溶于水,可用作制冷剂
3
答案A
解析A项,人呼出气体中含有的CO 可与NaO 反应生成O,故NaO 可用作呼吸面具的供氧剂,
2 2 2 2 2 2
正确;B项,ClO 具有强氧化性,可以用于自来水的杀菌消毒,错误;C项,SiO 可用于制造光导纤维
2 2
不是因为其硬度大,两者无对应关系,错误;D项,NH 易液化,是其可用作制冷剂的原因,错误。
3
5.在给定条件下,下列选项所示的物质间转化均能实现的是( )
A.Fe FeCl Fe(OH)
2 2B.S SO HSO
3 2 4
C.CaCO CaO CaSiO
3 3
D.NH NO HNO
3 3
答案C
解析A项,Fe与Cl 反应生成FeCl ,错误;B项,S与O 反应生成SO ,错误;C项,CaCO 高温分解
2 3 2 2 3
生成CaO和CO,碱性氧化物CaO与酸性氧化物SiO 在高温条件下反应生成CaSiO ,正确;D项,
2 2 3
NO与HO不反应,错误。
2
6.下列过程中最终的白色沉淀不一定是BaSO 的是( )
4
A.Fe(NO ) 溶液 白色沉淀
3 2
B.Ba(NO ) 溶液 白色沉淀
3 2
C.无色溶液 白色沉淀
D.无色溶液 无色溶液 白色沉淀
答案C
解析A项中N 、H+能将SO 氧化成S ,故能产生BaSO 白色沉淀。B项中H+、N 能将S
2 4
氧化成S ,能产生BaSO 沉淀。D项中加盐酸无现象,可排除Ag+的存在,再加入BaCl 溶
4 2
液,产生不溶于盐酸的白色沉淀,故D项中产生的是BaSO 沉淀。C项中不能排除AgCl沉淀的
4
可能。
7.下列除杂试剂选用正确且除杂过程不涉及氧化还原反应的是( )
物质(括号内为
除杂试剂
杂质)
FeCl 溶液
A 2 Fe粉
(FeCl)
3
NaCl溶液 NaOH溶液、稀盐
B
(MgCl) 酸
2
C Cl(HCl) HO、浓硫酸
2 2
D NO(NO) HO、无水CaCl
2 2 2
答案B
解析A项,主反应Fe+2FeCl 3FeCl 属于氧化还原反应,A不选;B项,加入足量NaOH溶液发
3 2
生复分解反应生成Mg(OH) 沉淀,过滤后用盐酸中和过量的NaOH得到不含MgCl 的NaCl溶
2 2
液,B正确;C项,除去Cl 中的HCl,可将混合气体通过饱和食盐水,然后再用浓硫酸干燥,C不
2
选;D项,主反应3NO +H O 2HNO+NO属于氧化还原反应,D不选。
2 2 3
8.下列关于物质性质的叙述中正确的是( )
A.Cl 能与金属活动性顺序中大多数金属反应
2
B.N 是大气中的主要成分之一,雷雨时可直接转化为NO
2 2
C.硫是一种黄色的能溶于水的晶体,既有氧化性又有还原性
D.硅是应用广泛的半导体材料,常温下化学性质活泼答案A
解析Cl 具有强氧化性,能与金属活动性顺序中大多数金属反应,A项正确;雷雨时N 与O 反应
2 2 2
可生成NO,而不是NO ,B项错误;硫不溶于水,C项错误;硅在常温下化学性质不活泼,D项错误。
2
9.下列实验中金属或氧化物可以完全溶解的是( )
A.1 mol Cu与含2 mol H SO 的浓硫酸共热
2 4
B.1 mol MnO 与含2 mol H O 的溶液共热
2 2 2
C.常温下1 mol Al投入足量的浓硫酸中
D.常温下1 mol Cu投入含4 mol HNO 的浓硝酸中
3
答案D
解析A中随着反应的进行浓硫酸逐渐变为稀硫酸,稀硫酸不与铜反应,根据Cu+2H SO (浓)
2 4
CuSO +SO↑+2H O,Cu不能完全溶解;B中MnO 作催化剂;C中铝会钝化;D中随着反应的进行
4 2 2 2
浓硝酸逐渐变为稀硝酸,但稀硝酸也与铜反应,依Cu+4HNO (浓) Cu(NO )+2H O+2NO ↑、
3 3 2 2 2
3Cu+8HNO (稀) 3Cu(NO )+4H O+2NO↑,Cu可以完全溶解。
3 3 2 2
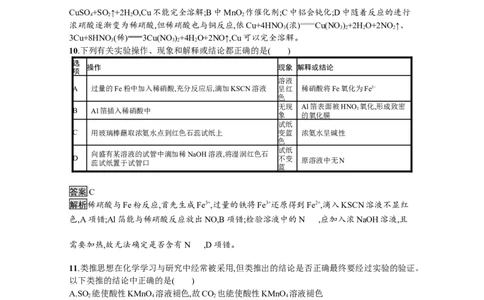
10.下列有关实验操作、现象和解释或结论都正确的是( )
选
操作 现象 解释或结论
项
溶液
A 过量的Fe粉中加入稀硝酸,充分反应后,滴加KSCN溶液 呈红 稀硝酸将Fe氧化为Fe3+
色
无现 Al箔表面被HNO 氧化,形成致密
B Al箔插入稀硝酸中 3
象 的氧化膜
试纸
C 用玻璃棒蘸取浓氨水点到红色石蕊试纸上 变蓝 浓氨水呈碱性
色
试纸
向盛有某溶液的试管中滴加稀NaOH溶液,将湿润红色石
D
蕊试纸置于试管口
不变 原溶液中无N
蓝
答案C
解析稀硝酸与Fe粉反应,首先生成Fe3+,过量的铁将Fe3+还原得到Fe2+,滴入KSCN溶液不显红
色,A项错;Al箔能与稀硝酸反应放出NO,B项错;检验溶液中的N ,应加入浓NaOH溶液,且
需要加热,故无法确定是否含有N ,D项错。
11.类推思想在化学学习与研究中经常被采用,但类推出的结论是否正确最终要经过实验的验证。
以下类推的结论中正确的是( )
A.SO 能使酸性KMnO 溶液褪色,故CO 也能使酸性KMnO 溶液褪色
2 4 2 4
B.盐酸与镁反应生成氢气,故硝酸与镁反应也生成氢气
C.SO 能使品红溶液褪色,故CO 也能使品红溶液褪色
2 2
D.常温下浓硫酸能使铁和铝钝化,故常温下浓硝酸也能使铁和铝钝化
答案D
解析A项中CO 无还原性,不能使酸性KMnO 溶液褪色;B项中金属与HNO 反应不产生H;C
2 4 3 2
项中CO 无漂白性,不能使品红溶液褪色。
2
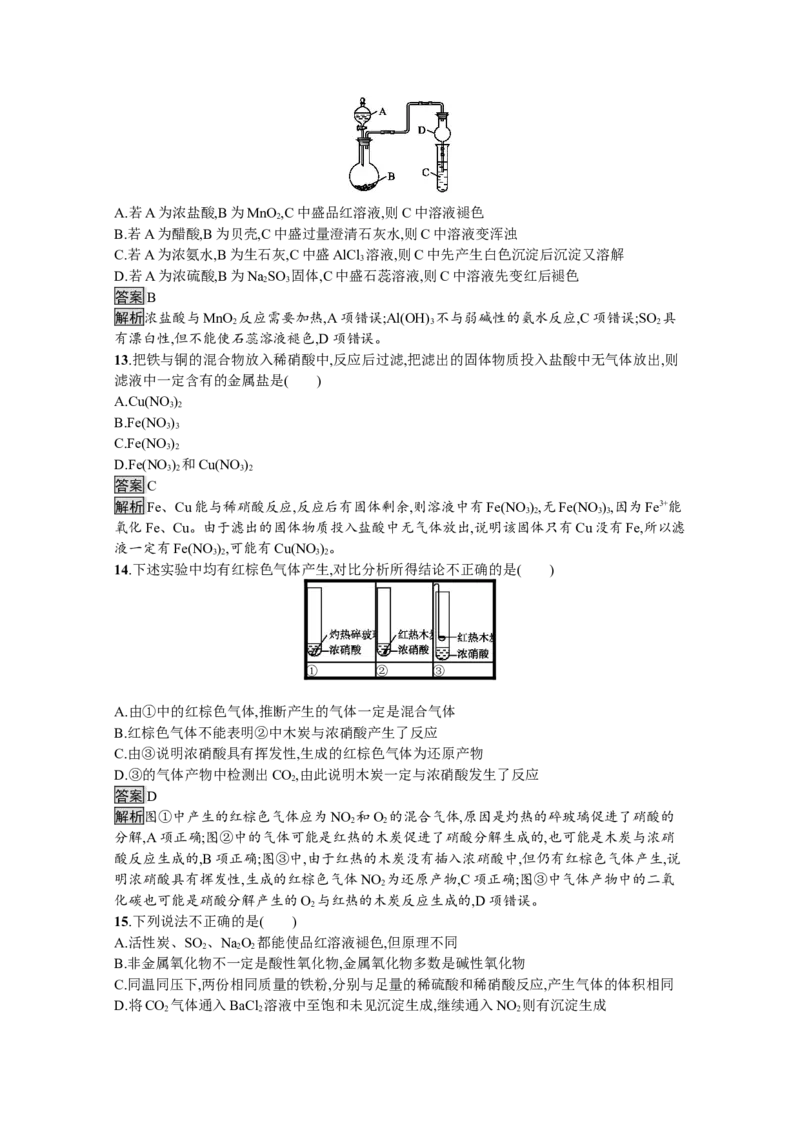
12.如图装置,将溶液A逐滴加入固体B中,下列叙述正确的是( )A.若A为浓盐酸,B为MnO ,C中盛品红溶液,则C中溶液褪色
2
B.若A为醋酸,B为贝壳,C中盛过量澄清石灰水,则C中溶液变浑浊
C.若A为浓氨水,B为生石灰,C中盛AlCl 溶液,则C中先产生白色沉淀后沉淀又溶解
3
D.若A为浓硫酸,B为NaSO 固体,C中盛石蕊溶液,则C中溶液先变红后褪色
2 3
答案B
解析浓盐酸与MnO 反应需要加热,A项错误;Al(OH) 不与弱碱性的氨水反应,C项错误;SO 具
2 3 2
有漂白性,但不能使石蕊溶液褪色,D项错误。
13.把铁与铜的混合物放入稀硝酸中,反应后过滤,把滤出的固体物质投入盐酸中无气体放出,则
滤液中一定含有的金属盐是( )
A.Cu(NO )
3 2
B.Fe(NO )
3 3
C.Fe(NO )
3 2
D.Fe(NO ) 和Cu(NO )
3 2 3 2
答案C
解析Fe、Cu能与稀硝酸反应,反应后有固体剩余,则溶液中有Fe(NO ),无Fe(NO ),因为Fe3+能
3 2 3 3
氧化Fe、Cu。由于滤出的固体物质投入盐酸中无气体放出,说明该固体只有Cu没有Fe,所以滤
液一定有Fe(NO ),可能有Cu(NO )。
3 2 3 2
14.下述实验中均有红棕色气体产生,对比分析所得结论不正确的是( )
① ② ③
A.由①中的红棕色气体,推断产生的气体一定是混合气体
B.红棕色气体不能表明②中木炭与浓硝酸产生了反应
C.由③说明浓硝酸具有挥发性,生成的红棕色气体为还原产物
D.③的气体产物中检测出CO,由此说明木炭一定与浓硝酸发生了反应
2
答案D
解析图①中产生的红棕色气体应为NO 和O 的混合气体,原因是灼热的碎玻璃促进了硝酸的
2 2
分解,A项正确;图②中的气体可能是红热的木炭促进了硝酸分解生成的,也可能是木炭与浓硝
酸反应生成的,B项正确;图③中,由于红热的木炭没有插入浓硝酸中,但仍有红棕色气体产生,说
明浓硝酸具有挥发性,生成的红棕色气体NO 为还原产物,C项正确;图③中气体产物中的二氧
2
化碳也可能是硝酸分解产生的O 与红热的木炭反应生成的,D项错误。
2
15.下列说法不正确的是( )
A.活性炭、SO 、NaO 都能使品红溶液褪色,但原理不同
2 2 2
B.非金属氧化物不一定是酸性氧化物,金属氧化物多数是碱性氧化物
C.同温同压下,两份相同质量的铁粉,分别与足量的稀硫酸和稀硝酸反应,产生气体的体积相同
D.将CO 气体通入BaCl 溶液中至饱和未见沉淀生成,继续通入NO 则有沉淀生成
2 2 2答案D
解析选项A,活性炭能使品红溶液褪色是利用了活性炭的吸附性,SO 能使品红溶液褪色是利用
2
了SO 可与品红生成不稳定的无色物质,Na O 具有强氧化性,使品红溶液褪色,三者使品红溶液
2 2 2
褪色的原理不同;选项B,如NO、CO不是酸性氧化物,大多数金属氧化物是碱性氧化物;选项C,
根据反应:Fe+H SO FeSO +H ↑,Fe+4HNO(稀) Fe(NO )+NO↑+2H O,同温同压下,等物质
2 4 4 2 3 3 3 2
的量的Fe参与反应时生成的H、NO的体积相等;选项D,继续通入NO ,NO 与水反应产生
2 2 2
HNO,但没有沉淀生成。
3
16.足量铜与一定量浓硝酸反应,得到硝酸铜溶液和NO 、NO、NO的混合气体,这些气体与1.68
2 2 4
L O (标准状况)混合后通入水中,所有气体完全被水吸收生成硝酸。若向所得硝酸铜溶液中加入
2
5 mol·L-1 NaOH溶液至Cu2+恰好完全沉淀,则消耗NaOH溶液的体积是( )
A.60 mL B.45 mL C.30 mL D.15 mL
答案A
解析根据题意可知,Cu与HNO 反应生成Cu(NO ) 所失电子的量与1.68 L O(标准状况)所得电
3 3 2 2
子的量相等,则n(Cu2+)=2n(O )=2× =0.15 mol,根据Cu2++2OH- Cu(OH) ↓可知,
2 2
使所得Cu(NO ) 溶液中Cu2+恰好完全沉淀,消耗NaOH的物质的量为0.3 mol,需5 mol·L-1
3 2
NaOH溶液的体积为 =60 mL。
二、非选择题(本题包括4小题,共52分)
17.(12分)A、B、C、D是中学化学常见的三种物质,它们之间的相互转化关系如下(反应条件及部
分产物已略去):
(1)若A是一种黄色固体单质,则反应②③的化学方程式分别为
; 。
(2)若A是一种金属单质,C是淡黄色固体,则反应③的化学方程式为
。
(3)①②③三步反应中,一定属于氧化还原反应的是 (填序号)。
答案(1)2SO +O 2SO SO +H O HSO
2 2 3 3 2 2 4
(2)2Na O+2H O 4NaOH+O ↑
2 2 2 2
(3)①②
解析图示中的上述反应就是常见的“连续氧化”。在中学教材中,这样的“连续氧化”有:C(或
CH 等)→CO→CO;Na→NaO→NaO;S(或HS)→SO →SO ;N (或NH )→NO→NO 等。据此可
4 2 2 2 2 2 2 3 2 3 2
知:
(1)的路线为:S→SO →SO →HSO ;
2 3 2 4
(2)的路线为:Na→NaO→NaO→NaOH;
2 2 2
根据上述分析可知,反应①②是单质或化合物被氧气氧化的反应,一定属于氧化还原反应,
而③则不一定。
18.(18分)(1)分别向盛有等量铜片的四支试管中加入等体积的①浓硫酸、②稀硫酸、③浓硝酸、
④稀硝酸,能随即发生剧烈反应的是(填序号,下同) ,常温下缓慢反应(或微热后能发生剧烈反应)的是 ,常温下不反应,但加热后发生剧烈反应的是 ,加热也不发生反应的
是 。由此可以得到上述四种酸氧化性由强到弱的顺序是 。
(2)先将铜与浓硫酸反应产生的气体X持续通入如图装置中,一段时间后再将铜与浓硝酸反应
产生的大量气体Y也持续通入该装置中,可观察到的现象包括 。
A.通入X气体后产生白色沉淀
B.通入X气体后溶液中无明显现象
C.通入Y气体后开始沉淀
D.通入Y气体后沉淀溶解
E.通入Y气体后溶液中无明显现象
由此可得到的结论是 。
A.HNO 的酸性比HSO 的强
3 2 4
B.盐酸的酸性比HSO 的强
2 3
C.BaSO 能溶于盐酸
3
D.HNO 能氧化HSO (或SO )
3 2 3 2
E.BaSO 不溶于水也不溶于HNO 溶液
4 3
答案(1)③ ④ ① ② ③>④>①>②
(2)BC BCDE
解析(2)因为盐酸的酸性比HSO 的强,所以SO 不与BaCl 反应,即持续通入X气体(SO )后溶
2 3 2 2 2
液中无明显现象。NO 与水反应生成HNO,HNO 氧化HSO (或SO )生成S ,所以通入Y气
2 3 3 2 3 2
体(NO )后开始生成沉淀BaSO。
2 4
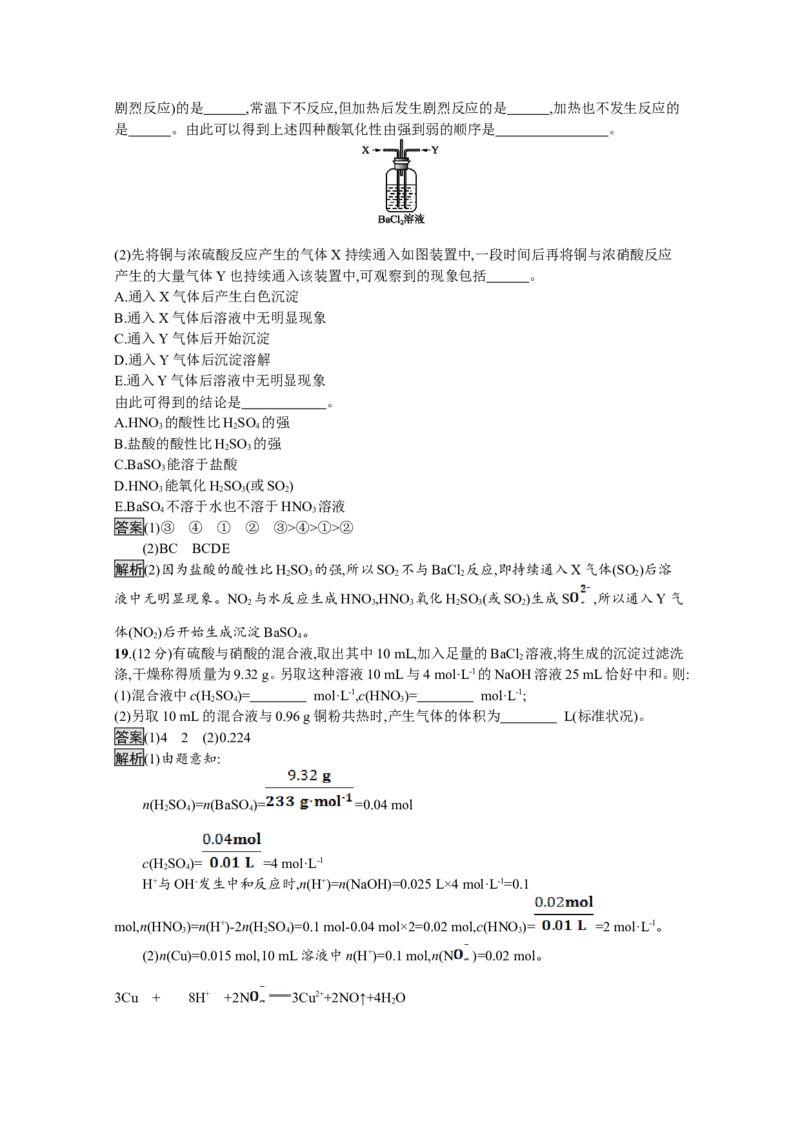
19.(12分)有硫酸与硝酸的混合液,取出其中10 mL,加入足量的BaCl 溶液,将生成的沉淀过滤洗
2
涤,干燥称得质量为9.32 g。另取这种溶液10 mL与4 mol·L-1的NaOH溶液25 mL恰好中和。则:
(1)混合液中c(H SO )= mol·L-1,c(HNO)= mol·L-1;
2 4 3
(2)另取10 mL的混合液与0.96 g铜粉共热时,产生气体的体积为 L(标准状况)。
答案(1)4 2 (2)0.224
解析(1)由题意知:
n(H SO )=n(BaSO)= =0.04 mol
2 4 4
c(H SO )= =4 mol·L-1
2 4
H+与OH-发生中和反应时,n(H+)=n(NaOH)=0.025 L×4 mol·L-1=0.1
mol,n(HNO)=n(H+)-2n(H SO )=0.1 mol-0.04 mol×2=0.02 mol,c(HNO)= =2 mol·L-1。
3 2 4 3
(2)n(Cu)=0.015 mol,10 mL溶液中n(H+)=0.1 mol,n(N )=0.02 mol。
3Cu + 8H+ +2N 3Cu2++2NO↑+4H O
23 mol 8 mol 2 mol 44.8 L
0.015 mol 0.1 mol 0.02 mol V(NO)
因0.1×3>0.015×8,故Cu与H+二者之中H+过量;又因0.02×3>0.015×2,故Cu 与N 二者之
中N 过量。则Cu、H+、N 三者之中H+与N 均过量,Cu全部溶解,生成NO的体积应据Cu
的物质的量来计算,V(NO)=0.015 mol× =0.224 L。
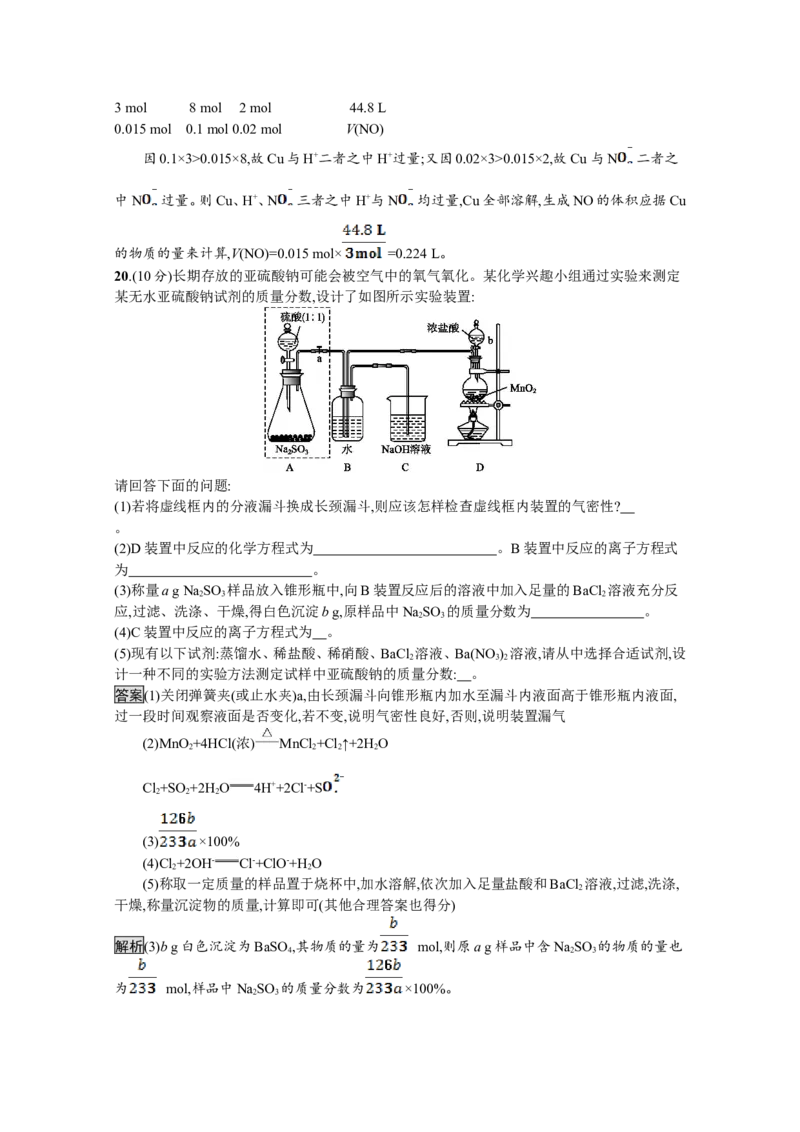
20.(10分)长期存放的亚硫酸钠可能会被空气中的氧气氧化。某化学兴趣小组通过实验来测定
某无水亚硫酸钠试剂的质量分数,设计了如图所示实验装置:
请回答下面的问题:
(1)若将虚线框内的分液漏斗换成长颈漏斗,则应该怎样检查虚线框内装置的气密性?
。
(2)D装置中反应的化学方程式为 。B装置中反应的离子方程式
为 。
(3)称量a g Na SO 样品放入锥形瓶中,向B装置反应后的溶液中加入足量的BaCl 溶液充分反
2 3 2
应,过滤、洗涤、干燥,得白色沉淀b g,原样品中NaSO 的质量分数为 。
2 3
(4)C装置中反应的离子方程式为 。
(5)现有以下试剂:蒸馏水、稀盐酸、稀硝酸、BaCl 溶液、Ba(NO ) 溶液,请从中选择合适试剂,设
2 3 2
计一种不同的实验方法测定试样中亚硫酸钠的质量分数: 。
答案(1)关闭弹簧夹(或止水夹)a,由长颈漏斗向锥形瓶内加水至漏斗内液面高于锥形瓶内液面,
过一段时间观察液面是否变化,若不变,说明气密性良好,否则,说明装置漏气
(2)MnO +4HCl(浓) MnCl +Cl↑+2H O
2 2 2 2
Cl+SO+2H O 4H++2Cl-+S
2 2 2
(3) ×100%
(4)Cl +2OH- Cl-+ClO-+H O
2 2
(5)称取一定质量的样品置于烧杯中,加水溶解,依次加入足量盐酸和BaCl 溶液,过滤,洗涤,
2
干燥,称量沉淀物的质量,计算即可(其他合理答案也得分)
解析(3)b g白色沉淀为BaSO,其物质的量为 mol,则原a g样品中含NaSO 的物质的量也
4 2 3
为 mol,样品中NaSO 的质量分数为 ×100%。
2 3