文档内容
3.1 铁及其化合物
知识点一 工业炼铁
【例1-1】(2020·云南省镇康县第一中学高一月考)下列关于铁的叙述错误的是
A.纯净的铁是光亮的银白色金属
B.铁能被磁铁吸引,在磁场作用下,铁自身也能产生磁性
C.铁是地壳中含量最多的金属元素,所以分布在地壳的铁有游离态也有化合态
D.纯铁的抗蚀能力相当强,在干燥的空气里不易被氧化
【答案】C
【解析】A.纯净的铁是光亮的银白色金属,正确;
B.铁是强磁性物质,在磁场作用下被磁化,正确;
C.铝是地壳中含量最多的金属元素,铁第二位,错误;
D.纯铁加上周围的空气又是干燥的,不能形成原电池,因此不会发生电化学腐蚀,故抗蚀能力很强,正
确。
【例1-2】(2020·全国课时练习)铁是地壳中含量非常丰富的元素,金属铁是在高炉中冶炼的,在冶金工
业中,常用焦炭来冶炼铁。
(1)写出焦炭在高炉中所参加的两个反应的化学方程式: ________________。
(2)写出赤铁矿被 还原成铁的化学方程式:__________________________。
(3)实验室中可用 还原 ,在加热 前应先_________,否则可能发生________现象;未反应
完的 ___________(填“能”或“不能”)排放到大气中,应做________处理。
【答案】(1)(2)
(3) 验纯 爆炸 不能 点燃
【解析】(1)在冶炼铁的过程中,为提高C的利用率,先发生反应 ,再发生反应
。
(2)赤铁矿的主要成分为三氧化二铁,故赤铁矿被 还原成铁的化学方程式为:
。
(3)一氧化碳属于可燃性气体,加热 之前应先检验 的纯度,否则可能发生爆炸;由于 有毒
故未反应完的 应点燃,以防污染环境。
根据金属活动性强弱,金属冶炼的方法通常包括:热还原法、电解法、热分解法等,要注意铝热法也属于
热还原法
【一隅三反】
1.(2019·全国高一)有关铁的叙述中不正确的是( )
A.铁能被磁铁吸引 B.人体的血红蛋白中含有铁元素
C.在空气中能剧烈燃烧 D.铁能与水蒸气反应
【答案】C
【解析】A.铁能被磁铁吸引,A项说法正确;
B. 人体的血红蛋白中含有铁元素,B项说法正确
C. 铁在氧气中能剧烈燃烧,在空气中不燃烧。故C项错误;
D. 铁能与水蒸气在高温条件下反应生成四氧化三铁和氢气,故D说法正确;故答案为C。
2.(2020·宁夏大学附属中学高一期末)高炉炼铁的主要反应是:Fe O+3CO=2Fe+3CO,该方法在治金
2 3 2
工业上称为
A.电解法 B.热还原法 C.热分解法 D.铝热法
【答案】B
【解析】铁较活泼,工业上采用高炉炼铁的主要反应是Fe O+3CO 2Fe+3CO ,是用还原剂在高温下
2 3 2还原氧化铁冶炼的,属于热还原法,故选B。
3.(2020·全国高一单元测试)工业炼铁的基本生产流程如图所示,请回答下列问题。
(1)写出设备A的名称:___________________________________________________。
(2)写出以赤铁矿为原料在高温下制取铁的化学方程式:__________________________。
(3)炼铁时焦炭的作用:
①________________________________________________________________________;
②________________________________________________________________________。
(4)石灰石的主要作用是造渣,造渣过程中涉及的主要反应有CaCO CaO+CO↑、__________(写化
3 2
学方程式)。
【答案】(1)炼铁高炉
(2) Fe O+3CO 2Fe+3CO
2 3 2
(3) 产生热量(或提高炉温) 生成还原剂CO
(4) CaO+SiO=CaSiO
2 3
【解析】(1)工业炼铁又称为高炉炼铁,因为工业炼铁使用的设备为:炼铁高炉;
(2)赤铁矿中的氧化铁在高温下与一氧化碳发生氧化还原反应,生成单质铁和气体二氧化碳,方程式为:
Fe O+3CO 2Fe+3CO;
2 3 2
(3)碳燃烧生成一氧化碳放出热量,同时一氧化碳具有还原性,炼铁时焦炭的作用:产生热量(或提高炉
温) 、生成还原剂CO;
(4)石灰石的主要作用是造渣生成硅酸钙,造渣过程中涉及的主要反应有CaCO CaO+CO↑、CaO
3 2
+SiO CaSiO 。
2 3
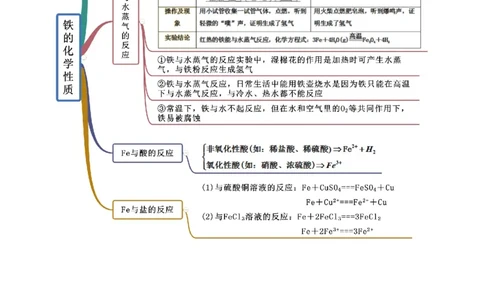
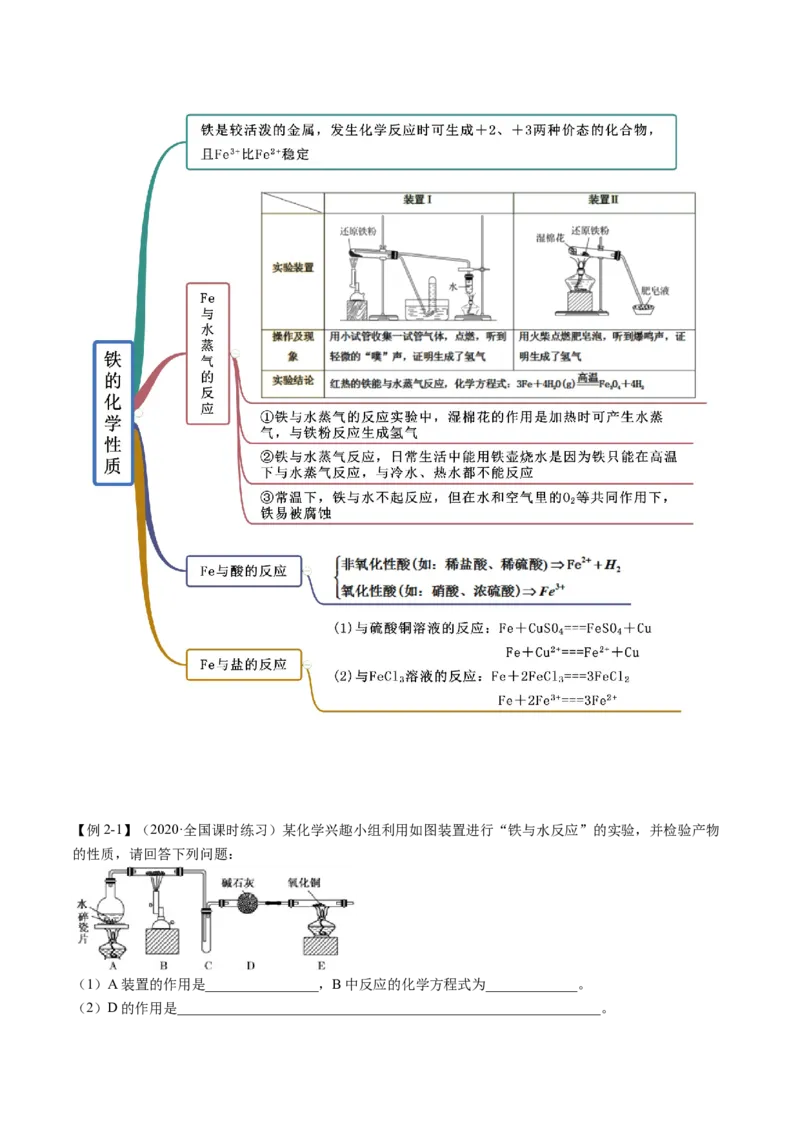
知识点二 铁的化学性质【例2-1】(2020·全国课时练习)某化学兴趣小组利用如图装置进行“铁与水反应”的实验,并检验产物
的性质,请回答下列问题:
(1)A装置的作用是________________,B中反应的化学方程式为_____________。
(2)D的作用是____________________________________________________________。(3)E中的现象是__________________________________________________________。
(4)A、B两个装置中应先点燃_______处的酒精灯,点燃E处酒精灯之前应进行的操作是
_______________________________________________________________________。
【答案】(1)产生水蒸气 3Fe+4HO(g) Fe O+4H
2 3 4 2
(2)吸收未反应的水蒸气
(3)黑色固体变为红色,右端管壁有水珠生成
(4)A 收集H,并检验其纯度
2
【解析】(1)铁与水蒸气反应的条件是高温,水的状态是气体,所以A装置的作用是产生水蒸气,B中
是铁与水蒸气反应生成氢气和四氧化三铁,方程式为3Fe+4HO(g) Fe O+4H;(2)生成的氢气
2 3 4 2
中含有水蒸气,则D中碱石灰的作用是吸收未反应的水蒸气;(3)氢气还原氧化铜得到铜和水即H+CuO
2
Cu+H O,所以实验现象是硬质玻璃管中黑色固体变为红色,硬质玻璃管右端管壁有液滴生成;
2
(4)若先点燃B处,铁会与氧气先发生反应,所以须先点燃A处;氢气是可燃性气体混有空气会发生爆
炸,所以点燃E处酒精灯之前应进行的操作是验证氢气的纯度。
【例2-2】(2020·全国高一课时练习)某同学在研究Fe与HSO 的反应时,进行了如下实验。
2 4
(1)实验Ⅰ中,铁与稀硫酸反应的离子方程式为______。
(2)实验Ⅱ中,铁丝表面迅速变黑,反应很快停止,其原因是______。
(3)实验Ⅲ中,加热后产生大量气体,B试管中溶液的红色褪去,D处始终未检测到可燃性气体。C试管
中反应的离子方程式是______。
(4)对比实验Ⅰ、Ⅱ和Ⅲ,同学们得出以下结论:
①浓硫酸和稀硫酸都具有氧化性,但原因不同。浓硫酸的氧化性源于+6价的硫元素,稀硫酸的氧化性源于
______。
②造成反应多样性的主要因素有______。
【答案】(1)Fe+2H+= Fe2++H↑
2
(2) 铁表面生成致密的氧化膜,阻止反应进一步进行
(3) SO +2OH-= SO 2-+HO
2 3 2
(4) +1价的氢元素 反应物的浓度、温度
【解析】(1)Fe和稀硫酸反应生成硫酸亚铁和氢气,离子方程式为Fe+2H+=Fe2++H ↑,故答案为
2
Fe+2H+=Fe2++H ↑;
2
(2)浓硫酸具有强氧化性,生成致密的氧化膜覆盖在Fe的表面,发生钝化,故答案为铁表面生成致密的
氧化膜,阻止反应进一步进行;(3)实验Ⅲ中,铁与稀硫酸反应生成氢气,和浓硫酸共热反应生成二氧化硫,实验中未检测到可燃性气
体,说明反应中没有氢气生成,二氧化硫具有漂白性,使品红溶液的红色褪去,二氧化硫是酸性氧化物,
与氢氧化钠溶液反应生成亚硫酸钠,反应的离子方程式为SO +2OH—=SO2—+HO,故答案为SO +2OH—
2 3 2 2
=SO2—+HO;
3 2
(4)①浓硫酸和稀硫酸都具有氧化性,但原因不同,浓硫酸的氧化性表现在+6价的硫元素上,稀硫酸的
氧化性表现在+1价的氢(H+)元素上,故答案为+1价H元素(H+);
②影响反应产物多样性的因素有浓度、温度、反应物的量等,故答案为浓度、温度、反应物的量等。
【一隅三反】
1.(2020·安徽马鞍山·)装置甲、乙、丙都是铁与水蒸气反应的实验装置,下列说法不正确的是
装置甲 装置乙 装置丙
A.选用丙装置,实验结束时先移去酒精灯,再将导气管拿出水面
B.甲装置中氯化钙的作用是除去氢气中混有的水蒸气
C.用乙装置实验时,蒸发皿中产生大量肥皂泡,点燃肥皂泡发出爆鸣声
D.三个装置相比较,乙装置简单、操作简便、节约原料、安全性好
【答案】A
【解析】A.选用丙装置,实验结束时先将导气管拿出水面,再移去酒精灯,以防发生倒吸,错误;
B.从硬质玻璃管导出的气体有生成的氢气和未反应的剩余的水蒸气,氯化钙的作用是除去氢气中混有的
水蒸气,正确;
C.用乙装置实验时,蒸发皿中产生大量肥皂泡,肥皂泡里是氢气,所以点燃肥皂泡发出爆鸣声,正确;
D.和甲、丙装置相比较,乙装置简单、操作简便、节约原料、安全性好,正确;
故选A。
2.(2020·全国课时练习)在一定条件下,下列铁与有关物质的反应,所得产物错误的是
A. B.
C. D.
【答案】C
【解析】A. 是强氧化剂,可将 氧化成 ,选项A正确;
B.S是弱氧化剂,可将 氧化成 ,选项B正确;
C. 与 反应生成 ,而不是 ,选项C错误;
D. 在 中燃烧生成 ,选项D正确。答案选C。
3.(2019·全国高一课时练习)已知红热的铁能与水蒸气反应生成氢气。现用如图所示装置进行铁在高温
下与水蒸气反应的实验,并用简单的方法收集、检验生成的氢气。请回答下列问题。(1)写出铁在高温下与水蒸气反应的化学方程式:_________________________。
(2)干燥管C中盛放的药品是__________________;干燥管的____________(填“m”或“n”)端与g导
管相连接。
(3)在D处画出用试管收集氢气的装置图(所需其他仪器自行选择)。______
(4)怎样用简单的方法检验收集到的气体是氢气?
简述实验操作步骤和现象:______________________________。
(5)若收集到标准状况下的H 22.4L,则参加反应的铁粉的质量为____________g。
2
(6)当固体质量增加32g时,生成H 的质量为________________g。
2
【答案】(1)
(2) 碱石灰(答案合理即可)
(3)
(4) 用拇指堵住试管口,试管口向上,靠近酒精灯火焰,松开拇指,发出爆鸣声,说明收集到的气体是
(5) 42
(6) 4
【解析】(1)铁在高温下与水蒸气反应生成四氧化三铁和氢气,反应的化学方程式:
。
(2)干燥管C中盛放的药品用来干燥氢气,可以是碱石灰;干燥气体时应该是粗口进,细口出,则干燥管的
n端与g导管相连接。(3)由于 的密度比空气小,可采用向下排空气法收集 ,装置图为 。
(4)检验 可采用“爆鸣”实验,即用拇指堵住试管口,试管口向上,靠近酒精灯火焰,松开拇指,发出
爆鸣声,说明收集到的气体是 。
(5)根据反应方程式 可得关系式: ,
,则 , 。
(6)固体质量增加的原因是 生成了 ,增加的质量为氧元素的质量,故生成氢气的质量为
。
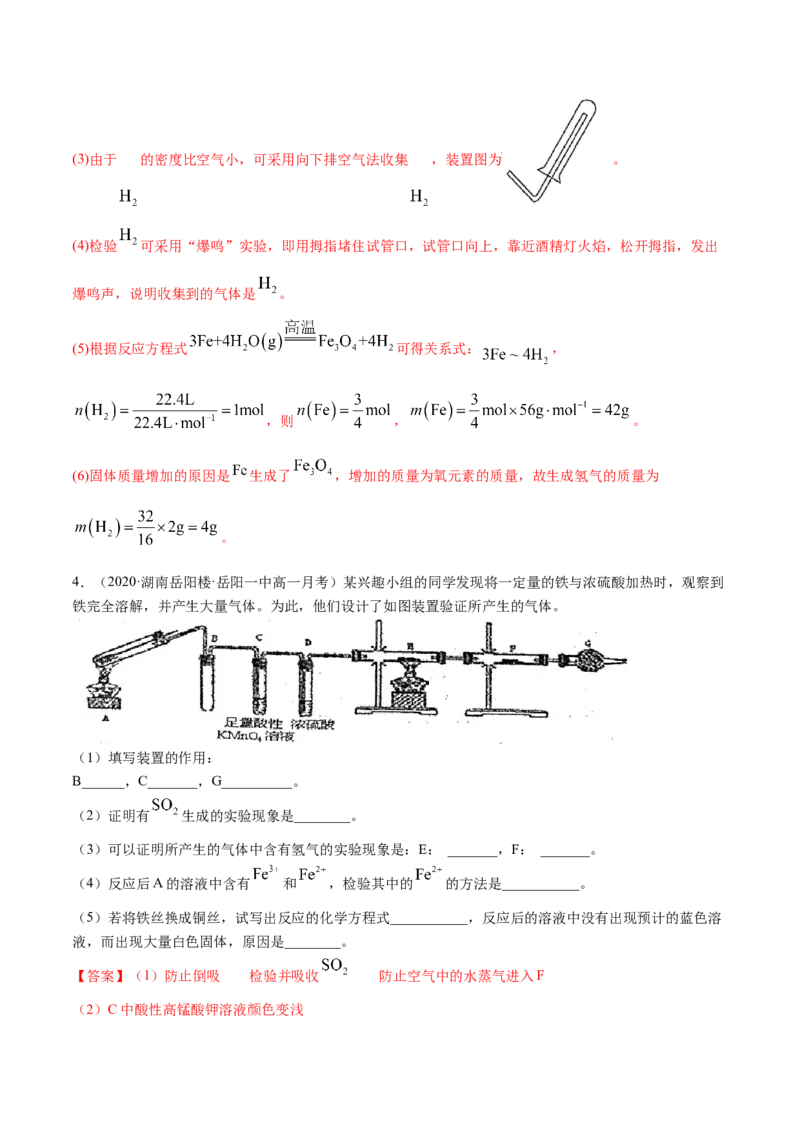
4.(2020·湖南岳阳楼·岳阳一中高一月考)某兴趣小组的同学发现将一定量的铁与浓硫酸加热时,观察到
铁完全溶解,并产生大量气体。为此,他们设计了如图装置验证所产生的气体。
(1)填写装置的作用:
B______,C_______,G__________。
(2)证明有 生成的实验现象是________。
(3)可以证明所产生的气体中含有氢气的实验现象是:E: _______,F: _______。
(4)反应后A的溶液中含有 和 ,检验其中的 的方法是___________。
(5)若将铁丝换成铜丝,试写出反应的化学方程式___________,反应后的溶液中没有出现预计的蓝色溶
液,而出现大量白色固体,原因是________。
【答案】(1)防止倒吸 检验并吸收 防止空气中的水蒸气进入F
(2)C中酸性高锰酸钾溶液颜色变浅(3)黑色固体变成红色 白色粉末变成蓝色
(4)取A的溶液滴加酸性高锰酸钾溶液,若紫(红)色褪去,证明有
(5) 浓 中的水很少,浓硫酸具有吸水性
【解析】(1)熄灭A装置中酒精灯时,A装置中气体冷却压强减小,C装置中溶液易进入A试管中产生倒吸
现象,所以B装置的作用是防止倒吸;酸性高猛酸钾溶液有强氧化性,二氧化硫能和酸性高猛酸钾溶液发
生氧化反应而使其褪色,所以酸性高猛酸钾的作用是验证有SO 生成,同时除去SO ;空气中含有水蒸气,
2 2
如果没有G装置,水蒸气进入F装置干扰实验,所以G的作用是:防止空气中的HO进入F;
2
(2)二氧化硫有还原性,酸性高猛酸钾有强氧化性,二者能发生氧化还原反应而使酸性高猛酸钾溶液颜色变
浅,所以证明有SO 生成的现象是酸性高锰酸钾变浅。
2
(3)生成的气体经洗气和干燥后剩余的气体就是氢气,氢气有还原性能和氧化铜在加热条件下发生置换反应
生成铜单质,生成的水遇无水硫酸铜时白色固体变蓝色,所以证明含有氢气的现象是:E中黑色(CuO)变成
红色(Cu),F中白色粉末变成蓝色;
(4)酸性高锰酸钾有强氧化性,亚铁离子能还原酸性高锰酸钾溶液而使其褪色,所以有铁离子共存时检验亚
铁离子的方法是:取A的溶液,滴加酸性高锰酸钾溶液,若紫色褪去,证明有Fe2+;
(5)若将铁丝换成铜丝,铜与浓硫酸加热反应生成硫酸铜、二氧化硫等,化学方程式:
Cu+2H SO =CuSO+SO+2H O;由于浓硫酸中水很少,浓硫酸具有吸水性,所以出现了大量白色固体;要
2 4 4 2 2
确认CuSO 生成,待试管冷却后,将浓硫酸倒出,在固体中加水即可。
4
知识点三 铁的氧化物
化学式 FeO Fe2O3 Fe3O4
俗名 铁红 磁性氧化铁
颜色状态 黑色粉末 红棕色粉末 黑色晶体(有晶体)
溶解性 难溶于水 难溶于水 难溶于水
铁的化合价 +2 +3 +2、+3
稳定性 不稳定 稳定 稳定
+O 2Fe O
6FeO 2 3 4
非氧化性酸 +2H+===Fe2++HO
2
FeO
(稀盐酸、稀硫酸)
O+6H+===2Fe3++3HO
2 3 2
Fe
O+8H+===Fe2++2Fe3++4H
3 4 2
Fe
氧化性酸 +10H++NO -===3Fe3++NO↑+5HO
3 2
3FeO
(硝酸、浓硫酸)
O+6H+===2Fe3++3HO
2 3 2
FeO+28H++NO -===9Fe3++NO↑+14HO
3 4 3 2
3Fe
与还原性酸(HI) +2H+===Fe2++HO
2
FeO
O+6H++2I-===2Fe2++I+3HO
2 3 2 2
Fe
O+8H++2I-===3FeI +I+4HO
3 4 2 2 2
Fe
【例3】(2020·全国专题练习)向一定量的Fe、FeO和 的混合物中加入120mL 的稀硝酸,
恰好使混合物完全溶解,放出2.688L (标准状况),向所得溶液中加入KSCN溶液,无红色出现。若用
足量的氢气在加热条件下还原相同质量的混合物,能得到铁的物质的量为( )
A.0.24mol B.0.21mol C.0.18mol D.0.14mol
【答案】C
【解析】向一定量的Fe、FeO和Fe O 的混合物中加入120mL 4mol/L的稀硝酸,恰好使混合物完全溶解,
2 3
所得溶液中加入KSCN溶液,无红色出现,则溶液中的溶质为Fe(NO ),2.668L NO(标准状况)的物质的量
3 2
为 =0.12mol,根据氮元素守恒,硝酸亚铁中的硝酸根离子的物质的量为0.12L×4mol/
L-0.12mol=0.36mol,所以硝酸亚铁的物质的量为 =0.18mol,由铁元素守恒可知,用足量的氢气在
加热条件下还原相同质量的混合物,得到铁的物质的量为n(Fe)=0.18mol,故选C。
【一隅三反】
1.(2019·全国高一课时练习)由FeO、Fe O、Fe O 组成的混合物,测得铁元素与氧元素的质量之比为
2 3 3 4
21∶8,这种混合物中FeO、Fe O、Fe O 的物质的量之比可能是( )
2 3 3 4
A.1∶2∶1 B.1∶2∶3 C.1∶3∶1 D.1∶1∶3
【答案】D
【解析】由于Fe O 中铁元素和氧元素的质量比为21:8,则Fe O 为任意量都可满足混合物中铁、氧元素
3 4 3 4
的质量之比为21:8;Fe O 可以写成FeO•Fe O,即FeO、Fe O 物质的量之比为1:1时,两种物质的混合
3 4 2 3 2 3
物中铁元素和氧元素的质量比也恰好为21:8,因此选项D正确。故答案选D。
2.(2020·全国课时练习)有FeO、 Fe O 的混合物若干克,在CO气流中加热充分反应,冷却后称剩余固
2 3
体比原混合物质量减轻1.6 g,若将同质量的混合物与盐酸反应,欲使其完全溶解需1 mol/L 的盐酸的体积
为( )
A.200mL B.100mL C.50mL D.无法计算
【答案】A
【解析】FeO、Fe O 的混合物若干克,在CO气流中加热充分反应,生成Fe,冷却后称剩余固体比原混合
2 3
物质量减轻1.6g,则减少的质量为O元素的质量,物质的量是0.1mol。将FeO、Fe O 的混合物与盐酸反应
2 3
生成FeCl 、FeCl 的混合物,相当于其中的O被Cl代替,根据化合价守恒,1个O被2个Cl代替,所以需
2 3
1 mol•L-1的盐酸的体积V(HCl)=0.2mol÷1mol/L=0.2L,即200mL,答案选A。3.(2020·全国高一课时练习)实验室用如图所示装置测定 和 固体混合物中 的质量,
装置的硬质玻璃管中的固体物质是 和 的混合物。
(1)写出 装置中发生反应的化学方程式:___________。
(2)装置 的作用是盛装的液体是__________,装置 中________,所起的作用是_________。
(3)若 和 固体混合物的质量为23.2g,反应完全后 形管的质量增加7.2g,则混合物中 的质
量为__________。
(4) 形管右边连接干燥管 的目的是____,若无干燥管 ,测得 的质量将_______(填“偏大”“偏
小”或“无影响”)。
(5)若反应后得到的残留固体中还有少量 ,测得的 质量将________(填“偏大”“偏小”或“无影
响”)。
【答案】(1) 、
(2)除去 中混有的氯化氢气体 浓硫酸 干燥
(3) 16g
(4)防止空气中的水蒸气进入 形管E中 偏大
(5) 偏小
【解析】(1)在加热条件下,氢气能还原金属氧化物,反应的化学方程式为 、
。
(2)由于生成的氢气中含有氯化氢和水蒸气,而这两种杂质都能干扰实验, 中盛有水,用来除去 中混
有的 气体;而 中盛有浓硫酸,用来干燥氢气。(3)设 和 固体的物质的量分别是 和 ,则 , 形管增加
的质量就是反应中生成的水的质量,因此有 ,解得; ,
则原混合物中 的质量是 。
(4)由于空气中也含有水蒸气,所以 装置的作用是防止空气中的水蒸气进入 中。若无干燥管F,空气中
的水蒸气被E吸收,则所测生成水的质量增大,导致氧的含量增大,所以测定结果偏大。
(5)若反应后得到的残留固体中还有少量 ,则 形管增加的质量偏小,导致氧的含量减小,所以测定
结果偏小。
知识点四 铁的氢氧化物
Fe(OH) Fe(OH)
2 3
物 物质类别 二元弱碱 三元弱碱
理 颜色状态 白色固体 红褐色固体
性 铁的价态 +2 +3
质 溶解性 难溶于水
与非氧化性 ①Fe(OH) 与盐酸反应:Fe(OH) +2H+===Fe2++HO
2 2 2
酸 ②Fe(OH) 与盐酸反应:Fe(OH) +3H+===Fe3++3HO
3 3 2
①Fe(OH) 与稀硝酸反应:3FeO+10H++NO -===3Fe3++NO↑+8HO
与氧化性酸 2 3 2
化 ②Fe(OH) 3 与稀硝酸反应:Fe(OH) 3 +3H+===Fe3++3H 2 O
学 ①Fe(OH) 与HI反应:FeO+2H+===Fe2++HO
与还原性酸 2 2
性 ②Fe(OH) 与HI反应:2Fe(OH) +6H++2I-===2Fe2++I+6HO
3 3 2 2
质
Fe(OH) 、Fe(OH) 受热均分解生成同价态的氧化物
2 3
①Fe(OH) :Fe(OH) =====FeO+HO
热稳定性 2 2 2
(隔绝空气生成FeO,在空气中最终转化为Fe O)
2 3
②Fe(OH) :2Fe(OH) =====Fe O+3HO
3 3 2 3 2
【例4】(2020·西安市航空六一八中学期末)已知A、B、C、D、G为中学化学中常见的物质,其中A为
单质,B、C、D、G均为化合物。它们之间存在以下的相互转化关系:
试回答:
(1)写出A的化学式___。
(2)如何用实验证明B溶液中是否含有G?(请写出实验的步骤、现象和结论)___。
(3)写出由E转变成F的化学方程式___。
(4)向G溶液中加入A的有关离子反应方程式___。【答案】(1)Fe(2)取少量B溶液于试管中,滴入几滴KSCN溶液,溶液显红色说明含有G,否则不含
G
(3)4Fe(OH)+2H O+O=4Fe(OH) (4) 2Fe3++Fe=3Fe2+
2 2 2 3
【解析】根据以上分析:
(1)A是单质铁,化学式为Fe。
(2)B是FeCl ,G是FeCl ,Fe3+遇KSCN变红色,取少量B溶液于试管中,滴入几滴KSCN溶液,溶液
2 3
显红色说明含有FeCl ,否则不含FeCl 。
3 3
(3)E是Fe(OH) 、F是Fe(OH) ,白色沉淀E在空气中变为红褐色沉淀F,化学方程式是4Fe(OH)
2 3
+2H O+O=4Fe(OH) 。
2 2 2 3
(4)向FeCl 溶液中加入铁粉生成FeCl ,反应方程式是2Fe3++Fe=3Fe2+。
3 2
【一隅三反】
1.(2020·福建鲤城·泉州五中高一单元测试)下列说法正确的是( )
①多数金属氧化物、氢氧化物不溶于水②多数不溶于水的金属氢氧化物可与酸反应,生成盐和水
③氧化铝是两性氧化物 ④氢氧化亚铁为灰绿色⑤氢氧化铁为红褐色
⑥铜绿的主要成分是Cu (OH) CO
2 2 3
A.①②③⑥ B.③④⑤⑥
C.①②③⑤⑥ D.②③④⑤⑥
【答案】C
【解析】①多数金属的氧化物、氢氧化物不溶于水,也不与水发生反应,如FeO、MgO、Fe(OH) 等故①
3
正确;
②多数不溶于水的金属氢氧化物可与酸反应,生成盐和水,如氢氧化铁、氢氧化镁分别与盐酸反应生成氯
化铁、氯化镁和水,故②正确;
③氧化铝既能与强酸反应生成盐和水,也能与强碱反应生成盐和水,所以氧化铝是两性氧化物,故③正确;
④氢氧化亚铁是白色不溶于水的物质,很容易被氧化,故④错误;
⑤氢氧化铁为红褐色,故⑤正确;
⑥铜在空气中能够发生反应生成铜绿,反应方程式为:2Cu+O +H O+CO= Cu (OH) CO,所以铜绿的主要
2 2 2 2 2 3
成分是Cu (OH) CO,故⑥正确;根据上面分析①、②、③、⑤、⑥的说法正确;答案选C。
2 2 3
2.(2020·全国高一单元测试)关于氢氧化铁和氢氧化亚铁的下列叙述中错误的是 ( )
A.都是不溶于水的固体B.都能与酸反应生成盐和水
C.不稳定,受热都能分解D.在空气中都容易被氧化
【答案】D
【解析】A、氢氧化铁、氢氧化亚铁都是不溶于水的固体,故A说法正确;
B、氢氧化铁、氢氧化亚铁属于碱,与酸发生中和反应,生成盐和水,故B说法正确;
C、氢氧化铁受热分解成Fe O 和HO,氢氧化亚铁隔绝空气受热分解为FeO和HO,故C说法正确;
2 3 2 2
D、氢氧化铁中Fe元素显+3价,处于最高价只具有氧化性,在空气中不易被氧化;而Fe(OH) 中铁元素
2
化合价为+2价,处于中间价态,以还原性为主,在空气中容易被氧化成Fe(OH) ,故D说法错误;答案为
3
D。
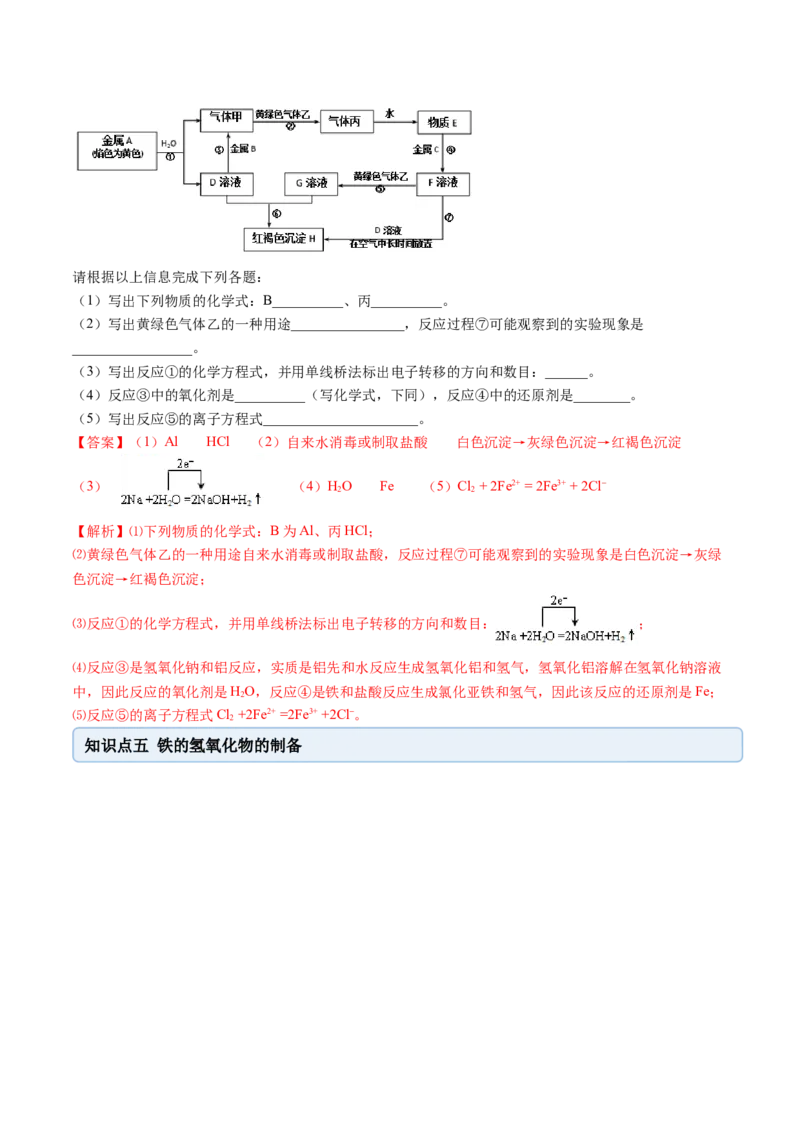
3.(2020·四川省宜宾市第四中学校高一月考)现有金属单质A、B、C和气体甲、乙、丙以及物质D、
E、F、G、H,它们之间的相互转化关系如图所示(图中有些反应的生成物和反应的条件没有标出)。请根据以上信息完成下列各题:
(1)写出下列物质的化学式:B__________、丙__________。
(2)写出黄绿色气体乙的一种用途________________,反应过程⑦可能观察到的实验现象是
_________________。
(3)写出反应①的化学方程式,并用单线桥法标出电子转移的方向和数目:______。
(4)反应③中的氧化剂是__________(写化学式,下同),反应④中的还原剂是________。
(5)写出反应⑤的离子方程式______________________。
【答案】(1)Al HCl (2)自来水消毒或制取盐酸 白色沉淀→灰绿色沉淀→红褐色沉淀
(3) (4)HO Fe (5)Cl + 2Fe2+ = 2Fe3+ + 2Cl–
2 2
【解析】⑴下列物质的化学式:B为Al、丙HCl;
⑵黄绿色气体乙的一种用途自来水消毒或制取盐酸,反应过程⑦可能观察到的实验现象是白色沉淀→灰绿
色沉淀→红褐色沉淀;
⑶反应①的化学方程式,并用单线桥法标出电子转移的方向和数目: ;
⑷反应③是氢氧化钠和铝反应,实质是铝先和水反应生成氢氧化铝和氢气,氢氧化铝溶解在氢氧化钠溶液
中,因此反应的氧化剂是HO,反应④是铁和盐酸反应生成氯化亚铁和氢气,因此该反应的还原剂是Fe;
2
⑸反应⑤的离子方程式Cl +2Fe2+ =2Fe3+ +2Cl–。
2
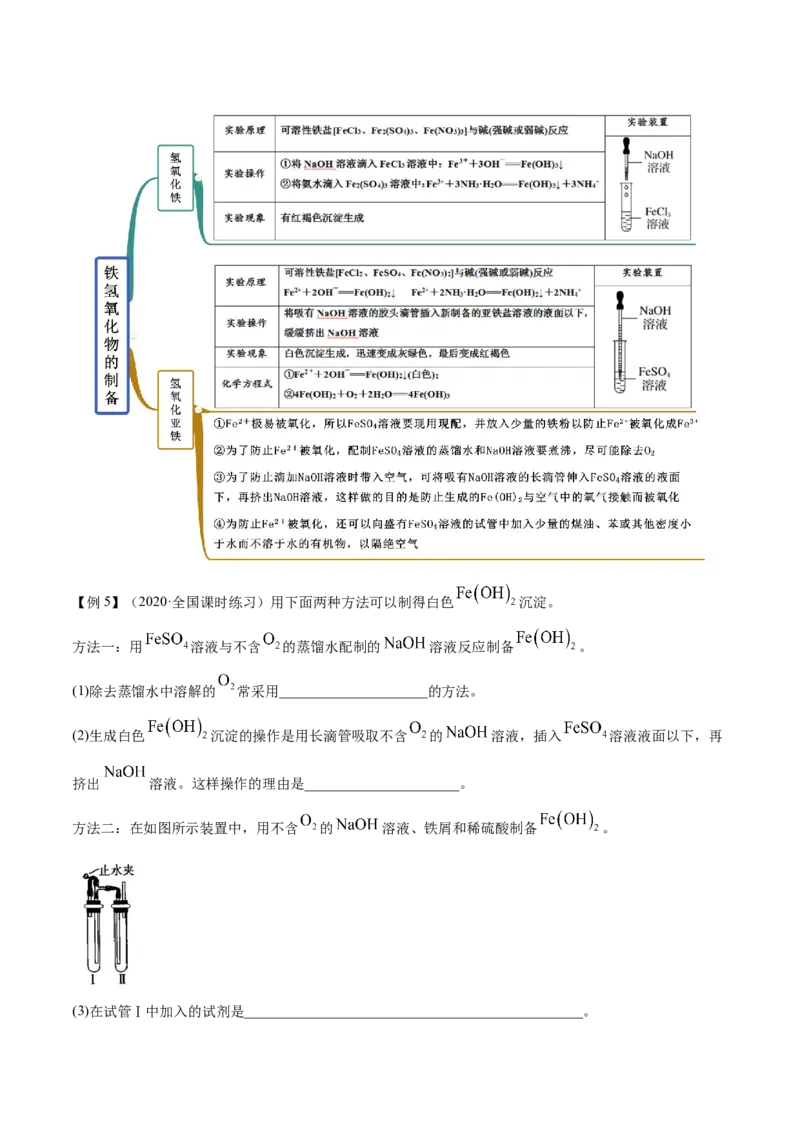
知识点五 铁的氢氧化物的制备【例5】(2020·全国课时练习)用下面两种方法可以制得白色 沉淀。
方法一:用 溶液与不含 的蒸馏水配制的 溶液反应制备 。
(1)除去蒸馏水中溶解的 常采用_____________________的方法。
(2)生成白色 沉淀的操作是用长滴管吸取不含 的 溶液,插入 溶液液面以下,再
挤出 溶液。这样操作的理由是______________________。
方法二:在如图所示装置中,用不含 的 溶液、铁屑和稀硫酸制备 。
(3)在试管Ⅰ中加入的试剂是________________________________________________。(4)在试管Ⅱ中加入的试剂是________________________________________________。
(5)为了制得白色 沉淀,在试管Ⅰ和试管Ⅱ中加入试剂,打开止水夹,塞紧塞子后的实验步骤是
________________________________________________________________________。
(6)这样生成的 沉淀能较长时间保持白色,其理由是
_____________________________________________________________________。
【答案】(1)煮沸
(2)避免生成的 沉淀接触 而被氧化
(3)稀硫酸﹑铁屑
(4)不含氧气的 溶液
(5) 检验试管Ⅱ出口处 的纯度,当排出的 纯净时,再夹紧止水夹
(6)试管Ⅰ中反应生成的 充满了试管Ⅰ和试管Ⅱ,且外界空气不易进入装置中
【解析】(1)常采用煮沸的方法除去蒸馏水中的 ;故答案为:煮沸。
(2)题述操作是为了防止滴加 溶液时带入空气,避免生成的 接触 ;故答案为:避免生
成的 沉淀接触 而被氧化。
(3)根据分析试管Ⅰ反应生成氢气和硫酸亚铁,因此加入的试剂是稀硫酸﹑铁屑;故答案为:稀硫酸﹑铁屑。
(4)根据分析试管Ⅱ发生硫酸亚铁和氢氧化钠反应生成氢氧化亚铁沉淀,试管Ⅰ是制备硫酸亚铁,因此试管
Ⅱ盛放的试剂是NaOH溶液;故答案为:不含氧气的 溶液。
(5)当把Fe与稀硫酸加入试管Ⅰ中后,打开止水夹,产生的 可排尽装置内的空气。最后关闭止水夹;故
答案为:检验试管Ⅱ出口处 的纯度,当排出的 纯净时,再夹紧止水夹。
(6)试管Ⅰ内产生的 无法逸出,压强增大将试管Ⅰ内的 溶液通过长导管压入试管Ⅱ内,在此过程
中,液体处于 氛围中, 不易被氧化,能较长时间保持白色;故答案为:试管Ⅰ中反应生成的
充满了试管Ⅰ和试管Ⅱ,且外界空气不易进入装置中。
【一隅三反】
1.(2019·全国高一课时练习)如图所示装置可用来制取Fe(OH) 和观察Fe(OH) 在空气中被氧化时的颜色
2 2
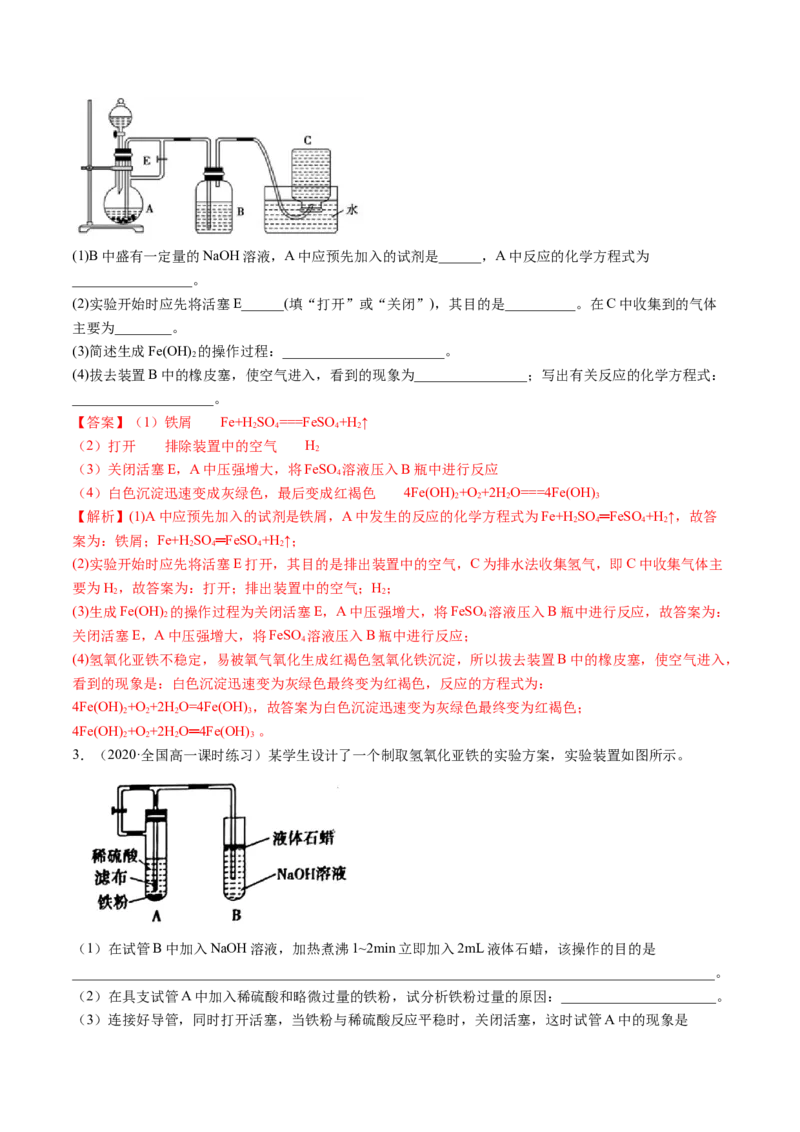
变化。实验时必须使用铁屑、6 mol·L−1硫酸,其他试剂任选。填写下列空白:(1)B中盛有一定量的NaOH溶液,A中应预先加入的试剂是______,A中反应的化学方程式为
_________________。
(2)实验开始时应先将活塞E______(填“打开”或“关闭”),其目的是__________。在C中收集到的气体
主要为________。
(3)简述生成Fe(OH) 的操作过程:_______________________。
2
(4)拔去装置B中的橡皮塞,使空气进入,看到的现象为________________;写出有关反应的化学方程式:
____________________。
【答案】(1)铁屑 Fe+H SO ===FeSO+H ↑
2 4 4 2
(2)打开 排除装置中的空气 H
2
(3)关闭活塞E,A中压强增大,将FeSO 溶液压入B瓶中进行反应
4
(4)白色沉淀迅速变成灰绿色,最后变成红褐色 4Fe(OH) +O +2H O===4Fe(OH)
2 2 2 3
【解析】(1)A中应预先加入的试剂是铁屑,A中发生的反应的化学方程式为Fe+H SO ═FeSO +H ↑,故答
2 4 4 2
案为:铁屑;Fe+H SO ═FeSO +H ↑;
2 4 4 2
(2)实验开始时应先将活塞E打开,其目的是排出装置中的空气,C为排水法收集氢气,即C中收集气体主
要为H,故答案为:打开;排出装置中的空气;H;
2 2
(3)生成Fe(OH) 的操作过程为关闭活塞E,A中压强增大,将FeSO 溶液压入B瓶中进行反应,故答案为:
2 4
关闭活塞E,A中压强增大,将FeSO 溶液压入B瓶中进行反应;
4
(4)氢氧化亚铁不稳定,易被氧气氧化生成红褐色氢氧化铁沉淀,所以拔去装置B中的橡皮塞,使空气进入,
看到的现象是:白色沉淀迅速变为灰绿色最终变为红褐色,反应的方程式为:
4Fe(OH) +O +2H O=4Fe(OH) ,故答案为白色沉淀迅速变为灰绿色最终变为红褐色;
2 2 2 3
4Fe(OH) +O +2H O═4Fe(OH) 。
2 2 2 3
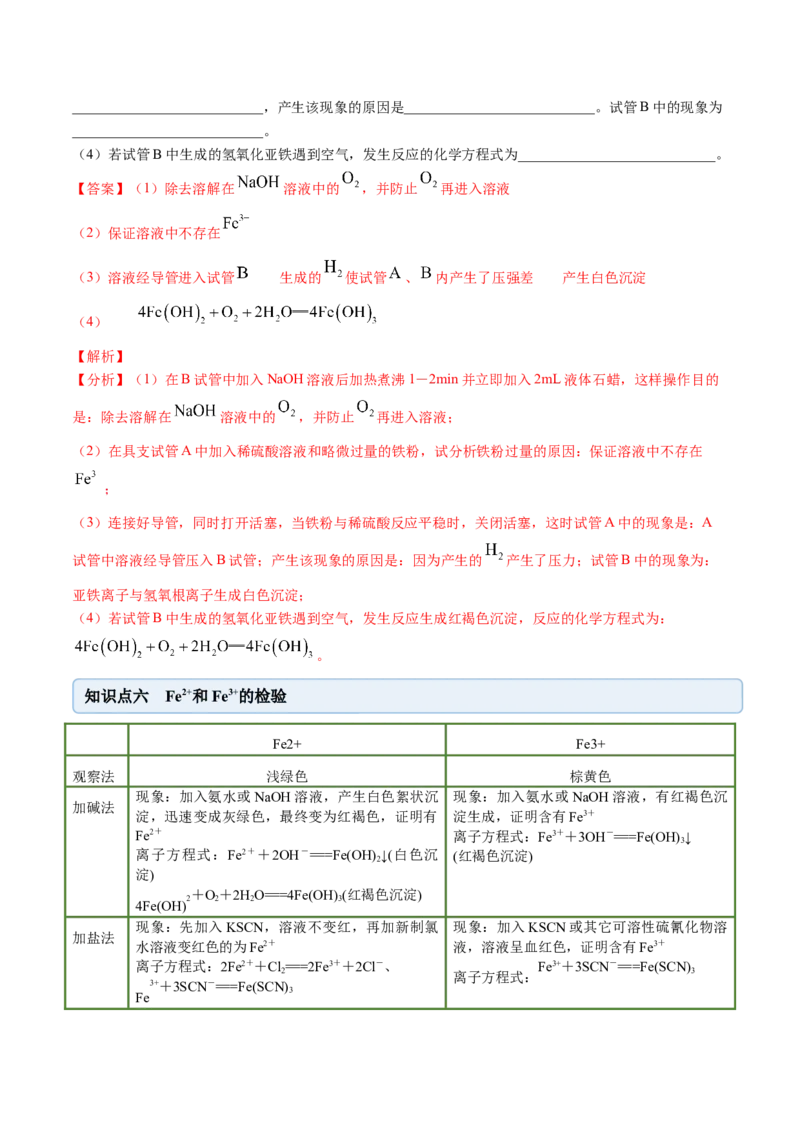
3.(2020·全国高一课时练习)某学生设计了一个制取氢氧化亚铁的实验方案,实验装置如图所示。
(1)在试管B中加入NaOH溶液,加热煮沸1~2min立即加入2mL液体石蜡,该操作的目的是
___________________________________________________________________________________________。
(2)在具支试管A中加入稀硫酸和略微过量的铁粉,试分析铁粉过量的原因:______________________。
(3)连接好导管,同时打开活塞,当铁粉与稀硫酸反应平稳时,关闭活塞,这时试管A中的现象是___________________________,产生该现象的原因是___________________________。试管B中的现象为
___________________________。
(4)若试管B中生成的氢氧化亚铁遇到空气,发生反应的化学方程式为____________________________。
【答案】(1)除去溶解在 溶液中的 ,并防止 再进入溶液
(2)保证溶液中不存在
(3)溶液经导管进入试管 生成的 使试管 、 内产生了压强差 产生白色沉淀
(4)
【解析】
【分析】(1)在B试管中加入NaOH溶液后加热煮沸1-2min并立即加入2mL液体石蜡,这样操作目的
是:除去溶解在 溶液中的 ,并防止 再进入溶液;
(2)在具支试管A中加入稀硫酸溶液和略微过量的铁粉,试分析铁粉过量的原因:保证溶液中不存在
;
(3)连接好导管,同时打开活塞,当铁粉与稀硫酸反应平稳时,关闭活塞,这时试管A中的现象是:A
试管中溶液经导管压入B试管;产生该现象的原因是:因为产生的 产生了压力;试管B中的现象为:
亚铁离子与氢氧根离子生成白色沉淀;
(4)若试管B中生成的氢氧化亚铁遇到空气,发生反应生成红褐色沉淀,反应的化学方程式为:
。
知识点六 Fe2+和Fe3+的检验
Fe2+ Fe3+
观察法 浅绿色 棕黄色
现象:加入氨水或NaOH溶液,产生白色絮状沉 现象:加入氨水或NaOH溶液,有红褐色沉
加碱法
淀,迅速变成灰绿色,最终变为红褐色,证明有 淀生成,证明含有Fe3+
Fe2+ 离子方程式:Fe3++3OH-===Fe(OH) ↓
3
离子方程式:Fe2++2OH-===Fe(OH) ↓(白色沉 (红褐色沉淀)
2
淀)
+O+2HO===4Fe(OH) (红褐色沉淀)
2 2 2 3
4Fe(OH)
现象:先加入KSCN,溶液不变红,再加新制氯 现象:加入KSCN或其它可溶性硫氰化物溶
加盐法
水溶液变红色的为Fe2+ 液,溶液呈血红色,证明含有Fe3+
离子方程式:2Fe2++Cl===2Fe3++2Cl-、 Fe3++3SCN-===Fe(SCN)
2 离子方程式: 3
3++3SCN-===Fe(SCN)
3
FeKMnO 法:加入少量酸性 KMnO 溶液,能使 淀粉KI试纸法:能使淀粉KI试纸变蓝,证
其他方 4 4
KMnO 溶液的紫红色变浅,证明有Fe2+ 明含有Fe3+
4
法 离子方程式:5Fe2++MnO -+8H+===5Fe3++ 离子方程式:2Fe3++2I-===2Fe2++I
4 2
Mn2++4HO 铜片法:加入铜片,铜片溶解且溶液变为蓝
2
色,证明含有Fe3+
2Fe3++Cu===2Fe2++Cu2+
离子方程式:
【例6】(2020·广东湛江·期末)某班同学用如下实验探究Fe2+、Fe3+的性质。回答下列问题:
(1)甲组同学取2mL FeCl 溶液,加入过量的铁粉,充分反应后,观察到溶液由________色变为________色。
3
(2)乙组同学取2mL FeCl 溶液,加入少量KI溶液,再加入少量淀粉溶液,淀粉变蓝,请说明淀粉变蓝的原
3
因______________________。
(3)丙组同学取2mL FeCl 溶液,加入几滴氯水,再加入2-3滴KSCN溶液,溶液变红,说明氯水可将Fe2+氧
2
化。FeCl 溶液与氯水反应的离子方程式为:__________________。
2
(4)丁组同学认为丙组的实验不够严谨,该组同学在2mLFeCl 溶液中先加入0.5mL植物油,再于液面下依
2
次加入几滴氯水和2-3滴KSCN溶液,溶液变红,植物油的作用是___________________________________。
(5)甲组同学和乙组同学的实验说明了Fe3+具有________性(填“氧化”或者“还原”,下同)。丙组同学和
丁组同学的实验说明了Fe2+具有________性。
【答案】(1)黄 浅绿
(2) 2FeCl + 2KI=I + 2FeCl + 2KCl
3 2 2
(3) 2Fe2++Cl=2Fe3++2Cl-
2
(4) 隔绝空气(排除氧气对实验的影响)
(5) 氧化 还原
【解析】(1)甲组同学取2mL FeCl 溶液,加入过量的铁粉,充分反应后氯化铁被铁还原生成氯化亚铁,因
3
此观察到溶液由黄色变为浅绿色。
(2)乙组同学取2mL FeCl 溶液,加入少量KI溶液,铁离子把碘离子氧化为单质碘,碘遇淀粉显蓝色,因此
3
再加入少量淀粉溶液,淀粉变蓝,反应的方程式为2FeCl + 2KI=I + 2FeCl + 2KCl。
3 2 2
(3)丙组同学取2mL FeCl 溶液,加入几滴氯水,氯水具有强氧化性,把氯化亚铁氧化为氯化铁,因此再加
2
入2~3滴KSCN溶液,溶液变红,FeCl 溶液与氯水反应的离子方程式为2Fe2++Cl=2Fe3++2Cl-。
2 2
(4)由于氯化亚铁也容易被空气中的氧气氧化为氯化铁,因此丁组同学认为丙组的实验不够严谨,所以需要
在2mLFeCl 溶液中先加入0.5mL植物油,其中植物油的作用是隔绝空气(排除氧气对实验的影响)。
2
(5)根据以上分析可知甲组同学和乙组同学的实验说明了Fe3+具有氧化性。丙组同学和丁组同学的实验说明
了Fe2+具有还原性。
【一隅三反】
1.(2020·全国课时练习)下列除杂试剂或方法不正确的是( )
选项 被提纯物质 杂质 除杂试剂或方法
A FeCl 溶液 FeCl 通入适量Cl
3 2 2
B FeCl 溶液 FeCl 加入过量铁粉并过滤
2 3
C 铁粉 铝粉 加入过量NaOH溶液并过滤
D Fe(OH) Fe(OH) 在空气中灼烧
3 2【答案】D
【解析】A.氯化亚铁和氯气反应生成氯化铁,故正确;
B.氯化铁和铁反应生成氯化亚铁,故正确;
C.铝和氢氧化钠反应生成偏铝酸钠和氢气,铁不与氢氧化钠反应,故正确;
D.氢氧化亚铁在空气中灼烧最后生成氧化铁,氢氧化铁灼烧生成氧化铁,故不能除杂,故错误
故选D。
2.(2020·全国课时练习)为了检验某未知溶液中是否含有 ,一位同学设计了以下实验方案:向一支
装有该未知溶液的试管中先通入 ,再滴加KSCN溶液,溶液呈红色,证明该未知溶液中含有 。回
答以下问题:
(1)你认为此方案是否合理?________________(填“合理”或“不合理”),若不合理,要检验
应如何操作?________________(若填“合理”,则此空可不答)。
(2)现向一支装有 溶液的试管中滴加 溶液,可观察到的现象是_____________________,有
关反应的化学方程式为_________________________________________。
(3)为了防止 变质,实验室在保存 溶液时常向其中加入铁粉,其原因是
_________________________________________(用离子方程式表示)。
【答案】(1)不合理 先滴加KSCN溶液,若无明显现象,再通入 ,溶液变为红色,则原未知溶液
中含有
(2)产生白色絮状沉淀,沉淀迅速变成灰绿色,最终变成红褐色
,
(3)
【解析】(1)若先向溶液中通入 ,再滴加KSCN溶液,溶液呈红色,说明通入 后的溶液中含
,但不能证明原未知溶液中含有 ,故应先滴加KSCN溶液,若无明显现象,再通入 溶液变
为红色,证明原未知溶液中含有 。故答案为:不合理;先滴加KSCN溶液,若无明显现象,再通入
,溶液变为红色,则原未知溶液中含有 ;
(2)向 溶液中滴加 溶液,产生 白色絮状沉淀,因 易被溶解在溶液中的O 氧化为 ,故沉淀会迅速变为灰绿色,最终变为红褐色的 。故答案为:产生白色絮状
2
沉淀,沉淀迅速变成灰绿色,最终变成红褐色; ,
;
(3)实验室在保存 溶液时常向其中加入铁粉,铁能将铁离子还原成亚铁离子, 。
故答案为: 。
3.(2020·全国课时练习)某班同学用如下实验探究Fe2+、Fe3+的性质。回答下列问题:
(1)分别取一定量氯化铁、氯化亚铁固体,均配制成0.1mol/L的溶液。在FeCl 溶液中需加入少量铁屑,其
2
目的是________________________________。
(2)甲组同学取2mL FeCl 溶液,加入几滴氯水,再加入1滴KSCN溶液,溶液变红,说明Cl 可将氧化。
2 2
FeCl 溶液与氯水反应的离子方程式为________________________。
2
(3)乙组同学认为甲组的实验不够严谨,该组同学在2mL FeCl 溶液中先加入0.5mL煤油,再于液面下依次
2
加入几滴氯水和1滴KSCN溶液,溶液变红,煤油的作用是________________________。
(4)丙组同学取10mL0.1mol/LKI溶液,加入6mL0.1mol/L FeCl 溶液混合。分别取2mL此溶液于3支试管中
3
进行如下实验:
①第一支试管中加入1mLCCl 充分振荡、静置,CCl 层显紫色;
4 4
②第二支试管中加入1滴K[(CN) ]溶液,生成蓝色沉淀;
3 6
③第三支试管中加入1滴KSCN溶液,溶液变红。
实验②检验的离子是________(填离子符号);实验①和③说明:在 过量的情况下,溶液中仍含有
________(填离子符号)。
【答案】(1)防止Fe2+被氧化
(2) 2Fe2++Cl=2Fe3++2Cl-
2
(3) 隔绝空气(排除氧气对实验的干扰)
(4) Fe2+ Fe3+
【解析】(1)Fe2+易被O 氧化为Fe3+,向FeCl 溶液中加入少量铁脣可防止Fe2+被氧化。
2 2
(2)溶液变红,说明有Fe3+生成,氯水将Fe2+氧化为Fe3+的离子方程式为2Fe2++Cl=2Fe3++2Cl-。
2
(3)因为空气中的O 也能将Fe2+氧化成Fe3+,加入煤油(密度小于水)隔绝空气,可以排除氧气对实验的干扰。
2
(4)实验②中的K[(CN) ]溶液用于检验Fe2+。根据实验①,CCl 层显紫色,说明有I 生成;根据实验②,生
3 6 4 2
成蓝色沉淀,说明有Fe2+生成;根据实验③,溶液变红,说明有Fe3+存在。