文档内容
3.2.2 pH的计算(分层作业)
1.25℃时,下列溶液的pH=12的是
A.0.002mol/LHCl溶液 B.0.005mol/L Ba(OH) 溶液
2
C.0.001mol/LKOH溶液 D.0.01mol/L HF溶液
2.若N 为阿伏加德罗常数的值。下列说法正确的是
A
A.标准状况下,11.2L CCl 的分子数为0.5N
4 A
B.4.0D 16O和14ND 的混合物中含有的电子数为2N
2 3 A
C.常温下,1LpH=2的硫酸溶液中含有H+的数目为0.02N
A
D.120g由NaHSO 和MgSO 组成的混合固体中SO2- 数目为N
4 4 4 A
3.下列说法不正确的是
A.测定0.1mol/L醋酸溶液的pH可证明醋酸是弱电解质
B.稀释氨水,溶液中c(H+)增加
C.常温下,将1mL pH=5的盐酸稀释至1L,c(H+)约为1×10-8mol/L
D.相同温度下,中和相同pH、相同体积的盐酸和醋酸溶液,消耗NaOH物质的量不同
4.常温下,关于溶液的稀释下列说法正确的是
A.pH=3的醋酸溶液稀释100倍,pH<5
B.pH=2的HSO 溶液加水稀释100倍,溶液中由水电离产生的c(H+)=1×10-4mol·L-1
2 4
C.将1L 0.1mol·L-1的HSO 溶液稀释为2L,pH=1.3
2 4
D.pH=8的NaOH溶液稀释1000倍,其pH=5
5.化学中常用pH表示水溶液的酸碱度,其定义为pH=-1g c(H+)。下列有关叙述不正确的是
A.等质量的NaOH分别与pH均为3的盐酸和醋酸溶液恰好完全反应,消耗盐酸的体积更少
B.0.1mol/L的盐酸和0.1mol/L醋酸分别加水稀释至pH=5,盐酸加水体积更多
C.pH=3的醋酸溶液加水稀释使其体积变为原来的10倍,所得溶液pH小于4
D.向pH=3的醋酸溶液中加入等体积pH=3的盐酸溶液,醋酸的电离平衡不移动
6.常温下将pH=1的硫酸平均分成两等份,一份加入适量水,另一份加入与该硫酸溶液物质的量浓度相同
的氢氧化钠溶液,两者pH都增大了1。加入水和NaOH溶液的体积比为
A.11∶1 B.10∶1 C.6∶1 D.5∶1
7.常温下将以下两溶液等体积混合后,所得溶液pH=7的是
A.0.1mol/L HCl与pH=11的NaOHB.0.1mol/L CHCOOH与0.1mol/L NaOH
3
C.pH=3的HSO 与pH=11的NaOH
2 4
D.pH=3的CHCOOH与pH=11的NaOH
3
8.求室温下,下列溶液的pH(已知:lg2≈0.3):
(1)某HSO 溶液的浓度是0.005mol·L-1
2 4
①此溶液的pH为 。
②用水稀释到原来体积的100倍,pH为 。
③再继续稀释104倍,pH为 。
(2)pH=3的盐酸与pH=5的硫酸等体积混合,pH为 。
(3)pH=10和pH=12的两种NaOH溶液等体积混合,pH为 。
(4)pH=12的NaOH溶液和pH=4的HCl溶液等体积混合,pH为 。
9.25℃时,pH=a的两种碱溶液各10mL,分别加水稀释到1000mL,其pH与溶液体积(V)的关系如图所示,
下列说法不正确的是
A.若a=11,则NOH为强碱
B.两种碱的物质的量浓度肯定不等
C.均稀释100倍以后,MOH溶液中水的电离程度大于NOH溶液
D.若两者均为弱碱,则a<11,且NOH碱性强于MOH
10.常温下,pH=11的X、Y两种碱溶液各5 mL,分别加水稀释至500 mL,其pH与溶液的体积(V)的关
系如图所示。下列说法正确的是A.Y溶液的导电性比X溶液的导电性强
B.稀释后,X溶液中水的电离程度比Y溶液中水的电离程度小
C.若X、Y都是弱碱,则a的值一定小于9
D.完全中和X、Y两溶液时,消耗同浓度稀硫酸的体积:V(X)>V(Y)
11.下列说法正确的是
A.常温时,若测得HA溶液pH=a,取该溶液10.0mL,加蒸馏水稀释至100.0mL,测得pH=b,
,则HA是弱酸
B.常温时,用pH=3和pH=2的醋酸溶液中和等量的NaOH溶液,所消耗的醋酸溶液的体积分别为V
a
和V,则V>V
b a b
C.常温时,将pH=2的硫酸溶液和pH=2的醋酸溶液分别稀释成pH=5的溶液,加水的体积:前者>后
者
D.常温时,由水电离出来的c(H+)=10-13mol/L的溶液中,K+、HCO- 、NO- 、I-可能大量共存
3 3
12.已知25 ℃时二元酸HA的K =1.3×10-7,K =7.1×10-15.下列说法正确的是
2 a1 a2
A.在等浓度的HA、NaHA溶液中,HA-电离程度相同
2
B.向0.1 mol·L-1的HA溶液中通入HCl气体(忽略溶液体积的变化)至pH=3,则HA的电离度为
2 2
0.013%
C.用蒸馏水润湿的pH试纸测HA溶液的pH值,测定结果一定偏低
2
D.取pH=a的HA溶液10 mL,加蒸馏水稀释至100 mL,则该溶液pH>a+1
2
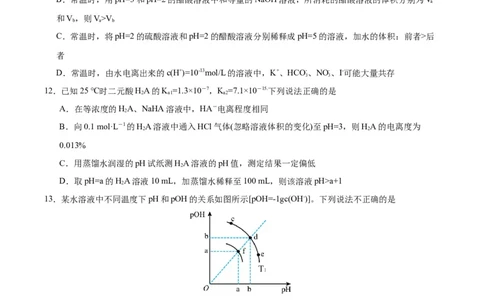
13.某水溶液中不同温度下pH和pOH的关系如图所示[pOH=-1gc(OH-)]。下列说法不正确的是
A.若a=7,则T<25℃
1
B.e点溶液中通入NH ,可使e点迁移至d点
3
C.若b=6,则该温度下将pH=2的稀硫酸与pH=10的KOH溶液等体积混合后,溶液显中性
D.f、d两点的K 比较,前者大
W
14.某温度下,HNO 和CHCOOH的电离常数分别为5.0×10-4和1.7×10-4,将pH和体积均相同的两种酸溶
2 3
液分别稀释,其pH随加水体积的变化如图所示。下列叙述正确的是A.b点酸的总物质的量浓度小于c点酸的总物质的量浓度
B.酸的电离程度:c>d;a点溶液中,c(NO )<c(CHCOO-)
3
C.导电能力强弱:d>c;a点K 的数值比d点K 的数值大
a a
D.c点和d点的两溶液分别与NaOH恰好中和后,溶液中n(Na+)相同
15.回答下列问题。
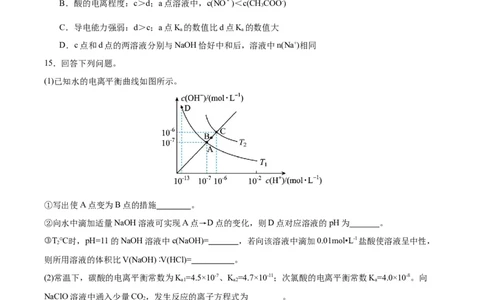
(1)已知水的电离平衡曲线如图所示。
①写出使A点变为B点的措施 。
②向水中滴加适量NaOH溶液可实现A点→D点的变化,则D点对应溶液的pH为 。
③T℃时,pH=11的NaOH溶液中c(NaOH)= ,若向该溶液中滴加0.01mol•L-1盐酸使溶液呈中性,
2
则所用溶液的体积比V(NaOH) ∶V(HCl)= 。
(2)常温下,碳酸的电离平衡常数为K =4.5×10-7、K =4.7×10-11;次氯酸的电离平衡常数K=4.0×10-8。向
a1 a2 a
NaClO溶液中通入少量CO,发生反应的离子方程式为 。
2
(3)已知次磷酸(H PO )是一元弱酸。
3 2
①写出HPO 的电离方程式 ,室温下,pH=2的次磷酸溶液中,由水电离出的c(H+)=
3 2
mol•L-1。