文档内容
第三章《铁 金属材料》教学设计
第二节 金属材料
第二课时 新型合金 物质的量在化学方程式计算中的应用
课题: 3.2.1 新型合金 物质的量在化学方程式 课时
1 授课年级 高一
计算中的应用
课标 知道生活中的新型合金,能基于物质的量认识物质的组成及其化学变化,运用物质的量及
要求 相关物理量根据化学方程式进行简单计算
本节内容是人教版(2019版)必修第一册中第三章第二节《金属材料》的内容。铁合金是
重要的金属材料,鉴于金属材料在国民经济中的重要地位和日常生活中的广泛应用,教材安排
了本节内容,反映化学与生产、生活实际的联系,让学生了解金属材料的重要作用和面临的挑
战,激发学生的爱国热情和社会责任感。本节内容包括"铁合金"、“铝和铝合金”、“新型合
金”及"物质的量在化学方程式计算中的应用"等内容。教材按照"铁合金→铝和铝合金→新型合
金"的顺序介绍了金属材料。在第二章的第三节学习了"物质的量"的基础上,为了分散学习难
点,把"物质的量在化学方程式计算中的应用"安排在本节里。
本节在介绍金属材料之前,先介绍了合金的结构特点。在介绍铁合金时,教材介绍了生铁
和钢,联系实际创设真实情境,配合图片说明了它们的用途,并采取框图的方式重点介绍了碳
素钢。教材还介绍了特种钢,并在"资料卡片"中介绍钢中合金元素的主要作用,在"科学·技术.
社会"中介绍了2017年我国成功研制的超级钢。另外,结合金属材料的检测,在"化学与职
业"栏目介绍了测试工程师这个与化学专业相关的职业。
在介绍铝和铝合金时,由于课程标准中没有要求系统介绍铝及其化合物的知识,而在主题
“物质结构基础与化学反应规律”中的“原子建构与元素周期律”中提及了铝元素。因此,教
材只从材料的角度简单介绍了铝单质和氧化铝的化学性质。通过实验、比较,得出铝和氧化铝
既能与碱反应又能与酸反应,并在此基础上引出两性氧化物的概念。教材紧接着介绍了铝和铝
教材 合金的特点及应用。为了体现金属材料的发展趋势,拓展学生的视野,教材特意安排了"三、
分析 新型合金"这部分内容,结合图片介绍了新型材料的应用。在"科学.技术.社会"中介绍了用途广
泛的稀土金属。依据课程标准要求,结合本节内容的特点,教学设计为“铁合金 铝和铝合
金”、“新型合金 物质的量在化学方程式计算中的应用”两个课时完成,另外,虽然课程标
准主题“常见的无机物及其应用”没有把铝作为典型的金属元素,但鉴于铝及其化合物在生
产、生活中的广泛应用,同时铝及其化合物还是高考重要考点之一,因此,为了拓宽学生的知
识视野,熟练掌握金属及其化合物的性质、转化及应用,本节还设计了“铝及其化合物的转化
关系及图像分析”1个专题,老师们可根据情况选择性使用。
本课时为第二课时“新型合金 物质的量在化学方程式计算中的应用”。该课时包括两部
分内容,首先是在上两课时学习铁合金以及铝合金的基础上,继续学习新型合金;其次是在之
前学习物质的量的基础上,深入学习物质的量在化学方程式中的应用。关于新型合金,教材主
要介绍新型合金的广泛应用和前景,“科学‧技术‧社会”栏目特地介绍了我国的稀土资源,
可激发学生的科学探究与创新意识。物质的量在化学方程式计算中的应用主要学习利用物质的
量、摩尔质量、气体摩尔体积、物质的量浓度的相互关系进行简单计算。这是物质的量相关知
识的拓展与应用,同时也是化学计算的基础,还是本课时教学的重点,教学中需要通过例题进
行强化。
1.通过阅读教材、查阅资料,了解储氢合金、钛合金等新型合金,感受化学科学对创造更
多新材料以满足人类生活需要和促进科技发展的重要作用。
教学
2.通过联系旧知、讨论交流,从物质的量的角度认识物质的组成及化学变化,能运用物质
目标
的量与其他物理量之间的换算关系进行有关计算。
3.通过对化学方程式本质的分析,能结合物质的量在化学方程式计算中的应用进行简单的
计算,了解常见的化学计算中常用的方法,进一步体会守恒思想,强化宏观辨识与微观探析能力。
教学 重点:物质的量在化学方程式计算中的应用
重、 难点:物质的量在化学方程式计算中的应用
难点
宏观辨识与微观探析:从宏观到微观理解方程式计算中,其化学计量数代表的不同意义,明确
在不同层次的运算中,都可以使用化学计量数。
核心 证据推理与模型认知:通过对物质的量在化学方程式中的应用,理解高中化学计算的基本概
素养 念,建立高中使用物质的量等概念进行方程式计算的基本模型。
科学精神与社会责任:通过对新型合金材料的学习,认识化学在促进社会发展中的重要作用,
体会科学、技术、社会之间的相互关系。
学生在之前的学习中对于物质的量、摩尔质量、气体摩尔体积以及物质的量浓度都有了基
学情 本认识,能够应用物质的量的计算公式解决一些实际的计算问题。但学生还不掌握将物质的量
分析 应用于化学方程式进行计算,学生需要从初中的计算思想出发,将初中过量与不足量的计算迁
移至高中物质的量的计算中,建立高中化学计算的基本思想,掌握计算的基本方法。
教学过程
教学 设计意
教学活动
环节 图
【回顾1】生铁和钢的区别及性能。
【学生1】生铁和钢是含碳量不同的两种 铁碳 合金。生铁的含碳量为 2%~4.3%,
钢的含碳量为0.03%~2% 。
【学生2】由于含碳量不司,钢和生铁在性能上有很大差异。例如,生铁硬度大、抗
压,性脆、可以铸造成型,是制造机座、管道的重要材料;钢有良好的延展性,机械
性能好,可以 锻轧和铸造 ,泛用于制造机械和交通工具等。
回顾旧
【回顾2】物质的量与其它物理量的关系。 知,为
环 学习新
【学生】联系物质的量与气体体积、质量、微粒数的、物质的量浓度的桥梁分别是
节 知做铺
气体摩尔体积、摩尔质量、阿伏伽德罗常数、溶液的体积 。
一 垫。
、 【预习1】储氢合金的概念、性能及用途。
生 创设生
情 活 【学生1】近年来,为满足某些尖端技术发展的需要,人们又设计和合成了许多 新 活情
景 情 型合金。例如,氢能是人类未来的理想能源之一,氢能利用存在两大难题: 制取和 境,激
导 境 储存。H 是种易燃易爆 的气体,要利用H ,关键要解决H 的 安全储存和运输问 发学习
2 2 2
入 题。 兴趣和
探究的
【预习2】化学方程式中化学计量数与粒子数、物质的量、气体体积的关系。 欲望。
【学生】化学方程式中各物质的化学计量数之比 等于 组成各物质的粒子数之比,也
等于 各物质的物质的量之比 ,还等于 相同条件下气体的体积之比 。
【导入】在之前的学习中,我们已经学习了铁合金和铝合金,这两种合金都是常用的
合金材料。而生活中除了这些常见的合金材料以外,随着科技的不断发展,也涌现了
很多具有特殊性能的新型合金,广泛用于航空航天、生物工程和电子工业等领域。
【过渡】近年来,为了满足某些尖端技术发展的需要,人们又实际合成了许多新型合
金,其中一种就是储氢合金。【问题1】阅读教材P83页内容,观察储氢合金的图片,结合教材内容思考储氢合金
有何特点?
【教师】投影:储氢合金的图片。
回归教
【学生1】一般情况下,H 采用气态或液态储存,如在高压下把 H 压入钢瓶,但运
2 2 材,了
送笨重的钢瓶既不方便也不安全。
活 解储氢
【学生2】储氢合金是一类能够大量吸收H ,并与H 结合成金属氢化物的材料。 合金的
2 2
性能及
【学生3】具有实用价值的储氢合金要求储氢量大,金属氢化物既容易形成,稍稍加
用途,
热又容易分解,室温下吸放氢的速率快,如Ti-Fe合金和La-Ni合金等。
形成新
型合金
【学生4】新型储氢合金材料的研究和开发将为氢气作为能源的实际应用起到重要的
的概
推动作用。
念。
【教师】评价、强调:除了储氢合金以外,人们还设计合成了很多新型合金材料,例
如:耐高温合金、记忆合金、高强度合金、生物性能合金等。
【问题2】阅读教材P83页内容,思考常见新型合金的有哪些主要性能和用途?完成
表格内容。
通过阅
【教师】投影表格、引导。 读教
材,进
【学生】阅读教材、完成表格内容,展示交流:
一步了
钛合金强度高、耐蚀性好、耐热性高。主要用于制作飞机发动机压 解新型
钛合金 合金的
气机部件,其次为火箭、导弹和高速飞机的结构件。
分类、
特性及
是能大量吸收H ,并与H 结合成金属氢化物的材料。如Ti-Fe合
2 2
储氢合金 特殊用
金、La-Ni合金。 途,培
养科学
动
环 是通过热弹性与马氏体相变及其逆变而具有形状记忆效应的由两种 探究的
节 活 形状记忆合 以上金属元素所构成的材料。形状记忆合金是形状记忆材料中形状 精神。
二
动 金
、 记忆性能最好的材料。
一
氧
是在高温使用环境条件下,具有组织稳定和优良力学、物理、化学
、
新
性能的合金。包括耐热钢、耐热铝合金、耐热钛合金、高温合金、
新
型 耐热合金
难熔合金等。耐热合金在高温下具有一定拉伸、蠕变、疲劳性能、
检测与
型
合 物理、化学性能和工艺性能。 评价,
合 通过反
金
馈,调
金 【教师】巡视、评价。
控课
的 【对应训练1】“双奥之城”——北京将迎来2022年冬奥会,滑雪是冬奥会的主要项 堂,提
目之一。下列滑雪用品涉及到的材料属于合金的是( ) 高课堂
分
教学效
A.滑雪杖杆——铝材(铝、镁等)
类 率。
B.滑雪板底板——塑料
C.滑雪手套——合成橡胶
D.滑雪服面料——尼龙
【答案】A
【解析】合金是指在一种金属中加热熔合其它金属或非金属而形成的具有金属特性的
物质;合金具有以下特点:①一定是混合物;②合金中至少有一种金属等。A项,滑
雪杖杆——铝材(铝、镁等)属于铝镁合金,正确;B项,滑雪板底板——塑料属于有
机物,属于有机高分子材料,不属于合金,错误;C项,滑雪手套——合成橡胶属于
有机物,属于有机高分子材料,不属于合金,错误;D项,滑雪服面料——尼龙属于有机物,属于有机高分子材料,不属于合金,错误。
【对应训练2】2022年科技创新结出累累硕果,加快了实现高水平建设科技强国。下
列有关说法错误的是( )
A.“北斗导航”系统应用一体化芯片手机,芯片成分为SiO
2
B.“奋斗者”号深海载人潜水器采用的Ti62A新型钛合金的硬度比纯钛的高
C.C919大飞机机身采用了第三代铝锂合金,具有密度低、强度高等优良特点
D.问天实验舱太阳翼配置的是三结砷化镓电池,砷化镓喻为“半导体贵族”
【答案】A
【解析】A.芯片的成分为晶体Si,A错误;B.合金比成分金属硬度高、韧性更
好,B正确;C.铝锂合金具有密度低、强度高等优良特点,适用于制作飞机机身,
C正确;D.砷化镓是良好的半导体材料,D正确;故选A。
【过渡】除了储氢合金以外,人们还设计合成了很多新型合金材料,例如:耐高温合
金、记忆合金、高强度合金、生物性能合金等。
进一步
【问题1】讨论交流:根据合金的定义,你认为合金形成的条件是什么?
认识合
金形成
【学生1】金属与金属形成合金时:合金是金属在熔化状态时相互混合形成的,熔化
的条
时的温度需达到成分金属中熔点最高的金属的熔点,但又不能超出成分金属中沸点最 件,了
解合金
低的金属的沸点。一种金属的熔点高于另一种金属的沸点时则不能形成合金。
的概
【学生2】金属与非金属形成合金时:部分不活泼非金属与金属可形成合金,活泼非 念。
金属与活泼金属则不能形成合金。
【教师】评价、强调。
创设社
【问题2】阅读教材P84页“科学‧技术‧社会”栏目,结合P86教材习题9:我国 会热点
发行的第五套人民币中,l元 、5角 和 1角 硬币的材质分别为钢芯镀镍 (1元 )、 钢 问题情
境,深
芯镀铜(5角 )和铝合金 (1角 )。 思考什么是稀土金属,有哪些应用?选择铸造硬币
度理解
的金属材料时应考虑哪些因素?
合金在
活 【学生1】镧系元素(57~71号元素)及钇和钪,共17种元素,称为稀土元素。 人类社
会发展
动 【学生2】我国是稀土资源大国。到目前为止,我国的稀土储量、稀土产量、稀土用
中的重
量和稀土出口量均居世界第一位。
二 要作
【学生3】稀土金属既可以单独使用,也可用于生产合金。在合金中加入适量稀土金 用,激
、
属,能大大改善合金的性能。因而,稀土元素又被称为“冶金工业的维生素”。例 发爱国
合 如,在钢中加入稀土元素,可以增加钢的塑性、韧性、耐磨性、耐热性、耐腐蚀性和 热情,
抗氧化性等。 培养科
金
学态度
【学生4】选择铸造硬币的金属材料时,应该考虑的因素有硬度、价格、光泽、耐磨
形 与社会
性、耐腐蚀性、易加工程度等.
责任的
成
学科核
【教师】评价、强调:稀土金属广泛应用在冶金、石油化工、材料工业(电子材料、
的 心素
荧光材料、发光材料、永磁材料、超导材料、染色材料、纳米材料、引火合金和催化
养。
条 剂等)、医药及农业等领域。杨sir化学,侵权必究
件 【对应训练1】社会的进步与时代的发展充满了人类智慧的结晶。下列有关说法中错
误的是( )
及
A.合金为纯净物,具有许多优良的物理、化学或机械性能
应 检测与
B.不锈钢是最常见的一种合金钢,不容易生锈。 评价,
用
通过反
C.商朝的“后母戊鼎”是我国较早使用的铜制品之一
馈,发
D.近年来,人们又设计和合成了许多新型合金。如储氢合金、钛合金等 现问
题,调【答案】A 控课
堂,提
【解析】A.合金是混合物,具有许多优良的物理、化学或机械性能,A错误;B.
高效
不锈钢是最常见的一种合金钢且不容易生锈,B正确;C.后母戊鼎是我国较早使用
率。
的铜制品之一,C正确;D.随着社会的发展,人们设计和合成了许多新型合金,如
储氢合金、钛合金等,D正确;故答案选A。
【对应训练2】下列说法正确的是( )
A.合金一般由多种元素组成,属于化合物
B.常温下,铝制品耐腐蚀是因为铝不活泼
C.新型储氢合金因具有较大空隙,通过物理吸附大量H 而广泛用于新能源汽车行业
2
D.合金中加入其他元素原子后,使原子层之间的相对滑动变得困难,导致合金的硬
度变大
【答案】D
【解析】A.合金是金属与金属或非金属熔合而成的具有金属特性的物质;属于混合
物,故A错误;B.常温下,铝制品耐腐蚀是因为铝和空气中氧气生成一层致密的氧
化膜,故B错误;C.合金具有在吸氢化学反应时放出大量热,而在放氢时吸收大量
热,因此新型储氢合金吸氢是化学变化,故C错误;D.合金内加入了其他元素或大
或小的原子,改变了金属原子有规则的层状排列,使原子层之间的相对滑动变得困
难。因此,在一般情况下,合金比纯金属硬度更大、更坚固,故D正确。故选D。
【过渡】有关化学方程式的计算,我们在初中就已经很熟悉了,知道化学反应中各反
应物和生成物的质量之间符合一定的关系。通过前面关于物质的量的学习,我们又知
道构成物质的粒子数与物质的质量之间可用物质的量做桥梁联系起来。 复习构
建以物
【问题1】请写出物质的量与质量、微粒数、气体体积、物质的量浓度等物理量之间
质的量
活的关系图,可得出什么结论?
为中心
的各物
【学生1】板书:以物质的量为中心的其它物理量的转化关系:
理量的
转化关
系,为
学习化
学方程
式的应
该计算
作铺
垫。
【教师】投影、强调:
【学生2】结论:物质的量是联系各物理量的纽带,可以简便的进行各量之间的转
活
换。
活
动 【教师】评价、补充:既然化学反应中各物质的质量之间符合一定的关系,那么,化 通过实
一 学反应中构成各物质的粒子数之间、物质的量之间是否也遵循一定的关系呢?能不能 例,构
、 建解答
把物质的量也应用于化学方程式的计算呢?
物 物质的
质 【问题2】根据化学反应的实质,以金属钠与水反应为例,思考微观粒子与化学方程 量在化
的 式有何关系?可得出什么结论? 学方程
量 式计算
【教师】追问:构成物质的基本粒子有哪些?物质发生的反应与粒子数目有何关系?
与 中的应
其 【学生1】物质是由原子、分子、离子等粒子构成的,物质之间的化学反应也是这些 用试题
他 粒子按一定的数目关系进行的。 的模型
物 和基本
环 理 【教师】板书: 2Na + 2H 2 O = 2NaOH + H 2 ↑ 方法。
节
三 量 化学计量数之比 2 2 2 1
之、 间 扩大N 倍 2N 2N 2N N
A A A A A
的
铁 关 物质的量之比 2mo l : 2mol : 2mol : ___1mol___ 通过典
物 系 标况下体积之比 44.8L : 44.8L : 44.8L : 22.4L 例剖
析,进
质
质量之比 46 g : 36g : 80g : 2g 一步明
的 确解题
【教师】根据上述分析,你可以得出什么结论?
思路,
量
【学生】结论:化学方程式中各物质的化学计量数之比等于其粒子数目之比,等于其 归纳解
在 物质的量之比,也等于同温同压下气体的体积之比。 题步
骤,培
化 【问题3】分析完成教材P85页【例题】,思考物质的量在化学方程式计算中的步骤
养证据
是什么?
学 推理和
【教师】投影:250 mL 2 mol·L-1的硫酸与足量的铁屑完全反应。计算: 模型认
方
知的学
程 (1)参加反应的铁屑的物质的量; 科核心
素养。
式
(2)生成的H
2
的体积(标准状况)。(写出解题步骤)
计 【教师】讲解:根据硫酸的体积和H 2 SO 4 的物质的量浓度求算可计算出参加反应的
HSO 的物质的量。然后根据化学反应中各物质之间的化学计量数之比,计算出参加反
算 2 4
应的铁屑的物质的量和生成的H 的体积。
2
中
【教师】板书:
的
解析:n(H SO )=0.25 L×2 mol·L-1=0.50 mol
2 4
应
(法1)(1)Fe + HSO ===FeSO+H↑ 检测与
2 4 4 2
用 评价,
1 1
通过反
n(Fe) 0.5 mol 馈,发
现问
=,n(Fe)=0.5 mol 题,提
高效
(2)Fe+HSO ===FeSO+H↑
2 4 4 2 率。
1 mol 22.4 L
0.5 mol V(H )
2
=,解得V(H )=11.2 L
2
(法2)Fe + HSO ===FeSO+H↑
2 4 4 2
1 mol 1 mol 22.4 L
n(Fe) 0.5 mol V(H )
2
==
故n(Fe)=0.5 mol,V(H )=11.2 L
2 通过归
答: (1)参加反应的铁屑的物质的量为0.5 mol; 纳总
结,突
(2)生成H 在标准状况的体积为11.2 L。
2 出重
【教师】提问:通过以上分析,利用化学方程式计算时要注意什么问题? 点、突
破难
【学生】计算时同种物质各种量(物质的量、质量、体积)的单位要统一。
点。
【教师】追问:物质的量在化学方程式计算中的应用的解题步骤时什么?
【学生】归纳总结:解题步骤
【教师】板书:第一步:转—将已知的物理量转化为物质的量;
第二步:写—写出相关的化学方程式;
第三步:标—在有关物质的化学式下面标出已知量何未知量(未知量可用相应物理量符合表示);
第四步:列—列出比例式;
第五步:解—根据比例式求解。
检测与
【教师】提问:在解答物质的量在化学方程式计算中的应用时要注意哪些问题? 评价,
及时巩
【学生1】书写格式规范化:在计算过程中应注意表达格式的规范化:各物理量、物
固所
质的名称、公式等尽量用符号表示,且数据的运算要公式化并带单位。
学。
【学生2】单位运用对应化:一般来说,在一个题目中如果都用统一的单位,不会出
现错误,但如果题目所给的两个量单位不一致,若换算成同一个单位,有时显得很繁
琐,这时只要做到两个量的单位“上下一致,左右相当”即可。
【学生3】各种符号的书写要规范,大写字母与小写字母的含义各不相同。如“M”表
示摩尔质量,“m”表示质量,“N”表示微粒数目,而“n”表示物质的量。
【教师】评价、强调:根据化学方程式所反映出的这些关系,可以进行多种计算。但
要根据题意,明确已知条件是什么,求解什么,从而合理选择比例量的单位。列比例
式时应注意,不同物质使用的单位可以不同,但要相对应,同一物质使用的单位必须
一致。
【对应训练】完全中和0.1 mol NaOH需HSO 的质量是多少?
2 4
解法一: 2NaOH +HSO = NaSO + 2H O
2 4 2 4 2
2mol 1mol
0.1mol n(H SO )
2 4
2/2mol==1/ n(H SO )
2 4
n(H SO )==0.1mol×1mol/2mol==0.05mol
2 4
m(HSO )==n(H SO )×M(HSO )==0.05mol×98g/mol==4.9g
2 4 2 4 2 4
答:所需H2SO4的质量是4.9g
解法二、用质量列比例式(略)
【教师】强调:只要上下单位一致,左右关系对应,则可列比例式计算。
活【过渡】将物质的量(n)、摩尔质量(M)、摩尔体积(Vm)物质的量浓度(C)
等概念应用于化学方程式进行计算,对于定量的研究化学反应中各物质之间的量的关
创设问
系会更加方便。同时,在解答问题过程中,还可以充分利用一些特定的关系,将复杂
题情
的问题问题简单化。
境,体
【问题1】以“一定量的铁粉和9 g硫粉混合加热,待其反应后再加入过量盐酸,将 验关系
生成的气体完全燃烧,共收集得9 g水,求加入的铁粉质量”为例,思考什么是关系 式法在
式法? 化学方
程式中
【教师】引导、分析并板书。
的应
解析:反应化学方程式Fe+S=====FeS , FeS+2HCl=FeCl +HS↑, 用。认
2 2
识关系
2HS+3O=====2SO +2HO,
2 2 2 2 式法的
Fe~HS~HO 基本内
2 2
涵,构
56g 18g
建解题
x 9 g x=28g 的基本
思路和
【教师】讲解:关系式法—解答连续反应类型计算题的捷径:当已知量和未知量之间 模型
是靠多个反应来联系时,只需直接确定已知量和未知量之间的比例关系,即“关系
式”,这种比例关系通常可从化学方程式或化学式中得到。例如:
2Al+2NaOH+2H O===
2 创设问
题情2NaAlO +3H ;有关Al和NaOH、H 的反应比例关系为:2Al⁓2NaOH⁓3H 。 境,体
2 2 2 2
验差量
【教师】追问:你认为关系式法的关键是什么?
法在化
【学生】找准已知量与未知量之间的关系,直接列式进行计算。 学方程
式中的
【问题2】以“为了检验某含有NaHCO 杂质的NaCO 样品的纯度,现将w g样品
3 2 3 1 应用。
加热,其质量变为w g,请列式计算该样品中NaCO 的质量分数”为例,思考什么
2 2 3 认识差
是差量法?
量法的
【教师】引导、分析并板书: 基本类
型,构
解析:样品加热发生的反应为
建解题
2NaHCO =====NaCO+HO+CO↑ Δm 的基本
3 2 3 2 2
思路和
168 106 62 模型
m(NaHCO ) (w -w ) g
3 1 2
样品中m(NaHCO )= g,
3
样品中m(Na CO)=w g- g,
2 3 1
其质量分数为×100%=×100%
活
动
=×100%。
二 【教师】讲解:差量法—化学方程式计算中的巧思妙解:所谓“差量”就是指反应过
、 程中反应物的某种物理量之和(始态量)与同一状态下生成物的相同物理量之和(终态
化 量)的差,这种物理量可以是质量、物质的量、气体体积、气体压强、反应过程中的 创设问
题情
学 热效应等。根据化学方程式求出理论上的差值(理论差量),结合题中的条件求出或表
境,体
计 示出实际的差值(实际差量),根据比例关系建立方程式并求出结果。 验守恒
法在化
算 【教师】追问:你认为差量法的关键是什么,有哪些类型? 学方程
中 【学生1】差量法的解题关键是找准研究对象。 式中的
应用。
的
【学生2】常见类型:①固体的质量差,研究对象是固体。②气体的质量差,研究对 认识守
常 恒法的
象是气体。③液体的质量差,研究对象是液体。
基本类
用
【教师】评价、强调。 型,构
方 建解题
【问题3】以“用1 mol·L-1的NaSO 溶液30 mL恰好将2×10-2 mol的XO — 还原,
2 3 4 的基本
法 已知氧化产物为 SO 2- ,求元素X在还原产物中的化合价”为例,思考什么是守恒
4 思路和
法?
模型
【教师】引导、分析并板书::
解析:氧化还原反应中得失电子总数相等,设元素X在还原产物中的化合价为x,则
有:1 mol·L-1×0.03 L×(6-4)=2×10-2 mol×(7-x),解得x=+4。
检测与
【教师】讲解:守恒法—质量守恒、得失电子守恒和电荷守恒:在化学反应中,遵循
评价,
质量守恒(即原子个数守恒—化学反应前后原子种类和数目均保持不变);在电解质
发现问
溶液中,阳离子所带正电荷总数=阴离子所带负电荷总数;在氧化还原反应中,还原
题,调
剂失电子总数=氧化剂得电子总数。
控课
【教师】追问:利用“守恒法”解题的关键是什么? 堂,提
高效
【学生】利用“守恒法”解题的关键是根据试题找准”守恒”类型,任何化学反应都
率。
存在质量守恒,电解质溶液都存在电荷守恒,氧化还原反应才存在得失电子守恒。
【对应训练1】Mg、Al组成的混合物与足量盐酸反应,产生标准状况下的氢气为
4.48 L。下列推断中不正确的是( )A.参加反应的Mg、Al共0.2 mol
B.参加反应的HCl为0.4 mol
C.Mg、Al在反应中共失去0.4 mol电子
D.若与足量的稀硫酸反应能产生0.2 mol H
2
【答案】A
【 解 析 】 反 应 的 实 质 为 Mg+2H+===Mg2++H ↑ , 2Al+6H+===2Al3++3H ↑ ,
2 2
n(H )=4.48L/(22.4L/mol)=0.2 mol,则参加反应的n(H+)=0.4 mol。若换成稀HSO ,
2 2 4
同样产生0.2 mol H 。依据得失电子守恒,由2H+―→H 得电子总数为0.2 mol×2=0.4
2 2
mol,故C正确。0.2 mol Mg提供0.4 mol电子,0.2 mol Al则提供0.6 mol电子,0.2
mol Mg、Al混合物提供的电子数大于0.4 mol、小于0.6 mol,A不正确。
【对应训练2】在一定条件下,RO和F 可发生如下反应:RO+F +2OH-===RO+
2 2
2F-+HO,从而可知在RO中,元素R的化合价是( )
2
A.+4 B.+5 C.+6 D.+7
【答案】B
【解析】方法1:根据电荷守恒有n+1×2=1+1×2,n=1。设元素R在RO中的化合
价为x,则x-2×3=-1,x=+5。
方法2:设元素R在RO中的化合价为x。根据氧化还原反应中,得失电子守恒有(7-
x)×1=[0-(-1)]×2,x=+5。
1.教材P86页3、7、8、10、11
2.社会的进步与时代的发展充满了人类智慧的结晶。下列有关说法中错误的是
( )
A.合金为纯净物,具有许多优良的物理、化学或机械性能
B.不锈钢是最常见的一种合金钢,不容易生锈。
C.商朝的“后母戊鼎”是我国较早使用的铜制品之一
D.近年来,人们又设计和合成了许多新型合金。如储氢合金、钛合金等
【答案】A
【解析】A.合金是混合物,具有许多优良的物理、化学或机械性能,A错误;
B.不锈钢是最常见的一种合金钢且不容易生锈,B正确;C.后母戊鼎是我国较早
使用的铜制品之一,C正确;D.随着社会的发展,人们设计和合成了许多新型合
金,如储氢合金、钛合金等,D正确;故答案选A。
3.钛和钛的合金具有很多优良的性能,如熔点高、密度小、可塑性好、易于加
工,尤其是钛合金与人体器官具有很好的“生物相容性”。根据它们的主要性能,下
列用途不切合实际的是( )
A.用来做保险丝 B.用于制造航天飞机
C.用来制造人造骨 D.用于家庭装修,做钛合金装饰门
【答案】A
【解析】物质的性质决定用途,钛和钛的合金有很多优良的性能,也有很多重要
的用途。A.保险丝应该用熔点比较低的金属材料做,而钛及其合金熔点高,不适合
做保险丝,故A错误;B.因为钛和钛的合金密度小、可塑性好、易于加工,所以可
用于制造航天飞机,故B正确;C.因为钛合金与人体有很好的“相容性”,所以可
用来制造人造骨,故C正确;D.因为钛和钛的合金密度小、可塑性好、易于加工,所以可用于家庭装修,做钛合金装饰门,故D正确;答案选A。
4.合金品种多、应用广泛,很多高品质合金是大国重器的原材料。关于合金的
下列叙述,不正确的是( )
A.“合金材料”中只含金属元素,不含非金属元素
B.生活中大量使用铝合金是因为它的密度小、强度高、抗腐蚀能力强
C.Ti—Fe合金和La—Ni合金都是新型合金,特点是室温下吸、放氢的速率快
环 D.焊锡(锡铅合金)熔点比金属锡低
节
【答案】A
四
、 【解析】A.“合金材料”如钢铁中不仅含金属元素,而且含非金属元素碳,A
及时巩
课
错误;B.生活中大量使用铝合金是因为它的密度小、强度高、抗腐蚀能力强,B正
固、消
后
作 确;C.Ti—Fe合金和La—Ni合金都是新型储氢合金,特点是室温下吸、放氢的速 化所
巩
业 率快,C正确;D.合金的熔点一般比成分金属的熔点低,焊锡(锡铅合金)熔点比金 学,促
固
设 属锡低,D正确; 故选A。 进掌握
计 必备知
5.将同体积同物质的量浓度的AgNO 溶液中的Ag+完全沉淀,则需同物质的量
3 识,评
浓度的NaCl、MgCl 、AlCl 三种溶液的体积比为( )
2 3 价教学
A.1∶2∶3 B.3∶2∶1 C.1∶1∶1 D. 效果,
6∶3∶2 为后期
优化教
【答案】D
学方案
提供依
【解析】分别加入足量的硝酸银溶液,Cl-沉淀完全时,同体积同物质的量浓度
据,培
的AgNO 溶液,消耗等物质的量的AgNO ,可知NaCl、MgCl 、AlCl 三种溶液中含
3 3 2 3 养分析
氯离子的物质的量相同,假设n(Cl-)=6 mol,根据物质的化学式可知:n(NaCl)=6
问题和
mol,n(MgCl )=3 mol,n(AlCl )=2 mol,溶液的浓度相同,由V=可知,物质的量
2 3 解决问
之比等于体积之比,均为6 mol∶3 mol∶2 mol=6∶3∶2,选D项。
题等关
6.镁和铝分别与等浓度、等体积的过量稀硫酸反应,产生气体的体积(V)与时 键能
力。
间(t)关系如右图。反应中镁和铝的( )
A.物质的量之比为3∶2
B.质量之比为3∶2
C.摩尔质量之比为2∶3
D.生成气体的物质的量之比为2∶3
【答案】A
【解析】根据方程式分析:Mg+HSO =MgSO +H↑、2Al+3HSO =
2 4 4 2 2 4
Al (SO ) +3H↑。A项,图中产生的氢气一样多,结合方程式分析,镁和铝的物质的
2 4 3 2
量比为3∶2,正确;B项,镁和铝的物质的量比为3∶2,质量比为3×24∶27×2=4∶3,错
误;C项,镁和铝的摩尔质量比为 24∶27=8∶9,错误;D项,生成气体物质的量相
等,错误。
7.6 g Fe和Fe O 的混合物,加入150 mL足量的稀硫酸,在标准状况下收集到1.12
2 3
L H ,向反应后的溶液中滴加KSCN溶液不变红。为中和过量的稀硫酸,并使Fe元
2
素全部转化为Fe(OH) 沉淀,恰好消耗了200 mL 3 mol·L-1的NaOH溶液,则该稀
2
HSO 的物质的量浓度为( )
2 4
A.2.25 mol·L-1 B.2 mol·L-1 C.3 mol·L-1 D.0.6 mol·L-1
【答案】B
【解析】根据题干信息可知,涉及反应有:Fe+HSO =FeSO +H↑、Fe O +
2 4 4 2 2 3
3HSO =Fe (SO ) +3HO、Fe+Fe (SO ) =3FeSO 、FeSO +2NaOH=Fe(OH) ↓+
2 4 2 4 3 2 2 4 3 4 4 2NaSO 、2NaOH+HSO =NaSO +2HO,即反应最后铁元素完全沉淀后,溶液中
2 4 2 4 2 4 2
的溶质只剩下NaSO ,根据Na+和SO 2-守恒可得:n(Na+)×1=n(SO 2-)×2,n(Na+)
2 4 4 4
=n(NaOH)=2n(SO 2-)=2n(H SO ),即n(NaOH)=2n(H SO ),则0.2 L×3 mol·L-1=
4 2 4 2 4
2×0.15 L×c(H SO ),解得c(H SO )=2 mol·L-1,故答案为B项。
2 4 2 4
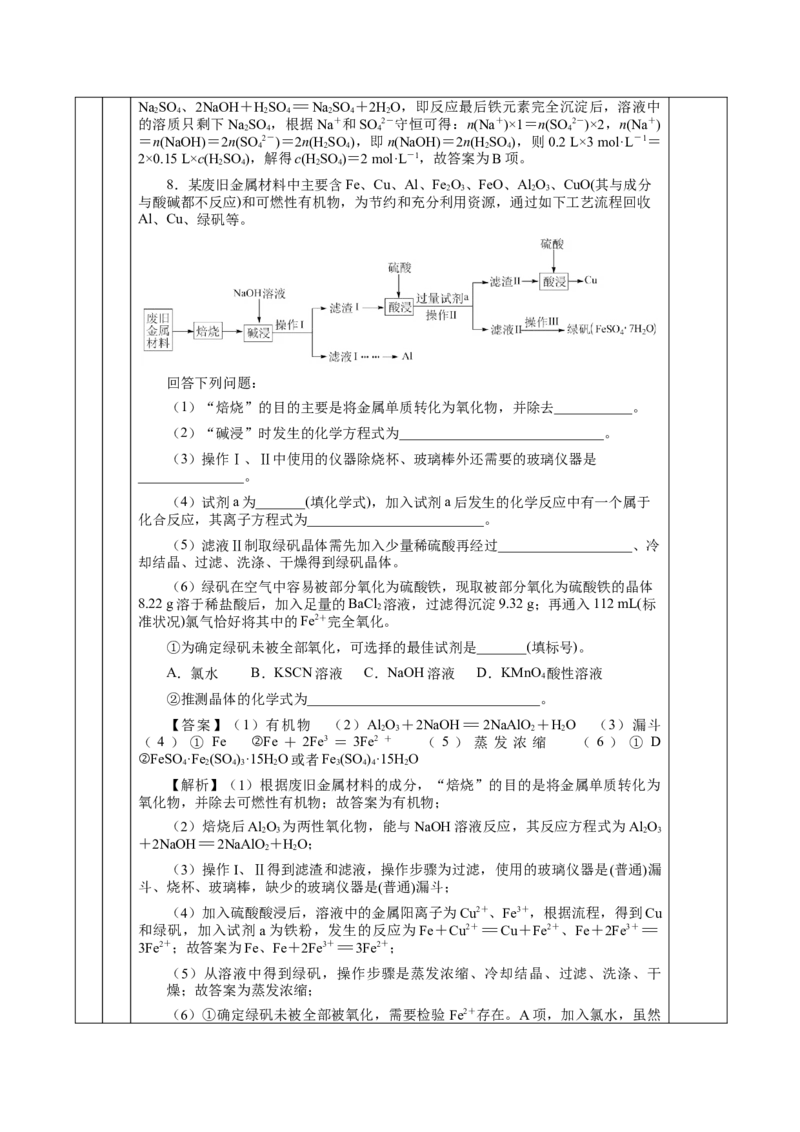
8.某废旧金属材料中主要含Fe、Cu、Al、Fe O、FeO、Al O、CuO(其与成分
2 3 2 3
与酸碱都不反应)和可燃性有机物,为节约和充分利用资源,通过如下工艺流程回收
Al、Cu、绿矾等。
回答下列问题:
(1)“焙烧”的目的主要是将金属单质转化为氧化物,并除去___________。
(2)“碱浸”时发生的化学方程式为_____________________________。
(3)操作Ⅰ、Ⅱ中使用的仪器除烧杯、玻璃棒外还需要的玻璃仪器是
_______________。
(4)试剂a为_______(填化学式),加入试剂a后发生的化学反应中有一个属于
化合反应,其离子方程式为_________________________。
(5)滤液Ⅱ制取绿矾晶体需先加入少量稀硫酸再经过___________________、冷
却结晶、过滤、洗涤、干燥得到绿矾晶体。
(6)绿矾在空气中容易被部分氧化为硫酸铁,现取被部分氧化为硫酸铁的晶体
8.22 g溶于稀盐酸后,加入足量的BaCl 溶液,过滤得沉淀9.32 g;再通入112 mL(标
2
准状况)氯气恰好将其中的Fe2+完全氧化。
①为确定绿矾未被全部氧化,可选择的最佳试剂是_______(填标号)。
A.氯水 B.KSCN溶液 C.NaOH溶液 D.KMnO 酸性溶液
4
②推测晶体的化学式为_________________________________。
【答案】(1)有机物 (2)Al O +2NaOH=2NaAlO +HO (3)漏斗
2 3 2 2
( 4 ) ① Fe ②Fe + 2Fe3 = 3Fe2 + ( 5 ) 蒸 发 浓 缩 ( 6 ) ① D
②FeSO ·Fe (SO )·15HO或者Fe (SO )·15HO
4 2 4 3 2 3 4 4 2
【解析】(1)根据废旧金属材料的成分,“焙烧”的目的是将金属单质转化为
氧化物,并除去可燃性有机物;故答案为有机物;
(2)焙烧后Al O 为两性氧化物,能与NaOH溶液反应,其反应方程式为Al O
2 3 2 3
+2NaOH=2NaAlO +HO;
2 2
(3)操作I、Ⅱ得到滤渣和滤液,操作步骤为过滤,使用的玻璃仪器是(普通)漏
斗、烧杯、玻璃棒,缺少的玻璃仪器是(普通)漏斗;
(4)加入硫酸酸浸后,溶液中的金属阳离子为Cu2+、Fe3+,根据流程,得到Cu
和绿矾,加入试剂a为铁粉,发生的反应为Fe+Cu2+=Cu+Fe2+、Fe+2Fe3+=
3Fe2+;故答案为Fe、Fe+2Fe3+=3Fe2+;
(5)从溶液中得到绿矾,操作步骤是蒸发浓缩、冷却结晶、过滤、洗涤、干
燥;故答案为蒸发浓缩;
(6)①确定绿矾未被全部被氧化,需要检验 Fe2+存在。A项,加入氯水,虽然氯水能将Fe2+氧化Fe3+,但溶液颜色变化不明显,不符合题意;B项,KSCN溶液是
检验Fe3+存在,无法证明Fe2+是否存在,不符合题意;C项,加入NaOH溶液,Fe3+
与OH-反应生成红褐色沉淀,Fe2+与OH-反应生成白色沉淀Fe(OH) ,氢氧化亚铁不
2
易观察出来,不符合题意;D项,利用高锰酸钾溶液强氧化性,能将Fe2+氧化成Fe3
+,紫红色褪去,溶液中加入酸性高锰酸钾溶液,紫红色褪去,说明绿矾未被全部氧
化,符合题意;答案为D项;②加入足量的BaCl 溶液,过滤得沉淀9.32 g,该沉淀
2
为BaSO ,即n(SO 2-)==0.04 mol,再通入氯气,发生2Fe2++Cl =2Fe3++2Cl-,
4 4 2
n(Fe2+)=2×=0.01 mol,根据电荷守恒,n(Fe3+)×3+n(Fe2+)×2=n(SO 2-)×2,n(Fe3
4
+)×3+0.01 mol×2=0.04 mol×2,解得:n(Fe3+)=0.02 mol,n(H O)==0.15 mol,该
2
晶体的化学式为FeSO ·Fe (SO) ·15H O或Fe (SO )·15H O。
4 2 4 2 3 4 4 2
课堂
总结
第三章 铁 金属材料
第二节 金属材料
第二课时 新型合金 物质的量在化学方程式计算中的应用
一、新型合金
1.新型合金的分类及应用
2.合金的形成条件
板书 二、物质的量在化学方程式计算中的应用
设计 1.物质的量与其他物理量之间的关系:
2.化学计算中的常用方法:
关系式法、差量法、守恒法
本课时包括新型合金、物质的量在化学方程式计算中的应用量部分,后者既是本节课的重
点也是本节课的难点。新型合金主要是在教师的引导下了解新型合金的种类及特殊用途,通过
稀土资源的介绍,激发爱国热情,培养科学态度与社会责任的学科核心素养。化学方程式计算
的教学通过典型实例,在教师引导下分析解题思路和方法,通过师生共同归纳总结,形成解题
教学
基本模型,明确解题的关键及要注意的问题,最后通过例题介绍常见计算的几种方法,突破学
反思 生有关化学计算的难点,让学生体会到成功的喜悦,增强学习的自信心。