文档内容
3.2 金属材料
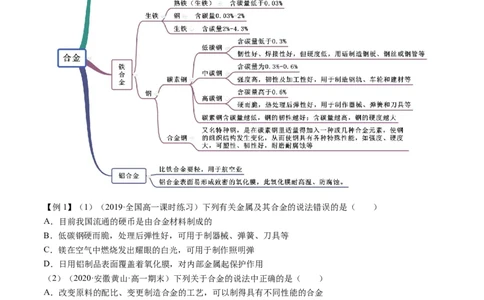
知识点一 铁合金与铝合金
【例1】(1)(2019·全国高一课时练习)下列有关金属及其合金的说法错误的是( )
A.目前我国流通的硬币是由合金材料制成的
B.低碳钢硬而脆,处理后弹性好,可用于制器械、弹簧、刀具等
C.镁在空气中燃烧发出耀眼的白光,可用于制作照明弹
D.日用铝制品表面覆盖着氧化膜,对内部金属起保护作用
(2)(2020·安徽黄山·高一期末)下列关于合金的说法中正确的是( )
A.改变原料的配比、变更制造合金的工艺,可以制得具有不同性能的合金
B.合金都是由不同金属单质组成的混合物
C.古代留下大量的青铜器文物是由于青铜比纯铜柔软,容易制成各种器皿
D.飞机机身使用的是镁铝合金而不是钢材,是因为钢材价格高
【答案】(1)B(2)A
【解析】(1)A.目前我国流通的硬币是由合金材料制成:1角的为不锈钢,5角的为钢芯镀铜,1元的为
钢芯镀镍,故A正确;
B.高碳钢硬而脆,处理后弹性好,可用于制器械、弹簧、刀具等,故B错误;
C.制造照明弹是利用了镁燃烧发出耀眼的白光,故C正确;
D.铝与氧气反应生成致密的氧化铝保护膜,对内部金属起保护作用,故D正确;故选B。(2)A.合金的性质与合金的原料配比以及制造工艺有关,所以改变原料的配比、变更制造合金的工艺,
可以制得具有不同性能的合金,故A正确;
B.合金可以是由金属单质与非金属单质组成,如碳素钢是铁和碳的合金,故B错误;
C.合金的硬度大于成分金属,青铜的硬度大于纯铜,故C错误;
D.镁铝合金的强度大,密度小,适合飞机机身使用,钢材的密度大,不利于飞机的起飞,故D错误。
故选:A。
合金是指在一种金属中加热熔合其它金属或非金属而形成的具有金属特性的物质.
合金概念有三个特点:①一定是混合物;②合金中各成分都是以单质形式存在;③合金中至少有一种金属。
【一隅三反】
1.(2020·江苏泗阳·桃州中学月考)2019年,我国第一艘国产航空母舰山东舰正式列装。优质钢材是建造
航空母舰的基础材料,钢材中含量最高的元素是( )
A.铁 B.碳 C.硅 D.锰
【答案】A
【解析】钢材是合金,钢材中除主要化学成分铁(Fe)以外,还含有少量的碳(C)、硅(Si)、锰(Mn)、磷
(P)、硫(S)、氧(O)、氮(N)、钛(Ti)、钒(V)等元素,所以钢材中含量最高的元素是铁,故选:A。
2.(2020·全国课时练习)下列说法正确的是
A.高碳钢的含碳量大于2% B.生铁既可铸造也可锻造
C.生铁和钢都属于铁合金 D.生铁是用途最广的合金
【答案】C
【解析】A.高碳钢属于钢中的碳素钢,钢的含碳量0.03%~2%,小于2%,故A错误;
B.生铁可铸但不可锻,故B错误;
C.铁合金通常包括生铁和钢两大类,故C正确;
D.钢是用途最广的合金,故D错误;
答案选C。
3.(2020·全国课时练习)下列物质中不属于铁合金的是
A.不锈钢 B.生铁 C.碳素钢 D.氧化铁
【答案】D
【解析】A. 不锈钢是铁的合金,故A项正确;
B. 生铁是含碳量大于2%的铁碳合金,故B项正确;
C. 碳素钢是碳含量低于2%,并有少量硅、锰以及磷、硫等杂质的铁碳合金,故C项正确;
D. 氧化铁是氧化物,属于纯净物,故D项错误;
答案选D。
4.(2020·全国课时练习)下列说法中不正确的是
A.生铁是铁的一种合金
B.合金是混合物
C.一般地说合金的熔点比它的各成分金属的熔点都高
D.铝制餐具不宜用来蒸煮或长期存放酸性或碱性食物
【答案】C【解析】A. 生铁是铁和碳的一种合金,故A正确;
B. 合金是一种金属与其它金属或非金属熔合而成的混合物,故B正确;
C. 一般地说合金的熔点比它的各成分金属的熔点都低,硬度比成分金属的大,故C错误;
D. 铝与酸、碱都能反应放出氢气,铝制餐具不宜用来蒸煮或长期存放酸性或碱性食物,故D正确。
答案选C。
5.(2020·南昌县莲塘第二中学期末)金属铝在生产生活中有广泛用途。
(1)用化学方程式表示工业制备铝单质______。
(2)铝热反应可用于焊接钢轨,如图为铝热反应的实验装置图。
①该铝热反应的化学方程式是______。
②铝热反应在工业上用于冶炼______金属(填编号)。
A.强还原性 B.难熔性 C.易导电 D.活泼
③反应结束后,从沙中取出生成的固体物质,有同学推测该固体是铁铝合金,他设计了如下实验证明此固
体中含有金属铝:取少量固体于试管中,滴加______,当观察到______现象时,证明固体中含有金属铝。
【答案】(1)2Al O(熔融) 4Al+3O ↑
2 3 2
(2)① 2Al+Fe O 2Fe+Al O ② B ③ NaOH溶液 固体部分溶解,且有无色气泡产生
2 3 2 3
【解析】(1)电解熔融氧化铝生成铝和氧气,化学方程式为:2Al O(熔融) 4Al+3O ↑;
2 3 2
(2)①铝与氧化铁高温反应生成铁和氧化铝,方程式为2Al+Fe O 2Fe+Al O;
2 3 2 3
②铝热反应放出大量的热,可以用于冶炼熔点高的金属;故选:B;
③铝能够与氢氧化钠溶液反应生成氢气,所以要证明此固体中含有金属铝:取少量固体于试管中,滴加
NaOH溶液,当观察到有气泡生成现象时,证明固体中含有金属铝;
故答案为:NaOH溶液;固体部分溶解,且有无色气泡产生。
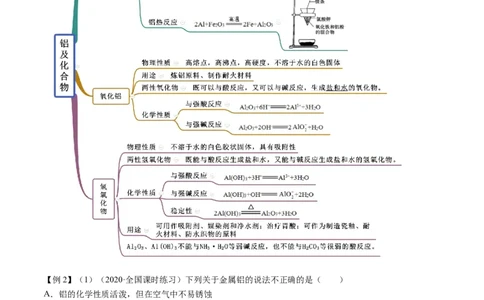
知识点二 铝及化合物【例2】(1)(2020·全国课时练习)下列关于金属铝的说法不正确的是( )
A.铝的化学性质活泼,但在空气中不易锈蚀
B.铝是比较活泼的金属,在化学反应中容易失去电子
C.铝箔在空气中受热可以熔化,且发生剧烈燃烧
D.铝箔在空气中受热可以熔化,但由于氧化膜的存在,熔化的铝并不滴落
(2)(2020·全国课时练习)足量下列物质与相同质量的铝反应,放出氢气的量相等且消耗溶质的物质的
量最少的是
A.氢氧化钠溶液 B.稀硫酸 C.盐酸 D.氢氧化钡溶液
【答案】(1)C(2)D
【解析】(1)A.铝的化学性质活泼,在空气中易与氧气反应,生成一层致密的氧化膜,故不易被锈蚀,
故A正确;B.铝的化学性质活泼,在化学反应中易失去电子,易被氧化,故B正确;
C.铝箔在空气中受热熔化的过程中表面生成致密氧化膜,阻止Al继续被氧化,则铝不可能剧烈燃烧,故
C 错误;
D.铝箔在空气中受热可以熔化,但表面形成的氧化膜熔点高,导致熔化的铝并不滴落,故D正确;
故答案为C。
(2)铝与 、 反应的离子方程式分别为 ,
,即 , ,可知 需
: , : , : , : ;综上分析,放出氢气的量相
等且消耗溶质的物质的量最少的是氢氧化钡溶液,答案选D。
1.Al与酸、碱反应的实质都是:Al Al3+,2H+ H,
2
故与酸或碱反应时,铝与氢气的关系均为2Al~3H↑,利用此性质可以方便地进行有关计算。
2
①等量Al分别与足量酸(H+)和碱(OH−)溶液反应,生成H 之比为1∶1,消耗H+和OH−之比为3∶1。
2
②足量Al分别与所含H+和OH−物质的量相等的溶液反应,生成H 之比为1∶3。
2
③若产生H 之比为< <,则必定是:
2
与酸反应时,Al过量、H+不足,而与碱反应时,Al不足、OH−过量。
【一隅三反】
1.(2020·南昌县莲塘第二中学期末)用坩埚钳夹住一小块刚用酸处理过的铝箔,在酒精灯上加热至熔化,
发现熔化的铝并不滴落。下列关于该实验现象的解释不正确的是( )
A.氧化铝与酸不反应 B.铝在空气中能很快形成氧化膜
C.氧化铝的熔点比铝高 D.铝箔表面未熔化
【答案】A
【解析】A.铝箔表面的氧化铝能与酸反应而溶解,如氧化铝和盐酸反应生成氯化铝和水,A错误;
B.铝化学性质活泼,铝在空气中易和氧气反应生成了氧化铝,形成氧化膜,B正确;
C.氧化铝的熔点高于铝的熔点,包住了熔化的铝,所以加热铝箔的时候铝熔化了但是不会滴落,C正确;
D.将铝箔用坩埚钳夹住放在酒精灯火焰上加热,发现熔化的铝并不滴落,则铝和氧气反应生成了氧化铝
(熔点高),导致铝箔表面未熔化,D正确;
故答案为A。
2.(2020·深圳市龙岗区科城实验学校高一月考)下列关于 Al O 的说法正确的是( )
2 3A.Al O 是金属氧化物,也是两性氧化物
2 3
B.Al O 加热易分解为铝和氧气
2 3
C.Al O 结构致密,所以可用铝制容器盛盐酸和 NaOH 溶液等
2 3
D.已擦去表面的氧化铝的铝条,在酒精灯上灼烧时,熔化的铝会滴落下来
【答案】A
【解析】A. Al O 既能与强酸反应生成铝盐和水,又能与强碱反应生成偏铝酸盐和水,则Al O 属于两性
2 3 2 3
金属氧化物,故选A;
B.Al O 很稳定加热不分解,由Al O 制取铝和氧气,则需电解熔融的Al O,故B不选;
2 3 2 3 2 3
C.Al O 属于两性金属氧化物,既能与强酸反应生成铝盐和水,又能与强碱反应生成偏铝酸盐和水,所以
2 3
不可以用铝制容器盛盐酸和 NaOH 溶液等,故C不选;
D.已擦去表面的氧化铝的铝条,在酒精灯上灼烧时,Al会与O 反应生成熔点比Al更高的Al O,把铝包
2 2 3
裹起来,熔化的铝不会滴落下来,故D不选;
答案选A。
3.(2020·深圳市龙岗区科城实验学校高一月考)下列关于 Al O 的说法正确的是( )
2 3
A.Al O 是金属氧化物,也是两性氧化物
2 3
B.Al O 加热易分解为铝和氧气
2 3
C.Al O 结构致密,所以可用铝制容器盛盐酸和 NaOH 溶液等
2 3
D.已擦去表面的氧化铝的铝条,在酒精灯上灼烧时,熔化的铝会滴落下来
【答案】A
【解析】A. Al O 既能与强酸反应生成铝盐和水,又能与强碱反应生成偏铝酸盐和水,则Al O 属于两性
2 3 2 3
金属氧化物,故选A;
B.Al O 很稳定加热不分解,由Al O 制取铝和氧气,则需电解熔融的Al O,故B不选;
2 3 2 3 2 3
C.Al O 属于两性金属氧化物,既能与强酸反应生成铝盐和水,又能与强碱反应生成偏铝酸盐和水,所以
2 3
不可以用铝制容器盛盐酸和 NaOH 溶液等,故C不选;
D.已擦去表面的氧化铝的铝条,在酒精灯上灼烧时,Al会与O 反应生成熔点比Al更高的Al O,把铝包
2 2 3
裹起来,熔化的铝不会滴落下来,故D不选;
答案选A。
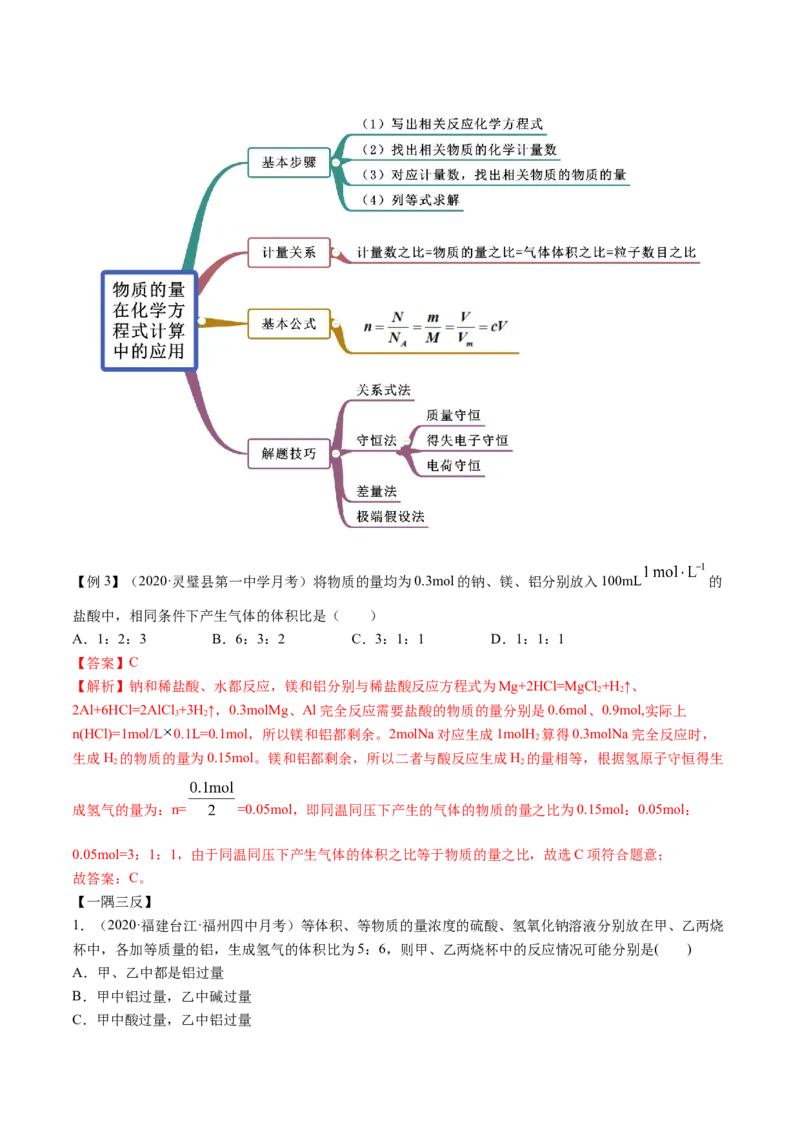
知识点三 物质的量在化学方程中的应用【例3】(2020·灵璧县第一中学月考)将物质的量均为0.3mol的钠、镁、铝分别放入100mL 的
盐酸中,相同条件下产生气体的体积比是( )
A.1:2:3 B.6:3:2 C.3:1:1 D.1:1:1
【答案】C
【解析】钠和稀盐酸、水都反应,镁和铝分别与稀盐酸反应方程式为Mg+2HCl=MgCl +H ↑、
2 2
2Al+6HCl=2AlCl +3H ↑,0.3molMg、Al完全反应需要盐酸的物质的量分别是0.6mol、0.9mol,实际上
3 2
n(HCl)=1mol/L 0.1L=0.1mol,所以镁和铝都剩余。2molNa对应生成1molH 算得0.3molNa完全反应时,
2
生成H 的物质的量为0.15mol。镁和铝都剩余,所以二者与酸反应生成H 的量相等,根据氢原子守恒得生
2 2
成氢气的量为:n= =0.05mol,即同温同压下产生的气体的物质的量之比为0.15mol:0.05mol:
0.05mol=3:1:1,由于同温同压下产生气体的体积之比等于物质的量之比,故选C项符合题意;
故答案:C。
【一隅三反】
1.(2020·福建台江·福州四中月考)等体积、等物质的量浓度的硫酸、氢氧化钠溶液分别放在甲、乙两烧
杯中,各加等质量的铝,生成氢气的体积比为5:6,则甲、乙两烧杯中的反应情况可能分别是( )
A.甲、乙中都是铝过量
B.甲中铝过量,乙中碱过量
C.甲中酸过量,乙中铝过量D.甲中酸过量,乙中碱过量
【答案】B
【解析】根据铝和硫酸、氢氧化钠反应的化学方程式:2Al+3H SO =Al(SO )+3H ↑,
2 4 2 4 3 2
2Al+2NaOH+2H O=2NaAlO +3H ↑可知:相同物质的量的铝,消耗的氢氧化钠少于消耗的硫酸,所以根据
2 2 2
生成的氢气是5︰6可知,铝在与稀硫酸反应时,铝是过量的,硫酸是不足的,而与氢氧化钠反应时,铝是
不足的,氢氧化钠是过量的,所以正确的答案选B。
2.(2019·东台创新高级中学月考)两份铝屑,第一份与过量的盐酸反应,第二份与过量的氢氧化钠溶液
反应,产生氢气的体积比为1∶2,则第一份与第二份铝屑的质量比为( )
A.1∶1 B.1∶2 C.1∶3 D.1∶4
【答案】B
【解析】铝与盐酸、氢氧化钠溶液反应的化学方程式分别为2Al+6HCl=2AlCl +3H↑、2Al+2NaOH+
3 2
2HO=2NaAlO +3H↑,由化学方程式可知,铝与产生氢气的物质的量关系式都为2Al~3H,若二者产生
2 2 2 2
氢气的体积比为1∶2,则第一份与第二份铝屑的物质的量之比为1∶2,质量比也为1∶2,答案选B。
3(2020·全国课时练习)质量比为2:3的金属铝分别与足量稀硫酸和NaOH溶液反应,相同条件下产生
的体积比为( )
A.1:2 B.1:3 C.2:3 D.3:2
【答案】C
【解析】因为稀硫酸和NaOH溶液是足量的,因此铝无论是与稀 反应生成 ,还是与NaOH溶液
反应生成 , 的量都是由铝的量决定的,故相同条件下产生 的体积比为2:3。
答案选C。
4.(2020·全国课时练习)将一定质量的Mg、Zn、Al混合物与足量稀HSO 反应,生成H 2.8L(标准状
2 4 2
况),原混合物质量可能是( )
A.2g B.4g C.10g D.12g
【答案】B
【解析】三种金属与稀硫酸反应离子方程式为:Mg+2H+=Mg2++H↑、Zn+2H+=Zn2++H↑、 Al+2 H+=
2 2
Al3++H↑,由此可得:产生标准状况下相同体积的氢气,消耗锌的质量最大,消耗铝的质量最少。标准
2
状况下2.8L H 的物质的量为n(H)= =0.125mol,假设金属全部为Zn时可求得金属的质量
2 2
为:0.125mol×65g·mol-1=8.125g;假设金属全部为Al时可求得金属的质量为:0.125mol× ×27g·mol-1=2.25g,则金属实际质量应介于2.25g~8.125g之间,所以A、C、D项错误,B项正确。综上所述,符合题意
的为B项。
5.(2020·全国课时练习)相同质量的Mg和Al分别与足量的盐酸反应,所生成的氢气在标准状况下的体
积比是( )
A.2:3 B.1:1 C.3:4 D.24:27
【答案】C
【解析】设金属都为1g,镁和铝的物质的量分别是1/24 mol、1/27 mol。根据方程式Mg+2HCl=
MgCl +H ↑、2Al+6HCl=2AlCl +3H ↑可知生成氢气的物质的量分别是1/24 mol、1/18 mol。标准状况下气
2 2 3 2
体的体积比等于其物质的量之比,则生成的氢气在标准状况下的体积比为(1/24 mol):(1/18 mol)=3:4,
答案选C。
6.(2020·全国课时练习)甲、乙两烧杯中各盛有100 mL 3 mol·L-1的盐酸和氢氧化钠溶液,向两烧杯中
分别加入等质量的铝粉,反应结束后生成的气体的体积比为甲∶乙=1∶2,则加入铝粉的质量为( )
A.5.4 g B.3.6 g C.2.7 g D.1.8 g
【答案】A
【解析】根据方程式,当铝分别和盐酸、氢氧化钠反应时,若消耗等量的铝,生成的气体体积比为1:1。
若铝过量,等量的盐酸和氢氧化钠,生成的气体体积比为2:1。所以当两烧杯中生成的气体体积比为1:2时,
可推知两烧杯中,生成的气体少的甲烧杯中铝有剩余,生成气体多的乙烧杯中铝不足。因为等量的铝消耗
的盐酸物质的量更大,故甲烧杯中装盐酸;乙烧杯中装氢氧化钠。盐酸和氢氧化钠溶液中溶质的物质的量
均为 ,又两烧杯中分别加入等质量的铝粉,反应结束后测得生成的气体体积比为
甲:乙=1:2,设铝与酸反应时酸完全反应,生成的氢气的物质的量为x,则
解得x=0.15mol,一定条件下,气体的物质的量之比等于体积之比,则碱与金属铝反应生成的氢气的物质
的量为 ,碱与金属铝反应时铝完全反应,设与碱反应的铝的物质的量为y,则
解得y=0.2mol,则铝的质量为 。
故答案选:A。
7.(2020·西安市第八十五中学期末)钠、镁、铝各0.4mol分别放入100mL1mol/L的盐酸中,同温同压下
产生的气体体积之比是( )
A.1:2:3 B.3:2:1 C.4:1:1 D.1:1:1
【答案】C
【解析】盐酸的物质的量0.1L× 1mol/L=0.1mol,将三种金属各0.4mol分别投入0.1mol的盐酸中,镁、铝有剩余,应按盐酸的量计算,镁、铝产生氢气物质的量相等。以镁为例,由Mg+2HCl=MgCl +H ↑可知,
2 2
产生氢气的物质的量为(0.1L×1mol/L)×1/2=0.05 mol。但金属钠活泼,能与水反应生成氢气,则生成氢气最
多的是钠,钠与水反应产生氢气应按钠的物质的量计算,2Na+2HO=2NaOH+H ↑,0.4mol钠产生0.2mol氢
2 2
气,故将钠、镁、铝各0.4mol分别放入100mL1mol/L的盐酸中,产生氢气的物质的量之比为
0.2mol:0.05mol:0.05mol=4:1:1,所以同温同压下产生的气体体积比是4:1:1,故选C。