文档内容
2020—2021 学年人教版(2019)选择性必修三章节自我
强化训练
3.5.3 有机合成的相关计算
1.维纶(聚乙烯醇缩甲醛纤维)可用于生产服装、绳索等。其合成路线如下:
下列说法不正确的是( )
A.反应①是加聚反应
B.高分子A的链节中只含有一种官能团
C.通过质谱法测定高分子B的平均相对分子质量,可得其聚合度
D.反应③的化学方程式为:
2.下列说法正确的是( )
A. 和 互为同系物
B.烯烃、炔烃、酚、醛都能使溴水褪色,因为它们都与溴水发生了加成反应。
C.某烃的结构用键线式表示为 ,该烃与Br 按物质的量之比1∶1加成时所得产物有5
2
种
D.105℃,1.01×105Pa时,aL某气态烃在bL氧气(足量)中完全燃烧,将所得混合气体通过浓
硫酸剩余气体cL,则烃燃烧生成的水蒸气的体积就是(a+b-c)L(气体体积在相同条件下
测定)
3.甲烷分子中的四个氢原子都可以被取代。甲烷分子的四个氢原子都被乙烯基( )取代
得到的产物的结构如下所示,下列对所得分子的描述中不正确的是( )A.分子式为
B.1 mol此分子在一定条件最多能与4 mol 发生反应
C.所有碳原子都在同一平面上
D.此物质属于烯烃类物质
4.两种气态烃以一定比例混合,在105℃ 时1 L该混合烃与9 L氧气混合,充分燃烧后恢复到原状
态,所得气体体积为11 L,下列混合烃中不符合条件的是( )
A. 和 B. 和 C. 和 D. 和
5.将等质量的下列各烃,完全燃烧生成 ,耗氧量最大的是( )
A. B. C. D.
6.下列说法正确的是( )
A.按系统命名法,化合物 的名称为2-2-二甲基己烷
B.等质量的聚乙烯、甲烷、乙炔分别充分燃烧,所耗氧气的量依次减少
C.用酒精消毒,其原理是酒精使细菌中的蛋白质变性而失去生理活性
D.蔗糖、麦芽糖和乳糖的分子式都为 ,均能发生银镜反应
7.如图为 在 和 氛围中受热发生变化的热重曲线。下列说法错误的是( )
A.物质A为 , 在隔绝空气条件下,420 ℃ 以下比较稳定,不会分解
B.无论在 氛围还是在 氛围中,A→B阶段均发生了氧化还原反应,但两氛围中的气态产
物不同
C.在酸性 溶液中加入少量 固体样品时,溶液褪色且有少量气泡产生
D.无论在 氛围还是在 氛围中,当1 mol 最终转变为C时,转移的电子的物
质的量相同
8.w g下列物质在足量的氧气中完全燃烧后,生成的产物全部通入足量的过氧化钠固体粉末中,
充分反应后固体增重m g,若w<m,则下列组合一定是 ( )
①氢气和甲醛②一氧化碳和甲醛③甲烷和乙二酸④甲烷和一氧化碳⑤甲烷和乙醇 ⑥乙醇和氢
气
A.④⑤⑥ B.①②③ C.③④⑤⑥ D.①②④⑤
9.下列与有机物的结构、性质的有关叙述中正确的是( )
A.等物质的量的乙烯与乙醇完全燃烧消耗氧气的物质的量相等
B.乙烯、氯乙烯、聚乙烯均可使酸性高锰酸钾溶液褪色
C.分馏、干馏都是物理变化,裂化、裂解都是化学变化D. 苯乙烯和甲苯分子内所有原子可能共平面
10.某物质的分子式为C H O,取该物质a g在足量的O 中充分燃烧后,将产物全部通入过量
x y z 2
的Na O 中,若Na O 固体的质量增加了b g,且a < b,则该物质的分子式可能是( )
2 2 2 2
A.C H O B.C H O C.CH O D.C H O
3 6 2 3 6 3 2 2 3 8 3
11.某有机物在氧气中充分燃烧,生成的水蒸气和二氧化碳的物质的量之比为1∶1,由此可以
得出的结论是( )。
A. 该有机物分子中碳、氢、氧原子个数比为1∶2∶3
B. 该有机物分子中碳、氢原子个数比为2∶1
C. 该有机物中必定含有氧元素
D. 无法判断该有机物中是否含有氧元素
12.有A, B两种烃,含碳的质量分数相等。关于A和B的下列叙述正确的是( )
A. A和B一定是同分异构体
B. A和B不可能是同系物
C. A和B的最简式相同
D. A和B各1 mol完全燃烧后生成二氧化碳的质量一定相等
13.现有乙酸和两种链状单烯烃的混合物,若其中氧的质量分数为a,则碳的质量分数是( )
A. B. C. D.
14.测得某乙酸乙酯和乙酸的混合物中含氢的质量分数为7.8%,则此混合物中含氧元素的质量
分数为( )
A. 56.4% B. 49.8% C. 45.4% D. 15.6%
15.下列说法正确的是( )
A.按系统命名法进行命名, 的名称是:2,3-二乙基丁烷B.对硝基甲苯的结构简式:
C.完全燃烧含等物质的量的碳原子的烷烃、烯烃、炔烃,耗氧量最大的是烷烃
D.乙烯的球棍模型:
16.请按要求填空
(1)① 的名称为:_________;② 的名称为:
____________;
③苯酚与浓溴水反应的化学方程式:________________________;
④甲醛与新制氢氧化铜悬浊液反应的化学方程式:________________________。
⑤某有机化合物A的分子式为 ,分子结构中有三个—CH ,两个 ,一个—Br,
3
则A的结构简式为_______________。
(2)某有机物A的相对分子质量为74,且红外光谱图如下图,则A的结构简式为
____________。
(3)1体积某烃的蒸气完全燃烧生成的CO 比生成的水蒸气少1体积(在同温同压下测定)。
2
0.1mol该烃完全燃烧的产物被碱石灰吸收,碱石灰增重39g。该烃的分子式为__________;若
该烃的一氯代物有3种,写出该烃所有可能的结构简式___________________。
17.0.2 mol某烃A在氧气中充分燃烧后,生成物B、C各1.2 mol。
(1)烃A的分子式为________。(2)①若烃A不能使溴水退色,但在一定条件下,能与 发生取代反应,其一氯代物只有一种,
则烃A的结构简式为_________________________________________________________。
②若烃A能使溴水退色,在催化剂作用下可与 加成,其加成产物分子中含有4个甲基,则
所有符合条件的烃A的结构简式为______________________________________________。
18.回答下列问题
(1)某学习小组为验证烃分子中含有碳、氢两种元素并测定产生 的质量,将其燃烧产物通
过: a.浓硫酸 b.澄清石灰水 c.无水硫酸铜 d.碱石灰
正确的操作顺序为________。
(2)该学习小组的同学欲推测烃A的结构,他们测得A的相对分子质量为72,该烃中碳元素的
质量分数为83.3%,完全燃烧0.1 mol A,生成22 g 气体。请回答下列问题:
A的分子式为___________________________________________________,
A可能的结构简式有________________种,A的一种同分异构体中没有支链,写出其结构简式
________________________________________________________________________。
19.写出下列各烷烃的分子式。
(1)烷烃A在同温同压下蒸气的密度是 的43倍:________。
(2)烷烃B的分子中含有400个氢原子:____________________________________。
(3)1 L烷烃C的蒸气完全燃烧时,生成同温同压下15 L水蒸气:________。
(4)0.1 mol烷烃E完全燃烧,消耗标准状况下的 11.2 L:________。
20.在常温下的一密闭容器中事先放入1.56 g过氧化钠,然后再通入乙烷与氧气的混合气体,
用电火花引爆,直至反应完全为止,恢复到原温度,容器内压强近似为零。
(1)相同条件下,通入的气体氧气和乙烷的体积比是多少?
(2)通入氧气的质量最大应是多少?参考答案
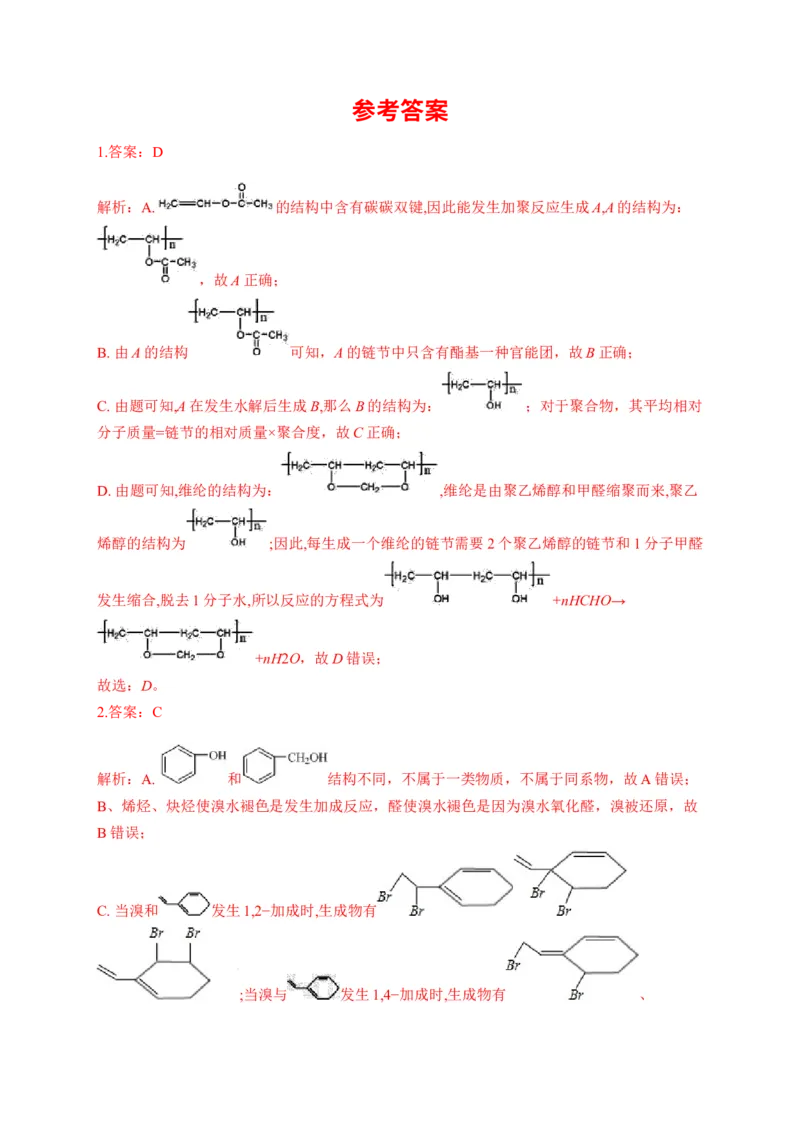
1.答案:D
解析:A. 的结构中含有碳碳双键,因此能发生加聚反应生成A,A的结构为:
,故A正确;
B. 由A的结构 可知,A的链节中只含有酯基一种官能团,故B正确;
C. 由题可知,A在发生水解后生成B,那么B的结构为: ;对于聚合物,其平均相对
分子质量=链节的相对质量×聚合度,故C正确;
D. 由题可知,维纶的结构为: ,维纶是由聚乙烯醇和甲醛缩聚而来,聚乙
烯醇的结构为 ;因此,每生成一个维纶的链节需要2个聚乙烯醇的链节和1分子甲醛
发生缩合,脱去1分子水,所以反应的方程式为 +nHCHO→
+nH2O,故D错误;
故选:D。
2.答案:C
解析:A. 和 结构不同,不属于一类物质,不属于同系物,故A错误;
B、烯烃、炔烃使溴水褪色是发生加成反应,醛使溴水褪色是因为溴水氧化醛,溴被还原,故
B错误;
C. 当溴和 发生1,2−加成时,生成物有
;当溴与 发生1,4−加成时,生成物有 、,显然所得产物有5种,故C正确;
D. aL某气态烃在bL氧气(足量)中完全燃烧,所得混合气体通过浓硫酸剩余气体cL,对于燃烧前
后体积不变化的反应,烃燃烧生成的水蒸气的体积是(a+b−c)L,但是若是燃烧前后体积变化的
反应,则不成立,故D错误。
故选C.
3.答案:C
解析:根据结构简式可直接数出碳、氢原子的数目从而得出分子式 ,A正确;1 mol该
分子含4 mol碳碳双键,故可与4 mol 发生加成反应,B正确;因含碳碳双键且只有C、H
两种元素,因此属于烯烃,D正确;甲烷分子中四个氢原子被四个 取代后,其正四
面体的基本结构不变,C项不正确。
4.答案:D
解析:设混合气体的平均分子组成为 、,则混合气体与氧气反应的化学方程式为
, ,由题意可知, ,即
,解得y=8,即混合气体分子中氢原子的平均个数为8。而 和 无论以何种比例混
合,氢原子的平均个数都不可能等于8,故选D。
5.答案:A
解析:A. 中C. H原子数目之比为1:4;
B. 中C. H原子数目之比为2:4=1:2;
C. 中C. H原子数目之比为6:6=1:1;
D. 中C. H原子数目之比为3:6=1:2;
故 中H的质量分数最大,相同质量甲烷消耗氧气最多,
故选:A.
6.答案:C
解析:A.烷烃命名时,选用最长的碳链为主链,故主链上有4个碳原子,从离支链较近的一端
给主链上的碳原子进行编号,在2号碳原子上有2个甲基,按照系统命名法,应该命名为2,2-二甲基丁烷,故A错误;
B.等质量的烃燃烧时,氢元素的百分含量越高,耗氧量越高,由于氢元素的百分含量:甲烷>
聚乙烯>乙炔,因此所耗氧气的量:甲烷>聚乙烯>乙炔,故B错误;
C.酒精使细菌中的蛋白质变性而失去生理活性,因此酒精能消毒,故C正确;
D.含醛基的物质能发生银镜反应,蔗糖和乳糖都不含醛基,不能发生银镜反应,故D错误。
【答案】C
7.答案:D
解析:根据题图中曲线所对应的数据计算可得,物质A为 、物质B为 、物质C
为CaO。温度在420 ℃ 以下, 氛围中物质A的质量随着温度的升高保持不变,说明在420
℃ 以下 比较稳定,不会分解,A正确;A→B阶段为 分解或被氧气氧化生成
的反应,均属于氧化还原反应,存在电子的转移,但两氛围中的气态产物不同, 氛
围中气态产物是 , 氛围中气态产物是CO,所以1 mol 最终转变为CaO时,
转移的电子数不同,B正确,D错误;在酸性 溶液中加入少量 固体样品时,发
生反应 ,溶液褪色且有少量气泡产生,
C正确。
8.答案:A
解析:
9.答案:A
解析:
10.答案:C
解析:A、C H O 中C原子数目大于氧原子数目,不符合题意,故A错误;
3 6 2
B、C H O 中C原子数目等于氧原子数目,过氧化钠增大的质量等于有机物的质量,不符合题
3 6 3
意,故B错误;
C、CH O 中C原子数目小于氧原子数目,过氧化钠增大的质量小于有机物的质量,符合题意,
2 2
故C正确;
D、C H O ,中C原子数目等于氧原子数目,过氧化钠增大的质量等于有机物的质量,不符合
3 8 3
题意,故D错误;
故选C.
11.答案:D解析:有机物燃烧生成二氧化碳和水,该有机物一定含有碳元素和氢元素,不能确定是否含有
氧元素。
12.答案:C
解析:因为A、B都是烃,碳的质量分数相同,则氢的质量分数一定也相同,则C、H的个数
比相同,即最简式相同,可能是同系物,例如 和 ,但分子式不一定相同。
13.答案:C
解析:分析解题的基点:混合物中碳、氢原子个数比恒定。
乙酸( )与两种单烯烃(通式为 )分子中的碳、氢原子个数比都是1∶2,碳、氢元素
的质量比为6∶1,氧的质量分数为a,碳、氢元素的质量分数之和为1-a,则碳元素的质量分
数为 。
14.答案:C
解析:分析解题的基点:混合物中碳、氢原子个数比恒定。
乙酸乙酯( )与乙酸( )分子中的碳、氢原子个数比都是1∶2,碳、氢元素的质量
比为6∶1,碳元素的质量分数为6×7.8%,氧元素的质量分数为1-7×7.8%= 45.4%。
15.答案:B
解析:根据系统命名法的命名规则可知,该烃的最长碳链含有6个C原子,所以该烃的名称应
是3,4-二甲基己烷,A错误;硝基中的氮原子应与苯环上的碳原子直接相连,B错误;碳原
子数相同时,烷烃含H量最大,所以其耗氧量最大,C正确;乙烯的球棍模型为
,故D错误。
16.答案:①
3-甲基-2-丁醇 ② 2-甲基-2,4-己二烯
③④
⑤
(2)
(3)
解析:
17.答案:(1) (2)① ② 、 、
解析: (1)因为烃充分燃烧只生成 和 ,由题意可知1 mol A燃烧生成的 和 各
6 mol,所以A为 。
(2)①根据A的分子式可知A的不饱和度为1,所以A的结构有两种情况:有一个双键或有一
个环。因为A不能使溴水退色,所以A中没有双键,又因为其一氯代物只有一种,所以A为
环己烷( )。②A与 加成的产物分子中含有四个甲基,说明A中有两个甲基在侧链,主
链上有4个碳原子,结构简式可能为 、 或
。
18.答案:(1)cabd (2) ;3;
解析: (1)本实验应按检验水→除去水→检验并吸收 →防止空气中水与 对测定
质量的干扰。 的质量为澄清的石灰水吸收 前后质量的变化值。无水硫酸铜遇水变成蓝色晶体,可用于检验产物中水的存在,澄清的石灰水中通入 ,溶液变浑浊,用于检验 。
浓硫酸可用于吸收产物中的水蒸气,碱石灰用于吸收空气中的 和 。因此连接顺序为
cabd。
(2)0.1 mol A中含有碳原子数为 ,每个分子中含有C原子个数为5个。H原
子质量分数为1-83.3%=16.7%,该烃分子中H原子个数为72 ×16.7%÷1 ≈12,所
以该烃的分子式为 。
19.答案:(1) (2) (3) (4)
解析:
20.答案:(1) (2)0.8 g
解析: (1)本题可通过方程式的叠加方法进行解答:
①
②
③
由于在室温下水是液体,可参加反应,也可不参加反应,因此可用极端法判断:
若水参加反应,则有①+②+1.5×③:
④若水不参加反应,则有①+②:
⑤
故不难得出正确结论。
(2)通入氧气最大量时按⑤进行。