文档内容
九年级化学单元检测试卷(11)盐 化肥
(时间:45分钟 满分:50分)
班级 姓名 得分
可能用到的相对原子质量:C:12 O:16 Na:23 Ca:40 Cl:35.5
一、单选题(共10×2=20分)
题号 1 2 3 4 5 6 7 8 9 10
答案
1、化学就在我们身边,生活中处处有化学。根据你所学过的化学知识,下列说法错误的是
A.食品工业中,发酵粉的主要成份是小苏打—NaHCO
3
B.医疗上用来配制生理盐水,农业上用来选种—NaCl
C.大量用于建筑业,还可用于作为补钙剂—CaCO
3
D.广泛应用于玻璃、造纸、纺织和洗涤剂生产—NaHCO
3
2、下列对实验过程的评价中,正确的是
A、固体加入稀盐酸,产生了无色气体,证明该固体一定含有碳酸根离子
B、面粉发酵生成有机酸,在做面食之前可以用纯碱去中和有机酸
C、某溶液中滴加氯化钡溶液,生成不溶于稀硝酸的白色沉淀,该溶液中一定含碳酸根离子
D、碳酸钙不能跟稀硫酸发生复分解反应
3、下列是关于“粗盐提纯”实验的几种说法,其中正确的是
A.为了加快过滤速度,应用玻璃棒不断搅拌过滤器内的液体
B.如果经两次过滤滤液仍浑浊,则应检查实验装置并分析原因
C.蒸发滤液时要用玻璃棒不断搅拌,用酒精灯持续加热直到蒸干为止
D.为使食盐快速溶解,应用较多的水溶解食盐
4、下列物质相互混合时,能发生化学反应,但无沉淀生成的是
A.硝酸钠溶液和氯化钾溶液 B.氢氧化铁和硫酸
C.碳酸钙和氯化钠溶液 D.硝酸银溶液和氯化镁溶液
5、某试验田的玉米叶色淡黄,有倒伏现象,你认为应施用的复合肥是
A.CO(NH) B.KCl C.Ca(HPO) D.KNO
2 2 2 4 2 3
6、下列是农业生产中的一些思路,你认为不妥当的是
A.将农家肥和化肥综合使用,以提高生产效益
B.对大棚中的植物施加适量的二氧化碳,以促进其光合作用
C.种植、养殖、制沼气相结合,可以改善环境也可以提高畜牧业的产量
D.将硝酸铵和熟石灰混合施用,在给农作物提供营养元素的同时,又能降低土壤的酸性
7、只用一种试剂来鉴别氢氧化钠、氢氧化钙、稀硫酸三种溶液,这种试剂是A.酚酞试液 B.石蕊试液 C.碳酸钠溶液
NHHCO NHCl KCl
D.二氧化碳 4 3 4
加试剂甲
8、右图是某同学鉴别NHHCO、NHC1、KCl三种化肥的过程,
4 3 4
有氨味 无氨味
其中试剂甲和乙分别可能是 NHHCO NHCl KCl
4 3 4
A.甲:熟石灰; 乙:稀盐酸 加试剂乙
有气泡 无气泡
B.甲:水; 乙:氢氧化钠溶液
NH HCO NH Cl
4 3 4
C.甲:氢氧化钠溶液; 乙: 水
D.甲:稀盐酸; 乙:氯化钠溶液
9、在没有指示剂的情况下,除去CaCl 溶液中混有的盐 酸,应加入的试剂是
2
A.CaCO B.CaO C.Ca(OH) D.NaCO
3 2 2 3
10、向HSO 和CuSO 的混合溶液中,不断加入NaOH溶液,下图曲线正确的是
2 4 4
C D
A B
二、填空题(每空1分,共17分)
11、在H、O、C、Cl、Na、Ca六种元素中,选择适当元素,组成符合下列要求的物质,将其化学式
填入空格中。
(1)人工降雨的氧化物____________________;
(2)可用于金属表面除锈的酸____________________;
(3)可改良酸性土壤的碱____________________;
(4)可做干燥剂的氧化物____________________;
(5)曾经由侯德榜制造生产而为中国人争光的盐____________________;
12、氢氧化钾是我国古代纺织业常用作漂洗的洗涤剂,古人将贝壳(主要成分是碳酸钙)灼烧
后的固体(主要成分是氧化钙)与草木灰(主要成分是碳酸钾)在水中相互作用,生成氢氧化
钾。请按要求用化学方程式表述上述有关反应。
(1)分解反应 ,
(2)化合反应 ,
(3)复分解反应 。
13、“酸雨”大家一定听说过,可“碱雨”呢?1958年以来,有人陆续在美国等地收集到碱
性雨水(即“碱雨”)。“碱雨”是如何形成的?原来,人们向植物施铵态氮肥时,由于某些
干旱地区土壤多呈碱性,使得铵态氮肥转化为氨气进入大气,进入大气中的氨遇雨而降便形
成了“碱雨”。回答下列问题:(1)“碱雨”的pH 7(填“大于”、“小于”或“等于”)。
(2)“酸雨”是因为工业生产过程中向大气中大量排放 造成的。
(3)酸雨的pH小于 。
(4)请为施用铵态氮肥提出一条合理措施。答:
。
14、如图是实验室制氨气的装置图,请回答:
①写出实验室制取氨气的化学反应方程式:____
_
②因为氨气的密度比空气的_____
(填“大”或“小”),所以收集氨气的方法是_____
(填序号).①向上排空气法 ②向下排空气法
③干燥氨气_____(填“能”或“不能”)用浓硫酸。
④氨气有刺激性气味,猜测实验装置中棉花的作用是:____
三、实验探究(每空1分,共8分)。
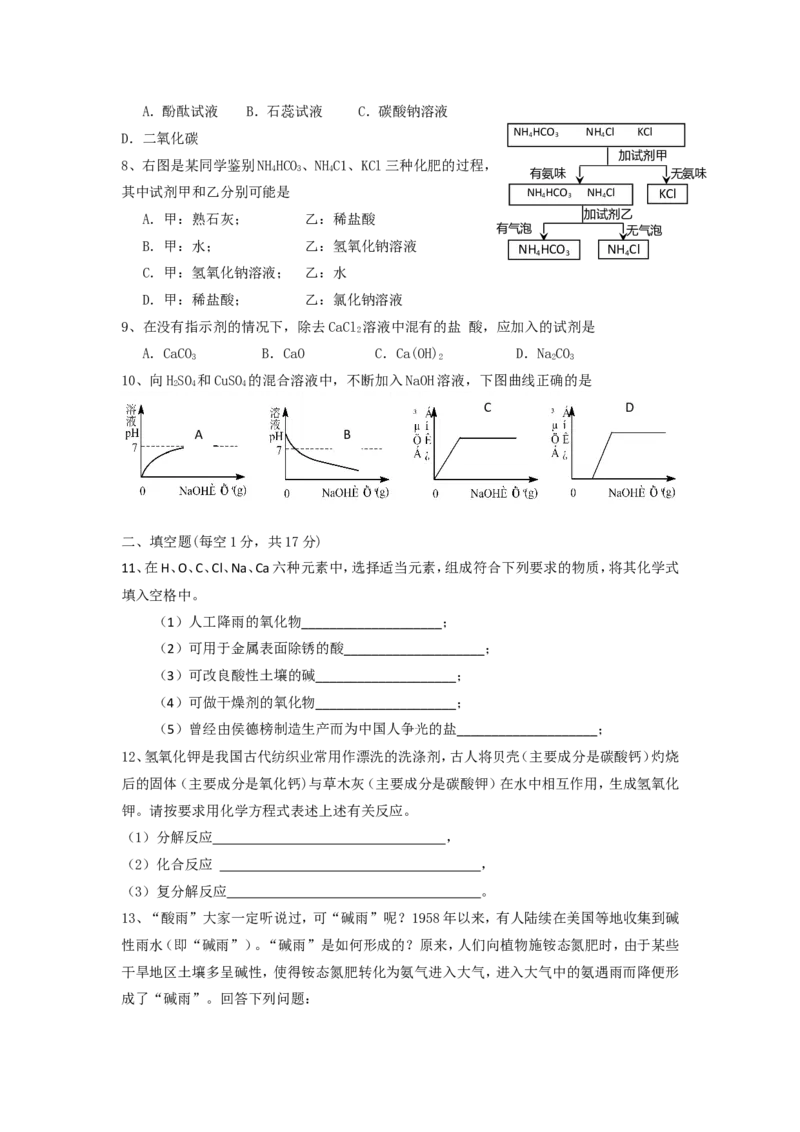
15、一同学用某种粗盐进行提纯实验,步骤见下图。
请回答:
(1)步骤①和②的操作名称是_____________。
(2)步骤③判断加入盐酸“适量”的方法是 _;步骤④加热蒸发时
要用玻棒不断搅拌,这是为了防止 。
(3)猜想和验证:
猜想 验证的方法 现象 结论
四、 计算
取少量固体A于试管中,滴加稀盐
题猜想Ⅰ:固体A中含 猜想Ⅰ(5
酸,并用涂有澄清石灰水的小烧
分)CaCO、MgCO。 成立
3 3
杯罩于试管口。
16、 家里
猜想Ⅱ:固体A中含 取少量固体A于试管中,先滴入 有气泡放出,
蒸馒 头用
BaCO。 ,再滴入NaSO 溶液 无白色沉淀
3 2 4
的纯 碱中
猜想Ⅲ:最后制得的 取少量NaCl晶体溶于试管中的蒸
含有 猜想Ⅲ少量
NaCl晶体中还含有 馏水, _
的氯 成立 化钠,
NaSO。 。
2 4课外探究小组的同学欲测定纯碱中碳酸钠的含量。他们取该纯碱样品11.0g,全部溶解在100.0g
水中,再加入氯化钙溶液141.0g,恰好完全反应。过滤干燥后,称得沉淀质量为10.0g。请计算:
(1)纯碱样品中碳酸钠的质量;(2)反应后所得滤液中溶质的质量分数。
(十一)
二
题号 1 2 3 4 5 6 7 8 9 10
11
答案 D B B B D D C A A D
、
CO HCl Ca(OH) CaO NaCO
2 2 2 3
12、 (1)CaCO CaO + CO↑(2)CaO + HO = Ca(OH)
3 2 2 2
(3)KCO + Ca(OH) =CaCO↓+ 2KOH
2 3 2 3
13.(1)大于(2)二氧化硫 二氧化氮 (3)5.6 (4)不能与碱性物质混合使用
14、①2NHCl+Ca(OH) CaCl+2HO+2NH↑ ②小 ②
4 2 2 2 3
③不能 ④防止氨气逸出,污染环境
三、15、(1)过滤
(2)滴加盐酸至无气泡放出为止;局部温度过高,造成固体(或溶液)飞溅;
(3)
猜想 验证的方法 现象 结论
有气泡放出,烧杯底变浑浊(或石灰水
变浑浊,或石灰水有白色沉淀)
滴入稀硝酸(或稀盐酸), 猜想Ⅱ不成立
滴入BaCl[或Ba(OH)、或 有白色沉淀
2 2
Ba(NO)]溶液,
3 2四、16、(1)10.6g(2)5%