文档内容
九年级化学单元检测试卷(10)酸和碱
(时间:45分钟 满分:50分)
班级 姓名 得分
可能用到的相对原子质量:H—1 O—16 Na—23 S—32
一、单选题(共10×2=20分)
题号 1 2 3 4 5 6 7 8 9 10
答案
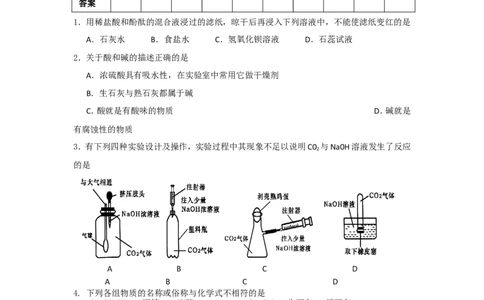
1.用稀盐酸和酚酞的混合液浸过的滤纸,晾干后再浸入下列溶液中,不能使滤纸变红的是
A.石灰水 B.食盐水 C.氢氧化钡溶液 D.石蕊试液
2.关于酸和碱的描述正确的是
A.浓硫酸具有吸水性,在实验室中常用它做干燥剂
B.生石灰与熟石灰都属于碱
C.酸就是有酸味的物质 D.碱就是
有腐蚀性的物质
3.有下列四种实验设计及操作,实验过程中其现象不足以说明C0 与Na0H溶液发生了反应
2
的是
A B C D
A B C D
4. 下列各组物质的名称或俗称与化学式不相符的是
A. CHOH 酒精 乙醇 B. CaO 生石灰 消石灰
2 5
C. Ca(OH) 熟石灰 氢氧化钙 D. NaOH 烧碱 苛性钠
2
5.右图是盐酸滴入氢氧化钠溶液中有关粒子间反应的示意
图。下列说法中错误的是
A.盐酸溶液中含有氢离子和氯离子
B.氢氧化钠溶液中含有钠离子和氢氧根离子
C.两种溶液混合时,氢离子与氢氧根离子结合生成了水分子
D.两种溶液混合时,钠离子与氯离子结合生成了氯化钠分子
6.以下说法正确的是A.中和反应有盐和水生成,因此有盐和水生成的反应一定是中和反应
B.氧化物中含有氧元素,而含氧元素的化合物不一定是氧化物
C.碱中都含有氢元素,所以含有氢元素的化合物一定是碱
D.置换反应一定有单质生成,所以有单质生成的反应一定是置换反应
7.下列除去杂质(在括号内)选用的试剂(在箭头右侧)错误的是
A.CO 气体(HO)→生石灰 B.C粉(CuO) →稀盐酸
2 2
C.CaCl 溶液(HC1) →碳酸钙粉末 D.CO气体(CO) →氢氧化钠溶液
2 2
8.下列做法不科学的是
A.用干冰人工降雨 B.服用氢氧化钠治胃病
C.用食醋除去水垢 D.用熟石灰给鱼塘消毒
9.下列实验能利用厨房中的食盐、食醋、纯碱三种物质做成功的是
①检验自来水中是否含有氯离子;②检验鸡蛋壳能否溶于酸;③除去热水瓶中的水垢。
A.②③ B.①③ C.①② D.①②③
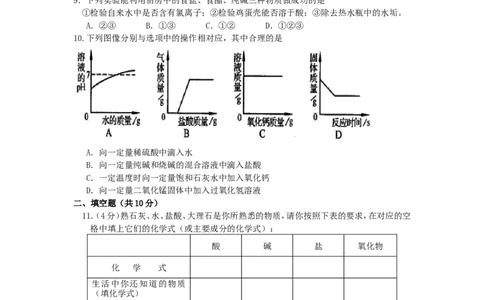
10.下列图像分别与选项中的操作相对应,其中合理的是
A.向一定量稀硫酸中滴入水
B.向一定量纯碱和烧碱的混合溶液中滴入盐酸
C.一定温度时向一定量饱和石灰水中加入氧化钙
D.向一定量二氧化锰固体中加入过氧化氢溶液
二、填空题(共10分)
11.(4分)熟石灰、水、盐酸、大理石是你所熟悉的物质,请你按照下表的要求,在对应的空
格中填上它们的化学式(或主要成分的化学式):
酸 碱 盐 氧化物
化 学 式
生活中你还知道的物质
(填化学式)
12.(2分)如右图是稀释浓硫酸实验的示意图。
(1)写出图中a、b两种仪器的名称:
a ,b 。
(2)b容器所盛的试剂是 (填“水”或“浓硫酸”)。
(3)稀释时,若两种试剂添加顺序颠倒,将会发生
。
13.(4分)化学与我们的生产密切相关,请试用所学过的化学知识解释下列现象或做法的原
因(用化学方程式表示):
(1)人的胃液中含有少量盐酸,服用含少量细铁粉的补血药品,能治疗缺铁性贫血(2)食品包装袋中的干燥剂(主要成分是氧化钙)有防潮作用
(3)用石灰浆粉刷墙壁,在一段时间内墙壁会“出汗”
(4)长期存放的氢氧化钠溶液,因保存不当而发生变质
。
三、实验题
稀盐酸
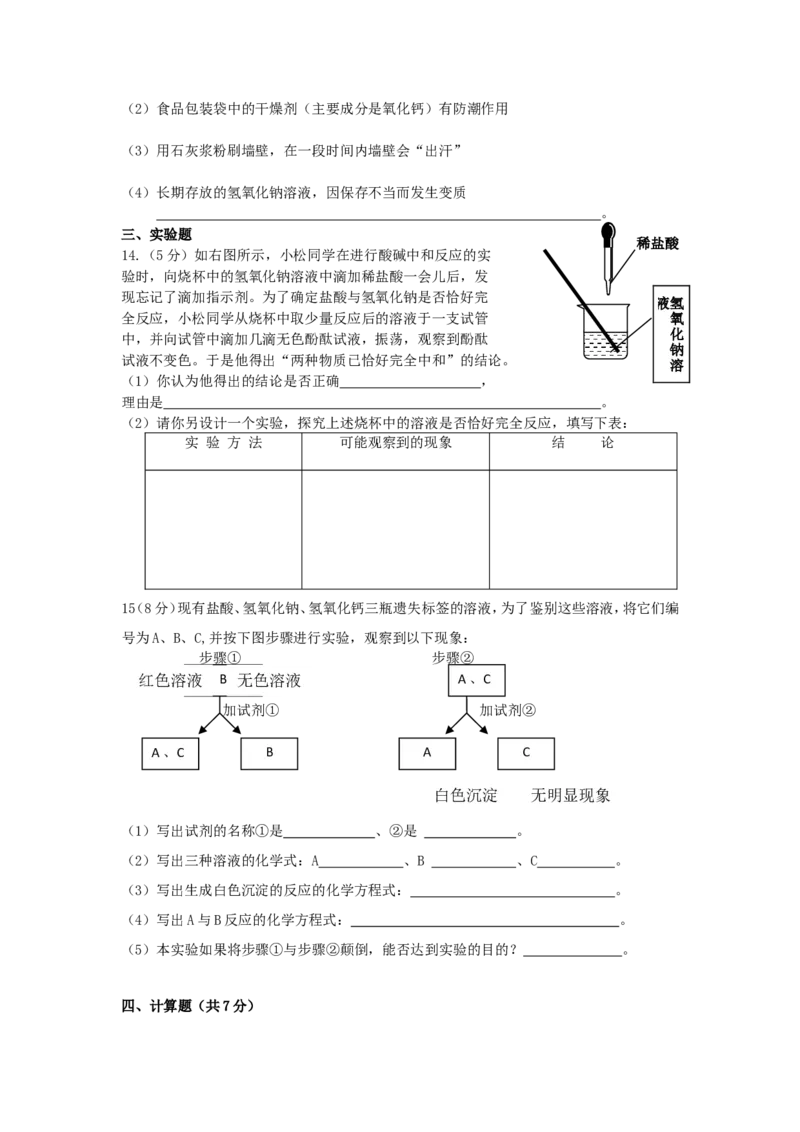
14.(5分)如右图所示,小松同学在进行酸碱中和反应的实
验时,向烧杯中的氢氧化钠溶液中滴加稀盐酸一会儿后,发
现忘记了滴加指示剂。为了确定盐酸与氢氧化钠是否恰好完
液氢
全反应,小松同学从烧杯中取少量反应后的溶液于一支试管 氧
化
中,并向试管中滴加几滴无色酚酞试液,振荡,观察到酚酞
钠
试液不变色。于是他得出“两种物质已恰好完全中和”的结论。
溶
(1)你认为他得出的结论是否正确 ,
理由是 。
(2)请你另设计一个实验,探究上述烧杯中的溶液是否恰好完全反应,填写下表:
实 验 方 法 可能观察到的现象 结 论
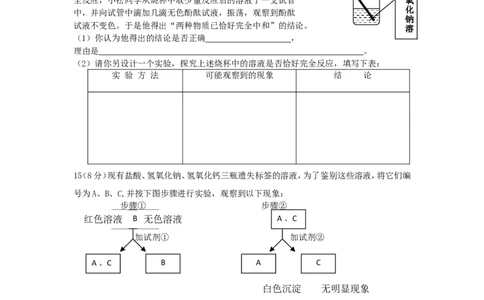
15(8分)现有盐酸、氢氧化钠、氢氧化钙三瓶遗失标签的溶液,为了鉴别这些溶液,将它们编
号为A、B、C,并按下图步骤进行实验,观察到以下现象:
步骤① 步骤②
红色溶液A、B、无C色溶液 A、C
加试剂① 加试剂②
A、C B A C
白色沉淀 无明显现象
(1)写出试剂的名称①是 、②是 。
(2)写出三种溶液的化学式:A 、B 、C 。
(3)写出生成白色沉淀的反应的化学方程式: 。
(4)写出A与B反应的化学方程式: 。
(5)本实验如果将步骤①与步骤②颠倒,能否达到实验的目的? 。
四、计算题(共7分)16.利用中和反应可以测定酸或碱溶液中溶质的质量分数。例如,在一定量的待测酸(或碱)
溶液中逐滴滴入已知质量分数的碱(或酸)溶液(这种溶液被称为标准溶液),直到酸、碱恰好
完全反应,根据消耗标准碱(或酸)溶液的多少即可求算出待测酸(或碱)溶液的溶质质量分
数。下图为某次测定过程中,溶液的pH随所滴加的某标准溶液体积的变化而变化的关系图。
(1)根据上图曲线可以判断在实验中是向
(填“酸”或“碱”,下同)溶液(待测液)中滴
加 溶液(标准液)。
(2)在这次测定中,为了指示中和反应刚好完全,用酚酞做
指示剂,即在待测溶液中先滴入几滴酚酞试液,若看
到 现象,则证明中和反应刚好完全。
(3)如果实验中使用的酸是硫酸溶液,碱是氢氧化钠溶液,且待测液和标准液 的密度均以
1.0g/mL计。若测定中取用待测液25mL,标准液溶质的质量分数为 4.5%,根据图中数据,计
算待测液溶质的质量分数。
(十)
题号 1 2 3 4 5 6 7 8 9 10
答案 B A D B D B A B A B
二、11.(每2空1分)
HCl Ca(OH) CaCO HO
2 3 2
此空只要答案合理均给分
12.(1)玻璃棒; 量筒 (2)浓硫酸 (3)酸液飞溅
13.(1)Fe+2HCl==FeCl+H↑(2)CaO+HO=Ca(OH)
2 2 2 2(3)Ca(OH)+CO===CaCO↓+HO(4)2NaOH+CO==NaCO+HO
2 2 3 2 2 2 3 2
三、14.(1)不正确 如果盐酸滴加过量,滴入酚酞试液也不变色
(2)(以下方法任写一种均可)
①取样,滴加紫色石蕊试液 试液变红 盐酸过量
②取样,滴加紫色石蕊试液 试液不变红 恰好中和
③取样,滴加碳酸钠溶液 有气泡产生 盐酸过量
④取样,滴加碳酸钠溶液 无气泡产生 恰好中和
⑤取样,加入锌粒等活泼金 有气泡产生 盐酸过量
属
⑥取样,加入锌粒等活泼金 无气泡产生 恰好中和
属
15.(1)酚酞,二氧化碳
(2)Ca(OH);HCl;NaOH (3)Ca(OH)+ CO =CaCO↓+ HO
2 2 2 3 2
(4)Ca(OH)+ 2HCl = CaCl +2HO (5)可以达到目的
2 2 2
四、16. (1) 碱 ;酸
(2)溶液的红色刚好褪去
(3)消耗掉的硫酸溶液质量:24.5mL×1.0g/mL=24.5g
消耗掉的硫酸溶液中溶质的质量:24.5g×4.5%=1.10g
解: 设待测液溶质质量分数为x
2NaOH + HSO4 = NaSO+2 HO
2 2 4 2
80 98
25 mL×1.0g/mL×x 1.10g
80 :98 = 25 mL×1.0g/mL×x :1.10g
x=0.036(即3.6%)
答: 待测液溶质质量分数为3.6%