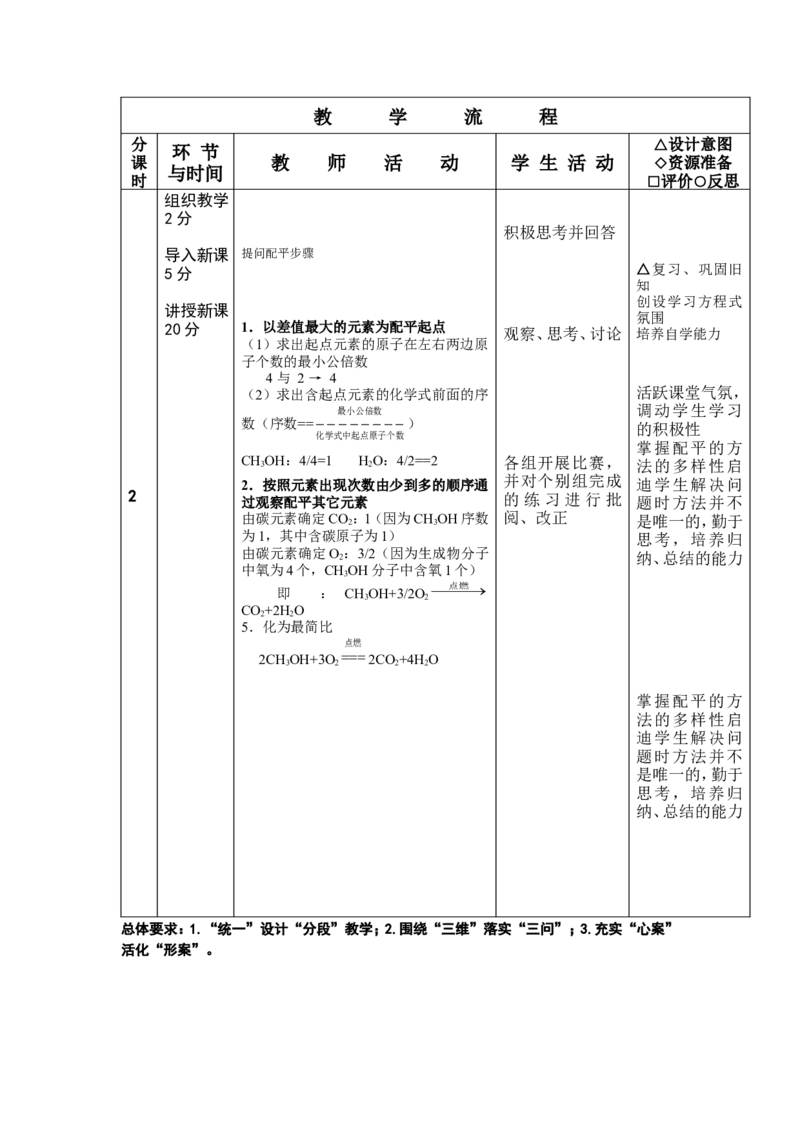文档内容
教 学 设 计
题 目 课题 2 如何正确书写化学方程式 总课时 5
学 校 教 者 年 级 八 学 科 化学
设计来
自我设计 教学时间 年 月 日— 月 日
源
在学习了化学方程式的基础上学习化学方程式当然书写,学生能够
教
更好的掌握所学知识。
材
分
析
学生在学习了一些实验的基础上,学习新课对于实验探究有一定程度 的基础,
学
对于学生的学习有一定的好处。对于本节课的学习,学生能够更深刻的认识世
情
界。
分
析
1.知识与技能: (1)进一步理解化学方程式的涵义
(2)能正确书写简单的化学方程式
教
(3)能真正了解书写化学方程式应遵循的两个原则
2.过程与方法:(1)在练习书写方程式的过程中掌握化学方程式的配平方法-最小公倍数
学 法。
(2)归纳正确书写化学方程式的步骤:①写②配③注④等
(3)初步学会用化程式来表所获得的信息
目
3.情感、态度与价值观(1)让学生在学习过程中意识到任何事都必须尊重客观事实,在
学习中体会学习的乐趣,体会化学用语的方便和实用。
(2)使学生体会到正确书写化学方程式的重要性
标
重
正确书写化学方程式。
点
难
化学方程式的配平方法
点
课
前
准
备
总体要求:1.“统一”设计“分段”教学;2.围绕“三维”落实“三问”;3.充实“心案”
活化“形案”。教 学 流 程
分 △设计意图
环 节
课 教 师 活 动 学 生 活 动 ◇资源准备
与时间
时 □评价○反思
组织教学
2分
积极思考并回答
完成有关化学方
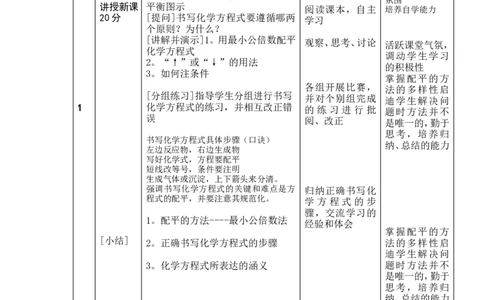
导入新课 质量守恒定律内容及微观解释2。化
5分 学方程式的定义3。写出前面已学过 程式的书写 △复习、巩固旧
知
的化学方程式3~4个
创设学习方程式
[阅读]指导学生阅读教材 P96中的
氛围
讲授新课 平衡图示
阅读课本,自主 培养自学能力
20分 [提问]书写化学方程式要遵循哪两
学习
个原则?为什么?
[讲解并演示]1。用最小公倍数配平
观察、思考、讨论 活跃课堂气氛,
化学方程式
调动学生学习
2。“↑”或“↓”的用法
的积极性
3。如何注条件
掌握配平的方
各组开展比赛, 法的多样性启
[分组练习]指导学生分组进行书写
并对个别组完成 迪学生解决问
1 化学方程式的练习,并相互改正错 的 练 习 进 行 批 题时方法并不
误
阅、改正 是唯一的,勤于
思考,培养归
书写化学方程式具体步骤(口诀)
纳、总结的能力
左边反应物,右边生成物
写好化学式,方程要配平
短线改等号,条件要注明
生成气体或沉淀,上下箭头来分清。
强调书写化学方程式的关键和难点是方 归纳正确书写化
程式的配平,并要注意其规范化。
学 方 程 式 的 步
骤,交流学习的
1。配平的方法----最小公倍数法
经验和体会
掌握配平的方
[小结] 2。正确书写化学方程式的步骤 法的多样性启
迪学生解决问
3。化学方程式所表达的涵义 题时方法并不
是唯一的,勤于
思考,培养归
纳、总结的能力
总体要求:1.“统一”设计“分段”教学;2.围绕“三维”落实“三问”;3.充实“心案”
活化“形案”。教 学 流 程
分 △设计意图
环 节
课 教 师 活 动 学 生 活 动 ◇资源准备
与时间
时 □评价○反思
练习巩固 课后习题
板书设计
课题2 如何正确书写化学方程式
一、化学方程式要遵循两个
原则
1. 以客观事实为基础
2. 遵循质量守恒定律
二、书写化学方程式的步骤
1.“写”
2.“配”
3.“注”
4.“等”
1
总体要求:1.“统一”设计“分段”教学;2.围绕“三维”落实“三问”;3.充实“心案”
活化“形案”。教 学 流 程
分 △设计意图
环 节
课 教 师 活 动 学 生 活 动 ◇资源准备
与时间
时 □评价○反思
组织教学
2分
积极思考并回答
导入新课 提问配平步骤
5分 △复习、巩固旧
知
创设学习方程式
讲授新课
氛围
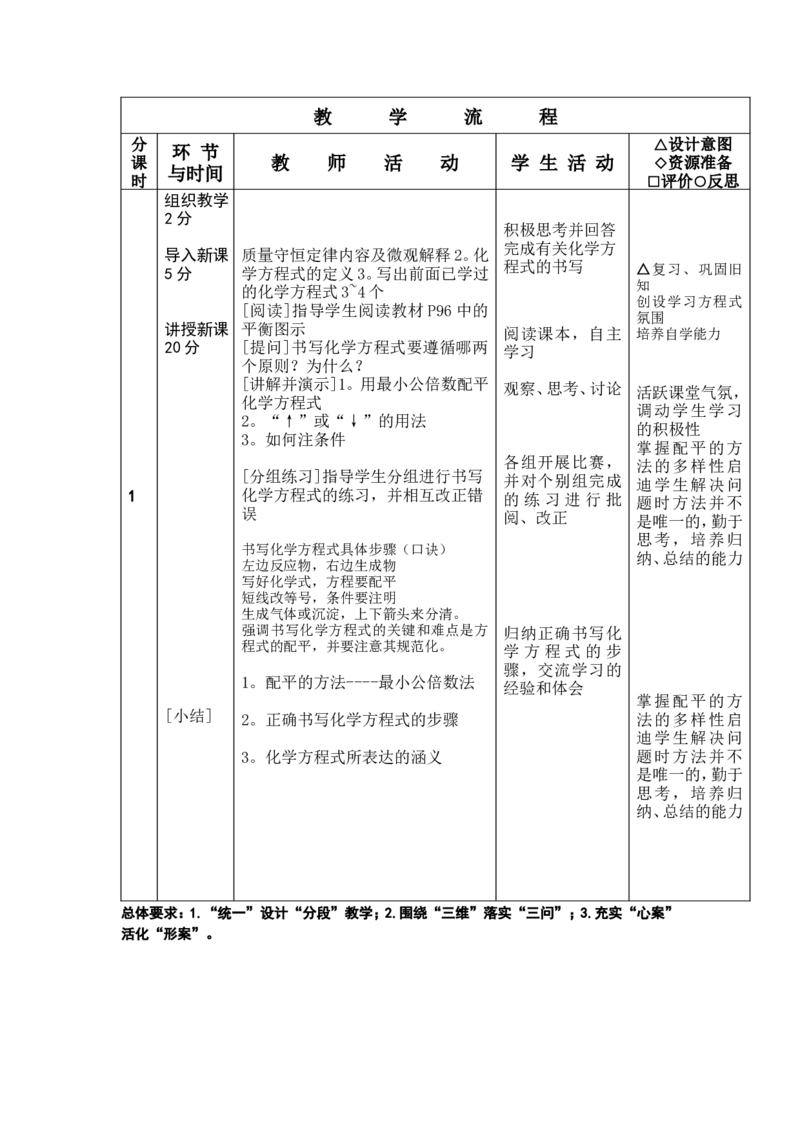
20分 1.以差值最大的元素为配平起点
观察、思考、讨论 培养自学能力
(1)求出起点元素的原子在左右两边原
子个数的最小公倍数
4 与 2 → 4
(2)求出含起点元素的化学式前面的序 活跃课堂气氛,
最小公倍数 调动学生学习
数(序数==)
的积极性
化学式中起点原子个数
掌握配平的方
CH 3 OH:4/4=1 H 2 O:4/2==2 各组开展比赛, 法的多样性启
2.按照元素出现次数由少到多的顺序通 并对个别组完成 迪学生解决问
2 过观察配平其它元素 的 练 习 进 行 批 题时方法并不
由碳元素确定CO:1(因为CHOH序数 阅、改正 是唯一的,勤于
2 3
为1,其中含碳原子为1) 思考,培养归
由碳元素确定O
2
:3/2(因为生成物分子
纳、总结的能力
中氧为4个,CHOH分子中含氧1个)
3
即 : CHOH+3/2O
点燃
3 2
CO+2H O
2 2
5.化为最简比
点燃
2CH OH+3O 2CO+4H O
3 2 2 2
掌握配平的方
法的多样性启
迪学生解决问
题时方法并不
是唯一的,勤于
思考,培养归
纳、总结的能力
总体要求:1.“统一”设计“分段”教学;2.围绕“三维”落实“三问”;3.充实“心案”
活化“形案”。教 学 流 程
分 △设计意图
环 节
课 教 师 活 动 学 生 活 动 ◇资源准备
与时间
时 □评价○反思
练习巩固 配平下列化学方程式:
点燃
10分
① P+O P O
2 2 5
二氧化锰
② ②H O H O+O ↑
2 2 2 2
点燃
③ Fe+O Fe O
2 3 4
通电
复习小结 ④ H 2 O H 2 +O 2
5分
布置作业
3分
2
总体要求:1.“统一”设计“分段”教学;2.围绕“三维”落实“三问”;3.充实“心案”
活化“形案”。教 学 流 程
分 △设计意图
环 节
课 教 师 活 动 学 生 活 动 ◇资源准备
与时间
时 □评价○反思
组织教学
2分
复习提问
5分
讲授新课 例1:(2005·长沙市)下列有关化学方程 △进行学生分层
20分 式2H+O 2HO的读法正确的是( 练习锻炼学生分
2 2 2
析问题解决问题
)
的能力
A . 氢 气 和 氧 气 生 成 水
B.氢气加氧气等于水
C.两个氢分子加一个氧分子等于两个水
分子 D.氢气和氧气在点燃条件下反
应生成水
解析 化学方程式所表示的意义有:
(1)表明了化学反应中反应物和生成物;
(2)表明了该反应进行的条件;(3)表明 学生练习,学生
了各物质之间的质量关系,即各物质之 分析回答问题。
间的质量比。本题中对化学方程式的读
3
法,化学方程式中“+”表示“和”的意
思,“=”表示生成的意思,反应条件也
要读出,故选D 。
答案:D
例2:(2002·北京东城区)下列有关铁的
化学方程式中,错误的是( )
A . 3Fe+2O FeO
2 3 4
B.2Fe+6HCl=2FeCl+3H↑
3 2
C . Fe + CuS0 ==FeSO + Cu
4 4
D. FeO+3CO 2Fe+3CO
2 3 2
解析 此题为判断化学方程式书写的
正误题.根据书写化学方程式的原则和步
骤可以判断出B项中Fe与HCl反应生成
FeCl ,而不是FeCl ,违背了客观事实.
2 3
答案:B
总体要求:1.“统一”设计“分段”教学;2.围绕“三维”落实“三问”;3.充实“心案”
活化“形案”。教 学 流 程
环 节
分 △设计意图
学 生 活
课 与时 教 师 活 动 ◇资源准备
动
时 间 □评价○反思
组 织 教 例3:(2003·南京市)航天飞机用金属铝和高氯
学 酸铵(NH 4 ClO 4 )的混合物体为固体燃料。加热铝
粉使其被氧化放出大量的热,使混合物中的高
2分
氯酸铵分解,同时生成四种气体,两种是空气中
导 入 新
的主要成分,一种气体是氯气,还有一种是常见
课 △通过教师设
的氧化物,因而产生巨大的推动力。
疑,激发兴趣
5分
试写出其中涉及到的化学方程式。
和求知欲
( 1 ) 铝 粉 被 氧 气 氧 化
;
( 2 ) 高 氯 的 铵 受 热 分 解
。
△ 联系生活,
让学生产
讲 授 新 生更多的
解析 该题为高新技术信息题、题中铝被氧化
课 的反应相对简单,难点在如何理解高氯酸铵的 学生练习,学 兴趣,让其
联系生活,
30分 分解上。高氯酸铵分解产生四种气体:一种为氯 生分析回答问
从而应用
气;两种是空气中的主要成分,应为氧气和氮
题。
于生活
气;另外一种是常见的氧化物,是什么元素的氧
3
化物呢?结合质量守恒定律分析,应该是氢的
氧化物——水蒸气。确定了反应物、生成物及反
应条件、应该不难写出化学方程式。
答案:(1)4Al+3O 2AlO (2)2NHClO
2 2 3 4 4
N ↑+O↑+Cl↑+4HO↑
2 2 2 2
例4:(2005·黄冈市课改区)甲、乙、丙是三个实
验的示意图,根据图中所发生的化学反应现
象及化学反应原理,进行总结归纳并回答下
列问题1)所发生的三个反应有多个共同的特
点 , 分 别 是 ① ; ②
;
③ ; ④
……(只答四点即可)
总体要求:1.“统一”设计“分段”教学;2.围绕“三维”落实“三问”;3.充实“心案”
活化“形案”。教 学 流 程
分 △设计意图
环 节
课 教 师 活 动 学 生 活 动 ◇资源准备
与时间
时 □评价○反思
(2)甲实验进行时,燃烧匙中硫的状态
是 。
(3)任选上述三个实验中的一个,写出
反 应 的 化 学 方 程 式 :
。
△ 通 过 教 师 设
解析 题中给出了提示:“从发生的
疑,激发兴趣和
化学反应现象及化学学原理进行归纳
求知欲
总结”。三个反应的共同有:①都是物
质跟氧气反应;②都是固体跟气体反 学生练习,学生
应;③反应都需点燃才能进行;④反应 分析回答问题。
都放热;⑤反应都是化合反应;⑥生成
物都是氧化物;⑦……甲实验时,硫先
△ 联系生活,让
熔化成液体又气化燃烧,燃烧匙中我们
学生产生更
看到的是液态硫;化学方程可任选一
多的兴趣,让
个。
其联系生活,
答案:⑴①反应都是化合反应;②反应
从而应用于
的条件都是点燃;③反应都是放出热
生活
量;④生成物都是氧化物。
⑵液态 ⑶S+O 点燃SO (或4P+5O 点燃
3 2 2 2
2P O 或4Al+3O 点燃2Al O )
小结8分 2 5 2 2 3
1.在化学方程式书写中常出现的错误是
不配平、反应条件不写、化学式写错等。
为避免化学式写错,可根据化学式中化
合价代数和是否为零来判断;对于方程
式不配平和反应条件不写,避免遗漏的
方法是在平时书写化学方程式时就要养
成写完方程式后仔细观察反应前后各元
素的原子个数是否相等以及随手写反应
条件及“↑”“↓”的良好习惯,
2.配平时只能在化学式前配上适当的化
学计量数,绝不能改动化学式右下角表
示原子或原子团个数的小数字,或在化
学式中添加小数字
总体要求:1.“统一”设计“分段”教学;2.围绕“三维”落实“三问”;3.充实“心案”
活化“形案”。教 学 流 程
分 △设计意图
环 节
课 教 师 活 动 学 生 活 动 ◇资源准备
与时间
时 □评价○反思
1.化学方程式 可读作(
)
A.硫加氧等于二氧化硫 B.硫
加氧气点燃后生成二氧化硫
C.硫和氧气点燃生成二氧化硫 D.一
个硫和一个氧点燃后生成一个二氧化硫
2.在一密闭容器内有X、Y、Z、Q四种物
质,在一定条件下充分反应,反应前后各 学生练习,学生
物质的质量如下表:
分析回答问题。
物 X Y Z Q
质
反 应 2 84 5
前 质 2
量/g
反 应 待 24 0 14
△进行学生分层
后 质 测
练习锻炼学生分
量/g
4 析问题解决问题
试判断该密闭容器中发生的反应属于(
的能力
)
A.化合反应 B.置换反应 C.
分解反应 D.复分解反应
3.科学实验证明,空气中的微量臭氧
(O)可以抵抗阳光中紫外线对人体的危
3
害,空调和冰箱中的致冷剂“氟里昂”
是一种氟氯烃(以M代替),它可以破坏
臭氧层,其反应过程为:M+ O →MO+ O
3 2
MO+O→M+ O ,则 M 在该反应中是(
2
)
A.氧化剂 B.还原剂 C.催化剂
D.稳定剂
总体要求:1.“统一”设计“分段”教学;2.围绕“三维”落实“三问”;3.充实“心案”
活化“形案”。教 学 流 程
△设计意
环
图
分
节 学 生 ◇资源准
课 教 师 活 动
与时 活 动 备
时
间 □评价○
反思
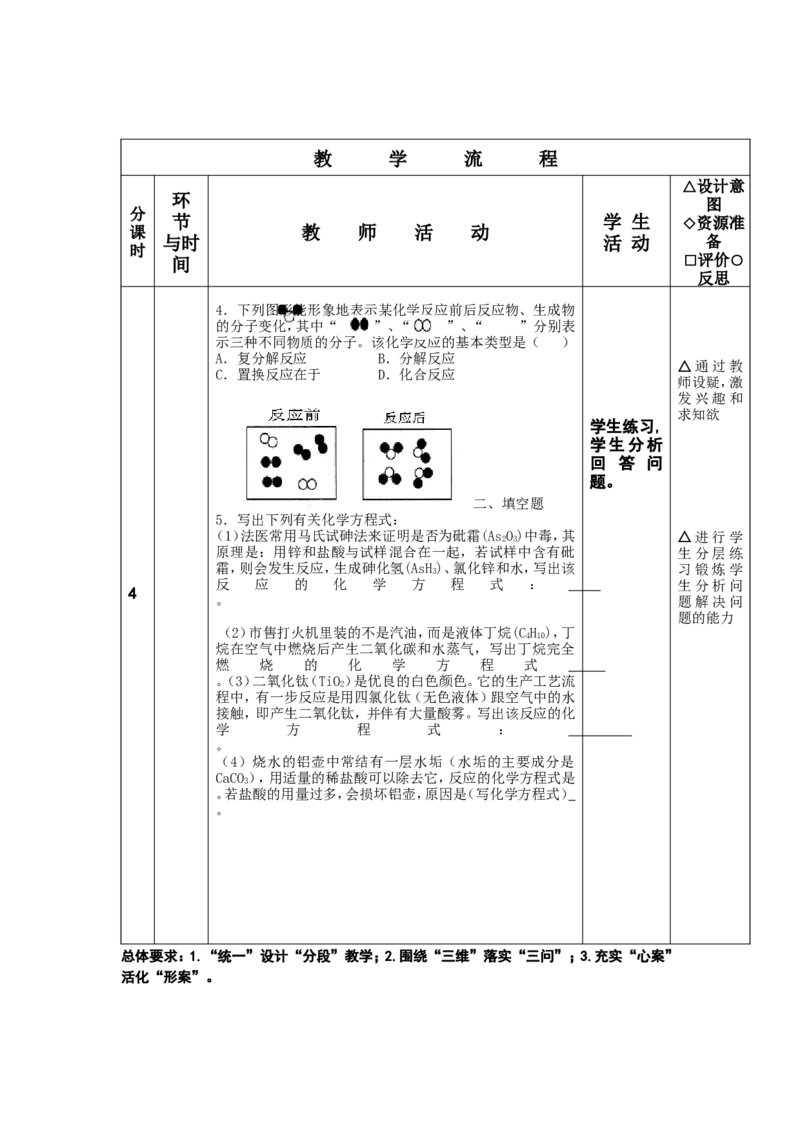
4.下列图形能形象地表示某化学反应前后反应物、生成物
的分子变化,其中“ ”、“ ”、“ ”分别表
示三种不同物质的分子。该化学反应的基本类型是( )
A.复分解反应 B.分解反应
△通过教
C.置换反应在于 D.化合反应
师设疑,激
发兴趣和
求知欲
学生练习,
学生分析
回 答 问
题。
二、填空题
5.写出下列有关化学方程式:
(1)法医常用马氏试砷法来证明是否为砒霜(AsO)中毒,其 △进行学
2 3
原理是:用锌和盐酸与试样混合在一起,若试样中含有砒 生分层练
霜,则会发生反应,生成砷化氢(AsH)、氯化锌和水,写出该 习锻炼学
3
反 应 的 化 学 方 程 式 : 生分析问
4
。 题解决问
题的能力
(2)市售打火机里装的不是汽油,而是液体丁烷(CH ),丁
4 10
烷在空气中燃烧后产生二氧化碳和水蒸气,写出丁烷完全
燃 烧 的 化 学 方 程 式
。(3)二氧化钛(TiO)是优良的白色颜色。它的生产工艺流
2
程中,有一步反应是用四氯化钛(无色液体)跟空气中的水
接触,即产生二氧化钛,并伴有大量酸雾。写出该反应的化
学 方 程 式 :
。
(4)烧水的铝壶中常结有一层水垢(水垢的主要成分是
CaCO),用适量的稀盐酸可以除去它,反应的化学方程式是
3
。若盐酸的用量过多,会损坏铝壶,原因是(写化学方程式)
。
总体要求:1.“统一”设计“分段”教学;2.围绕“三维”落实“三问”;3.充实“心案”
活化“形案”。教 学 流 程
分 △设计意图
环 节
课 教 师 活 动 学 生 活 动 ◇资源准备
与时间
时 □评价○反思
6.通过学习,我们已经知道了下列反应:
①C+O CO ②2CO+O 2CO
2 2 2 2
③ CH+2O CO+2HO
4 2 2 2 △进行学生分层
④CH OH+3O 2CO+3HO 练习锻炼学生分
2 -5 2 2 2
通过对上述四个反应的化学方程式的分 析问题解决问题
析,你能总结出哪些规律性的结论? 的能力
学生练习,学生
7.在化学反应中,物质所含元素的化合
分析回答问题。
价发生变化的反应就是氧化-还原反
应。
0 0 +1—1
例如:2Na +Cl=2NaCl 反应前后,Na、Cl
2
元素的化合价发生了变化,该反应是氧
化-还原反应。(1)根据化合价是否变化
分析,下列反应属于氧化-还原反应的
是(填序号): 。
A.2Mg + O 点燃 2MgO B.CaO + HO
2 2
5
= Ca(OH) C.2KClO
催化剂
2 K Cl+3O
2 3 2
△
↑
D.CaCO 高温 CaO + CO ↑ E.H +
3 2 2
CuO 加热 Cu + HO F.HCl + NaOH =
2
NaCl +HO
2
(2)根据上面的分析和推理,对四种基本
反应类型是否属于氧化还原反应,做出
恰当概括:
置换反应 ;
化合反应 ;
分解反应 ;
复 分 解 反 应
;
总体要求:1.“统一”设计“分段”教学;2.围绕“三维”落实“三问”;3.充实“心案”
活化“形案”教 学 流 程
环
△设计图
分
节 学 生 活 ◇资源备
课 教 师 活 动
与时 动 □评价○
时
间 反思
8.把铁粉和硫粉以适当的质量比均匀混合,堆放在石棉
网,然后用烧红的玻璃棒的一端接触混合物。这时部分混
合物迅速变成红热状态,移开玻璃棒后,反应继续剧烈进
行,全部混合物呈红热状态,冷却后得到黑色的固体化合
物——硫化亚铁。
① 这 一 变 化 的 化 学 方 程 式 是
。
②铁跟硫 反应时是 吸收 热量还是放出热量?
。 学生练习,
③用什么实验可以证实反应中铁已从游离态变成化合态 学 生 分 析
。 回答问题。
④从理论上计算,为使铁粉和硫粉都能全部反应,两者最
△进行学
佳质量比应是 。
生分层练
9.经过学习我们可以初步认识到:化学反应的快慢、现象、
习锻炼学
生成物等与反应物量的多少、反应条件有着密切的关系。
生分析问
请各举一例说明:
题解决问
(1)使用催化剂,能改变化学反应的速率:
题的能力
。
( 2 ) 反 应 物 的 量 不 同 , 生 成 物 可 能 不 同 :
5
。
小结 8
(3)反应物的量不同,反应现象可能不同:
分 。
10.用好化学用语和溶解性表,对日后化学的学习是非常
有帮助的。请按要求写出以下反应的化学方程式(所选的
反应物在右表的范围内,
并且不能重复选用):
1)一种酸和一种碱 ;
2)一种酸和一种盐 ;
3)一种碱和一种盐 ;
4)一种盐和另一种盐 。
OH- NO - Cl- SO 2- CO 2-
3 4 3
H+ — 溶、挥 溶、挥 溶 溶、挥
Na+ 溶 溶 溶 溶 溶
Ca2+ 微 溶 溶 微 不
Ba2+ 溶 溶 溶 不 不
Cu2+ 不 溶 溶 溶 不
总体要求:1.“统一”设计“分段”教学;2.围绕“三维”落实“三问”;3.充实“心案”
活化“形案”