文档内容
检测·知能升级
一、选择题(本题包括8小题)
1.有关物质的分类中,说法错误的是( )
A.KNO 属于硝酸盐 B.CaO属于氧化物
3
C.NaHCO 属于酸 D.NaCO 属于钠盐
3 2 3
2.植物在缺氮的情况下,叶色发黄、生长迟缓。这时需施用的化肥是( )
A.KCl B.NHHCO C.KCO D.Ca(HPO)
4 3 2 3 2 4 2
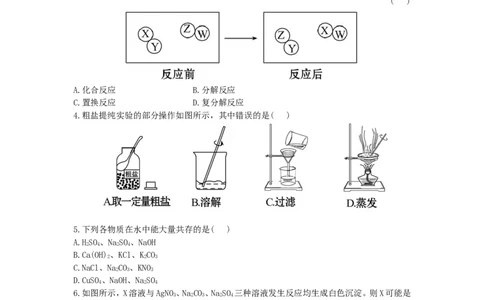
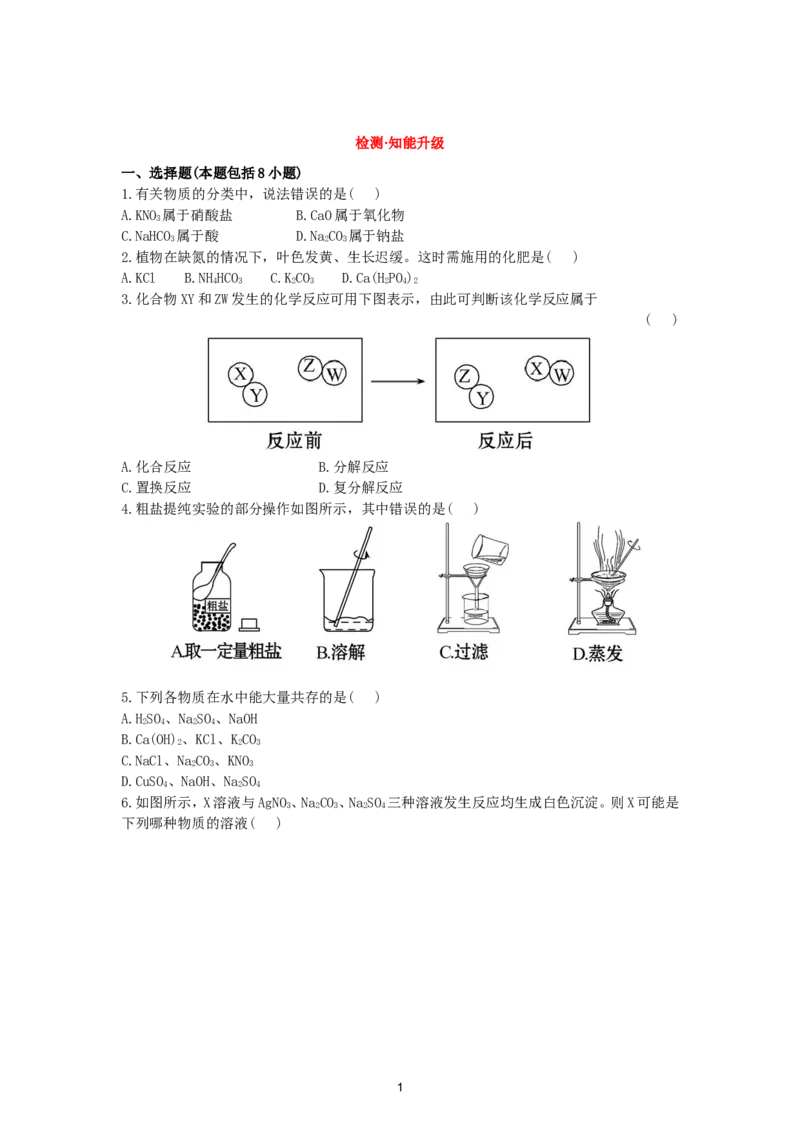
3.化合物XY和ZW发生的化学反应可用下图表示,由此可判断该化学反应属于
( )
A.化合反应 B.分解反应
C.置换反应 D.复分解反应
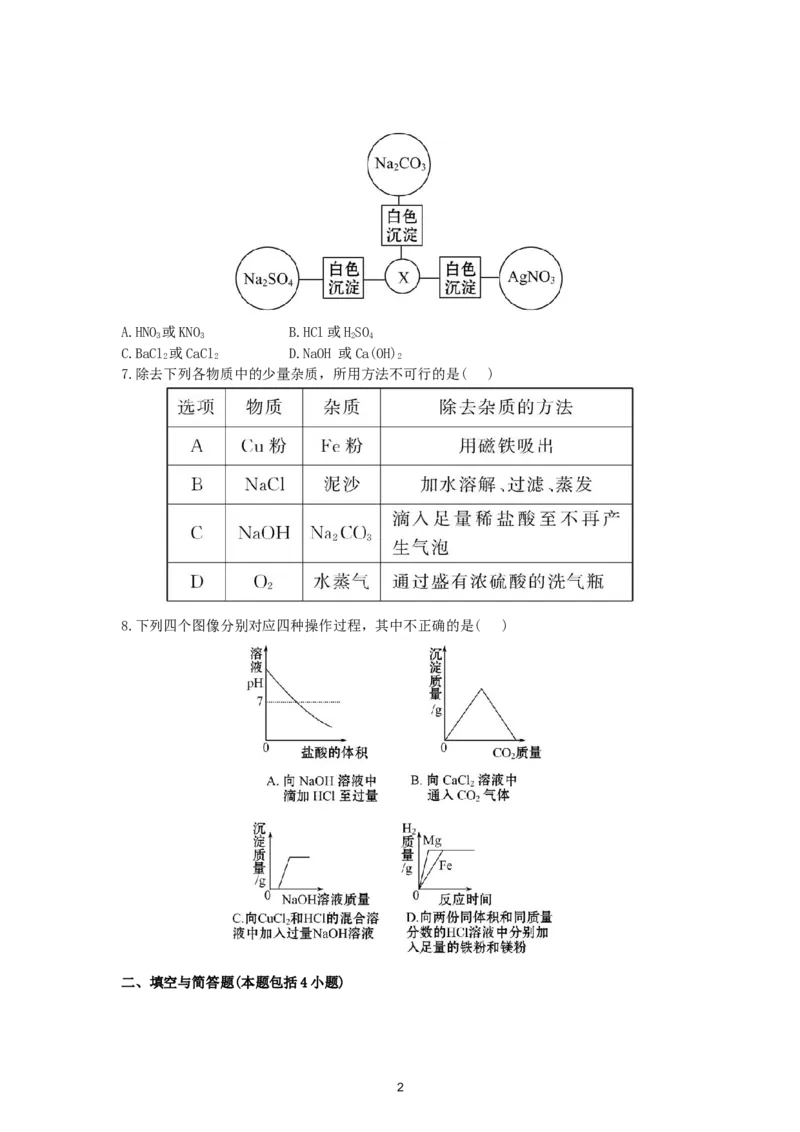
4.粗盐提纯实验的部分操作如图所示,其中错误的是( )
5.下列各物质在水中能大量共存的是( )
A.HSO、NaSO、NaOH
2 4 2 4
B.Ca(OH)、KCl、KCO
2 2 3
C.NaCl、NaCO、KNO
2 3 3
D.CuSO、NaOH、NaSO
4 2 4
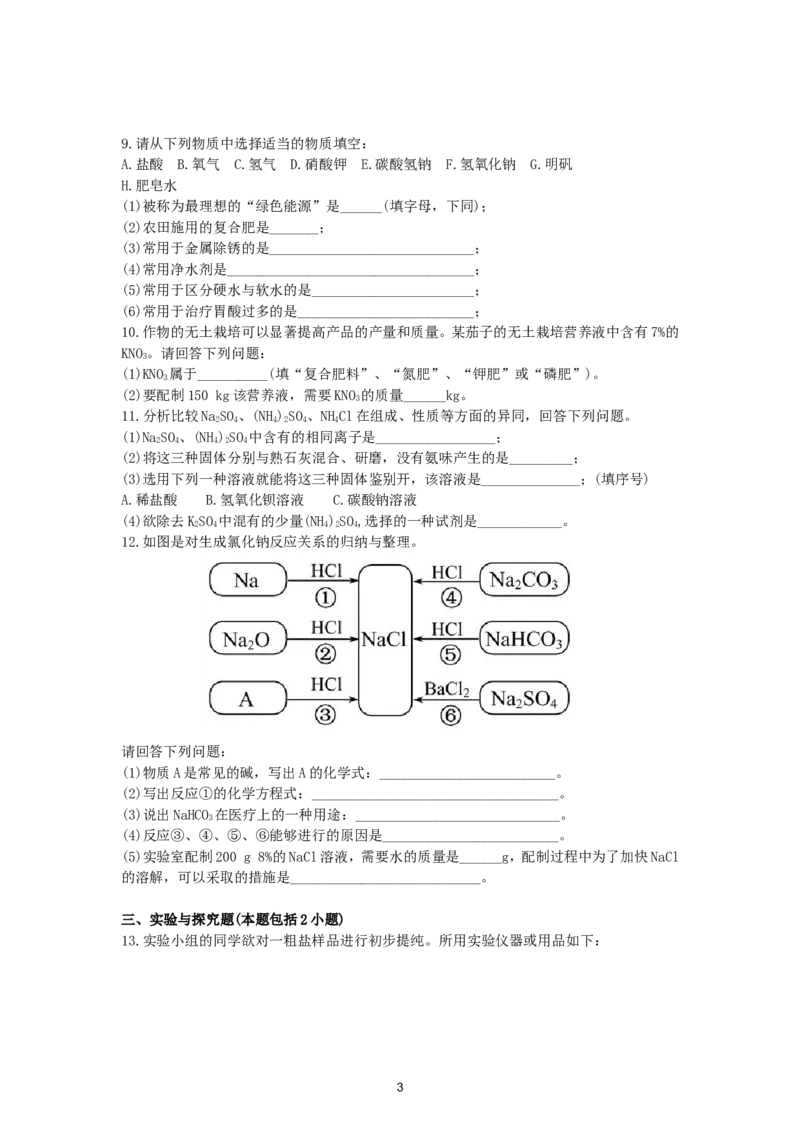
6.如图所示,X溶液与AgNO、NaCO、NaSO 三种溶液发生反应均生成白色沉淀。则X可能是
3 2 3 2 4
下列哪种物质的溶液( )
1A.HNO 或KNO B.HCl或HSO
3 3 2 4
C.BaCl 或CaCl D.NaOH 或Ca(OH)
2 2 2
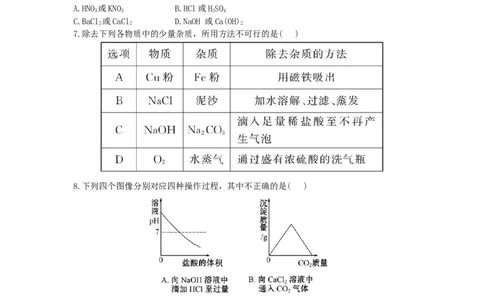
7.除去下列各物质中的少量杂质,所用方法不可行的是( )
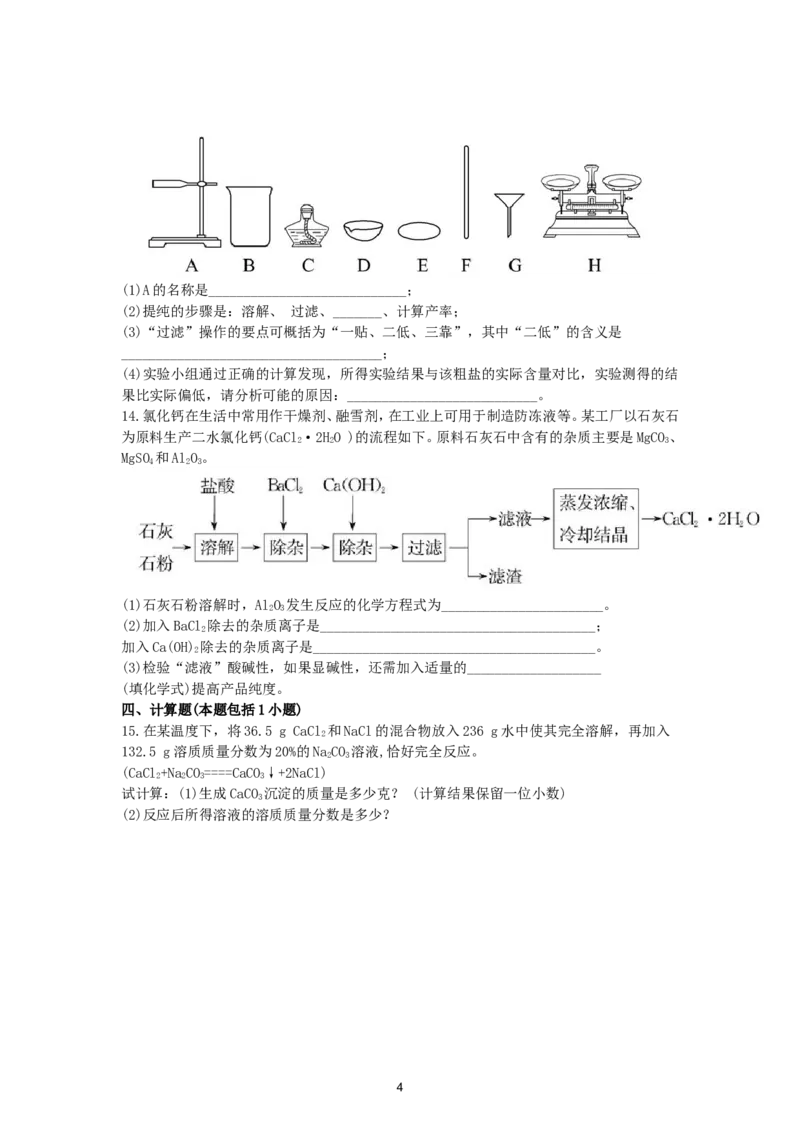
8.下列四个图像分别对应四种操作过程,其中不正确的是( )
二、填空与简答题(本题包括4小题)
29.请从下列物质中选择适当的物质填空:
A.盐酸 B.氧气 C.氢气 D.硝酸钾 E.碳酸氢钠 F.氢氧化钠 G.明矾
H.肥皂水
(1)被称为最理想的“绿色能源”是______(填字母,下同);
(2)农田施用的复合肥是_______;
(3)常用于金属除锈的是_____________________________;
(4)常用净水剂是___________________________________;
(5)常用于区分硬水与软水的是_______________________;
(6)常用于治疗胃酸过多的是_________________________;
10.作物的无土栽培可以显著提高产品的产量和质量。某茄子的无土栽培营养液中含有7%的
KNO。请回答下列问题:
3
(1)KNO 属于__________(填“复合肥料”、“氮肥”、“钾肥”或“磷肥”)。
3
(2)要配制150 kg该营养液,需要KNO 的质量______kg。
3
11.分析比较NaSO、(NH)SO、NHCl在组成、性质等方面的异同,回答下列问题。
2 4 4 2 4 4
(1)NaSO、(NH)SO 中含有的相同离子是_________________;
2 4 4 2 4
(2)将这三种固体分别与熟石灰混合、研磨,没有氨味产生的是_________;
(3)选用下列一种溶液就能将这三种固体鉴别开,该溶液是______________;(填序号)
A.稀盐酸 B.氢氧化钡溶液 C.碳酸钠溶液
(4)欲除去KSO 中混有的少量(NH)SO,选择的一种试剂是____________。
2 4 4 2 4
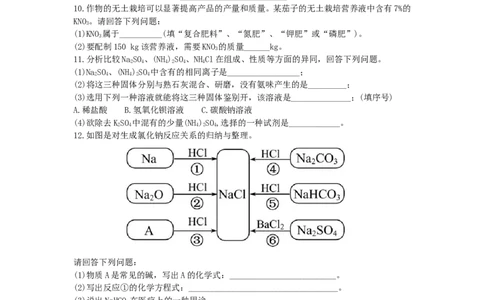
12.如图是对生成氯化钠反应关系的归纳与整理。
请回答下列问题:
(1)物质A是常见的碱,写出A的化学式:_________________________。
(2)写出反应①的化学方程式:___________________________________。
(3)说出NaHCO 在医疗上的一种用途:_____________________________。
3
(4)反应③、④、⑤、⑥能够进行的原因是_________________________。
(5)实验室配制200 g 8%的NaCl溶液,需要水的质量是______g,配制过程中为了加快NaCl
的溶解,可以采取的措施是___________________________。
三、实验与探究题(本题包括2小题)
13.实验小组的同学欲对一粗盐样品进行初步提纯。所用实验仪器或用品如下:
3(1)A的名称是____________________________;
(2)提纯的步骤是:溶解、 过滤、_______、计算产率;
(3)“过滤”操作的要点可概括为“一贴、二低、三靠”,其中“二低”的含义是
_____________________________________;
(4)实验小组通过正确的计算发现,所得实验结果与该粗盐的实际含量对比,实验测得的结
果比实际偏低,请分析可能的原因:___________________________。
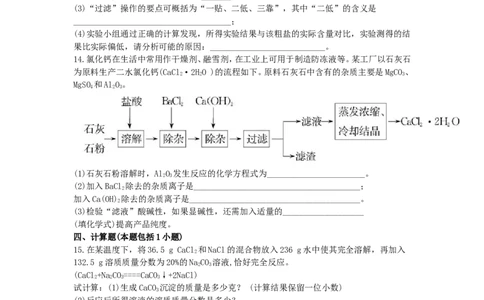
14.氯化钙在生活中常用作干燥剂、融雪剂,在工业上可用于制造防冻液等。某工厂以石灰石
为原料生产二水氯化钙(CaCl·2HO )的流程如下。原料石灰石中含有的杂质主要是MgCO、
2 2 3
MgSO 和AlO。
4 2 3
(1)石灰石粉溶解时,AlO 发生反应的化学方程式为_______________________。
2 3
(2)加入BaCl 除去的杂质离子是_______________________________________;
2
加入Ca(OH) 除去的杂质离子是________________________________________。
2
(3)检验“滤液”酸碱性,如果显碱性,还需加入适量的___________________
(填化学式)提高产品纯度。
四、计算题(本题包括1小题)
15.在某温度下,将36.5 g CaCl 和NaCl的混合物放入236 g水中使其完全溶解,再加入
2
132.5 g溶质质量分数为20%的NaCO 溶液,恰好完全反应。
2 3
(CaCl+NaCO====CaCO↓+2NaCl)
2 2 3 3
试计算:(1)生成CaCO 沉淀的质量是多少克? (计算结果保留一位小数)
3
(2)反应后所得溶液的溶质质量分数是多少?
4答案解析
1.【解析】选C。酸是指电离时生成的阳离子全部是氢离子的化合物,从碳酸氢钠的化学式可
知,该物质中电离出的阳离子除氢离子外还有钠离子,故不属于酸。
2.【解析】选B。从题中信息知,植物需要施用的是氮肥,分析题给的四种物质可知,只有B项
碳酸氢铵中含有氮元素,属于氮肥,故选B。
3.【解析】选D。由该反应的示意图可看出,该反应的两种化合物经交换成分生成两种新的化
合物,故该反应属于复分解反应。
4.【解析】选C。过滤操作为避免液体溅出,应用玻璃棒引流,漏斗下端管口应与烧杯内壁接
触。
5.【解析】选C。离子的共存问题是中考化学的基础性考题,解题的关键在于明确离子间不能
共存的条件:两种离子相互作用如果有水、气体或沉淀等物质生成,则这两种离子不能共存
于同一溶液中。选项A中会发生酸碱中和反应;选项B中有碳酸钙沉淀生成;选项D中有氢氧
化铜沉淀生成;选项C中三种物质两两不反应,能共存于水中。
6.【解析】选C。本题是根据反应现象考查盐的性质。BaCl 或CaCl 与NaCO 反应可生成碳酸
2 2 2 3
钡或碳酸钙白色沉淀,与AgNO 反应可生成氯化银白色沉淀,与NaSO 反应可生成硫酸钡或
3 2 4
CaSO 白色沉淀。
4
7.【解析】选C。Cu粉不能被磁铁吸引,而Fe粉能被磁铁吸引,据此可用磁铁除去Cu粉中的
Fe粉;NaCl溶于水,而泥沙不溶于水,经加水溶解、过滤、蒸发除去氯化钠中的泥沙;NaOH和
NaCO 都能与盐酸反应,滴入足量稀盐酸会造成NaOH变质;浓硫酸具有吸水性,且不能与O
2 3 2
反应,故可除去O 中的水蒸气。
2
8.【解析】选B。向NaOH溶液中滴加HCl至过量,溶液由碱性溶液逐渐变为酸性溶液,溶液的
pH由大于7逐渐到小于7,图像A正确;CaCl 溶液中通入CO 气体,不会发生反应,假设能反
2 2
应,反应的方程式为CaCl+HO+CO====
2 2 2
CaCO↓+2HCl,成了弱酸(HCO)制取强酸(HCl),这样就违背了“强酸制取弱酸”的规律,
3 2 3
故图像B错误;向CuCl 和HCl的混合溶液中加入过量的NaOH 溶液,NaOH先和HCl发生中和
2
反应,然后NaOH与CuCl 反应生成Cu(OH) 沉淀,CuCl 反应完后,沉淀的质量不再发生变化,
2 2 2
图像C正确;镁比铁活泼,镁与盐酸的反应速率快,先结束反应。镁和铁均过量,与同体积、同
质量分数的盐酸反应产生的氢气的质量一样多。故图像D正确。
9.【解析】本题考查的是对常见物质用途的认识,解答的关键是熟悉各物质的主要用途及其
特点。如最理想的绿色能源为氢气;复合肥的特点是组成中含有两种及两种以上营养元素,
硝酸钾中因含有钾元素和氮元素,因而属于复合肥;明矾因能将细小物质吸附使之聚集为较
大颗粒而沉降从而起到净水作用,故常用作絮凝剂用以净水;区分硬水和软水时,常利用软
水能使肥皂水产生大量泡沫,而硬水不能的性质,用肥皂水区分硬水和软水;要减少胃液中
的多余胃酸,需加入能与盐酸发生反应的碱性物质,但又不能有腐蚀性,因而应选用碳酸氢
钠,不能选用氢氧化钠。
答案:(1)C (2)D (3)A (4)G (5)H (6)E
10.【解析】(1)KNO 中含有K、N两种营养元素,属于复合肥料;(2)配制150 kg该营养液需要
3
KNO 的质量为:150 kg×7%=10.5 kg。
3
答案:(1)复合肥料 (2)10.5
11.【解析】(1)由两物质的化学式可知,其中所含的阴离子相同,即都含有相同的硫酸根离子;
5(2)只有含有铵根离子的化合物能与碱性物质反应生成氨气,题给三种物质中,硫酸铵和氯
化铵中均含有铵根离子,故只有硫酸钠与熟石灰混合时不会有氨味产生;(3)要选用一种物
质区分三种物质,所选物质与三种物质反应时需产生三种不同的现象,因硫酸钠和硫酸铵中
都含有硫酸根离子,故两者与氢氧化钡溶液反应时都会有沉淀生成,而硫酸铵和氯化铵中都
有铵根离子,故两者与氢氧化钡溶液反应时都会有氨味的气体产生,因而可以用氢氧化钡溶
液区分三种固体;(4)要除去硫酸钾中的硫酸铵,即除去其中的铵根离子,可以选用碱溶液,
为避免引入新杂质,应选用氢氧化钾。
答案:(1)SO2- (2)NaSO (3)B (4)KOH
4 2 4
12.【解析】(1)A是碱并且能与HCl反应生成NaCl,可知A一定是NaOH;
(2)活泼金属与酸反应生成盐与氢气;(3)NaHCO 在医疗上是治疗胃酸过多的一种药剂;
3
(4)③、④、⑤、⑥发生的都是复分解反应,能够发生是因为符合复分解反应发生的条件,有水、
气体或沉淀之一生成;(5)根据溶质质量分数的计算式,需要氯化钠的质量是:200 g×8%=16
g,水的质量是:200 g-16 g=184 g,为了加快溶质的溶解速率,可用玻璃棒不断搅拌。
答案:(1)NaOH (2)2Na+2HCl====2NaCl+H↑
2
(3)治疗胃酸过多的一种药剂 (4)有水、气体或沉淀生成
(5)184 用玻璃棒不断搅拌
13.【解析】实验结果比实际结果偏低可能的原因很多:如称量错误、过滤时滤液溅出、蒸发时
沸液溅出等。
答案:(1)铁架台 (2)蒸发 (3)滤纸边缘低于漏斗边缘,母液液面低于滤纸边缘
(4)蒸发时液滴飞溅(称量时操作或读数错误等)
14.【解析】石灰石粉加盐酸溶解时,其中的AlO 与盐酸反应生成氯化铝和水,钡离子与硫酸
2 3
根离子生成硫酸钡沉淀,则溶液中加入BaCl 除去的杂质离子是硫酸根离子。氢氧根离子与
2
铝离子、镁离子反应分别生成氢氧化铝沉淀、氢氧化镁沉淀,则溶液中加入Ca(OH) 除去的杂
2
质离子是镁离子或铝离子。中和滤液的碱,需加入酸,为不引入新的杂质,需要加入盐酸进行
中和。
答案:(1)AlO+6HCl====2AlCl+3HO
2 3 3 2
(2)硫酸根离子(或SO2-) 镁离子(或Mg2+)和铝离子(或Al3+)
4
(3)HCl
15.【解析】设生成CaCO 沉淀的质量是x。
3
NaCO+CaCl====CaCO↓+2NaCl
2 3 2 3
106 100
132.5 g×20% x
132.5 g20% x
106 100
x=25.0 g
根据质量守恒定律,反应后溶液质量为:36.5 g+236 g+132.5 g-25 g=380 g,
反应后溶液中溶质质量为:380 g-[236 g+132.5 g×(1-20%)]=38 g,
反应后溶液中溶质质量分数为: 38 g
100%10%。
380 g
答案:(1)25.0 g (2)10%
6