文档内容
检测·知能升级
一、选择题(本题包括8小题)
1.实验室中下列物质不需要密封保存的是( )
2.物质的分类非常重要。下列按酸、碱、盐的顺序排列的一组是( )
A.HSO、NaCO、NaCl
2 4 2 3
B.Ca(OH)、HCl、NaSO
2 2 4
C.NaOH、HCO、NaCl
2 3
D.HSO、NaOH、NaCO
2 4 2 3
3.下列说法正确的是( )
A.盐酸能使紫色石蕊试液变蓝
B.浓硫酸露置于空气中,溶质的质量分数变大
C.长期露置于空气中的固体氢氧化钠,其成分不会发生变化
D.打开盛浓盐酸的试剂瓶,瓶口会产生白雾
4.在做酸和碱中和反应的实验时,有时需要借助指示剂颜色的变化判断反应是否发生、完成。
向含有酚酞的NaOH溶液的烧杯中,不断滴入稀盐酸。此过程烧杯中溶液颜色的变化是( )
A.由红色变成蓝色 B.由蓝色变成红色
C.由红色变成无色 D.由无色变成红色
5.物质X可发生下列所示的两个反应,则X可能是( )
①X+碱→盐+HO ②X+金属氧化物→盐+HO
2 2
A.CaO B.CO C.NaOH D.HSO
2 2 4
6.可以一次性鉴别出蒸馏水、稀盐酸、石灰水的试剂是( )
A.酚酞试液 B.碳酸钠溶液
C.稀硫酸 D.氯化钠溶液
17.下列各组物质,能在pH=1的溶液中大量共存,且形成无色溶液的是( )
A.NaNO HCl NaSO
3 2 4
B.NaNO NaCl CuSO
3 4
C.NaCl NaSO NaCO
2 4 2 3
D.NaOH BaCl NaSO
2 2 4
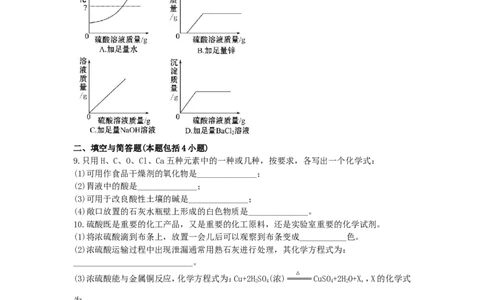
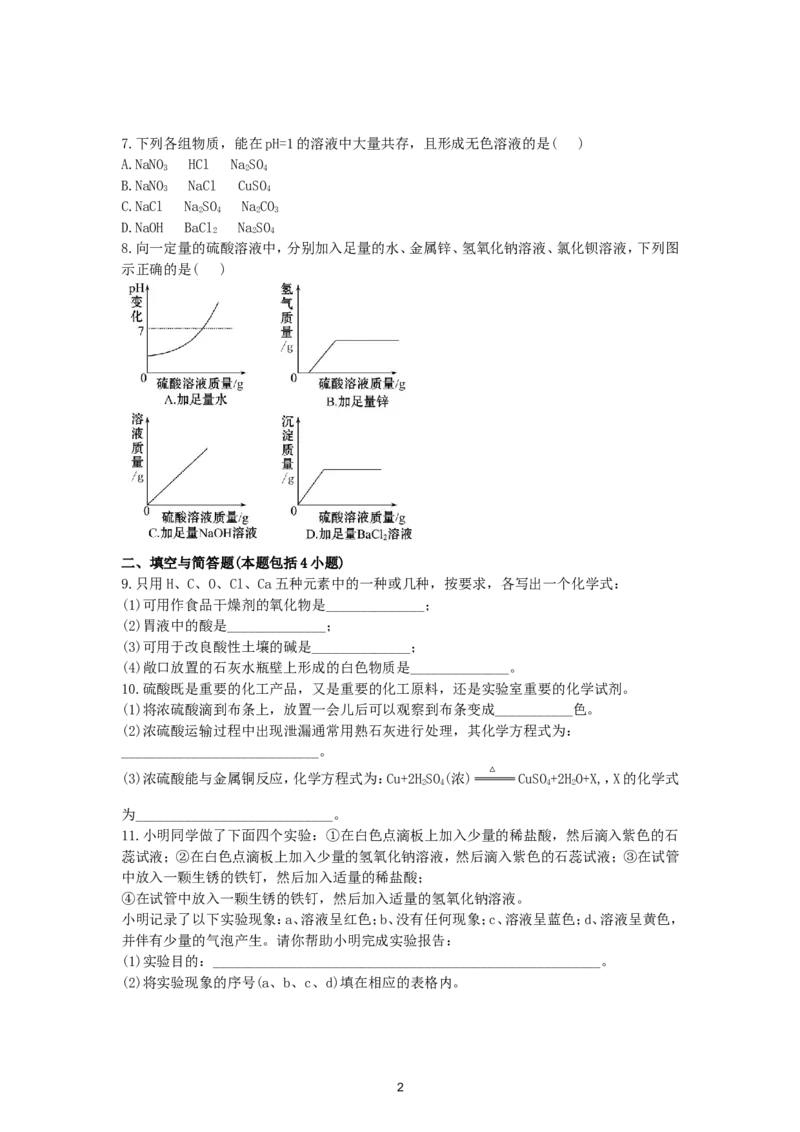
8.向一定量的硫酸溶液中,分别加入足量的水、金属锌、氢氧化钠溶液、氯化钡溶液,下列图
示正确的是( )
二、填空与简答题(本题包括4小题)
9.只用H、C、O、Cl、Ca五种元素中的一种或几种,按要求,各写出一个化学式:
(1)可用作食品干燥剂的氧化物是______________;
(2)胃液中的酸是______________;
(3)可用于改良酸性土壤的碱是______________;
(4)敞口放置的石灰水瓶壁上形成的白色物质是______________。
10.硫酸既是重要的化工产品,又是重要的化工原料,还是实验室重要的化学试剂。
(1)将浓硫酸滴到布条上,放置一会儿后可以观察到布条变成___________色。
(2)浓硫酸运输过程中出现泄漏通常用熟石灰进行处理,其化学方程式为:
____________________________。
△
(3)浓硫酸能与金属铜反应,化学方程式为:Cu+2HSO(浓) CuSO+2HO+X,,X的化学式
2 4 4 2
为____________________________。
11.小明同学做了下面四个实验:①在白色点滴板上加入少量的稀盐酸,然后滴入紫色的石
蕊试液;②在白色点滴板上加入少量的氢氧化钠溶液,然后滴入紫色的石蕊试液;③在试管
中放入一颗生锈的铁钉,然后加入适量的稀盐酸;
④在试管中放入一颗生锈的铁钉,然后加入适量的氢氧化钠溶液。
小明记录了以下实验现象:a、溶液呈红色;b、没有任何现象;c、溶液呈蓝色;d、溶液呈黄色,
并伴有少量的气泡产生。请你帮助小明完成实验报告:
(1)实验目的:_______________________________________________________。
(2)将实验现象的序号(a、b、c、d)填在相应的表格内。
2(3)请写出有气体生成的反应的化学方程式_________________________,该反应属于
___________反应。假如小明将稀盐酸换成稀硫酸进行同样的实验,会产生类似的现象,原因
是_______________________________________________。
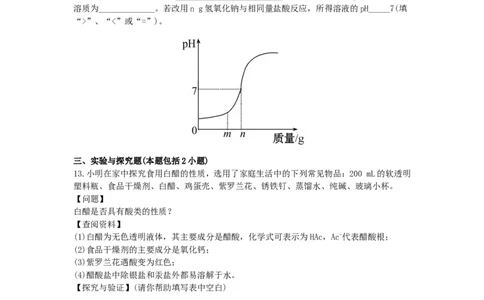
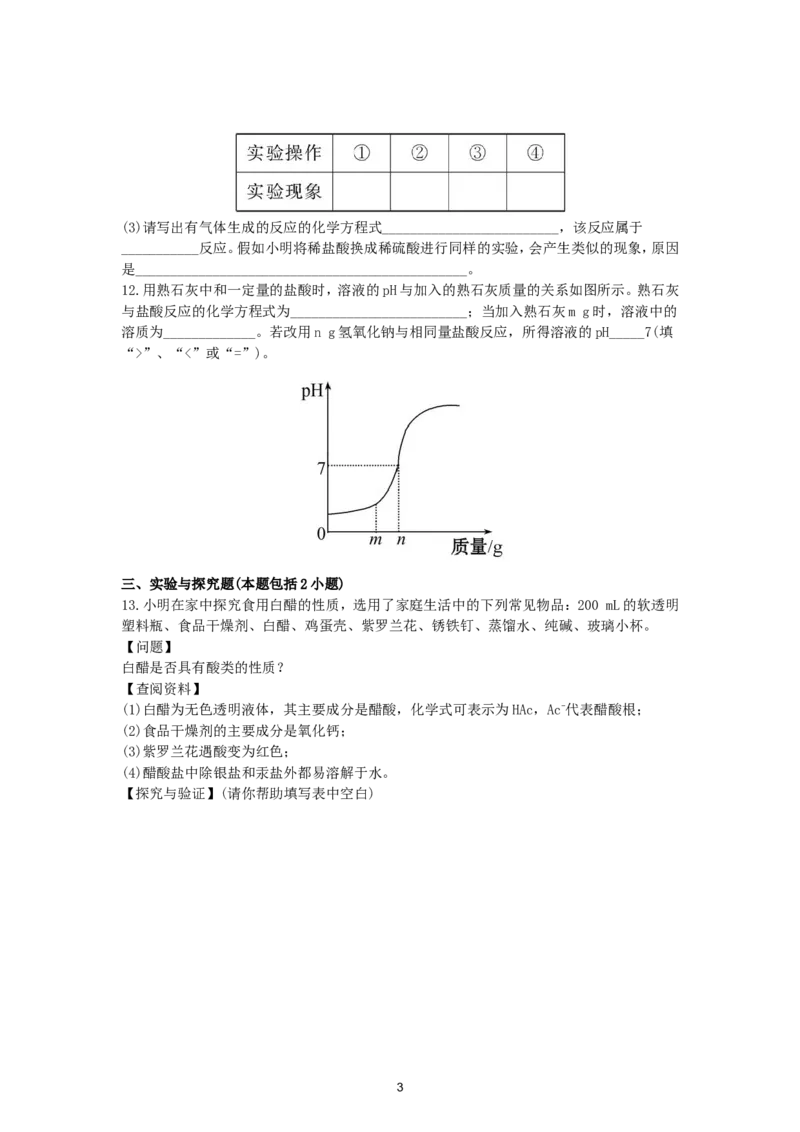
12.用熟石灰中和一定量的盐酸时,溶液的pH与加入的熟石灰质量的关系如图所示。熟石灰
与盐酸反应的化学方程式为_________________________;当加入熟石灰m g时,溶液中的
溶质为_____________。若改用n g氢氧化钠与相同量盐酸反应,所得溶液的pH_____7(填
“>”、“<”或“=”)。
三、实验与探究题(本题包括2小题)
13.小明在家中探究食用白醋的性质,选用了家庭生活中的下列常见物品:200 mL的软透明
塑料瓶、食品干燥剂、白醋、鸡蛋壳、紫罗兰花、锈铁钉、蒸馏水、纯碱、玻璃小杯。
【问题】
白醋是否具有酸类的性质?
【查阅资料】
(1)白醋为无色透明液体,其主要成分是醋酸,化学式可表示为HAc,Ac-代表醋酸根;
(2)食品干燥剂的主要成分是氧化钙;
(3)紫罗兰花遇酸变为红色;
(4)醋酸盐中除银盐和汞盐外都易溶解于水。
【探究与验证】(请你帮助填写表中空白)
3【反思与评价】(1)小明将干燥剂袋口打开一段时间后,袋中的白色颗粒粘在了一起,请写出
变化的化学方程式________________________。
(2)上面“实验结论”中,错误的是(填实验序号)___________。
(3)上述实验三的现象还不足以得出表中所述的相应结论,为此还需要补充相应的实验,写
出该实验发生反应的化学方程式________________________。
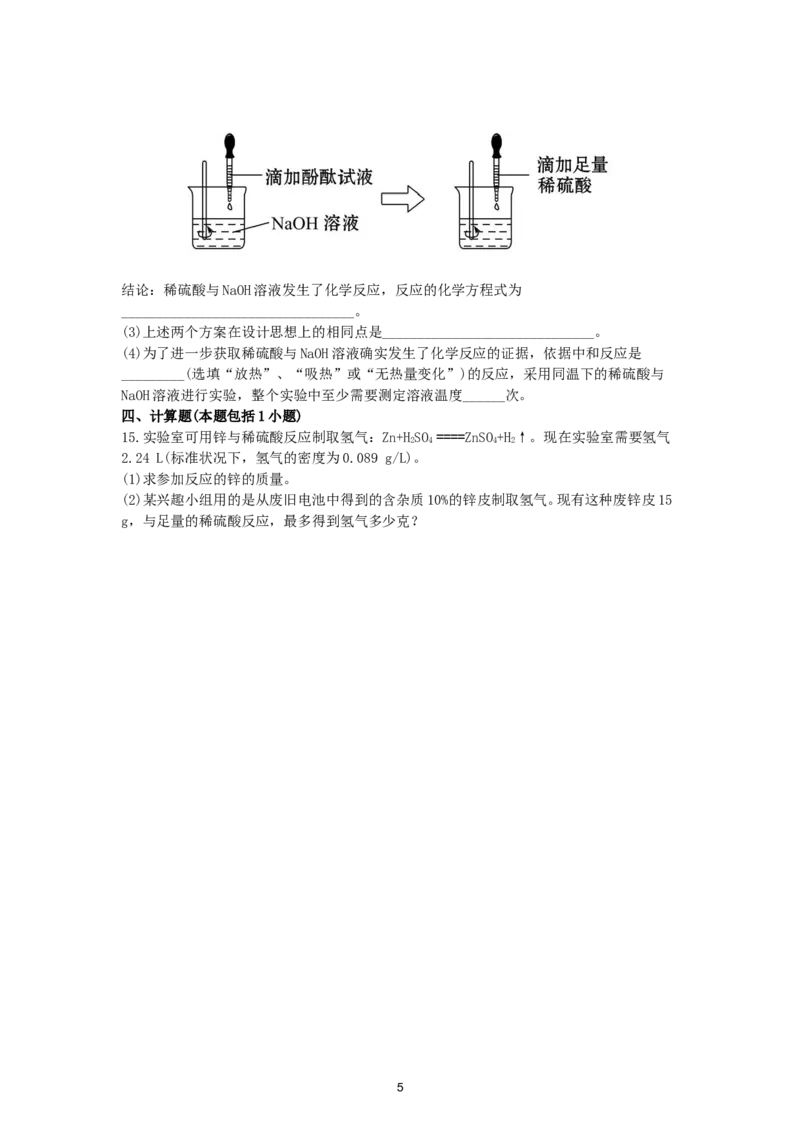
14.在研究酸和碱的化学性质时,某小组同学想证明:稀硫酸与NaOH溶液混合后,虽然仍为
无色溶液,但确实发生了化学反应。请与他们一起完成实验方案的设计、实施和评价。
(1)方案一:测定稀硫酸与NaOH溶液混合前后的pH(20 ℃)。测定某NaOH溶液的pH,
pH_______7(选填“大于”、“等于”或“小于”)。将一定量的稀硫酸加入该NaOH溶液中,
混合均匀后测定其pH,pH 小于7。
结论:稀硫酸与NaOH溶液发生了化学反应,并且________过量。
(2)方案二:观察________________________________________。(根据图示实验步骤,概括
方案要点)
4结论:稀硫酸与NaOH溶液发生了化学反应,反应的化学方程式为
_________________________________。
(3)上述两个方案在设计思想上的相同点是______________________________。
(4)为了进一步获取稀硫酸与NaOH溶液确实发生了化学反应的证据,依据中和反应是
_________(选填“放热”、“吸热”或“无热量变化”)的反应,采用同温下的稀硫酸与
NaOH溶液进行实验,整个实验中至少需要测定溶液温度______次。
四、计算题(本题包括1小题)
15.实验室可用锌与稀硫酸反应制取氢气:Zn+HSO ====ZnSO+H↑。现在实验室需要氢气
2 4 4 2
2.24 L(标准状况下,氢气的密度为0.089 g/L)。
(1)求参加反应的锌的质量。
(2)某兴趣小组用的是从废旧电池中得到的含杂质10%的锌皮制取氢气。现有这种废锌皮15
g,与足量的稀硫酸反应,最多得到氢气多少克?
5答案解析
1.【解析】选A。不需要密封保存的物质应既不与空气中的物质反应,本身也不具有挥发性或
吸水性等。生石灰易吸收水分变成熟石灰而变质;氢氧化钠既吸水也与二氧化碳反应而变质;
浓盐酸具有挥发性,只有石灰石长期露置在空气中不会发生变化。
2.【解析】选D。A项中HSO、NaCO、NaCl分别属于酸、盐、盐;B项中Ca(OH)、HCl、NaSO 分
2 4 2 3 2 2 4
别属于碱、酸、盐;C项中NaOH、HCO、NaCl分别属于碱、酸、盐,上述三项都不符合题意,可以
2 3
排除。只有D项HSO、NaOH、NaCO 是按酸、碱、盐的顺序排列的。
2 4 2 3
3.【解析】选D。盐酸能使紫色石蕊试液变红,A错;浓硫酸露置于空气中会吸收空气中的水分,
溶质的质量分数变小,B错;氢氧化钠固体可吸收空气中的二氧化碳变成碳酸钠,C错。
4.【解析】选C。含有酚酞的氢氧化钠溶液显红色,故B、D不对,再滴加盐酸,发生中和反应,
恰好反应时,溶液呈中性,在中性溶液中酚酞为无色,故在整个变化中,酚酞由红色刚好变成
无色。
5.【解析】选D。因物质X能与碱反应生成盐和水,也能与金属氧化物反应生成盐和水,说明X
具备酸的性质,故选D。
6.【解析】选 B。要通过一种试剂将三种溶液一次性鉴别,所加试剂与三种物质混合后需产生
三种不同的现象,虽蒸馏水为中性、盐酸呈酸性、石灰水呈碱性,但因酚酞试液在中性和酸性
溶液中均为无色,故不能用酚酞试液鉴别;而蒸馏水与碳酸钠混合后无明显现象,与稀盐酸
反应生成CO 气体,因而有气泡产生,与石灰水反应生成碳酸钙沉淀,出现了三个不同的现象,
2
故可以用碳酸钠溶液区分。
7.【解析】选A。CuSO 溶液呈蓝色,选项B不符合题意;C中在pH=1(酸性,含大量H+)的溶液中,
4
CO2-能和H+结合,生成二氧化碳气体和水,故选项C不符合题意;D中NaOH中的OH-能与H+结
3
合生成水且BaCl 与NaSO 反应生成BaSO 沉淀,故D选项不符合题意。
2 2 4 4
8.【解析】选D。随着水的加入,硫酸酸性逐渐减弱,溶液的pH逐渐增大,接近于7但不会超过
7,A错误;硫酸中加入锌时会立即有气泡放出,B错误;因为原来就有一定质量的稀硫酸,因
而刚开始溶液的质量不能为0,C错误;生成沉淀的质量随着氯化钡的滴加逐渐增多,当反应
结束后不再增加,D正确。
9.【解析】本题采用给定元素符号的方式,考查对物质用途的理解。解题时应注意:①只能从
给出的元素中选择来组成物质,②熟悉相关物质的用途。
答案:(1)CaO (2)HCl (3)Ca(OH) (4)CaCO
2 3
10.【解析】(1)浓硫酸具有脱水性,能使布条脱水碳化而变为黑色。(2)浓硫酸与熟石灰发生
如下中和反应:HSO+Ca(OH) ====CaSO+2HO。(3)根据质量守恒定律可知,反应前后原子的
2 4 2 4 2
种类、数目不变,可得X的化学式为SO。
2
答案:(1)黑
(2)HSO+Ca(OH) ====CaSO+2HO (3)SO
2 4 2 4 2 2
11.【解析】(1)由题中的实验知,小明同学做的是盐酸和氢氧化钠溶液分别与酸碱指示剂、生
锈铁钉之间反应的实验,因而探究的应是酸、碱的性质;(2)因酸溶液能使紫色石蕊试液变红,
碱溶液能使其变蓝色,故①中的现象与a对应,②中的现象与c对应;又因盐酸能与氧化铁反
应,而氢氧化钠溶液与氧化铁不反应,故③中现象与d对应,④中现象与b对应。(3)因铁钉
表面的氧化铁被除去后,铁会与盐酸反应,因而气泡应是铁与稀盐酸反应所得;盐酸和硫酸
进行相同的实验,能产生相类似的现象,即盐酸和硫酸有相似的性质,根据组成和结构决定
6物质的性质,可以从两者组成的共同点上找答案。
答案:(1)探究酸和碱的性质 (2)a c d b
(3)Fe+2HCl====FeCl+H↑ 置换 盐酸和硫酸溶液中都含有氢离子
2 2
12.【解析】当加入熟石灰m g时,溶液pH<7,说明溶液中盐酸没有被完全中和,溶液中的溶质
为Ca(OH) 与HCl反应生成的CaCl 和剩余的HCl。图示中n g熟石灰与盐酸恰好完全反应,
2 2
由关系式:
Ca(OH)→2HCl 2NaOH→2HCl
2
74 73 80 73
可以看出,用同质量的氢氧化钠和熟石灰中和同质量的盐酸,氢氧化钠的质量不足,因此改
为等质量的氢氧化钠后,盐酸剩余,溶液的pH小于7。
答案:Ca(OH)+2HCl====CaCl+2HO CaCl 和HCl <
2 2 2 2
13.【解析】醋酸具有酸的共性,能使紫色石蕊变红,能与金属氧化物反应,能与铁反应放出氢
气;实验四中的纯碱不是碱,属于盐,因此结论中应该为:白醋能与盐反应;验证二氧化碳通
常用澄清石灰水。
答案:
(1)CaO+HO====Ca(OH) (2)四
2 2
(3)CO+Ca(OH) ====CaCO↓+HO
2 2 3 2
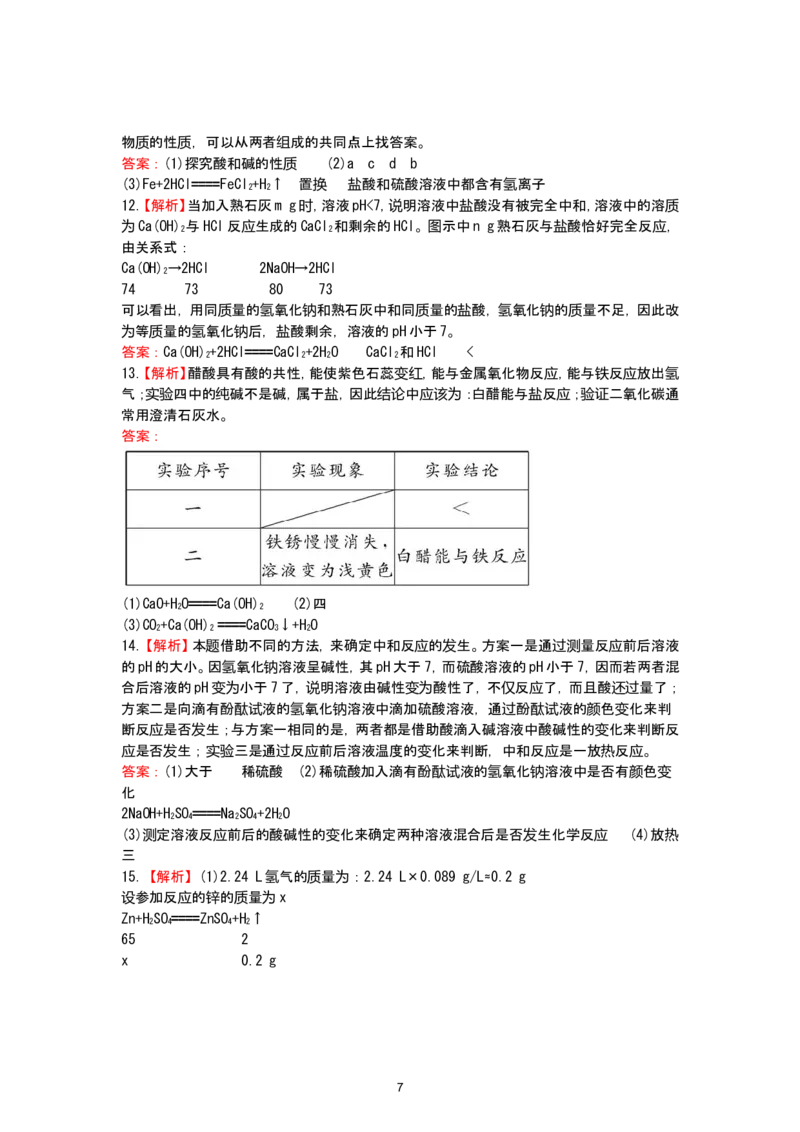
14.【解析】本题借助不同的方法,来确定中和反应的发生。方案一是通过测量反应前后溶液
的pH的大小。因氢氧化钠溶液呈碱性,其pH大于7,而硫酸溶液的pH小于7,因而若两者混
合后溶液的pH变为小于7了,说明溶液由碱性变为酸性了,不仅反应了,而且酸还过量了;
方案二是向滴有酚酞试液的氢氧化钠溶液中滴加硫酸溶液,通过酚酞试液的颜色变化来判
断反应是否发生;与方案一相同的是,两者都是借助酸滴入碱溶液中酸碱性的变化来判断反
应是否发生;实验三是通过反应前后溶液温度的变化来判断,中和反应是一放热反应。
答案:(1)大于 稀硫酸 (2)稀硫酸加入滴有酚酞试液的氢氧化钠溶液中是否有颜色变
化
2NaOH+HSO====NaSO+2HO
2 4 2 4 2
(3)测定溶液反应前后的酸碱性的变化来确定两种溶液混合后是否发生化学反应 (4)放热
三
15.【解析】(1)2.24 L氢气的质量为:2.24 L×0.089 g/L≈0.2 g
设参加反应的锌的质量为x
Zn+HSO====ZnSO+H↑
2 4 4 2
65 2
x 0.2 g
765 2
x 0.2 g
650.2 g
x= =6.5 g
2
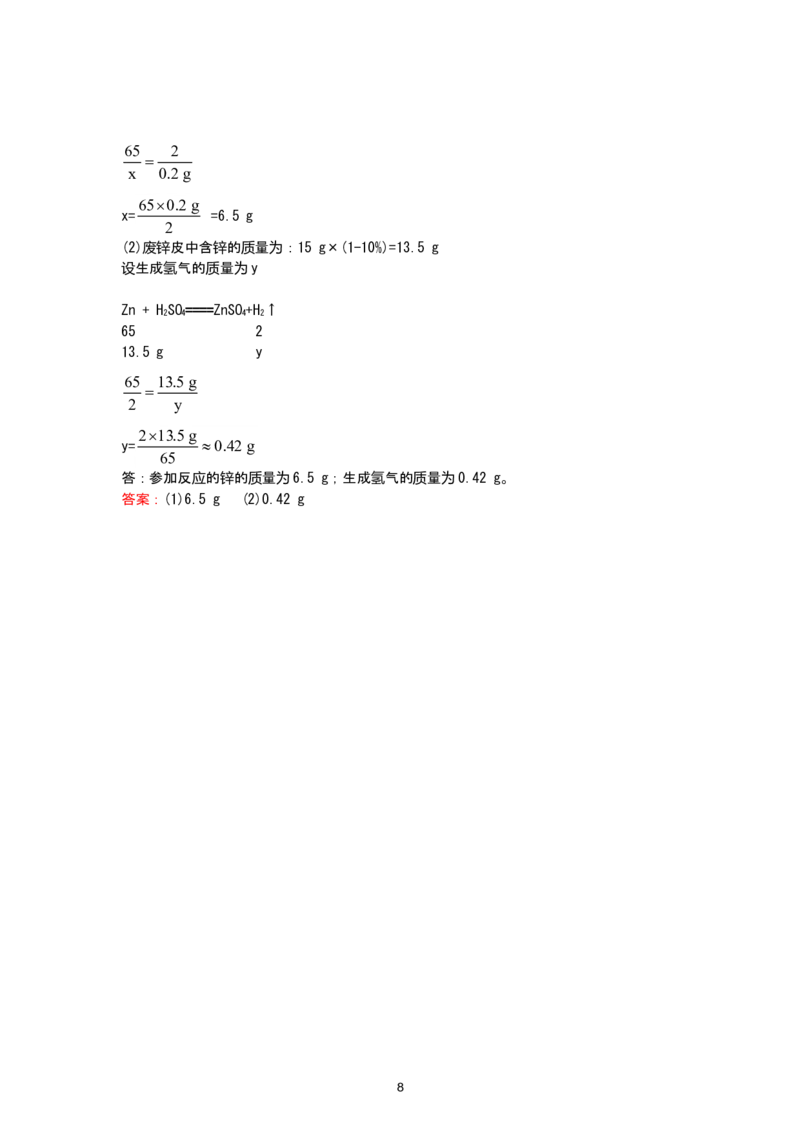
(2)废锌皮中含锌的质量为:15 g×(1-10%)=13.5 g
设生成氢气的质量为y
Zn + HSO====ZnSO+H↑
2 4 4 2
65 2
13.5 g y
65 13.5 g
2 y
213.5 g
y= 0.42 g
65
答:参加反应的锌的质量为6.5 g;生成氢气的质量为0.42 g。
答案:(1)6.5 g (2)0.42 g
8