文档内容
专项测试卷10
第十单元《酸和碱》
第一部分 常见的酸和碱
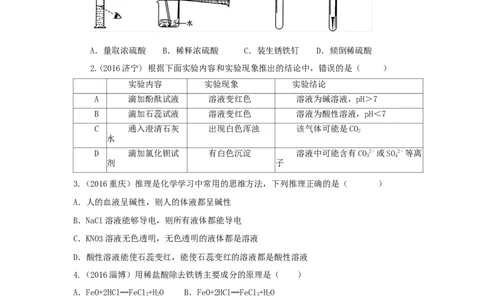
1.(2016福州)实验室配制一定溶质质量分数的稀硫酸并用其除铁锈,部分操作如图2
所示,其中正确的是( )
A.量取浓硫酸 B.稀释浓硫酸 C.装生锈铁钉 D.倾倒稀硫酸
2.(2016济宁) 根据下面实验内容和实验现象推出的结论中,错误的是( )
实验内容 实验现象 实验结论
A 滴加酚酞试液 溶液变红色 溶液为碱溶液,pH>7
B 滴加石蕊试液 溶液变红色 溶液为酸性溶液,pH<7
C 通入澄清石灰 出现白色浑浊 该气体可能是CO
2
水
D 滴加氯化钡试 有白色沉淀 溶液中可能含有CO2﹣或SO2﹣等离
3 4
剂 子
3.(2016重庆)推理是化学学习中常用的思维方法,下列推理正确的是( )
A.人的血液呈碱性,则人的体液都呈碱性
B.NaCl溶液能够导电,则所有液体都能导电
C.KNO3溶液无色透明,无色透明的液体都是溶液
D.酸性溶液能使石蕊变红,能使石蕊变红的溶液都是酸性溶液
4.(2016淄博)用稀盐酸除去铁锈主要成分的原理是( )
A.FeO+2HCl═FeCl+HO B.FeO+2HCl═FeCl+HO
2 2 3 2
C.FeO+6HCl═2FeCl+3HOD.FeO+6HCl═2FeCl+3HO
2 3 2 2 2 3 3 2
5.下列物质敞口放置一段时间后,质量增加但溶质成分没有改变的是( )
A.氢氧化钠溶液 B.石灰水
C.浓盐酸 D.浓硫酸
6.酸类物质具有相似的化学性质,本质的原因是( )
A.酸都含有酸根 B.酸都能与指示剂作用
C..酸在水溶液中都能解离出H+ D.酸是由多种元素组成的7.下列物质的性质属于物理性质的是( )
A.浓盐酸的挥发性 B.浓硫酸的腐蚀性
C.浓硫酸的吸水性 D.碳酸的不稳定性
8.下列关于氢氧化钠的说法错误的是( )
A.白色固体,易潮解 B.有强腐蚀性,俗称苛性钠
C.极易溶于水,溶解时放出大量的热 D.它能与CO发生化学反应
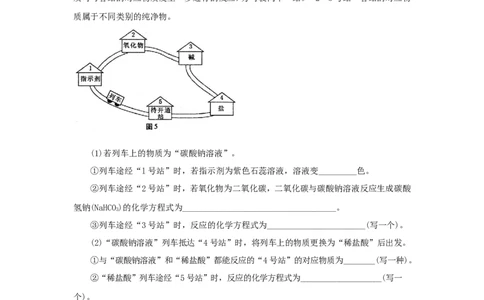
9. (2016福州)请同学们搭乘“化学地铁”一起畅游物质世界吧!如图5所示,列车上的物
质可与各站的对应物质发生一步进行的反应,方可驶向下一站。“2~5号站”各站的对应物
质属于不同类别的纯净物。
(1)若列车上的物质为“碳酸钠溶液”。
①列车途经“l号站”时,若指示剂为紫色石蕊溶液,溶液变_________色。
②列车途经“2号站”时,若氧化物为二氧化碳,二氧化碳与碳酸钠溶液反应生成碳酸
氢钠(NaHCO)的化学方程式为____________________________________。
3
③列车途经“3号站”时,反应的化学方程式为_______________________(写一个)。
(2)“碳酸钠溶液”列车抵达“4号站”时,将列车上的物质更换为“稀盐酸”后出发。
①与“碳酸钠溶液”和“稀盐酸”都能反应的“4号站”的对应物质为________(写一种)。
②“稀盐酸”列车途经“5号站”时,反应的化学方程式为_____________________(写一
个)。
③“稀盐酸”列车途经“l、2、3号站”时,原“碳酸钠溶液”列车途经某站的对应物质
必须更换为_________(写一种物质),“稀盐酸”列车方能走完全程。
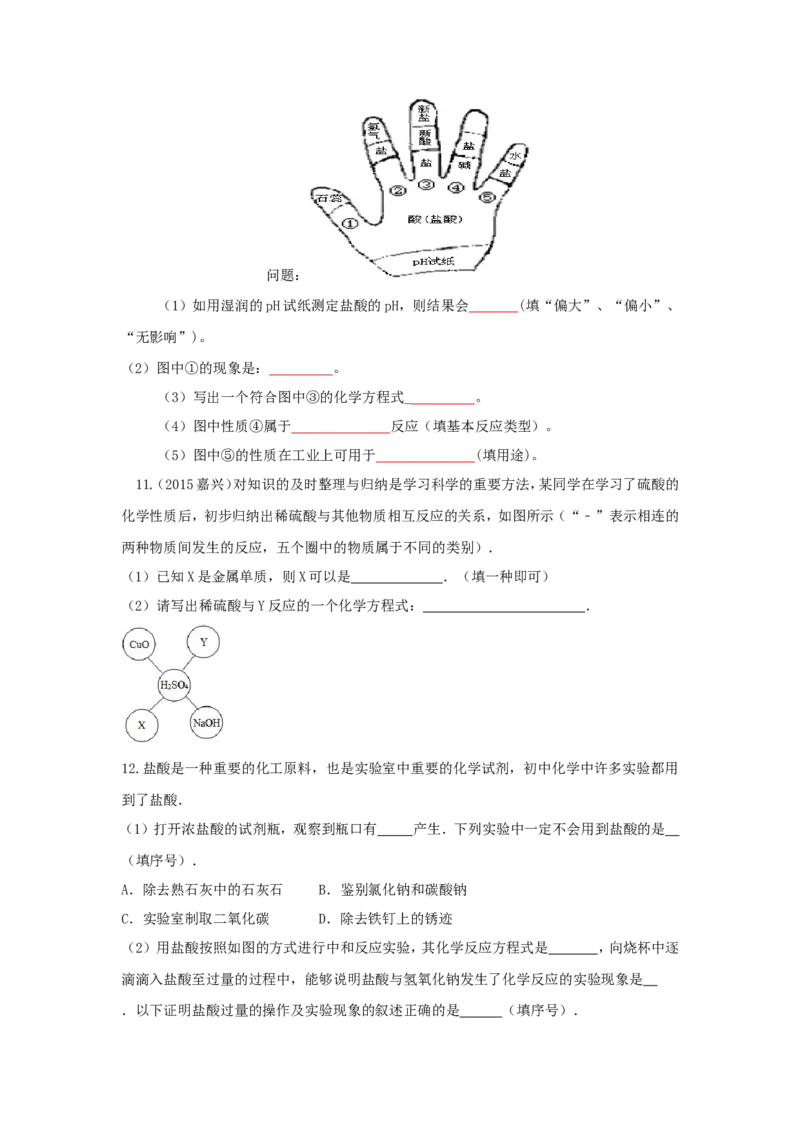
10. (2015黄冈)李华同学利用左手构建酸的性质知识网络,如图所示,请结合图示回答下列问题:
(1)如用湿润的pH试纸测定盐酸的pH,则结果会 (填“偏大”、“偏小”、
“无影响”)。
(2)图中①的现象是: 。
(3)写出一个符合图中③的化学方程式_ 。
(4)图中性质④属于 反应(填基本反应类型)。
(5)图中⑤的性质在工业上可用于 (填用途)。
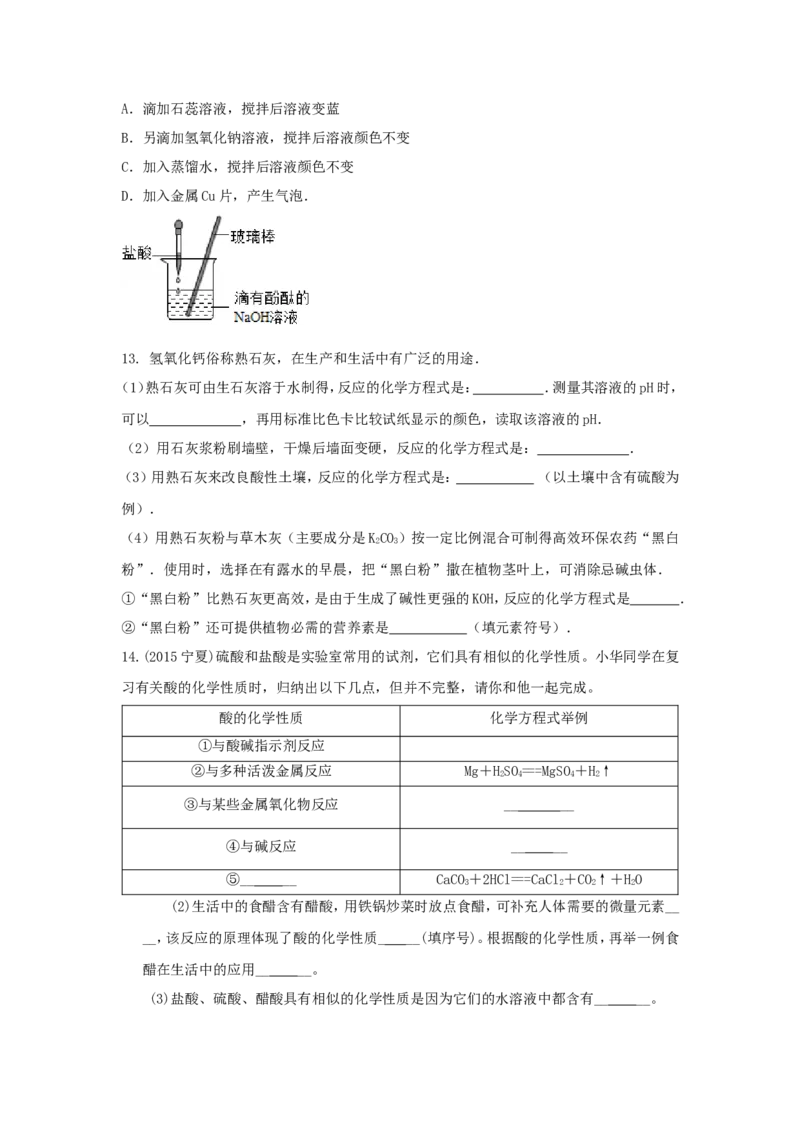
11.(2015嘉兴)对知识的及时整理与归纳是学习科学的重要方法,某同学在学习了硫酸的
化学性质后,初步归纳出稀硫酸与其他物质相互反应的关系,如图所示(“﹣”表示相连的
两种物质间发生的反应,五个圈中的物质属于不同的类别).
(1)已知X是金属单质,则X可以是 .(填一种即可)
(2)请写出稀硫酸与Y反应的一个化学方程式: .
12.盐酸是一种重要的化工原料,也是实验室中重要的化学试剂,初中化学中许多实验都用
到了盐酸.
(1)打开浓盐酸的试剂瓶,观察到瓶口有 产生.下列实验中一定不会用到盐酸的是
(填序号).
A.除去熟石灰中的石灰石 B.鉴别氯化钠和碳酸钠
C.实验室制取二氧化碳 D.除去铁钉上的锈迹
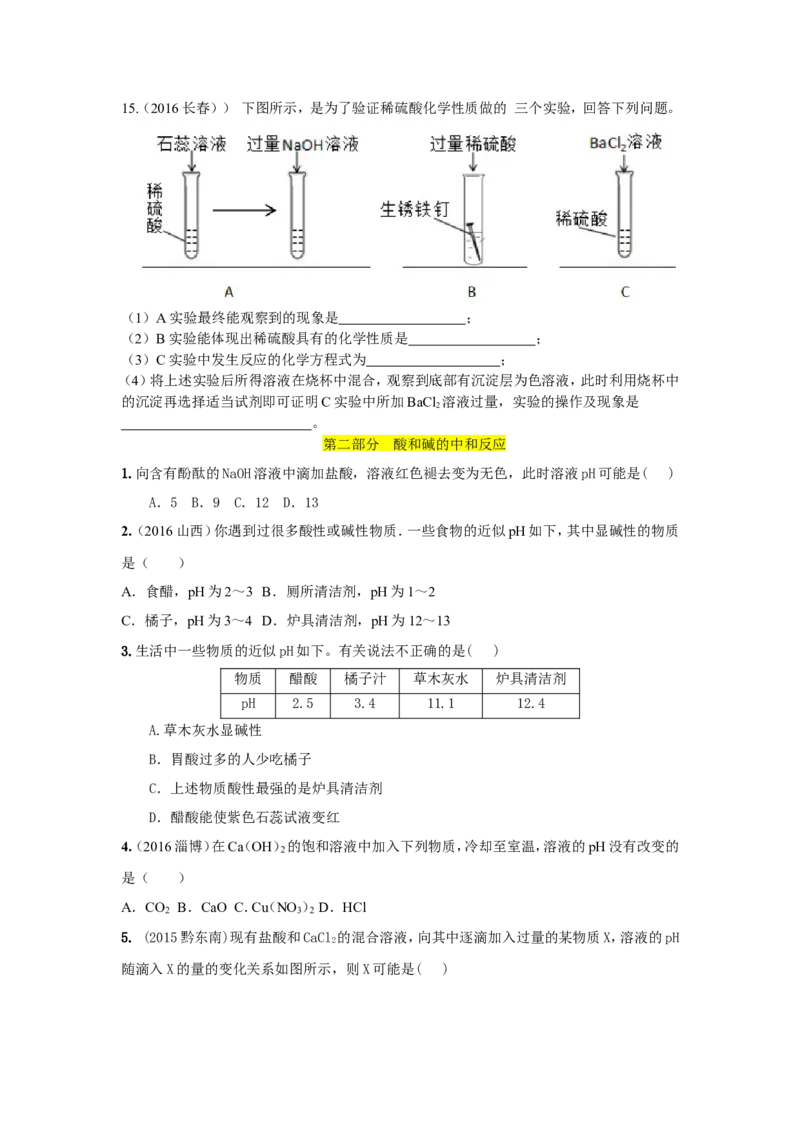
(2)用盐酸按照如图的方式进行中和反应实验,其化学反应方程式是 ,向烧杯中逐
滴滴入盐酸至过量的过程中,能够说明盐酸与氢氧化钠发生了化学反应的实验现象是
.以下证明盐酸过量的操作及实验现象的叙述正确的是 (填序号).A.滴加石蕊溶液,搅拌后溶液变蓝
B.另滴加氢氧化钠溶液,搅拌后溶液颜色不变
C.加入蒸馏水,搅拌后溶液颜色不变
D.加入金属Cu片,产生气泡.
13. 氢氧化钙俗称熟石灰,在生产和生活中有广泛的用途.
(1)熟石灰可由生石灰溶于水制得,反应的化学方程式是: .测量其溶液的pH时,
可以 ,再用标准比色卡比较试纸显示的颜色,读取该溶液的pH.
(2)用石灰浆粉刷墙壁,干燥后墙面变硬,反应的化学方程式是: .
(3)用熟石灰来改良酸性土壤,反应的化学方程式是: (以土壤中含有硫酸为
例).
(4)用熟石灰粉与草木灰(主要成分是KCO)按一定比例混合可制得高效环保农药“黑白
2 3
粉”.使用时,选择在有露水的早晨,把“黑白粉”撒在植物茎叶上,可消除忌碱虫体.
①“黑白粉”比熟石灰更高效,是由于生成了碱性更强的KOH,反应的化学方程式是 .
②“黑白粉”还可提供植物必需的营养素是 (填元素符号).
14.(2015宁夏)硫酸和盐酸是实验室常用的试剂,它们具有相似的化学性质。小华同学在复
习有关酸的化学性质时,归纳出以下几点,但并不完整,请你和他一起完成。
酸的化学性质 化学方程式举例
①与酸碱指示剂反应
②与多种活泼金属反应 Mg+HSO===MgSO+H↑
2 4 4 2
③与某些金属氧化物反应 __ __
④与碱反应 __ __
⑤__ __ CaCO+2HCl===CaCl+CO↑+HO
3 2 2 2
(2)生活中的食醋含有醋酸,用铁锅炒菜时放点食醋,可补充人体需要的微量元素__
__,该反应的原理体现了酸的化学性质_ __(填序号)。根据酸的化学性质,再举一例食
醋在生活中的应用__ __。
(3)盐酸、硫酸、醋酸具有相似的化学性质是因为它们的水溶液中都含有__ __。15.(2016长春)) 下图所示,是为了验证稀硫酸化学性质做的 三个实验,回答下列问题。
(1)A实验最终能观察到的现象是 ;
(2)B实验能体现出稀硫酸具有的化学性质是 ;
(3)C实验中发生反应的化学方程式为 ;
(4)将上述实验后所得溶液在烧杯中混合,观察到底部有沉淀层为色溶液,此时利用烧杯中
的沉淀再选择适当试剂即可证明C实验中所加BaCl 溶液过量,实验的操作及现象是
2
。
第二部分 酸和碱的中和反应
1.向含有酚酞的NaOH溶液中滴加盐酸,溶液红色褪去变为无色,此时溶液pH可能是( )
A.5 B.9 C.12 D.13
2.( 2016山西)你遇到过很多酸性或碱性物质.一些食物的近似pH如下,其中显碱性的物质
是( )
A.食醋,pH为2~3 B.厕所清洁剂,pH为1~2
C.橘子,pH为3~4 D.炉具清洁剂,pH为12~13
3.生活中一些物质的近似pH如下。有关说法不正确的是( )
物质 醋酸 橘子汁 草木灰水 炉具清洁剂
pH 2.5 3.4 11.1 12.4
A.草木灰水显碱性
B.胃酸过多的人少吃橘子
C.上述物质酸性最强的是炉具清洁剂
D.醋酸能使紫色石蕊试液变红
4.( 2016淄博)在Ca(OH)的饱和溶液中加入下列物质,冷却至室温,溶液的pH没有改变的
2
是( )
A.CO B.CaO C.Cu(NO )D.HCl
2 3 2
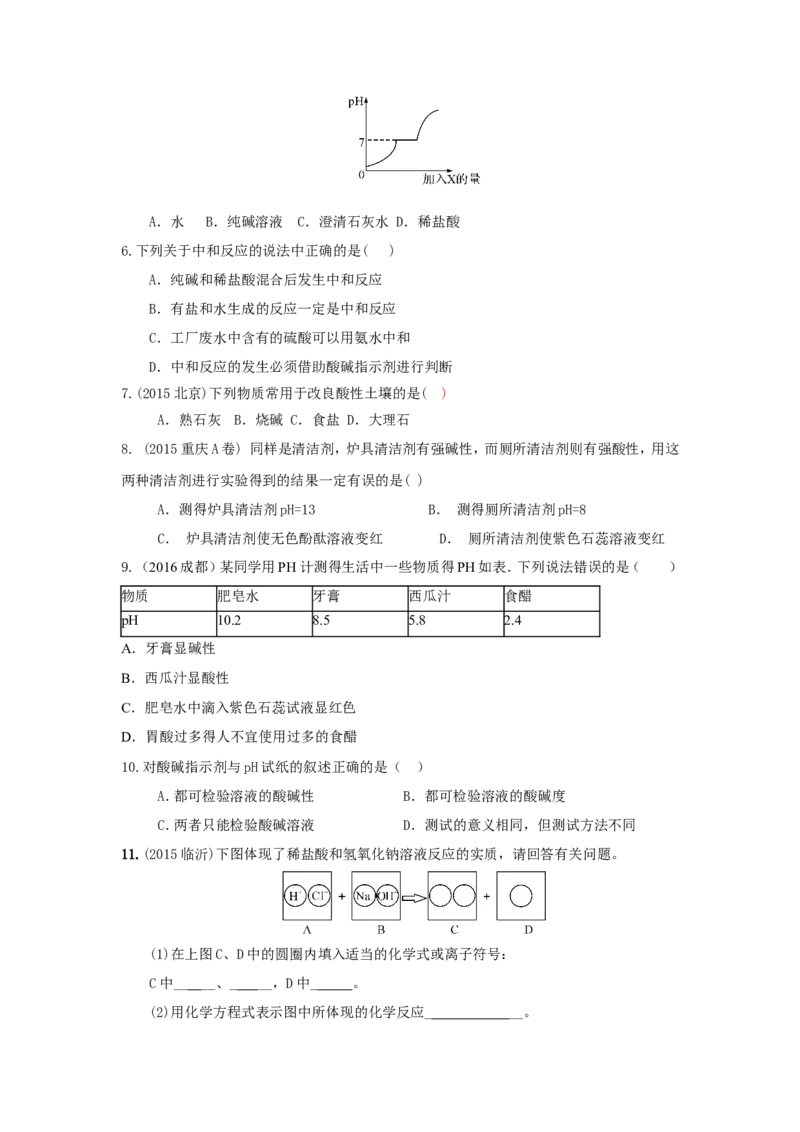
5. (2015黔东南)现有盐酸和CaCl 的混合溶液,向其中逐滴加入过量的某物质X,溶液的pH
2
随滴入X的量的变化关系如图所示,则X可能是( )A.水 B.纯碱溶液 C.澄清石灰水 D.稀盐酸
6.下列关于中和反应的说法中正确的是( )
A.纯碱和稀盐酸混合后发生中和反应
B.有盐和水生成的反应一定是中和反应
C.工厂废水中含有的硫酸可以用氨水中和
D.中和反应的发生必须借助酸碱指示剂进行判断
7.(2015北京)下列物质常用于改良酸性土壤的是( )
A.熟石灰 B.烧碱 C.食盐 D.大理石
8. (2015重庆A卷) 同样是清洁剂,炉具清洁剂有强碱性,而厕所清洁剂则有强酸性,用这
两种清洁剂进行实验得到的结果一定有误的是( )
A.测得炉具清洁剂pH=13 B. 测得厕所清洁剂pH=8
C. 炉具清洁剂使无色酚酞溶液变红 D. 厕所清洁剂使紫色石蕊溶液变红
9. (2016成都)某同学用PH计测得生活中一些物质得PH如表.下列说法错误的是( )
物质 肥皂水 牙膏 西瓜汁 食醋
pH 10.2 8.5 5.8 2.4
A.牙膏显碱性
B.西瓜汁显酸性
C.肥皂水中滴入紫色石蕊试液显红色
D.胃酸过多得人不宜使用过多的食醋
10.对酸碱指示剂与pH试纸的叙述正确的是( )
A.都可检验溶液的酸碱性 B.都可检验溶液的酸碱度
C.两者只能检验酸碱溶液 D.测试的意义相同,但测试方法不同
11.(2015临沂)下图体现了稀盐酸和氢氧化钠溶液反应的实质,请回答有关问题。
(1)在上图C、D中的圆圈内填入适当的化学式或离子符号:
C中__ __、_ __,D中_ _ _。
(2)用化学方程式表示图中所体现的化学反应_ __。(3)以上变化的基本反应类型是_ __。
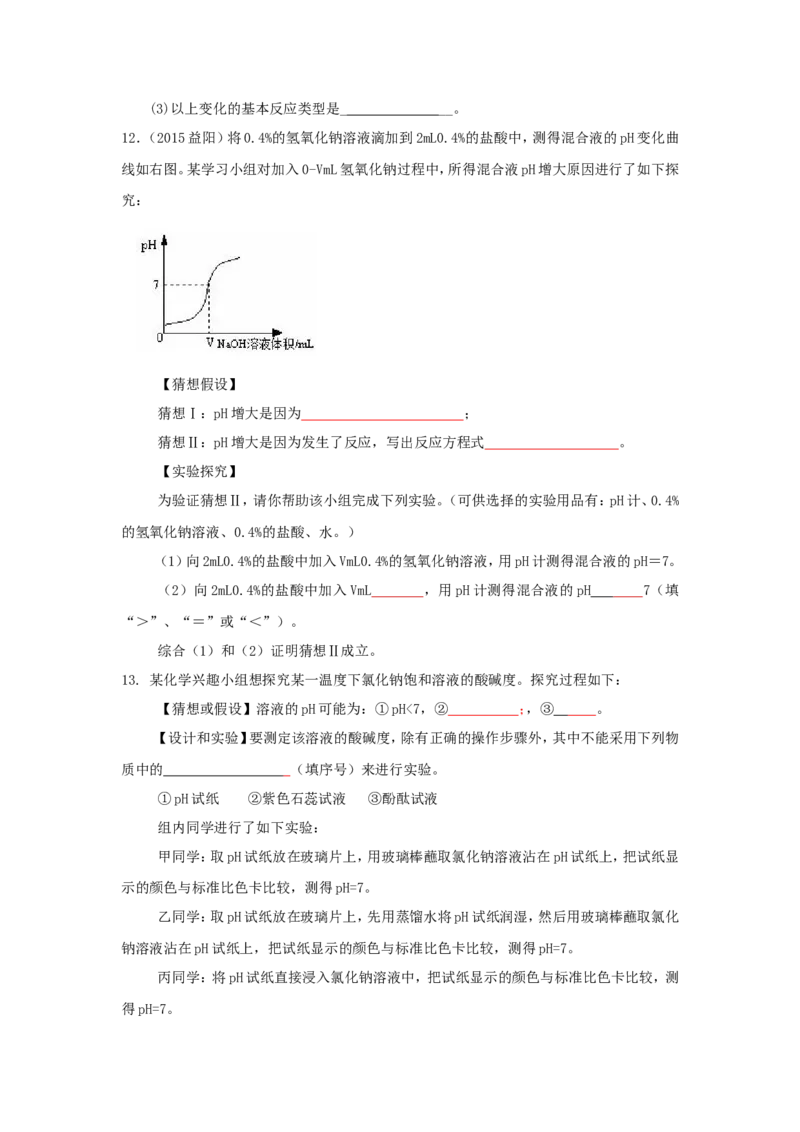
12.(2015益阳)将0.4%的氢氧化钠溶液滴加到2mL0.4%的盐酸中,测得混合液的pH变化曲
线如右图。某学习小组对加入0-VmL氢氧化钠过程中,所得混合液pH增大原因进行了如下探
究:
【猜想假设】
猜想Ⅰ:pH增大是因为 ;
猜想Ⅱ:pH增大是因为发生了反应,写出反应方程式 。
【实验探究】
为验证猜想Ⅱ,请你帮助该小组完成下列实验。(可供选择的实验用品有:pH计、0.4%
的氢氧化钠溶液、0.4%的盐酸、水。)
(1)向2mL0.4%的盐酸中加入VmL0.4%的氢氧化钠溶液,用pH计测得混合液的pH=7。
(2)向2mL0.4%的盐酸中加入VmL ,用pH计测得混合液的pH 7(填
“>”、“=”或“<”)。
综合(1)和(2)证明猜想Ⅱ成立。
13. 某化学兴趣小组想探究某一温度下氯化钠饱和溶液的酸碱度。探究过程如下:
【猜想或假设】溶液的pH可能为:①pH<7,② ;,③ 。
【设计和实验】要测定该溶液的酸碱度,除有正确的操作步骤外,其中不能采用下列物
质中的 (填序号)来进行实验。
①pH试纸 ②紫色石蕊试液 ③酚酞试液
组内同学进行了如下实验:
甲同学:取pH试纸放在玻璃片上,用玻璃棒蘸取氯化钠溶液沾在pH试纸上,把试纸显
示的颜色与标准比色卡比较,测得pH=7。
乙同学:取pH试纸放在玻璃片上,先用蒸馏水将pH试纸润湿,然后用玻璃棒蘸取氯化
钠溶液沾在pH试纸上,把试纸显示的颜色与标准比色卡比较,测得pH=7。
丙同学:将pH试纸直接浸入氯化钠溶液中,把试纸显示的颜色与标准比色卡比较,测
得pH=7。【评价与反思】三位同学中操作正确的是 同学。
指出其于同学的操作错误: 同学: ; 同学 : ;
【结论与分析】丙同学得出:“凡是盐溶液的 pH都等于7”,你认为该同学结论
(填“正确”或“不正确”)。如不正确,请举一例说明 (如正确,该处不填)。
14. 实验室有两瓶失去标签的稀盐酸和氢氧化钠溶液(记作A、B),小强用下列方法鉴别,回
答下列问题.
(1)他取适量的A、B两种溶液于试管中,分别加入适量氯化铁溶液,观察到A中产生红褐色
沉淀,则A是 ,发生反应的化学方程式为 ;
(2)他另取适量的A、B两种溶液于试管中,分别加入适量碳酸钠溶液,观察到B中的现象为
,发生反应的化学方程式为 ;
(3)他通过测定溶液的酸碱度来鉴别:若pH 7,则溶液为 ;
(4)他还利用了下列试剂进行鉴别,其中能鉴别的试剂是 .(填字母)
A、锌 B、硝酸钠 C、石蕊试液.
15.(2016德州) 小红同学进行酸碱中和反应的实验(如图所示).她向氢氧化钠溶液中滴加一
定量稀盐酸后,想起氢氧化钠溶液中事先没有滴加指示剂,为了确定盐酸与氢氧化钠的反应
程度,她从烧杯中取了少量溶液于试管中,并向试管中滴加几滴无色酚酞试液,震荡,观察到
试管中溶液颜色没有变化.于是她对烧杯中的溶液进行了以下探究:
(1)小红认为此时烧杯中的溶液可能有以下三种情况:
①盐酸与氢氧化钠恰好完全反应;②氢氧化钠有剩余;③盐酸过量.
小明同学却断定不可能“氢氧化钠有剩余”,他的理由是: ;
(2)他们共同设计了一个实验方案,欲对上述其他两种可能情况进行验证.请根据相关内容
填写如表:
试验方法 可能观察到的现 结论
象
将少量锌粒放入试管中,然后从烧杯中取适量 如果 则盐酸过量
溶液至试管中.
如果 则盐酸与氢氧化钠恰好完
全反应
(3)经过讨论,他们认为利用下列几种物质代替锌粒,也可以达到验证目的.你认为其中不正
确的是 (填序号).
A.生锈的铁钉 B.碳酸钠粉末 C.硫酸钠粉末 D.氢氧化铜
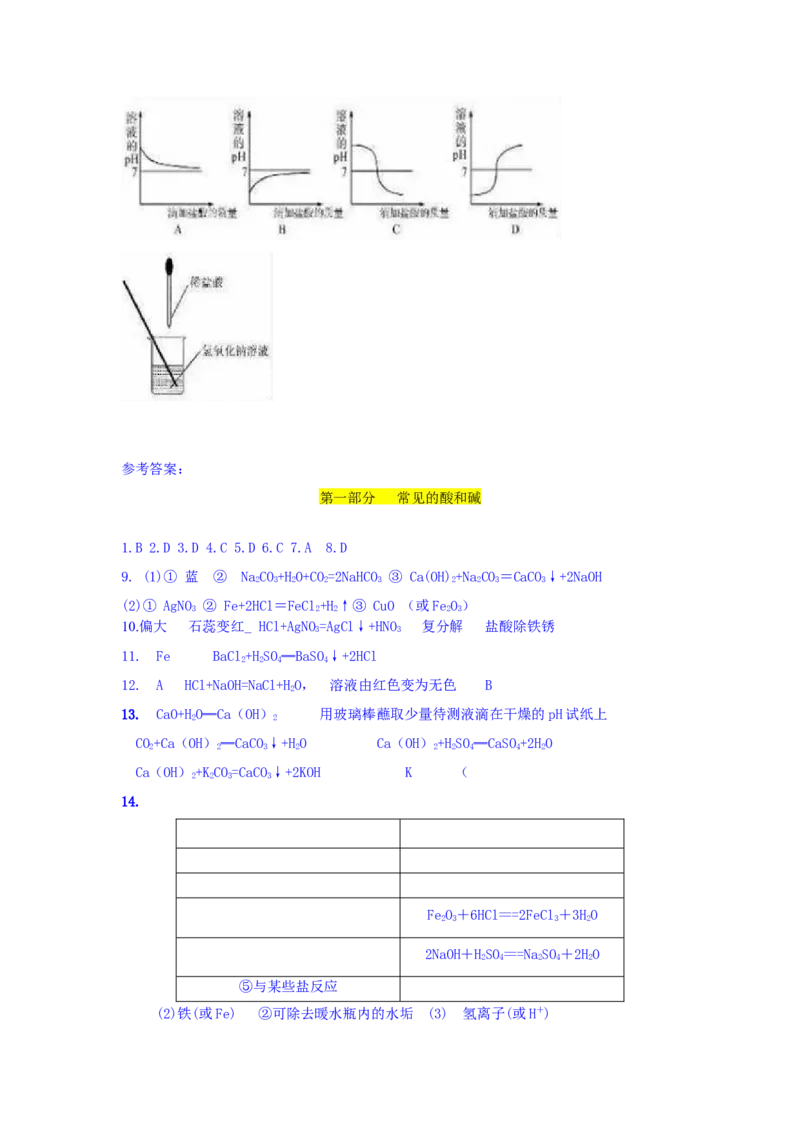
(4)如图曲线能够表示小红所做试验中溶液pH变化趋势的是 (填序号).参考答案:
第一部分 常见的酸和碱
1.B 2.D 3.D 4.C 5.D 6.C 7.A 8.D
9. (1)① 蓝 ② NaCO+HO+CO=2NaHCO ③ Ca(OH)+NaCO=CaCO↓+2NaOH
2 3 2 2 3 2 2 3 3
(2)① AgNO ② Fe+2HCl=FeCl+H↑③ CuO (或FeO)
3 2 2 2 3
10.偏大 石蕊变红_ HCl+AgNO=AgCl↓+HNO 复分解 盐酸除铁锈
3 3
11. Fe BaCl+HSO═BaSO↓+2HCl
2 2 4 4
12. A HCl+NaOH=NaCl+HO, 溶液由红色变为无色 B
2
13. CaO+HO═Ca(OH) 用玻璃棒蘸取少量待测液滴在干燥的pH试纸上
2 2
CO+Ca(OH)═CaCO↓+HO Ca(OH)+HSO═CaSO+2HO
2 2 3 2 2 2 4 4 2
Ca(OH)+KCO=CaCO↓+2KOH K (
2 2 3 3
14.
FeO+6HCl===2FeCl+3HO
2 3 3 2
2NaOH+HSO===NaSO+2HO
2 4 2 4 2
⑤与某些盐反应
(2)铁(或Fe) ②可除去暖水瓶内的水垢 (3) 氢离子(或H+)15. ( 1 ) 溶 液 呈 蓝 色 ; ( 2 ) 能 与 活 泼 金 属 或 金 属 氧 化 物 反 应 ; ( 3 )
HSO +BaCl ==BaSO ↓+2HCl;
2 4 2 4
(4)向沉淀中加入足量稀硝酸,始终有白色固体剩余
第二部分 酸和碱的中和反应
1.A 2.D 3.C 4.B 5.B 6.C 7.A 8.B 9.C 10.A
11.(1) __Cl-__、__Na+___HO__。(2) __NaOH+HCl===NaCl+HO__(3) __复分解反应__。
2 2
12.盐酸被NaOH溶液稀释 NaOH+HCl=NaCl+HO 水 <
2
13.②pH=7;,③ pH>7。 ②③ 甲 乙: pH试纸不能润湿; 丙 pH试纸不能直接
放入待测溶液中; 不正确 碳酸钠
4.(1) NaOH 3NaOH+FeCl═Fe(OH)↓+3NaCl ;
3 3
(2)有气泡产生 2HCl+NaCO═2NaCl+HO+CO↑ ;
2 3 2 2
3) > 氢氧化钠 (4)AC
15.(1)因为酚酞溶液没有变色
(2)
有气泡冒出
无现象
(3) C
(4) C