文档内容
第五单元《化学方程式》测试题(附答案)
可能用到的相对原子质量:
H 1 C 12 O 16 N 14 Cl 35.5 S 32 Zn 65 Fe 56 Mg 24 K 39 Mn 55
一、选择题 (每题只有一个答案 一题3分,共30分)
1.关于质量守恒定律,下列叙述正确的是( )
A.煤燃烧化为灰烬,该反应不符合质量守恒定律;
B.24g镁在空气中完全燃烧生成40g氧化镁,实际消耗空气的质量为16g;
C.无数实验证明化学反应都遵循质量守恒定律;
D. 质量守恒定律只适合于有气体或固体生成的化学反应。
2.某公司研发了一种由甲醇为原料的新型手机电池,其容量为锂电池的10倍,
可连续使用一个月才充一次电,其电池反应原理为:
2CH OH + 3X + 4NaOH == 2Na CO + 6H O,其中X的化学式为( )
3 2 3 2
A.O B.CO C.CO D.H
2 2 2
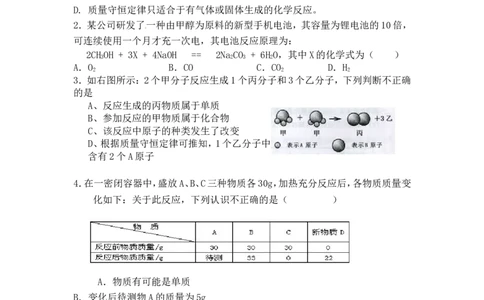
3.如右图所示:2个甲分子反应生成1个丙分子和3个乙分子,下列判断不正确
的是
A、反应生成的丙物质属于单质
B、参加反应的甲物质属于化合物
C、该反应中原子的种类发生了改变
D、根据质量守恒定律可推知,1个乙分子中
含有2个A原子
4.在一密闭容器中,盛放A、B、C三种物质各30g,加热充分反应后,各物质质量变
化如下:关于此反应,下列认识不正确的是( )
A.物质有可能是单质
B.变化后待测物A的质量为5g
C.该变化的基本反应类型是分解反应
D.C物质中所含有的元素种类是A、B、D三种物质中所有元素种类之和
5.在反应A+2B=C+2D中,9.8gA与8gB完全反应,生成14.2gC,则下列结论正确的
是( )
A、生成D1.8g B、质量比为49∶40∶71∶18
C、生成D7.2g D、相对分子质量比98∶80∶142∶36
6.将m g硫在n g氧气中燃烧,所生成二氧化硫的质量下列答案中你认为最合理
的是(m可与n相等,也可不相等)( )
A.一定等于(m+n)g B.一定小于(m–n)g
1C.可能是小于或等于(m+n)g D.以上答案都正确
7. A、B两元素可形成多种化合物,已知在A B化合物中,A和B的质量比为7:4,
2
则符合A与B质量比为7:12的化合物是 ( )
A、 AB B、 A B C、AB D、A B
2 2 3 2 5
8.某有机物燃烧后生成CO2和H2O两种物质,则此有机物的组成是( )
A、只含有碳、氢元素 B、一定含有碳、氢元素,可能含有氧元素
C、一定含有碳、氢、氧元素 D、肯定含有碳、氧元素
9.化学方程式aC2H2+bO2 = cH2O+dCO2则a、b、c、d等数之和为( )
A、15 B、14 C、13 D、10
10.在反应2A + B = 3C + D中,A和B的相对分子质量之比为5﹕1,已知
20克A与一定质量的B恰好反应,生成5克D,则在此反应中B和C的质量比为(
)
A、4﹕19 B、3﹕5 C、1﹕3 D、2﹕17
二、本题包括3个小题,共27分
11(10分).用元素符号或化学式表示
(1)氧化铁 (2)2个铁离子
(3)碳酸根的化合价为-2价 (4)4个硫酸根离子
(5)硝酸铵
12(10分)梅县东山工业区某化工厂以食盐和水为主要原料生产多种化工产品。
(1)以食盐和水为反应物,经过电解制得Cl 、H 、NaOH三种物质,该反应的化
2 2
学方程式
(2)氯气是一种有毒的气体,溶于水可生成次氯酸(HClO)和盐酸(HCl),该反
应的化学方程式 __________________________
(3)氢气可在氯气中燃烧,生成氯化氢气体(HCl),该反应的化学方程
式 _______________________
13.(7分)用纳米级的某种氧化物做催化剂,使汽车尾气中的CO跟NO反应转
化为两种气体,其中一种可参与植物的光合作用,另一种是空气中含量最多的气
体。这两种气体是______和_______ 。写出 CO 和 NO 反应的化学方程式
_________________________。
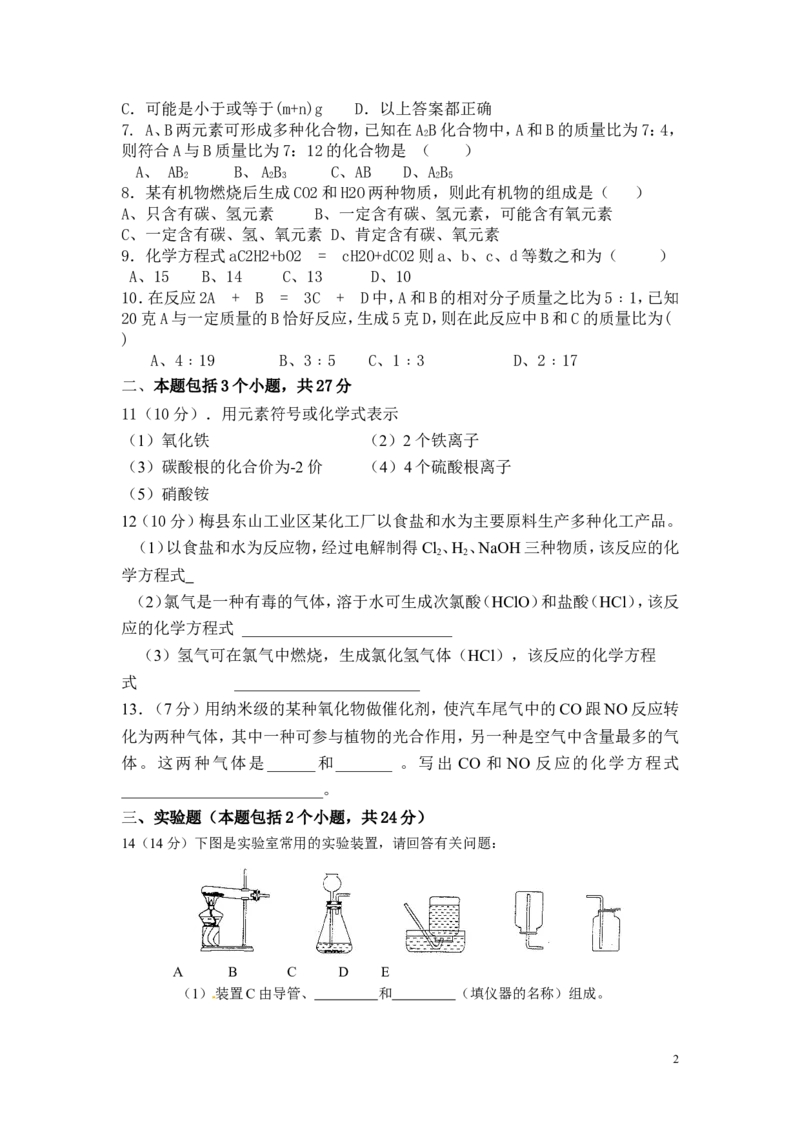
三、实验题(本题包括2个小题,共24分)
14(14分)下图是实验室常用的实验装置,请回答有关问题:
A B C D E
(1)装置C由导管、 和 (填仪器的名称)组成 。
2(2)实验室用HO 和MnO 制取O 的化学方程式为 ,选用的发生装置是
2 2 2 2
(填序号,下同);若用KClO 和MnO 制取O 时,则选用的发生装置是 。
3 2 2
(3)实验室制取CO 的化学方程式为 。若制得的CO 中混有HCl和HO,提纯时用
2 2 2
NaOH固体除去杂质,你认为这种方法 (填“可行”或“不可行”),理由是
。
(4)实验室制取H 应选用的收集装置是 或 。
2
15(10分).下面是某科研小组对“蜡烛燃烧前后各物质质量之和会发生变化
吗?”的问题进行实验探究的例子,他给出了实验探究的一般步骤。
假设:①会发生变化 ②不会发生变化
收集、整理资料:(1)蜡烛燃烧需要氧气,生成二氧化碳和水;(2)氧气、二氧化碳
等为气体;(3)由(1)(2)可知实验必须在密闭容器中进行。
设计并进行实验:(1)将一支蜡烛放在集气瓶中,塞上塞子,称其质量为W1g;
(2)将蜡烛点燃,立即塞上塞子;(3)待蜡烛熄灭,集气瓶冷却,再称其质量为
W2g。
分析现象,得出结论:(1)如果W =W ,则蜡烛燃烧前后物质的质量之和不变。
1 2
(2)如果W1≠W2,则蜡烛燃烧前后物质的质量之和发生变化。
请模仿上例,对“液化石油气里含氢元素吗?”的问题进行实验探究。
四、本大题包括2个小题,共19分
16. 甲醇( CH OH )是一种有毒,有酒的气味的可燃性液体。甲醇在氧气中不完
3
全燃烧可发生如下反应: 8CH O H +nO mCO +2CO + 16H O。若反
3 2 2 2
应生成
3.6g 水,请计算:
( 1 )m值是 ;
( 2 )参加反应的氧气质量是多少克?(写出规范计算步骤)
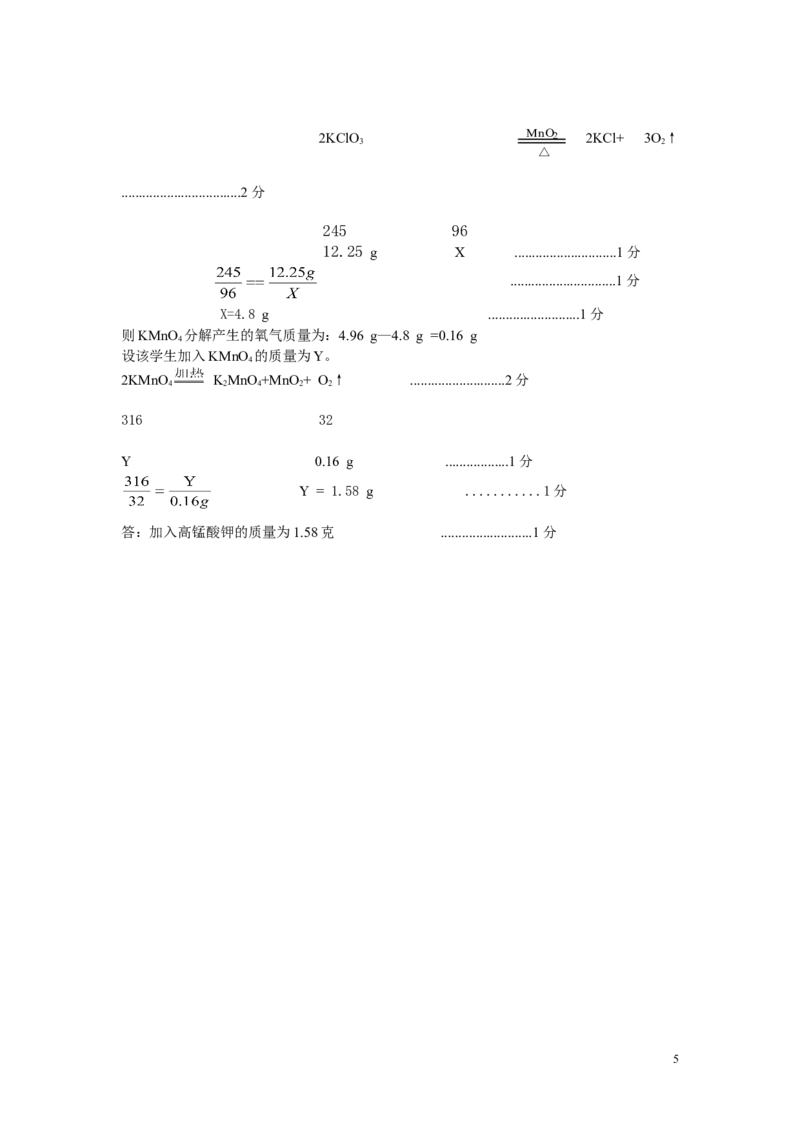
17.某学生称取12.25 g氯酸钾(KClO )制氧气,他用少量高锰酸钾(KMnO )代
3 4
替二氧化锰(MnO ),待反应完毕后,制得氧气4.96g。该学生加入了多少克高锰
2
酸钾?
3第五单元测试题(二)
一、选择题(本题包括10小题,每小题3分,共30分。
题
1 2 3 4 5 6 7 8 9 10
号
答 C A C B B C B B C A
案
二、本题包括3个小题,共27分
11.每空2分 共10分
(1)FeO (2)Fe3+ (3)CO (4)SO2- (5)NHNO
2 3 3 4 4 3
12.每空3分 共9分
(1)2NaCl+2 HO Cl↑+H ↑+2NaOH(2)Cl+ HO == HCl + HClO
2 2 2 2 2
(3)H+ Cl 2 HCl
2 2
13. 2分 CO N 2CO+2NO 2CO+ N
2 2分 2 2 2 3分
三、本题包括2个小题,共24分
14. 化学方程式3分 其余1分 共14分
(1)集气瓶 水槽
(2)2HO MnO 2HO+O↑ B A
2 2 2 2 2
(3)CaCO +2HCL=CaCL +H O+CO↑ 不行 能与二氧化碳反应
3 2 2 2
(4)B D
15.参考答案:(共10分)一、假设:(1)液化石油气中含氢元素 (2)液化石油气中不含氢
元素 二、收集、整理资料 (1)液化石油气能燃烧 (2)含氢元素的燃料燃烧后有水生成
三、设计实验 (1)将液化石油气点燃 (2)在火焰上方罩一个干而冷的烧杯 四、分
析现象,得出结论:(1)如果烧杯内壁有水珠生成,说明液化石油气的组成中含有氢元素
(2)如果烧杯内壁没有水珠生成,说明液化石油气的组成中不含有氢元素
四、本题包括2个小题,共19分
16. 8分
解:(1)根据质量守恒定律得:m+2=8,所以m= 6 ..........................1分
(2)设:参加反应的氧气质量为X,根据质量守恒定律得n=11 .........1分
8CH O H +11O 6CO+2CO + 16H O ..................................2分
3 2 2 2
352 288
X 3.6g .................................1分
== ..................1分
X=4.4g ....................................1分
答:参加反应的氧气的质量为4.4克。 ...................................1分
27.11分
解:设KClO 分解制得氧气的质量为X。 ..........................1分
3
42KClO MnO2 2KCl+ 3O↑
3 2
△
..................................2分
245 96
12.25 g X .............................1分
..............................1分
X=4.8 g ..........................1分
则KMnO 分解产生的氧气质量为:4.96 g—4.8 g =0.16 g
4
设该学生加入KMnO 的质量为Y。
4
2KMnO KMnO +MnO+ O↑ ...........................2分
4 2 4 2 2
316 32
Y 0.16 g ..................1分
Y = 1.58 g ...........1分
答:加入高锰酸钾的质量为1.58克 ..........................1分
5