文档内容
第四章 物质结构 元素周期律
第二节 元素周期律
由于第一节内容后连的比较多,所以这一节内容就是个概念形成和
具体应用的一节,所以内容较少,结合上一节内容一起看才能体会
元素周期表和元素周期律的真正含义
一、粒子半径大小的比较
影响粒子半径大小的因素有:
①电子层数的多少;
②原子核对核外电子的吸引力的大小;
③核外电子的多少。
(1)同周期、同主族原子半径的比较
①同一周期,从左到右,核电荷数依次增大,
原子半径依次减小。如r(Na)>r(Mg)>r(Al)>r(Si)>r(P)>r(S)>r(Cl)。
②同一主族,自上而下,电子层数依次增多,
原子半径依次增大。如r(Li)r(O)。
②电子层数相同时看核电荷数,荷少径大,
如r(F-)>r(Na+)。
③电子层数、核电荷数都相同时看电子数,
电子数多的半径大,如r(Cl-)>r(Cl)、r(Fe2+)>r(Fe3+)。
对点练习1
(2020·天津宝坻区·北大宝坻附属实验学校高三月考)已知X+、Y2+、Z-、W2-四种离子均具
有相同的电子层结构下列关于X、Y、Z、W四种元素的描述,不正确的是
A.原子半径: X>Y>Z>W B.原子序数:Y>X>Z> W
C.原子最外层电子数Y>X> Z> W D.金属性X>Y,还原性: W2-> Z-二、 主族元素主要化合价的确定
(1)主族元素的最高化合价=族序数(O、F除外)。
(2)非金属元素最低负价=8-原子的最外层电子数(H除外)。
对点练习2
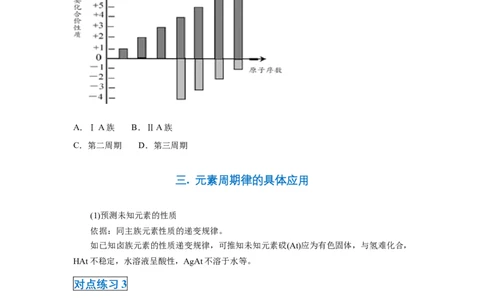
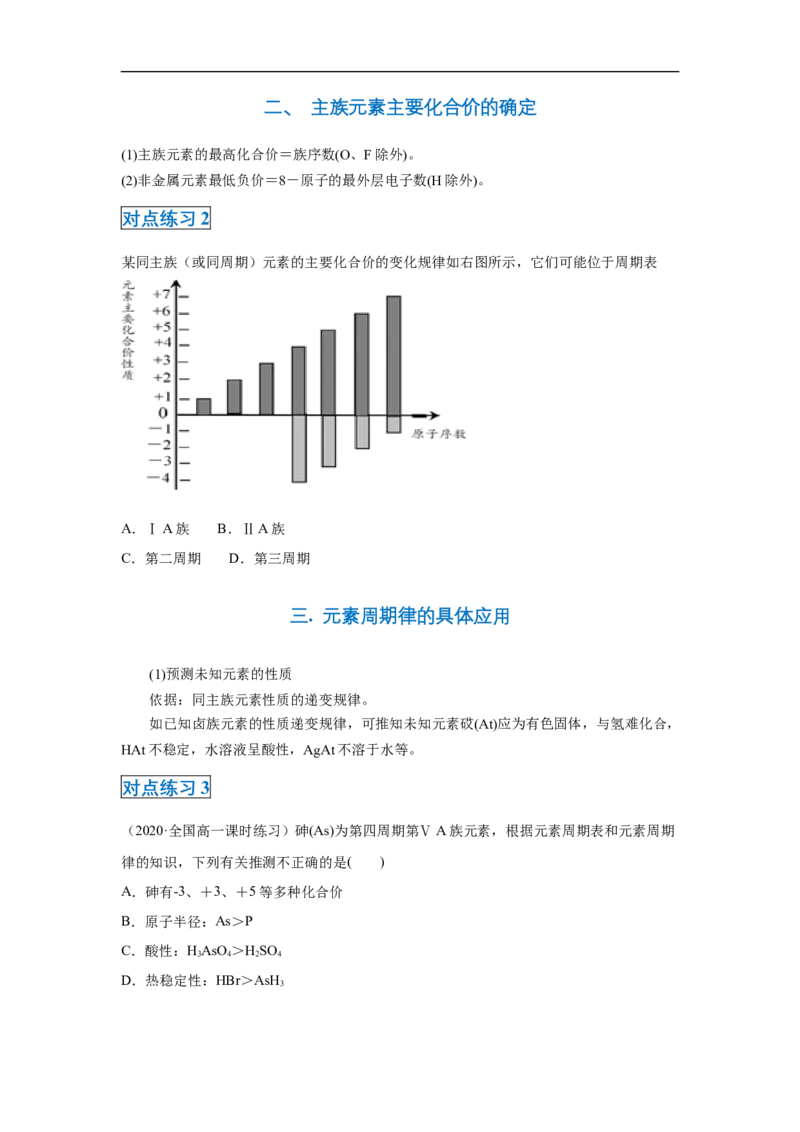
某同主族(或同周期)元素的主要化合价的变化规律如右图所示,它们可能位于周期表
A.ⅠA族 B.ⅡA族
C.第二周期 D.第三周期
三. 元素周期律的具体应用
(1)预测未知元素的性质
依据:同主族元素性质的递变规律。
如已知卤族元素的性质递变规律,可推知未知元素砹(At)应为有色固体,与氢难化合,
HAt不稳定,水溶液呈酸性,AgAt不溶于水等。
对点练习3
(2020·全国高一课时练习)砷(As)为第四周期第ⅤA族元素,根据元素周期表和元素周期
律的知识,下列有关推测不正确的是( )
A.砷有-3、+3、+5等多种化合价
B.原子半径:As>P
C.酸性:HAsO >HSO
3 4 2 4
D.热稳定性:HBr>AsH
3(2)比较元素的性质
依据:元素周期律。
如比较HSO 和HSeO 的酸性强弱,因为S、Se同主族,自上至下,元素的非金属性
2 4 2 4
减弱,最高价氧化物对应的水化物酸性减弱,故酸性:HSO >H SeO。
2 4 2 4
对点练习4
(2020·宁波市北仑中学高一期中)下列有关性质的比较,不能用元素周期律解释的是(
)
A.酸性: B.与氧气反应产物种类:
C.碱性: D.沸点:
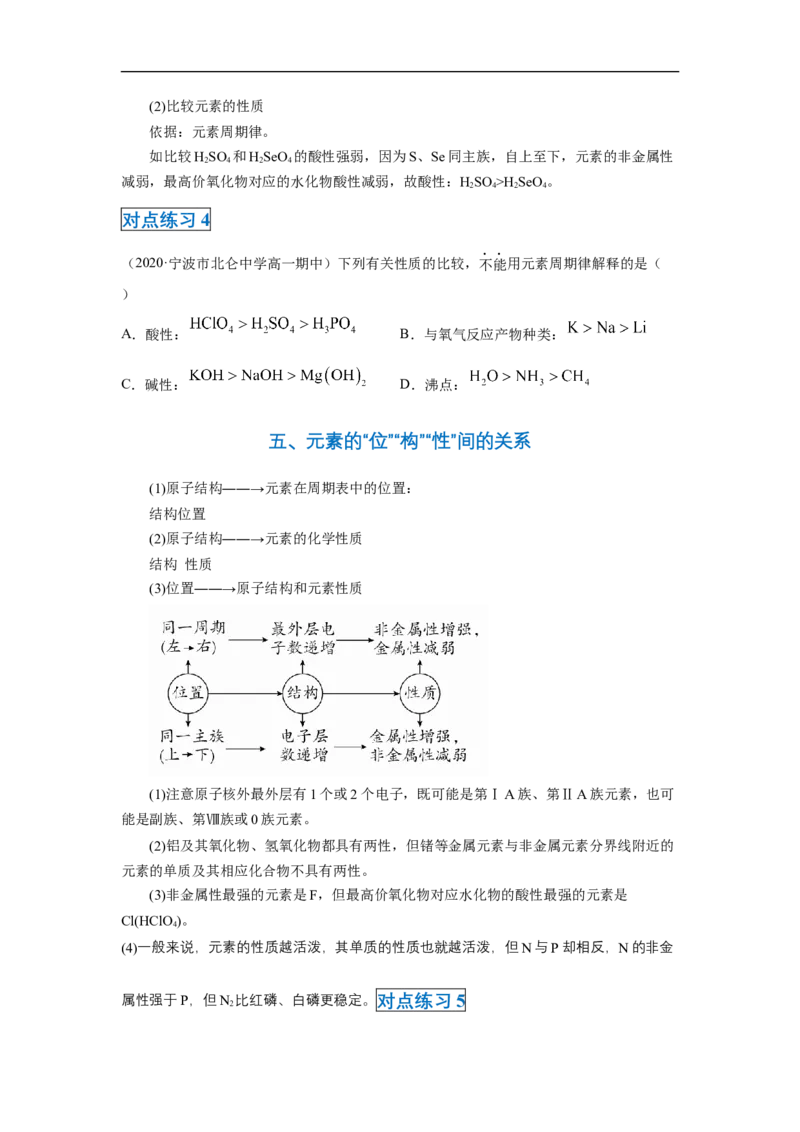
五、元素的“位”“构”“性”间的关系
(1)原子结构――→元素在周期表中的位置:
结构位置
(2)原子结构――→元素的化学性质
结构 性质
(3)位置――→原子结构和元素性质
(1)注意原子核外最外层有1个或2个电子,既可能是第ⅠA族、第ⅡA族元素,也可
能是副族、第Ⅷ族或0族元素。
(2)铝及其氧化物、氢氧化物都具有两性,但锗等金属元素与非金属元素分界线附近的
元素的单质及其相应化合物不具有两性。
(3)非金属性最强的元素是F,但最高价氧化物对应水化物的酸性最强的元素是
Cl(HClO )。
4
(4)一般来说,元素的性质越活泼,其单质的性质也就越活泼,但N与P却相反,N的非金
属性强于P,但N 比红磷、白磷更稳定。对点练习5
2(2020·浙江高一期中)Q、W、X、Y、Z为短周期元素,Q是原子半径最小的元素,W是
地壳中含量最高的元素,X原子的质子数等于Z与Y的质子数之和: Z与Y位于同一周期,
Y原子核外最外层电子比次外层多3个电子,非金属Z的一种固体单质可导电。回答下列
问题:
(1)Y、 Z的元素名称分别为___________、___________。
(2)X在周期表中的位置是______________________,其离子结构示意图为___________;Y
与Z之间形成的化学键属于___________。
(3)X、Y、Z三种元素原子半径由大到小的顺序为___________(填元素符号);X单质既可与
盐酸反应,又可溶于氢氧化钠溶液,写出X单质与氢氧化钠溶液反应的化学方程式
___________。
(4)化合物XZ 遇QW发生反应生成ZQ, ZQ 的空间构型为 ___________,请完成该反
4 3 2 4 4
应的化学方程式___________。
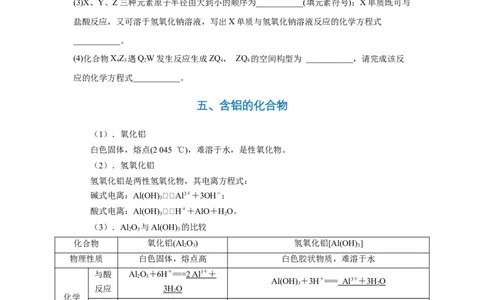
五、含铝的化合物
(1).氧化铝
白色固体,熔点(2 045 ℃),难溶于水,是性氧化物。
(2).氢氧化铝
氢氧化铝是两性氢氧化物,其电离方程式:
碱式电离:Al(OH) Al3++3OH-;
3
酸式电离:Al(OH) H++AlO+HO。
3 2
(3).Al O 与Al(OH) 的比较
2 3 3
化合物 氧化铝(AlO) 氢氧化铝[Al(OH) ]
2 3 3
物理性质 白色固体,熔点高 白色胶状物质,难溶于水
与酸 Al O+6H+=== 2 Al 3 + +
2 3
Al(OH) +3H+=== Al 3 + + 3H O
3 2
反应 3HO
2
化学
与碱 Al O+2OH-=== 2AlO +
2 3
性质 Al(OH) +OH-=== AlO + 2H O
3 2
反应 HO
2
加热 — 2Al(OH) ===== Al O + 3H O
3 2 3 2
①Al3+与氨水反应:Al3++3NH ·H O===Al(OH) ↓
3 2 3
Al(OH)
3
加 热 分 解 : +3NH
制备方法 2Al(OH) 3 ===== Al 2 O 3 + ②AlO溶液中通入过量CO 2 气体:
3H 2 O AlO+CO+2HO===Al(OH) ↓+HCO
2 2 3
③ AlCl 溶液中滴加 NaAlO 溶液:Al3++3AlO+
3 26HO===4Al(OH) ↓
2 3
作耐火材料、冶炼铝的原
主要用途 制药、净水
料
对点练习6
(2020·周口市中英文学校高三期中)既能跟稀盐酸反应,又能跟氢氧化钠溶液反应的化合
物是( )
①NaHCO ②Al O ③Al(OH) ④Al
3 2 3 3
A.①②③ B.①④ C.②③④ D.①②③
本节跟踪练习
1.(2020·河北高碑店市·高碑店一中高一月考)已知短周期元素的离子:A2+、B+、C3-、
a b c
D-都具有相同的电子层结构,则下列叙述正确的是( )
d
A.原子半径A>B>D>C
B.原子序数d>c>b>a
C.离子半径C3->D->B+>A2+
D.单质的还原性A>B>D>C
2.(2020·天津河西区·高三期中)下列叙述正确的是( )
A.沸点:
B.原子半径:
C.最高正化合价:
D.碱性:
3.(2019·宁县第二中学高一期中)元素的性质随着原子序数的递增呈现周期性的变化的
根本原因是( )
A.元素相对原子质量的递增,量变引起质变
B.元素的金属性和非金属性呈周期性变化
C.元素原子核外电子排布呈周期性变化
D.元素化合价呈周期性变化
4.(2020·上海市向明中学高一期中)卤素单质及化合物在许多性质上都存在着递变规律。下列有关说法正确的是( )
A.卤化氢的稳定性按HF、HCl、HBr、HI 的顺序依次减弱
B.卤化银的颜色按AgCl、AgBr、AgI的顺序依次变浅
C.卤素单质的熔点按Cl、Br 、I 的顺序依次减小
2 2 2
D.卤素单质与氢气化合按Cl、Br 、I 的顺序由难变易
2 2 2
5.砹( )属于卤族元素,下列关于砹( )及其化合物具有的性质的推测不正确的
是( )
A.单质砹易溶于某些有机溶剂
B. 是难溶于水的有色固体
C. 的酸性比 的弱
D. 受热很难分解
6.(2020·贵州铜仁伟才学校高二月考)短周期主族元A、B、C、D在周期表中的位置如
图所示,其中B是地壳中含量最多的元素,下列说法正确的是( )
A B
C D
A.元素B位于第二周期第IVA族
B.元素的非金属性B>C
C.原子半径D>C
D.简单气态氢化物的稳定性A>B
7.(2020·上海高三期末)能用于比较硫、氯两种元素非金属性强弱的是
A.熔点:S > Cl B.酸性:HClO > H SO
2 4 2 4
C.相对原子质量:Cl > S D.氧化性:HClO>HSO
2 3
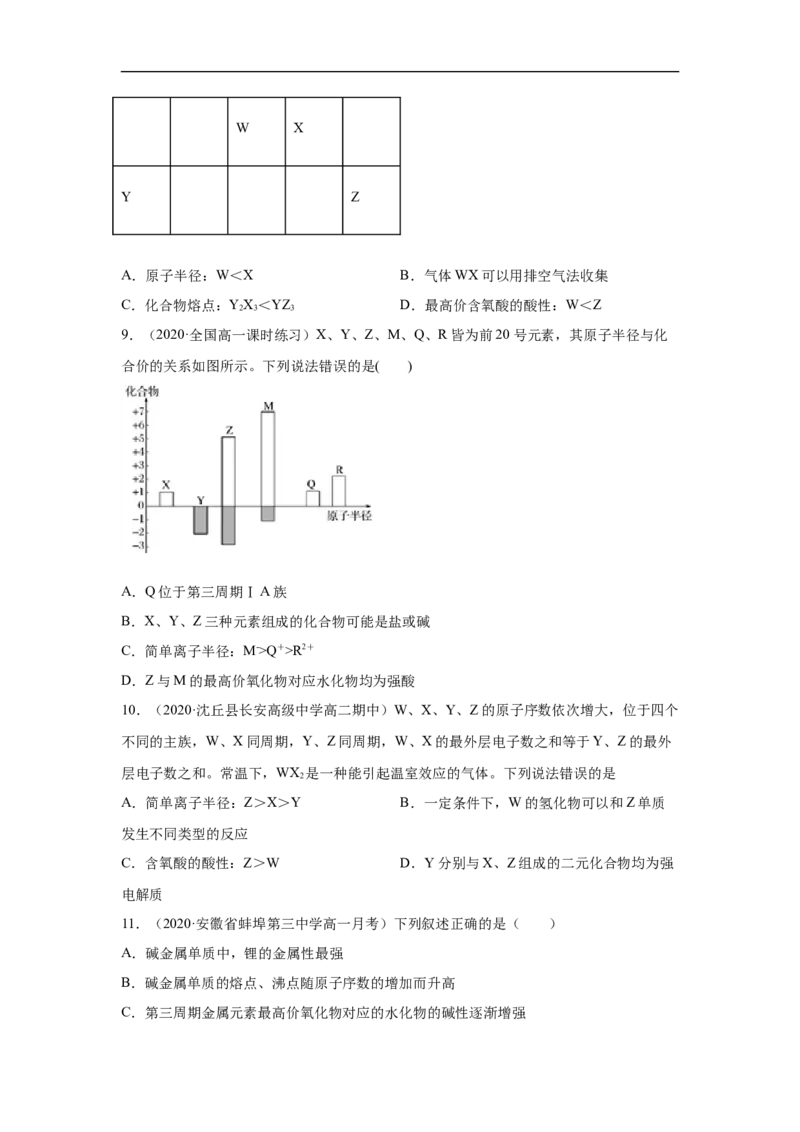
8.(2020·浙江高二开学考试)短周期元素W、X、Y和Z在周期表中的相对位置如表所
示,这四种元素原子的最外层电子数之和为21,下列关系正确的是W X
Y Z
A.原子半径:W<X B.气体WX可以用排空气法收集
C.化合物熔点:YX<YZ D.最高价含氧酸的酸性:W<Z
2 3 3
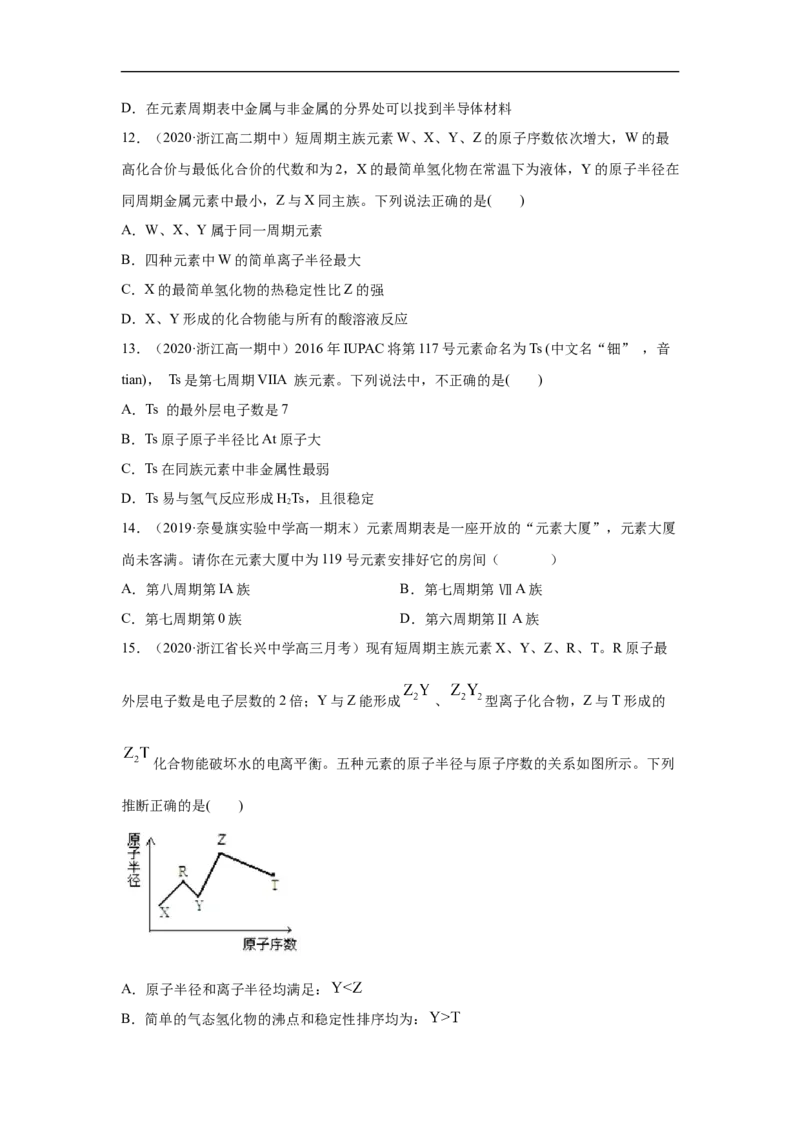
9.(2020·全国高一课时练习)X、Y、Z、M、Q、R皆为前20号元素,其原子半径与化
合价的关系如图所示。下列说法错误的是( )
A.Q位于第三周期ⅠA族
B.X、Y、Z三种元素组成的化合物可能是盐或碱
C.简单离子半径:M->Q+>R2+
D.Z与M的最高价氧化物对应水化物均为强酸
10.(2020·沈丘县长安高级中学高二期中)W、X、Y、Z的原子序数依次增大,位于四个
不同的主族,W、X同周期,Y、Z同周期,W、X的最外层电子数之和等于Y、Z的最外
层电子数之和。常温下,WX 是一种能引起温室效应的气体。下列说法错误的是
2
A.简单离子半径:Z>X>Y B.一定条件下,W的氢化物可以和Z单质
发生不同类型的反应
C.含氧酸的酸性:Z>W D.Y分别与X、Z组成的二元化合物均为强
电解质
11.(2020·安徽省蚌埠第三中学高一月考)下列叙述正确的是( )
A.碱金属单质中,锂的金属性最强
B.碱金属单质的熔点、沸点随原子序数的增加而升高
C.第三周期金属元素最高价氧化物对应的水化物的碱性逐渐增强D.在元素周期表中金属与非金属的分界处可以找到半导体材料
12.(2020·浙江高二期中)短周期主族元素W、X、Y、Z的原子序数依次增大,W的最
高化合价与最低化合价的代数和为2,X的最简单氢化物在常温下为液体,Y的原子半径在
同周期金属元素中最小,Z与X同主族。下列说法正确的是( )
A.W、X、Y属于同一周期元素
B.四种元素中W的简单离子半径最大
C.X的最简单氢化物的热稳定性比Z的强
D.X、Y形成的化合物能与所有的酸溶液反应
13.(2020·浙江高一期中)2016年IUPAC将第117号元素命名为Ts (中文名“钿” ,音
tian), Ts是第七周期VIIA 族元素。下列说法中,不正确的是( )
A.Ts 的最外层电子数是7
B.Ts原子原子半径比At原子大
C.Ts在同族元素中非金属性最弱
D.Ts易与氢气反应形成HTs,且很稳定
2
14.(2019·奈曼旗实验中学高一期末)元素周期表是一座开放的“元素大厦”,元素大厦
尚未客满。请你在元素大厦中为119号元素安排好它的房间( )
A.第八周期第IA族 B.第七周期第ⅦA族
C.第七周期第0族 D.第六周期第ⅡA族
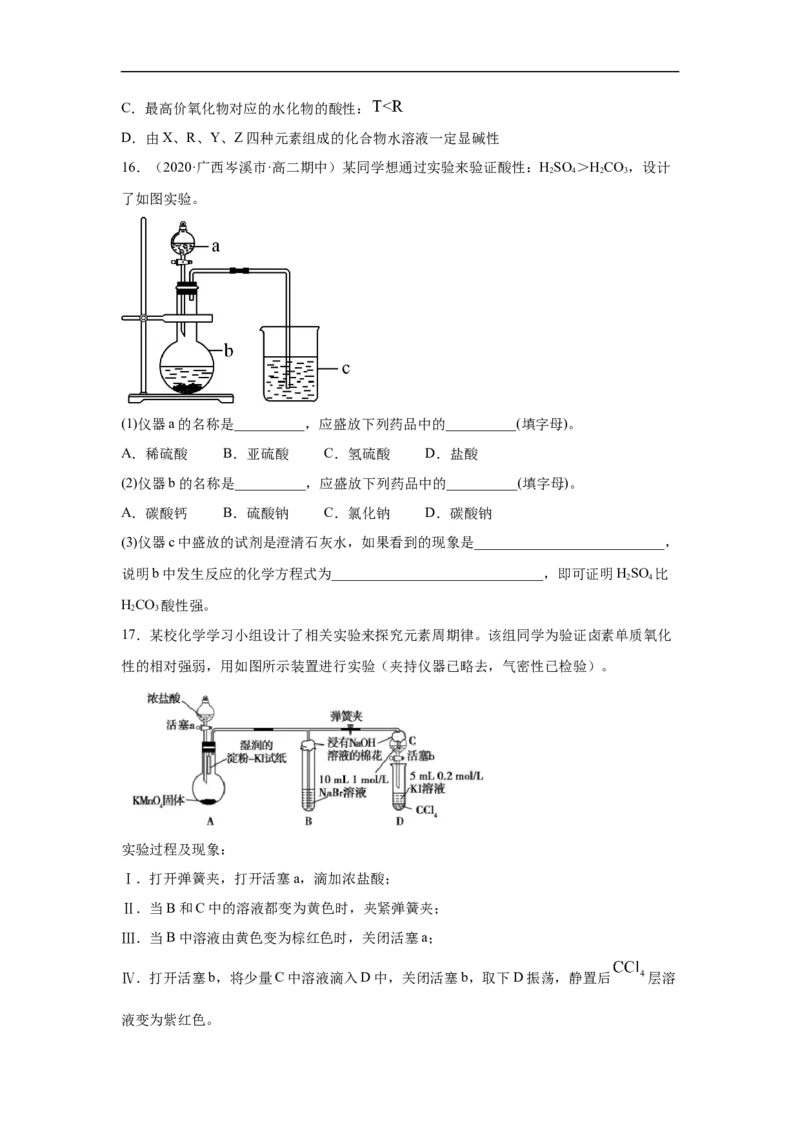
15.(2020·浙江省长兴中学高三月考)现有短周期主族元素X、Y、Z、R、T。R原子最
外层电子数是电子层数的2倍;Y与Z能形成 、 型离子化合物,Z与T形成的
化合物能破坏水的电离平衡。五种元素的原子半径与原子序数的关系如图所示。下列
推断正确的是( )
A.原子半径和离子半径均满足:
B.简单的气态氢化物的沸点和稳定性排序均为:C.最高价氧化物对应的水化物的酸性:
D.由X、R、Y、Z四种元素组成的化合物水溶液一定显碱性
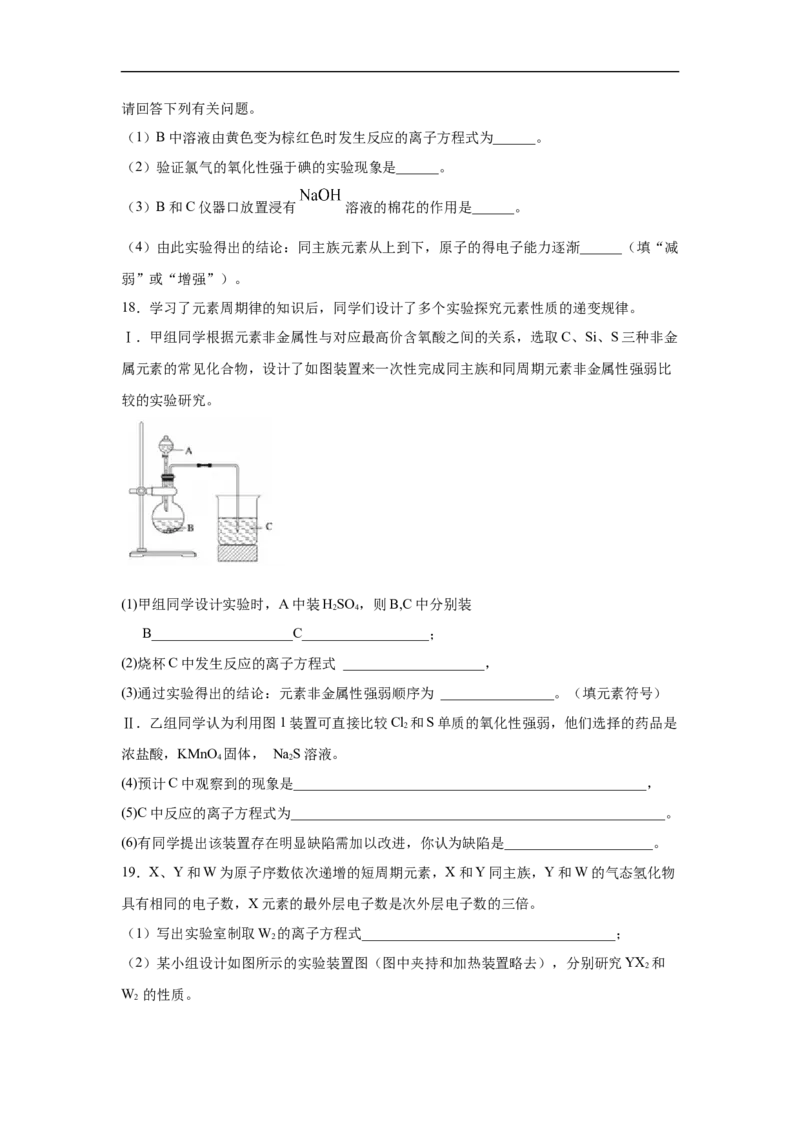
16.(2020·广西岑溪市·高二期中)某同学想通过实验来验证酸性:HSO >HCO,设计
2 4 2 3
了如图实验。
(1)仪器a的名称是__________,应盛放下列药品中的__________(填字母)。
A.稀硫酸 B.亚硫酸 C.氢硫酸 D.盐酸
(2)仪器b的名称是__________,应盛放下列药品中的__________(填字母)。
A.碳酸钙 B.硫酸钠 C.氯化钠 D.碳酸钠
(3)仪器c中盛放的试剂是澄清石灰水,如果看到的现象是___________________________,
说明b中发生反应的化学方程式为______________________________,即可证明HSO 比
2 4
HCO 酸性强。
2 3
17.某校化学学习小组设计了相关实验来探究元素周期律。该组同学为验证卤素单质氧化
性的相对强弱,用如图所示装置进行实验(夹持仪器已略去,气密性已检验)。
实验过程及现象:
Ⅰ.打开弹簧夹,打开活塞a,滴加浓盐酸;
Ⅱ.当B和C中的溶液都变为黄色时,夹紧弹簧夹;
Ⅲ.当B中溶液由黄色变为棕红色时,关闭活塞a;
Ⅳ.打开活塞b,将少量C中溶液滴入D中,关闭活塞b,取下D振荡,静置后 层溶
液变为紫红色。请回答下列有关问题。
(1)B中溶液由黄色变为棕红色时发生反应的离子方程式为______。
(2)验证氯气的氧化性强于碘的实验现象是______。
(3)B和C仪器口放置浸有 溶液的棉花的作用是______。
(4)由此实验得出的结论:同主族元素从上到下,原子的得电子能力逐渐______(填“减
弱”或“增强”)。
18.学习了元素周期律的知识后,同学们设计了多个实验探究元素性质的递变规律。
Ⅰ.甲组同学根据元素非金属性与对应最高价含氧酸之间的关系,选取C、Si、S三种非金
属元素的常见化合物,设计了如图装置来一次性完成同主族和同周期元素非金属性强弱比
较的实验研究。
(1)甲组同学设计实验时,A中装HSO ,则B,C中分别装
2 4
B____________________C__________________;
(2)烧杯C中发生反应的离子方程式 ____________________,
(3)通过实验得出的结论:元素非金属性强弱顺序为 ________________。(填元素符号)
Ⅱ.乙组同学认为利用图1装置可直接比较Cl 和S单质的氧化性强弱,他们选择的药品是
2
浓盐酸,KMnO 固体, NaS溶液。
4 2
(4)预计C中观察到的现象是__________________________________________________,
(5)C中反应的离子方程式为_____________________________________________________。
(6)有同学提出该装置存在明显缺陷需加以改进,你认为缺陷是_____________________。
19.X、Y和W为原子序数依次递增的短周期元素,X和Y同主族,Y和W的气态氢化物
具有相同的电子数,X元素的最外层电子数是次外层电子数的三倍。
(1)写出实验室制取W 的离子方程式____________________________________;
2
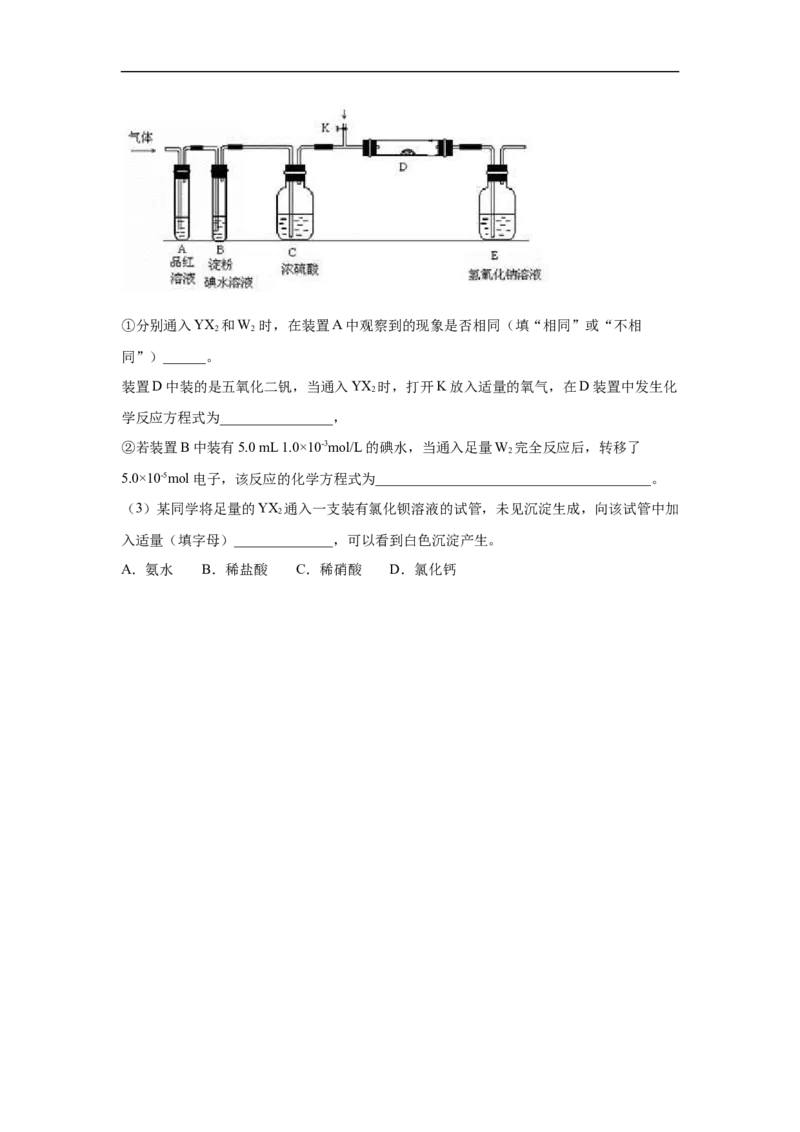
(2)某小组设计如图所示的实验装置图(图中夹持和加热装置略去),分别研究YX 和
2
W 的性质。
2①分别通入YX 和W 时,在装置A中观察到的现象是否相同(填“相同”或“不相
2 2
同”)______。
装置D中装的是五氧化二钒,当通入YX 时,打开K放入适量的氧气,在D装置中发生化
2
学反应方程式为________________,
②若装置B中装有5.0 mL 1.0×10-3mol/L的碘水,当通入足量W 完全反应后,转移了
2
5.0×10-5mol电子,该反应的化学方程式为_______________________________________。
(3)某同学将足量的YX 通入一支装有氯化钡溶液的试管,未见沉淀生成,向该试管中加
2
入适量(填字母)______________,可以看到白色沉淀产生。
A.氨水 B.稀盐酸 C.稀硝酸 D.氯化钙