文档内容
高一化学试题
说明:
1.本试卷分为第I卷(选择题)和第II卷(非选择题)两部分,考试时间90分钟,满分100
分。
2.第I卷(选择题)答案涂在答题卡上。第II卷必须用黑色中性笔作答,答案必须写在答题
卡各题目指定区域内相应的位置,不能写在试题卷上。
3.可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 Mg 24 S 32 Cl 35.5 K 39 Mn 55
Fe 56 Cu 64
第Ⅰ卷(选择题,共48分)
一、选择题(包括16个小题,每小题只有一个选项符合题意,每小题3分,共48分)
1.化学科学的形成、发展与应用过程中,下列科学家与其成就不相对应的是( )
A. 英国科学家波义尔提出化学元素的概念
B. 法国科学家拉瓦锡提出原子论
C. 意大利科学家阿伏加德罗提出分子学说
D. 我国科学家屠呦呦发现了青蒿素,有效降低了疟疾患者的死亡率
2.下列表格中物质的类别与其对应的物质都正确的是( )
选项 酸 碱 盐 碱性氧化物 电解质
A 醋酸 纯碱 明矾 生石灰 水
B 次氯酸 氢氧化铁 高锰酸钾 氧化锂 硫酸钡
C 硝酸 烧碱 五氯化磷 过氧化钠 盐酸
D 硫酸 熟石灰 小苏打 氧化镁 二氧化硫
A. A B. B C. C D. D
3.下列关于金属钠的叙述正确的是( )
A. 金属钠是银白色金属,密度大,熔点高
B. 金属钠硬度小,很容易用小刀切割成小块
C. 在空气中加热时,金属钠剧烈燃烧,产生黄色火焰和白色固体D. 将金属钠投入硫酸铜溶液中,钠迅速反应,产生红色固体
4.下列电解质的电离方程式书写不正确的是( )
A. HCO=2H++CO 2﹣ B. Ca(OH) =Ca2++2OH﹣
2 3 3 2
C. KNO=K++NO﹣ D. (NH )SO =2NH ++SO2﹣
3 3 4 2 4 4 4
5.下列对氧化还原反应的认识正确的是( )
A. 具有氧化性的物质在化学反应中一定作氧化剂
B. 氧化还原反应的本质是化合价发生变化
C. 还原剂具有还原性, 在反应中被还原,得到还原产物
D. 置换反应一定是氧化还原反应,复分解反应一定不属于氧化还原反应
6.下列关于氯气的叙述不正确的是( )
A. 氯气是一种黄绿色、有刺激性气味、有毒的气体
B. 氯气溶于水得到浅黄绿色的氯水,该过程涉及化学变化
C. 氯气化学性质活泼,因此自然界中不存在游离态的氯元素
D. 氢气在盛有氯气的集气瓶中燃烧,产生苍白色火焰和白烟
7.下列叙述与胶体性质有关的是( )
A. 利用醋酸除去锅炉中的水垢
B. 家用滤芯式净水器中利用活性炭净水
C. 清晨在树林中可以看到一缕缕光束
D. 向氯化铁溶液中滴加氢氧化钠溶液产生红褐色沉淀
8.下表中有关物质用途、性质的叙述均正确,且有因果关系的是( )
选项 用途 性质
A 钠钾合金用作原子反应堆的导热剂 钠化学性质很活泼
B KI可用于制作加碘盐 I﹣具有还原性,易被氧化为I
2
C 84消毒液用于环境消毒 NaClO与HO、CO 反应生成HClO
2 2
D NaCO 用作食品膨松剂 NaCO 遇酸能产生气体
2 3 2 3
A. A B. B C. C D. D
9.下列氯化物中,既能由金属和氯气直接化合制得,又能由金属和盐酸反应制得的是( )
①CuCl ②FeCl ③MgCl ④ZnCl
2 2 2 2A. ③④ B. ②③ C. ②③④ D. ①②③④
10.用N 代表阿伏加德罗常数的数值,下列说法正确的是( )
A
.
A N 个臭氧分子(O )与N 个二氧化碳分子质量相等
A 3 A
B. 常温常压下,2.24L氮气含有的氮原子数大于0.2N
A
C. 2.3g金属钠与足量氧气完全反应,转移电子数为0.1N
A
D. 100mL0.5mol·L﹣1硫酸溶液中含有0.05N 个HSO 分子
A 2 4
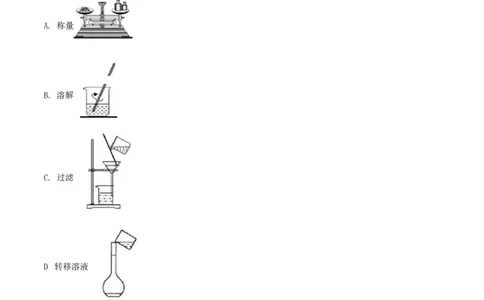
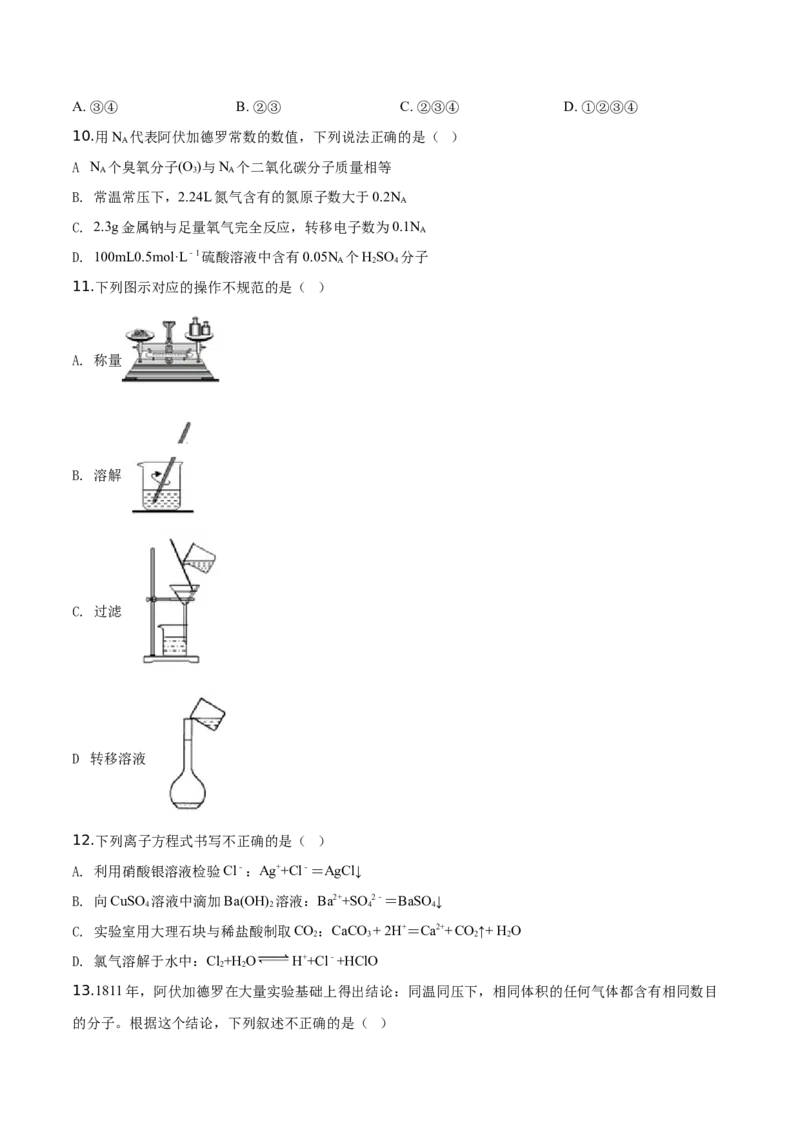
11.下列图示对应的操作不规范的是( )
A. 称量
B. 溶解
C. 过滤
.
D 转移溶液
12.下列离子方程式书写不正确的是( )
A. 利用硝酸银溶液检验Cl﹣:Ag++Cl﹣=AgCl↓
B. 向CuSO 溶液中滴加Ba(OH) 溶液:Ba2++SO2﹣=BaSO↓
4 2 4 4
C. 实验室用大理石块与稀盐酸制取CO:CaCO + 2H+=Ca2++ CO↑+ H O
2 3 2 2
D. 氯气溶解于水中:Cl+H O H++Cl﹣+HClO
2 2
13.1811年,阿伏加德罗在大量实验基础上得出结论:同温同压下,相同体积的任何气体都含有相同数目
的分子。根据这个结论,下列叙述不正确的是( )A. 同温同压下,等质量的氮气和一氧化碳体积相同
B. 同温同压下,等体积的两种气体原子数不一定相等
C. 同温同压下,气体 的体积与分子数成正比
D. 两种分子数和体积都相等的气体,所处的温度和压强一定相同
14.4℃时,100mL水中溶解了33.6L(STP)HCl气体,所得盐酸密度为1.18g·mL﹣1。下列有关说法不正确的
是( )
A. 该盐酸的物质的量浓度为15mol·L﹣1
B. 该盐酸溶质的质量分数为35.4%
C. 该温度下HCl的溶解度可能大于336(气体溶解度以体积比计算)
D. 相同条件下,一定量水中溶解HCl气体越多,所得盐酸密度越大
15.高铁酸钠(Na FeO)具有强氧化性,是一种新型高效水处理剂。高铁酸钠投入水中发生反应:NaFeO+
2 4 2 4
HO→Fe(OH) (胶体)+NaOH+O ↑(未配平)。下列有关说法正确的是( )
2 3 2
A. 氧气的氧化性强于高铁酸钠
B. Fe(OH) (胶体)在水处理过程中能起到杀菌消毒作用
3
C. 该反应中O 是氧化产物,NaOH既不是氧化产物也不是还原产物
2
D. 1mol高铁酸钠的消毒能力(依据反应中转移电子数计)相当于3mol氯气
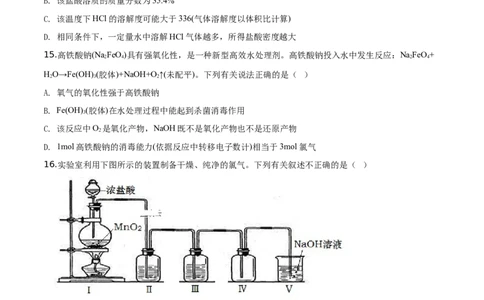
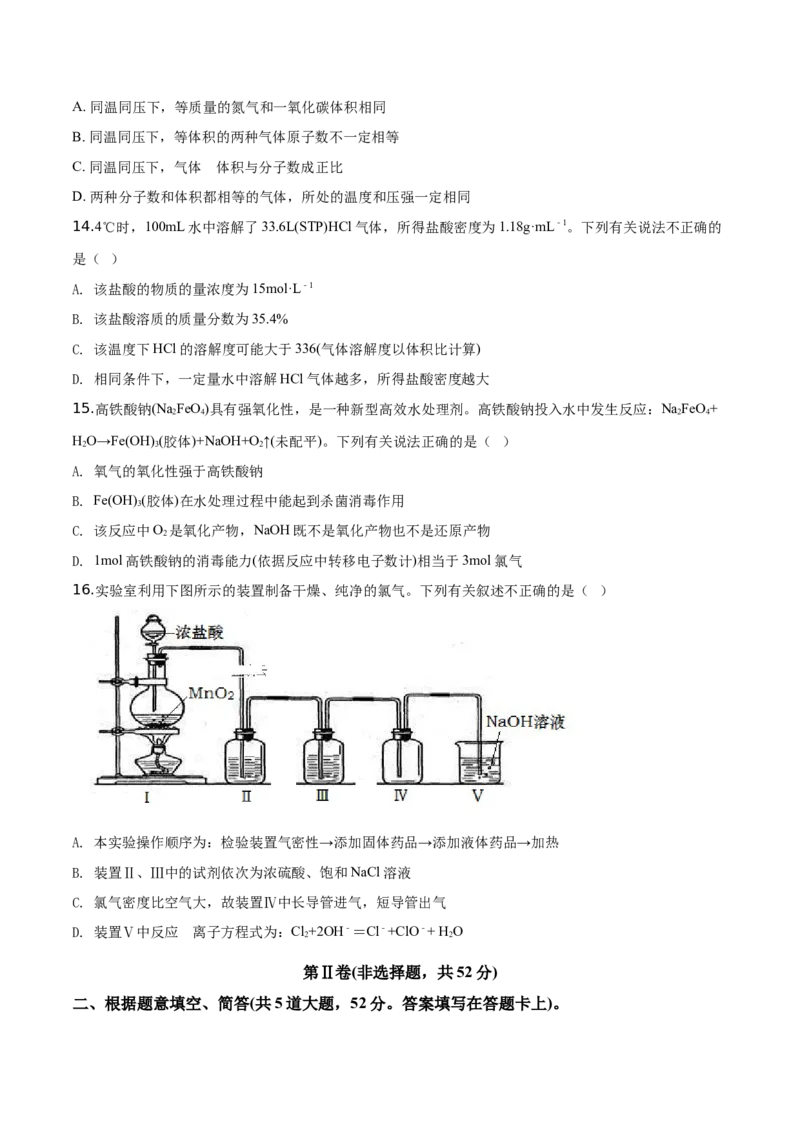
16.实验室利用下图所示的装置制备干燥、纯净的氯气。下列有关叙述不正确的是( )
A. 本实验操作顺序为:检验装置气密性→添加固体药品→添加液体药品→加热
B. 装置Ⅱ、Ⅲ中的试剂依次为浓硫酸、饱和NaCl溶液
C. 氯气密度比空气大,故装置Ⅳ中长导管进气,短导管出气
D. 装置Ⅴ中反应 的离子方程式为:Cl+2OH﹣=Cl﹣+ClO﹣+ H O
2 2
第Ⅱ卷(非选择题,共52分)
二、根据题意填空、简答(共5道大题,52分。答案填写在答题卡上)。17.下图为实验室某浓硫酸试剂瓶标签上的相关数据,据此回答有关问题:
(1)该浓硫酸物质的量浓度为________________。
(2)取用任意体积的该浓硫酸时,下列物理量中不随所取体积的多少而变化的是_________(填字母序号)。
a.溶液中HSO 的物质的量 b.溶液的浓度 c.溶液的密度
2 4
(3)某同学欲用上述浓硫酸和蒸馏水配制500mL0.400mol·L﹣1的稀硫酸。提供的仪器有:胶头滴管、玻璃
棒、烧杯、量筒、细口试剂瓶。
①配制稀硫酸时,还缺少的仪器有_______________(写名称),该仪器上标有_____(填字母序号)。
a.温度 b.浓度 c.容量 d.压强 e.刻度线
②该学生需要量取_________mL上述浓硫酸进行配制。
③在配制过程中,下列实验操作对所配制得稀硫酸的物质的量浓度有何影响? (在横线上填写“偏大”、“偏
小”或“无影响”)用量筒量取浓硫酸时俯视观察凹液面__________________;定容、摇匀后静置,液面低于
刻度线,继续加水至刻度线________________。
18.现有四种溶液:A.盐酸B.稀硫酸C.NaOH溶液D.Ba(OH) 溶液。这些溶液溶质物质的量浓度均为
2
0.3mol/L。根据溶液取用情况,判断得到的溶液中存在的主要离子及其浓度;或者根据最终离子的情况,
推断最终溶液可能是哪些溶液按怎样的体积比混合的结果(忽略溶液混合后的体积变化)
溶液取用情况 溶液中存在的主要离子及其浓度
溶液A和B按体积比2:1混合 ①____________
②____________ Na+和Cl﹣物质的量浓度均为0.15 mol/L
等体积混合溶液B和C ③____________
溶液A和D按体积比2:1混合 ④____________
Ba2+物质的量浓度为0.1 mol/L,OH﹣物质的量浓度为0.2
⑤____________
mol/L
19.双氧水是一种“绿色试剂”,可作为矿业废液处理剂。如要消除采矿业废液中的氰化物(KCN),化学方程式为:KCN+H O+H O=X+NH ↑。
2 2 2 3
(1)生成物X的化学式为_________________。
(2)已知:上述反应中,N元素化合价不发生变化,则KCN中C元素的化合价为_____;该反应的氧化
剂是_______(填化学式)。
(3)双氧水作为“绿色试剂”的原因是____________________________________。
(4)在标准状况下有448L氨气生成时,转移的电子数为___________________。
20.粗盐含有泥沙以及Ca2+、Mg2+、SO 2﹣等杂质,其提纯过程一般经过以下流程:
4
某兴趣小组按上述方案进行粗盐提纯实验,实验室提供了粗盐样品、稀盐酸、NaOH溶液、BaCl 溶液、
2
NaCO 溶液等药品以及必备的实验仪器若干。请回答下列问题:
2 3
(1)操作①粗盐样品加水之前,需要将大颗粒粗盐变为细小颗粒或粉末,此时在实验室中需要用到的仪
器为__________。
(2)操作②、④过滤后的滤液仍有浑浊,需要进行的操作是___________________。
(3)操作③按abc顺序依次加入过量的试剂。若a为NaOH溶液,则c为________。加入c发生反应的离
子方程式为_________________________________________________。
(4)加盐酸调溶液pH的目的是________________________________。
(5)步骤⑥操作名称是______________。
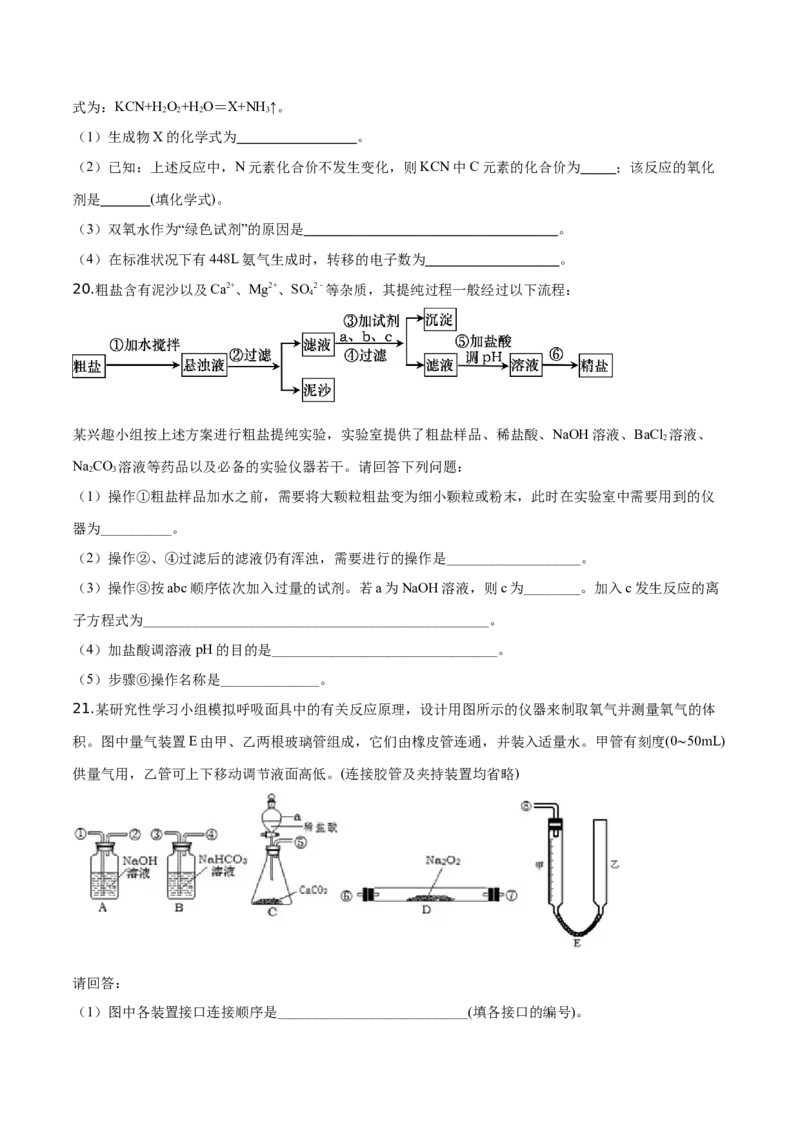
21.某研究性学习小组模拟呼吸面具中的有关反应原理,设计用图所示的仪器来制取氧气并测量氧气的体
积。图中量气装置E由甲、乙两根玻璃管组成,它们由橡皮管连通,并装入适量水。甲管有刻度(0 50mL)
供量气用,乙管可上下移动调节液面高低。(连接胶管及夹持装置均省略) ∼
请回答:
(1)图中各装置接口连接顺序是___________________________(填各接口的编号)。(2)装置A的作用是______________,反应的化学方程式为________________。
(3)装置B的作用是________________,反应的离子方程式为______________。
(4)装置C中仪器a的名称是______;装置D中反应的化学方程式为________。
(5)实验结束读取氧气体积时,若乙中液面高于甲中液面,会使测得的氧气体积___(填偏大、偏小、无影
响)。若有影响,应向__________(填“上”或“下”)移动乙管,使甲乙液面相平(注:若第一格填无影响,第二
格不用填写)。