文档内容
高一模拟选课调考
化学
考生注意:
1.本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分,共 100 分。考试时间 90 分钟。
2 请将各题答案填写在答题卡上。
3.本试卷主要考试内容:人教版必修第一册第一、二章。
4.可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 S 32 Fe 56 Ba 137
第Ⅰ卷(选择题共 40 分)
一、单项选择题:本题包括 10 小题,每小题 2 分,共计 20 分。每小题只有一个选项符合题意。
1.下列古诗词的描述中发生的是化学变化的是( )
A. 千淘万漉虽辛苦,吹尽狂沙始到金
B. 忽如一夜春风来,千树万树梨花开
C. 春蚕到死丝方尽,蜡炬成灰泪始干
D. 日照香炉生紫烟,遥看瀑布挂前川
2.下列图标与名称对应不相符的是( )
A. 锐器 B. 明火 C. 用电 D. 洗手
3.科学实验研究结果表明:某种固体单质(由单原子构成)在棱长为 1×10-7cm 的立方体中含有 20 个原子,其
密度为 4g·cm-3。则此单质的相对原子质量最接近( )
A. 32 B. 65 C. 120 D. 150
4.下列生活中的常见操作或现象中不涉及氧化还原反应的是( )
A. 家用天然气的燃烧为炒菜提供热量
B. 烧菜用过的铁锅经水洗后常出现红棕色锈迹
.
C 洗涤剂清洗油污
D. 饭菜久置后变质腐败
5.贮存 Cl 的钢瓶上应贴的标签为( )
2
A. 有毒品 B. 爆炸品 C. 易燃品 D. 腐蚀品
6.常温下,下列分散系中最稳定的是( )A. 泥水 B. 豆浆 C. 氢氧化铁胶体 D. 氯化钠溶液
7.KClO 在酸性溶液中可将 VO2+氧化成 VO + ,而自身被还原为 Cl-。欲使 3 mol VO +成 VO2+ ,则需要氧化
3 2 2
剂KClO 的物质的量是( )
3
A. 0.2 mol B. 0.5mol C. 1 mol D. 3mol
8.下列各组仪器:①集气瓶②漏斗③分液漏斗④容量瓶⑤托盘天平⑥胶头滴管⑦蒸馏烧瓶⑧量筒。其中常
用于物质分离的有
.
A ②③⑦ B. ②⑥⑦ C. ①④⑧ D. ④⑥⑧
9.新制氯水在干燥的空气中久置后,下列微粒在溶液中的数增加的是( )
A. Cl B. Cl- C. HCIO D. HO
2 2
10.下列实验方法能达到实验目的的是( )
A. 用 NaOH 溶液除去 H 中混有的少量 HCl
2
B. 用导电性实验区分 NaCl 和 KCl
C. 通过冷却热饱和溶液的方法提纯混有少量 KCl 的 NaCl
D. 用铂丝蘸取某溶液后灼烧,火焰呈黄色,证明该溶液 NaSO 溶液
2 4
二、不定项选择题:本题包括 5 小题,每小题 4 分,共计 20 分。每小题只有一个或两个选项符合
题意。若正确 答案只包括一个选项,多选时,该小题得 0 分;若正确答案包括两个选项,只选一个
且正确的得 2 分,选两个且 都正确的得满分,只要选错一个,该小题就得 0 分。
11.设 N 为阿伏加德罗常数的值,下列说法正确的是( )
A
A. 18g H O 中含有 的质子数为 10 N
2 A
B. 0.5 mol·L-1 H SO 溶液中含有的 H+数目为N
2 4 A
C. 1 mol CO 与 0.5molO 反应后的原子数为 3 N
2 A
D. NaO 与水反应,生成 1mol O 时转移电子数为 4 N
2 2 2 A
12.下列实验中的颜色变化,与氧化还原反应有关的是( )
A B C D
NaOH溶液滴入 石蕊溶液滴入稀盐 NaCl 溶 液 滴 入 热铁钉插入硫酸铜
实验
FeCl 3 溶液中 酸中 AgNO 中 溶液中
3
现象 生成红褐色沉淀 溶液变红 有白色沉淀生成 铁钉表面有红色物质产生
A. A B. B C. C D. D13.常温下,下列各组离子在指定溶液中能大量共存的是( )
A. 0.1mol·L-1 H SO 溶液: Na+、Mg2+、NO - 、Cl-
2 4 3
B. c(H+)=0.1 mol·L-1 的溶液: Mg2+、K+、SO 2-、Cl-
4
C. 与 Zn 反应放出 H 的溶液: H+、K+、NO - 、CO2-
2 3 3
D. 0.1 mol·L-1NaOH 溶液: Ca2+、Na+、SO 2-、HCO -
4 3
14.将 mg 密度为 1.42 g·cm-3 的硫酸加入足量的 Ba(NO ) 溶液中,分反应后,过滤、干燥、称重,发现沉
3 2
淀的质量也为 mg,则加入的硫酸中溶质的物质的量浓度约为( )
.
A 5.38 mol·L-1. B. 6. 09 mol·L-1. C. 7.42 mol·L-1 D. 8.25 mol.L-I
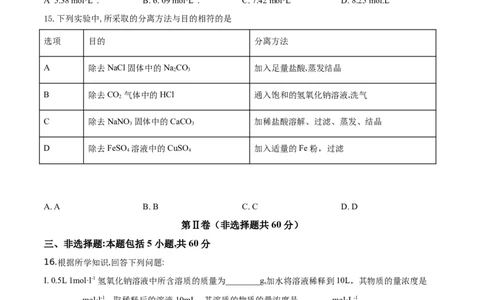
15.下列实验中,所采取的分离方法与目的相符的是
选项 目的 分离方法
A 除去 NaCl 固体中的 NaCO 加入足量盐酸,蒸发结晶
2 3
B 除去 CO 气体中的 HCl 通入饱和的氢氧化钠溶液,洗气
2
C 除去 NaNO 固体中的 CaCO 加稀盐酸溶解、过滤、蒸发、结晶
3 3
D 除去 FeSO 溶液中的 CuSO 加入适量的 Fe 粉,过滤
4 4
A. A B. B C. C D. D
第Ⅱ卷(非选择题共 60 分)
三、非选择题:本题包括 5 小题,共 60 分
16.根据所学知识,回答下列问题:
I. 0.5L 1mol·l-1 氢氧化钠溶液中所含溶质的质量为________g,加水将溶液稀释到10L,其物质的量浓度是
_________mol·l-1,取稀释后的溶液 10mL,其溶质的物质的量浓度是________mol·L-1.
Ⅱ.标准状况下,比较等物质的量 HS、NH 、CH 三种气体,并完成下列填空。
2 3 4
(1)体积之比________
(2)质量之比为________
(3)原子数之比为________
(4)氢原子数之比为________
17.NaHCO 是生活中常见的物质,请回答下列问题:
3
(1)写出 NaHCO 在水溶液中电离的方程: ________
3(2)NaHCO 属于“酸”、“碱”、“盐”中的________
3
(3)①写出 NaHCO 溶液与 NaOH 溶液反应的离子方程式________
3
②写出足量的NaHCO 溶液与澄清石灰水反应的离子方程式________
3
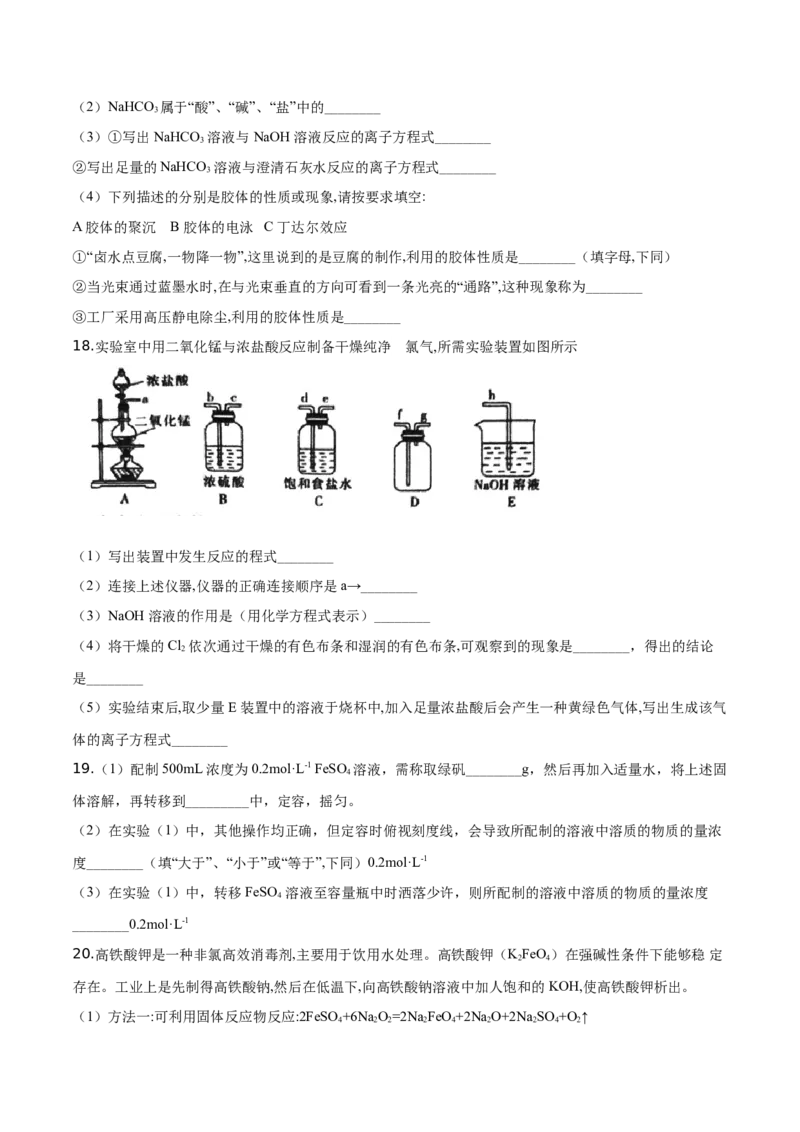
(4)下列描述的分别是胶体的性质或现象,请按要求填空:
A 胶体的聚沉 B 胶体的电泳 C 丁达尔效应
①“卤水点豆腐,一物降一物”,这里说到的是豆腐的制作,利用的胶体性质是________(填字母,下同)
②当光束通过蓝墨水时,在与光束垂直的方向可看到一条光亮的“通路”,这种现象称为________
③工厂采用高压静电除尘,利用的胶体性质是________
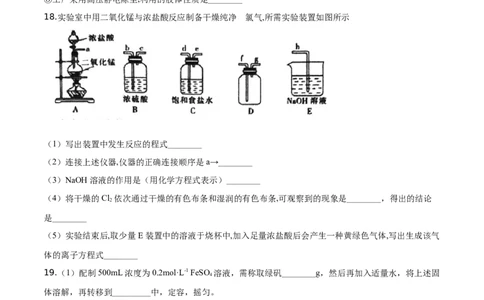
18.实验室中用二氧化锰与浓盐酸反应制备干燥纯净 的氯气,所需实验装置如图所示
(1)写出装置中发生反应的程式________
(2)连接上述仪器,仪器的正确连接顺序是 a→________
(3)NaOH 溶液的作用是(用化学方程式表示)________
(4)将干燥的 Cl 依次通过干燥的有色布条和湿润的有色布条,可观察到的现象是________,得出的结论
2
是________
(5)实验结束后,取少量 E 装置中的溶液于烧杯中,加入足量浓盐酸后会产生一种黄绿色气体,写出生成该气
体的离子方程式________
19.(1)配制 500mL 浓度为 0.2mol·L-1 FeSO 溶液,需称取绿矾________g,然后再加入适量水,将上述固
4
体溶解,再转移到_________中,定容,摇匀。
(2)在实验(1)中,其他操作均正确,但定容时俯视刻度线,会导致所配制的溶液中溶质的物质的量浓
度________(填“大于”、“小于”或“等于”,下同)0.2mol·L-1
(3)在实验(1)中,转移 FeSO 溶液至容量瓶中时洒落少许,则所配制的溶液中溶质的物质的量浓度
4
________0.2mol·L-1
20.高铁酸钾是一种非氯高效消毒剂,主要用于饮用水处理。高铁酸钾(KFeO)在强碱性条件下能够稳 定
2 4
存在。工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加人饱和的 KOH,使高铁酸钾析出。
(1)方法一:可利用固体反应物反应:2FeSO+6Na O=2Na FeO+2Na O+2Na SO +O ↑
4 2 2 2 4 2 2 4 2①生成物 NaFeO 中铁元素的化合价为________
2 4
②该反应中的还原剂是________,每生成 1mol Na FeO 转移_______mol 电子。
2 4
(2)方法二:
反应:Fe(OH)+ClO-+OH-——FeO2-+Cl- +H O(未配平)
3 4 2
① 配平离子反应方程式:_____Fe(OH)+______ClO-+_____OH-=_____FeO 2-+______Cl- +________H O
3 4 2
②若反应过程中转移了 3mol 电子,则还原产物的物质的量为_______mol
(3)向 NaFeO 溶液中加入适量饱和的 KOH 溶液,有 KFeO 析出,请写出该反应的化学方程式________
2 4 2 4