文档内容
竞赛试题资源库——实验操作、设计、定量
1i.某学生用量筒量取液体,将量筒平放且面对刻度平视测量。初次视线与量筒内凹液面
的最低处保持水平,读数为20mL。倒出部分液体后,俯视凹液面的最低处,读数为5mL,则
该学生实际倒出液体的体积
A 大于15mL B 小于15mL C 等于15mL D 无法确定
2ii.如下图所示,夹子开始处于关闭状态,
将液体A滴入试管②与气体B充分反应,打开
夹子,可发现试管①内的水立刻沸腾了。则液
体A和气体B的组合可能是下列的
A 氢氧化钠溶液、二氧化碳
B 硫酸、氮气
C 酒精、氧气
D 水、一氧化碳
3iii.烟道气中含有CO、CO、N、O 和其他一些杂质。为测定其中各气体的含量,先把有
2 2 2
害气体和其他杂质除去,使气体仅为上述四种气体的混合物。在测定时,用不同的试剂按一
定顺序从混合气中分别吸收各种气体,最后剩下的是不能吸收的N,通过每次吸收前后气体
2
体积变化的数据按一定的计算方法求出气体分别的含量。已知:①吸收O 用苯三酚的碱性溶
2
液,它可以把O 吸收得相当完全。②用CuCl的氨溶液吸收CO,为防止CuCl的氧化,在该溶
2
液中加一些铜丝。这样吸收CO效率很高。③用KOH吸收CO,非常完全。④N 不被吸收,最
2 2
后剩余的气体中有它。试回答:
(1)为防止干扰,吸收的气体先后顺序为
(2)若把吸收CO 与吸收O 的顺序颠倒,会引起的后果
2 2
(3)若把吸收O 与吸收CO的顺序颠倒,会产生的后果
2
(4)通过吸收CO、CO、O 各试剂后剩余气体有三种,并检测得他们有三种元素,他们是
2 2
(5)为准确测定剩余气体中N 的体积,还要将该气体用 处理后,才能检测出
2
N 的体积。
2
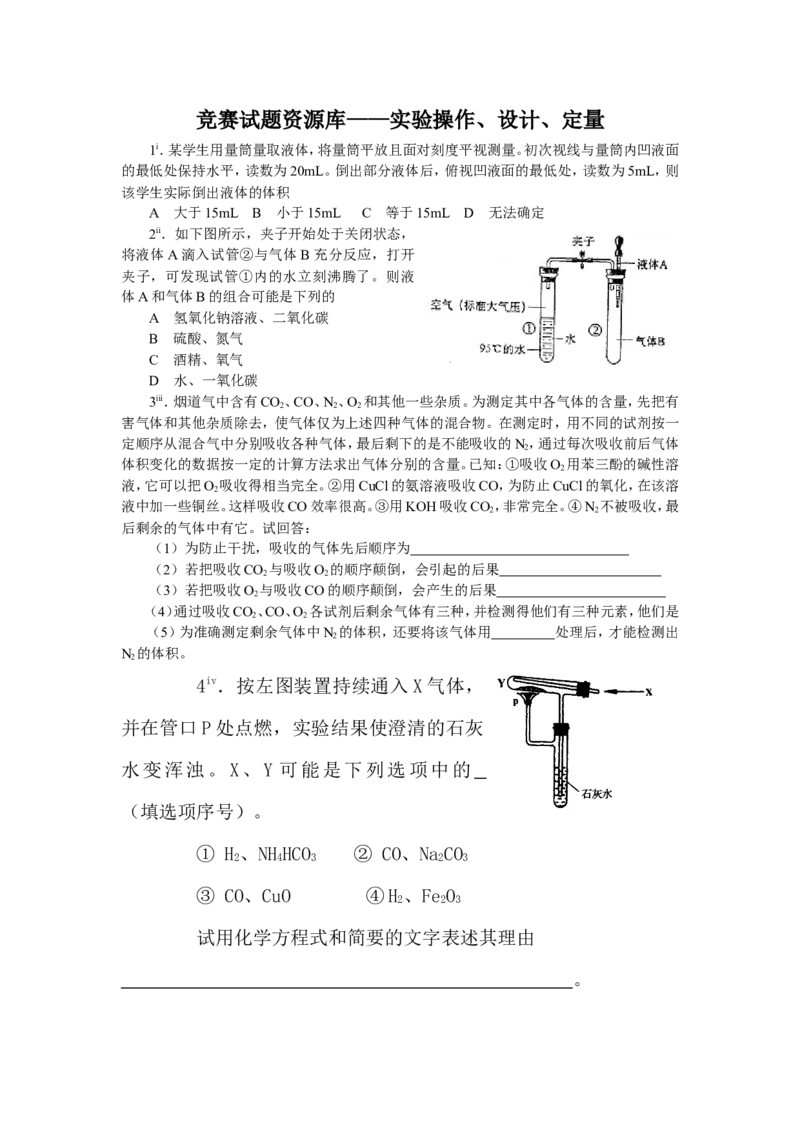
4iv.按左图装置持续通入 X 气体,
并在管口 P 处点燃,实验结果使澄清的石灰
水变浑浊。X、Y 可能是下列选项中的
(填选项序号)。
① H 、NH HCO ② CO、Na CO
2 4 3 2 3
③ CO、CuO ④H 、Fe O
2 2 3
试用化学方程式和简要的文字表述其理由
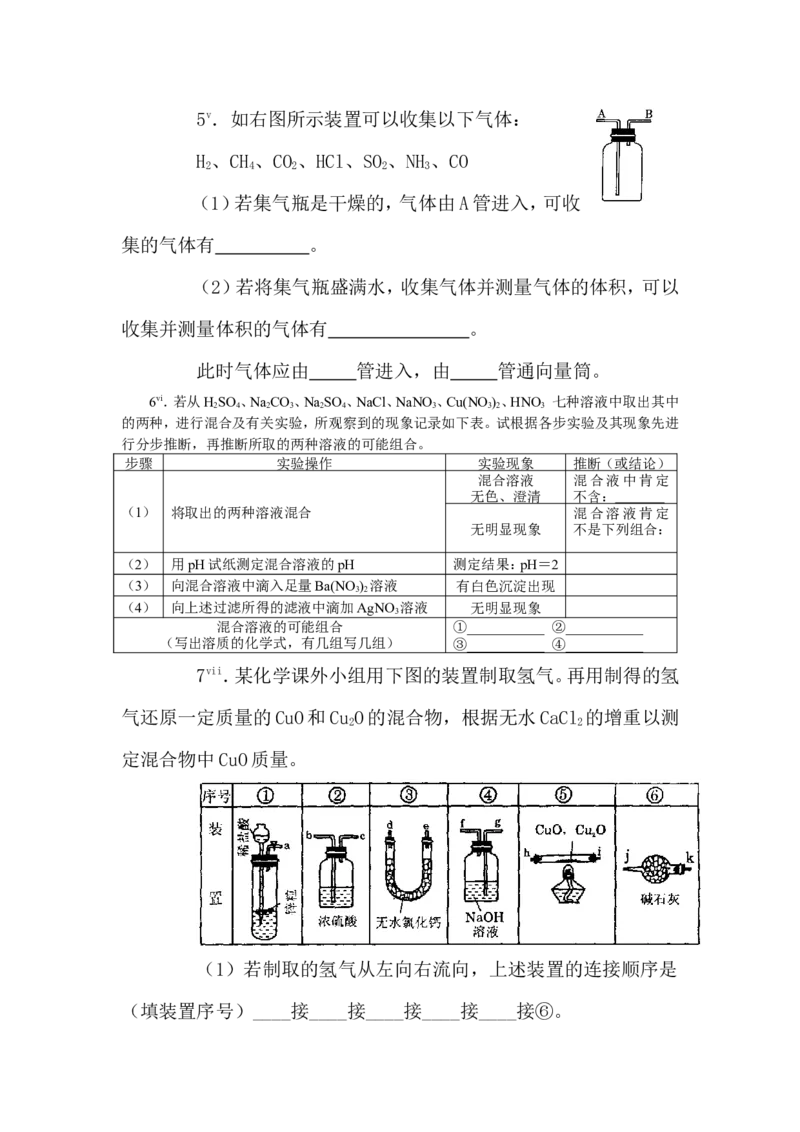
。5v.如右图所示装置可以收集以下气体:
H 、CH 、CO 、HCl、SO 、NH 、CO
2 4 2 2 3
(1)若集气瓶是干燥的,气体由A管进入,可收
集的气体有 。
(2)若将集气瓶盛满水,收集气体并测量气体的体积,可以
收集并测量体积的气体有 。
此时气体应由 管进入,由 管通向量筒。
6vi.若从HSO 、NaCO、NaSO 、NaCl、NaNO、Cu(NO)、HNO 七种溶液中取出其中
2 4 2 3 2 4 3 3 2 3
的两种,进行混合及有关实验,所观察到的现象记录如下表。试根据各步实验及其现象先进
行分步推断,再推断所取的两种溶液的可能组合。
步骤 实验操作 实验现象 推断(或结论)
混合溶液 混合液中肯定
无色、澄清 不含:
(1) 将取出的两种溶液混合 混合溶液肯定
无明显现象 不是下列组合:
(2) 用pH试纸测定混合溶液的pH 测定结果:pH=2
(3) 向混合溶液中滴入足量Ba(NO ) 溶液 有白色沉淀出现
3 2
(4) 向上述过滤所得的滤液中滴加AgNO 溶液 无明显现象
3
混合溶液的可能组合 ①___________ ②___________
(写出溶质的化学式,有几组写几组) ③___________ ④___________
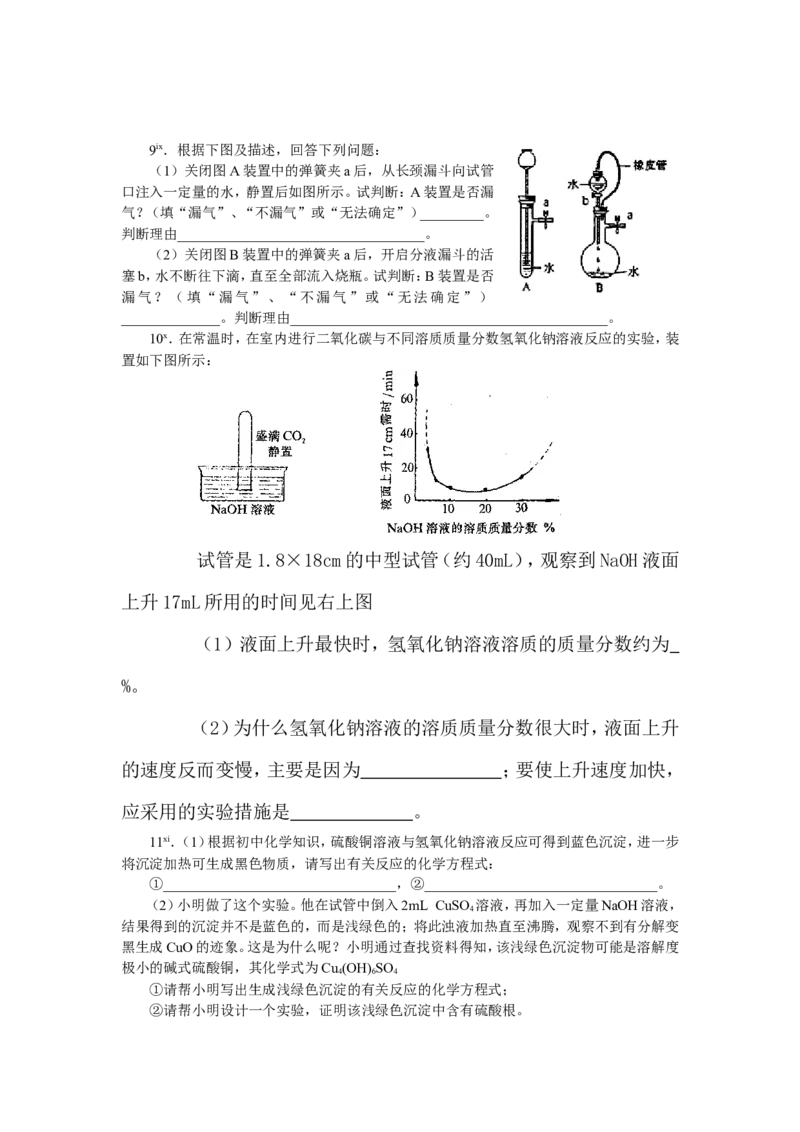
7vii.某化学课外小组用下图的装置制取氢气。再用制得的氢
气还原一定质量的CuO和Cu O的混合物,根据无水CaCl 的增重以测
2 2
定混合物中CuO质量。
(1)若制取的氢气从左向右流向,上述装置的连接顺序是
(填装置序号)____接____接____接____接____接⑥。(2)制取干燥、纯净的氢气时,所需装置的连接顺序是(填各
接口的代码字母)____接____,____接____。
(3)若测得CuO、Cu O混合物的总质量为Wg;混合物全部还
2
原后U型管增重mg,则混合物中CuO的质量为 g。
(4)装置最后连接盛有碱石灰的干燥管的目的是 ,
若不连接此装置,则测得的混合物中CuO的质量 (填偏大、偏小
或无影响)。
(5)若反应后所得红色物质中有少量的Cu O,则测得的混合
2
物中CuO的质量_______(填偏大、偏小或无影响)。
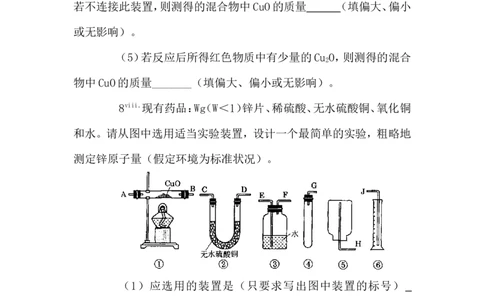
8viii.现有药品:Wg(W<1)锌片、稀硫酸、无水硫酸铜、氧化铜
和水。请从图中选用适当实验装置,设计一个最简单的实验,粗略地
测定锌原子量(假定环境为标准状况)。
(1)应选用的装置是(只要求写出图中装置的标号)
。
(2)所用装置的连接顺序是(填各接口的字母,连接胶管省
略) 。
(3)操作中,怎样加放试剂以保证不漏出氢气?
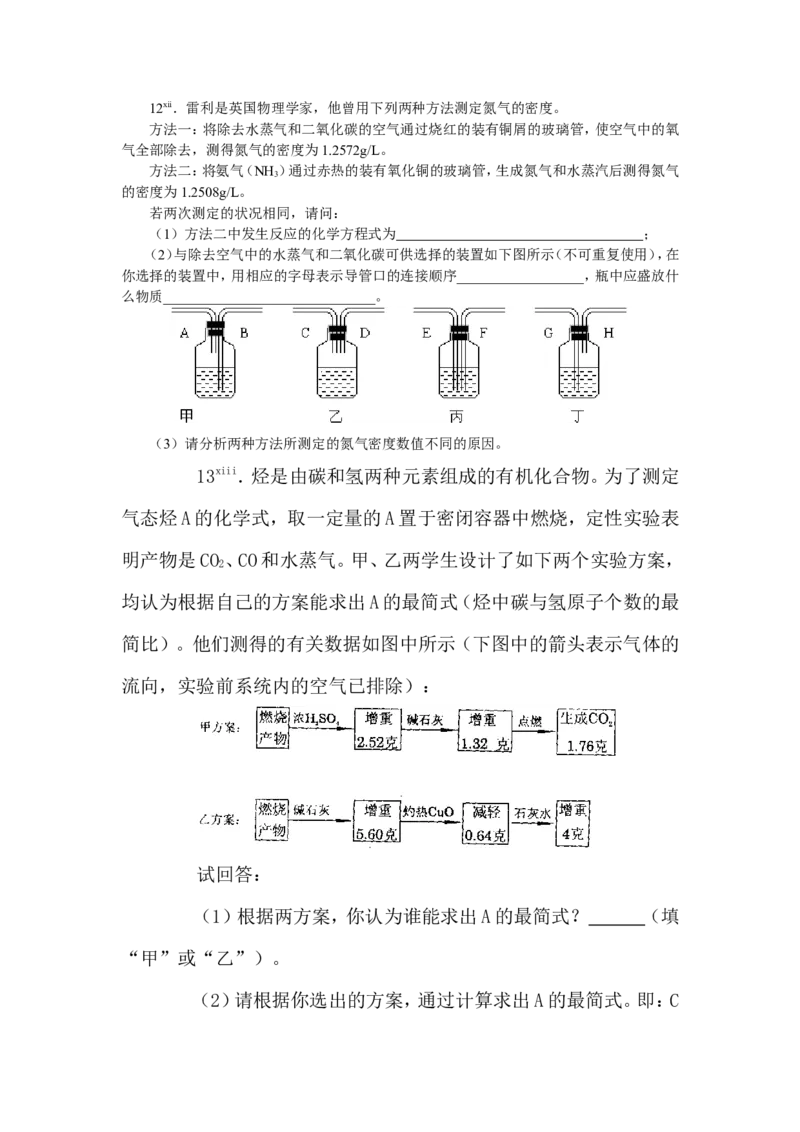
。9ix.根据下图及描述,回答下列问题:
(1)关闭图A装置中的弹簧夹a后,从长颈漏斗向试管
口注入一定量的水,静置后如图所示。试判断:A装置是否漏
气?(填“漏气”、“不漏气”或“无法确定”)_________。
判断理由___________________________________。
(2)关闭图B装置中的弹簧夹a后,开启分液漏斗的活
塞b,水不断往下滴,直至全部流入烧瓶。试判断:B装置是否
漏气?(填“漏气”、“不漏气”或“无法确定”)
______________。判断理由_____________________________________________。
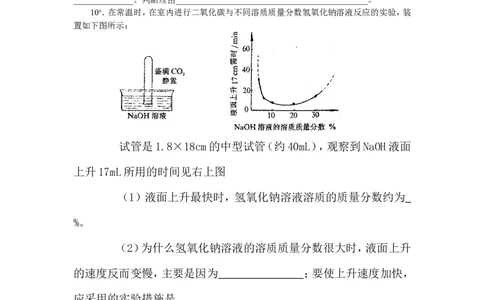
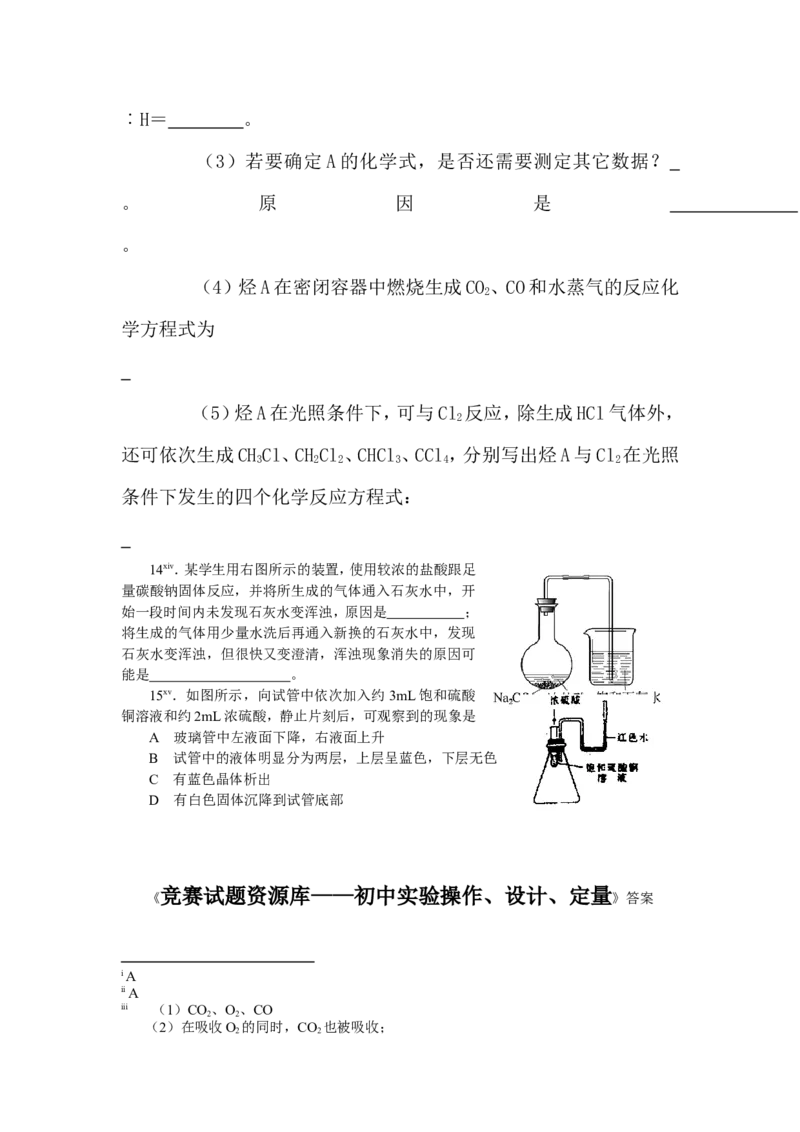
10x.在常温时,在室内进行二氧化碳与不同溶质质量分数氢氧化钠溶液反应的实验,装
置如下图所示:
试管是1.8×18cm的中型试管(约40mL),观察到NaOH液面
上升17mL所用的时间见右上图
(1)液面上升最快时,氢氧化钠溶液溶质的质量分数约为
%。
(2)为什么氢氧化钠溶液的溶质质量分数很大时,液面上升
的速度反而变慢,主要是因为 ;要使上升速度加快,
应采用的实验措施是 。
11xi.(1)根据初中化学知识,硫酸铜溶液与氢氧化钠溶液反应可得到蓝色沉淀,进一步
将沉淀加热可生成黑色物质,请写出有关反应的化学方程式:
①_________________________________,②_________________________________。
(2)小明做了这个实验。他在试管中倒入2mL CuSO 溶液,再加入一定量NaOH溶液,
4
结果得到的沉淀并不是蓝色的,而是浅绿色的;将此浊液加热直至沸腾,观察不到有分解变
黑生成CuO的迹象。这是为什么呢?小明通过查找资料得知,该浅绿色沉淀物可能是溶解度
极小的碱式硫酸铜,其化学式为Cu (OH) SO
4 6 4
①请帮小明写出生成浅绿色沉淀的有关反应的化学方程式;
②请帮小明设计一个实验,证明该浅绿色沉淀中含有硫酸根。12xii.雷利是英国物理学家,他曾用下列两种方法测定氮气的密度。
方法一:将除去水蒸气和二氧化碳的空气通过烧红的装有铜屑的玻璃管,使空气中的氧
气全部除去,测得氮气的密度为1.2572g/L。
方法二:将氨气(NH )通过赤热的装有氧化铜的玻璃管,生成氮气和水蒸汽后测得氮气
3
的密度为1.2508g/L。
若两次测定的状况相同,请问:
(1)方法二中发生反应的化学方程式为 ;
(2)与除去空气中的水蒸气和二氧化碳可供选择的装置如下图所示(不可重复使用),在
你选择的装置中,用相应的字母表示导管口的连接顺序__________________,瓶中应盛放什
么物质______________________________。
(3)请分析两种方法所测定的氮气密度数值不同的原因。
13xiii.烃是由碳和氢两种元素组成的有机化合物。为了测定
气态烃A的化学式,取一定量的A置于密闭容器中燃烧,定性实验表
明产物是CO 、CO和水蒸气。甲、乙两学生设计了如下两个实验方案,
2
均认为根据自己的方案能求出A的最简式(烃中碳与氢原子个数的最
简比)。他们测得的有关数据如图中所示(下图中的箭头表示气体的
流向,实验前系统内的空气已排除):
试回答:
(1)根据两方案,你认为谁能求出A的最简式? (填
“甲”或“乙”)。
(2)请根据你选出的方案,通过计算求出A的最简式。即:C︰H= 。
(3)若要确定 A 的化学式,是否还需要测定其它数据?
。 原 因 是
。
(4)烃A在密闭容器中燃烧生成CO 、CO和水蒸气的反应化
2
学方程式为
(5)烃A在光照条件下,可与Cl 反应,除生成HCl气体外,
2
还可依次生成CH Cl、CH Cl 、CHCl 、CCl ,分别写出烃A与Cl 在光照
3 2 2 3 4 2
条件下发生的四个化学反应方程式:
14xiv.某学生用右图所示的装置,使用较浓的盐酸跟足
量碳酸钠固体反应,并将所生成的气体通入石灰水中,开
始一段时间内未发现石灰水变浑浊,原因是 ;
将生成的气体用少量水洗后再通入新换的石灰水中,发现
石灰水变浑浊,但很快又变澄清,浑浊现象消失的原因可
能是 。
15xv.如图所示,向试管中依次加入约3mL饱和硫酸
铜溶液和约2mL浓硫酸,静止片刻后,可观察到的现象是
A 玻璃管中左液面下降,右液面上升
B 试管中的液体明显分为两层,上层呈蓝色,下层无色
C 有蓝色晶体析出
D 有白色固体沉降到试管底部
竞赛试题资源库——初中实验操作、设计、定量
《 》答案
i A
ii A
iii (1)CO、O、CO
2 2
(2)在吸收O 的同时,CO 也被吸收;
2 2(3)在吸收CO的同时,O 可以氧化CuCl而被消耗;
2
(4)N、NH 、HO
2 3 2
(5)浓HSO 吸收。
2 4
iv ①、③ 选①是因为H 具有可燃性:2H +O 2HO H 与NH HCO 不反应,
2 2 2 2 2 4 3
NH HCO 受热分解。NH HCO NH ↑+CO↑+HO,CO 能使澄清石灰水变浑浊:
4 3 4 3 3 2 2 2
CO+Ca(OH)=CaCO ↓+HO。选③的理由是:CO可使CuO还原。CO+CuO Cu+
2 2 3 2
CO,生成的CO 能使澄清石灰水变浑浊:CO+Ca(OH)=CaCO ↓+HO,没有反应完
2 2 2 2 3 2
的CO可以燃烧:2CO+O 2CO。
2 2
v (1)HCl、CO、SO (2)H、CH、CO B A
2 2 2 4
vi HSO 与NaCO 或HNO 与NaCO 溶液呈酸性,所以一定有酸性物质存在。如HSO
2 4 2 3 3 2 3 2 4
或HNO HSO 或NaSO 或(HSO 和NaSO 同时共存) 不含NaCl ①HNO 、
3 2 4 2 4 2 4 2 4 3
HSO ;②HNO、NaSO ;③HSO 、NaSO ;④HSO 、NaNO
2 4 3 2 4 2 4 2 4 2 4 3
vii (1)①接④接②接⑤接③接⑥ (2)a、g、f、b、c (3)10m-5W/4
(4)防止无水CaCl 吸收空气中的水后使测定结果产生误差 偏大 (5)偏小
2
viii (1)③、④、 ⑥
(2)G、F、E、J
(3)向试管中加入足量稀HSO 后,将试管稍为倾斜,再把锌片放在试管内壁上,塞紧塞
2 4
子,慢慢直立,使锌片滑下与稀HSO 反应。
2 4
(4)22.4W/VH
2
ix (1)不漏气 由于不漏气,加水后试管内气体体积减小,导致压强增大,长颈漏斗内的
水面高出试管内的水面。
(2)无法确定 由于分液漏斗和烧瓶间有橡皮管相连;使分液漏斗中液面上方和烧瓶上
方的压强相同,无论装置是否漏气,都不影响分液漏斗中的水滴入烧瓶。
x (1)20
(2)表面生成NaCO 膜阻碍CO 与NaOH反应,振荡试管,使不能生成NaCO 晶膜
2 3 2 2 3
xi (1)CuSO +2NaOH=Cu(OH) ↓+NaSO Cu(OH) CuO+HO
4 2 2 4 2 2
(2)①4CuSO +6NaOH= Cu (OH) SO +3NaSO
4 4 6 4 2 4
②将绿色的浊液过滤,并把得到的绿色沉淀用蒸馏水多次洗涤,至洗涤液中用BaCl 溶液
2
检验不出SO 2-后,用稀盐酸溶解绿色沉淀,此时再用BaCl 溶液检验,溶解液中有大量
4 2
白色BaSO 生成,表示浅绿色沉淀中有SO 2-。
4 4
xii (1)2NH +3CuO N+3HO+3Cu
3 2 2
(2)BAGH或GHBA 上述装置顺序中,第一个盛放NaOH溶液,第二个盛放浓HSO
2 4
(3)空气中含有少量密度比氮气大的气体,是的方法一的测定值偏高
xiii (1)甲
(2)1︰4
(3)不需要。A的最简式就是化学式
(4)4CH+7O 2CO+2CO+8HO
4 2 2 2
(5)CH+Cl CHCl+HCl ;CHCl+Cl CHCl+HCl ;CHCl+Cl
4 2 3 3 2 2 2 2 2 2
CHCl +HCl;CHCl +Cl CCl +HCl
3 3 2 4
xiv 挥发出来的HCl进入石灰水,与Ca(OH) 作用而阻碍了CO 与Ca(OH) 的作用
2 2 2
CO 与生成的CaCO 作用,生成Ca(HCO )
2 3 3 2
xv A、C