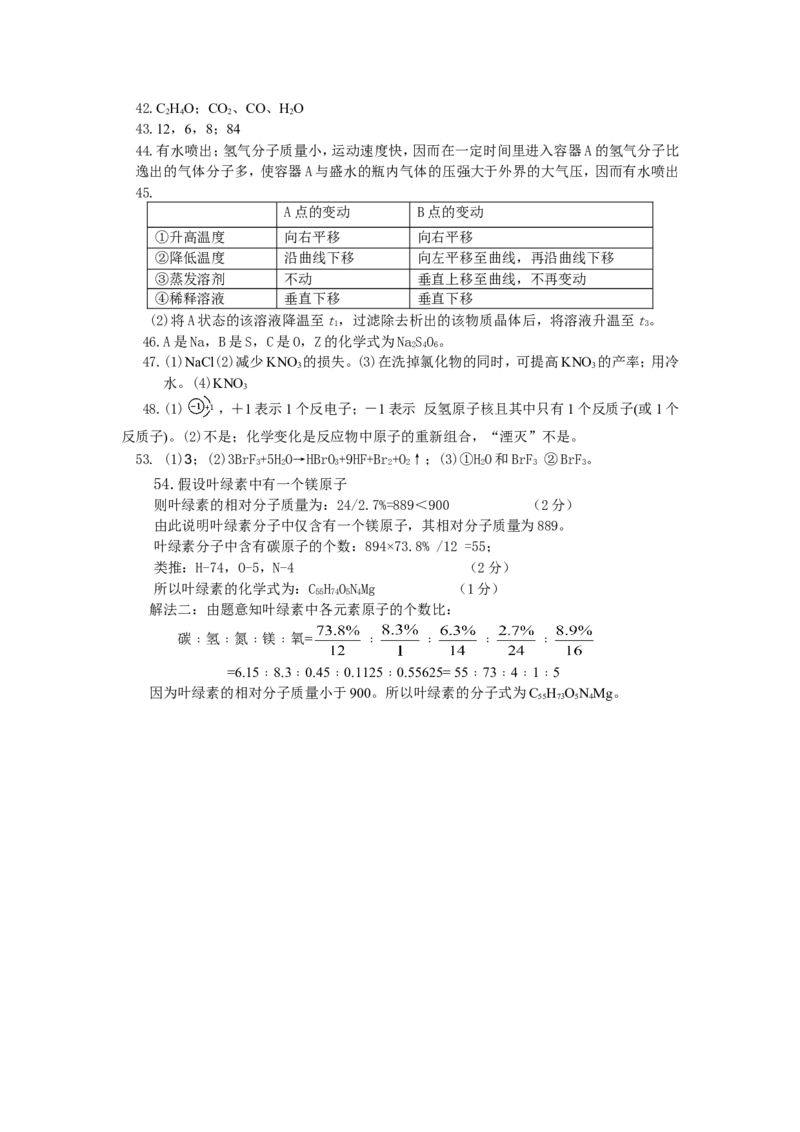文档内容
精选练习2—— 基本概念和基本理论
姓名________________
一、选择题:
2
+1 - +4 +2
5.有 H、O 、C、Ca四种元素,按指定化合价最多可以组成化合物的种数是……………(
)
(A)5 (B)6 (C)7 (D)8
6.某含氧酸的化学式为H XO ,则X的同价态的氧化物的化学式,可能是……………(
n 2N-1
)
(A)XO (B)XO (C)XO (D)XO
2 2 2 3 3
7.某元素氧化物分子量为a,价态相同的硫酸盐分子量为b,则此元素的化合价可能是(
)
(A)b-a/80 (B)a-b/80 (C)2b-a/80 (D)b-a/40
11.按照核外电子排布规律:各电子层最多容纳电子数为2n(2 n为电子层数);最外层电子
数不超过8个;次外层电子数不超过18个,预测核电荷数为118的元素的原子核外电子层排
布是……………………………………………………………………………………………(
)
(A)2,8,18,32,32,18,8 (B)2,8,18,32,50,8
(C)2,8,18,32,18,8 (D)2,8,18,32,50,18,8
13.碳元素与某非金属元素R可形成化合物CR ,已知在一个分子中各原子的电子数之和
X
为74,则R的原子序数和X的值分别是…………………………………………………………(
)
(A)16,2 (B)35,4 (C)17,4 (D)26,3
15.等电子体具有原子数目相同,电子数目相同的特征。下列各组物质中属于等电子体的
是……………………………………………………………………………………………(
)
(A)NO和O+ (B)CO和N (C)NO 和CO (D)SO 和C1O
2 2 2 2 2 2
17.Rn+离子有两个电子层且已达稳定结构。与Rn+的电子数相等的微粒(分子、原子和离子,
但不包括Rn+本身)可有………………………………………………………………………(
)
(A)6种 (B)7种 (C)8种 (D)9种
19.原子的核电荷数小于18的某元素x,其原子的电子层数为n,最外层电子数为2n+1,原
子核内质子数是 2n2-l。下列有关 x 的说法中不正确的…………………………………
( )
(A)X能形成化学式为X(OH) 的碱 (B)X可能形成化学式为KXO 的含氧酸钾盐
3 3
(C)X原子的最外层电子数和核电荷数肯定为奇数 (D)X能与某些金属元素形成化
合物
21.两位美国科学家彼得.阿格雷和罗德里克·麦金农,因为发现细胞膜水通道,以及对离
子通道结构和机理研究作出的开创性贡献而获得2003年诺贝尔化学奖。他们之所以获得诺
贝尔化学奖而不是生理学或医学奖是因为……………………………………………………(
)
(A)他们的研究和化学物质水有关
(B)他们的研究有利于研制针对一些神经系统疾病和心血管疾病的药物(C)他们的研究深入到分子、原子的层次
(D)他们的研究深入到细胞的层次
22.氢氧化钙在80℃时的溶解度为x克,20℃时Ca(OH) 溶解度为y克,取80℃时
2
Ca(OH) 的饱和溶液a克蒸发掉w克水后,再恢复至20℃,滤去折出固体,滤液中Ca(OH)
2 2
的 质 量 分 数 为 z% , 则 x 、 y 、 z 的 关 系 正 确 的
是…………………………………………………………( )
(A)x>y>z (B)yz
23.已知某盐在不同温度下的溶解度如下表。若把质量百分比浓度为32%的该盐溶液,由
50℃逐渐冷却,则开始有晶体析出的温度范围是………………………………………………(
)
温度(℃) 0 10 20 30 40
溶解度(克) 13.3 20.9 31.6 45.8 63.9
(A)0℃~10℃ (B)10℃~20℃ (C)20℃~30℃ (D)30℃~40℃
24.60℃时,化合物甲的溶解度比乙大。分别取等质量60℃时的甲、乙的饱和溶液,降温至
20℃后,析出甲和乙的质量分别为ag和bg(甲、乙均无结晶水)。以下叙述中正确的是…(
)
(A)60℃时等质量的甲饱和溶液与乙饱和溶液相比,前者所含溶质的质量大
(B)a一定大于b
(C)20℃时,若甲的溶解度仍比乙的大,则a一定小于b
(D)20℃时,若甲的溶解度比乙的小,则a一定大于b
25.研究物质变化时可使用具有放射性的18O作为“示踪原子”。科学家希尔和尼尔研究
证明,光合作用的通式应更合理地表达为:6CO+12H18O CH O+6HO+618O。在光照充分
2 2 6 12 6 2 2
的环境里,将一种植物黑藻放入含有“示踪原子”18O 的水中,一段时间后,分析“示踪原
2
子 ” , 最 有 可 能
是……………………………………………………………………………………( )
(A)在植物体的周围的空气中发现 (B)在植物体内的葡萄糖(CH O)中发现
6 12 6
(C)在植物体内的淀粉和蛋白质中发现 (D)无法确定示踪原子在什么地方出现
26.18O是科实验中常用的一种示踪原子,用仪器可以观测到它在化学变化中的行踪。在某
一饱和硫酸铜溶液(不含18O)中加入ag带标记18O的无水硫酸铜粉末(CuSO 中的氧元索全部
4
为18O),如果保持温度不变,其结果是…………………………………………………………(
)
(A)无水硫酸铜不再溶解,ag带标记18O的无水硫酸铜粉末没有发生改变
(B)溶液中可找到带标记18O的SO2-,且白色粉末变为蓝色晶体,其质量小于ag
4
(C)溶液中可找到带标记18O的SO2-,且白色粉末变为蓝色晶体,其质量大于ag
4
(D)有部分带标记18O的SO2-进入溶液中,但固体质量保持不变
4
29.天然气、液化石油气燃烧的化学方程式分别为: CH+2O→CO+2HO;
4 2 2 2
CH+5O→3CO+4HO。现有一套以天然为燃料的灶具,要改为以液化石油气为燃料的灶具,应
3 8 2 2 2
该采取的措施是( )
(A)燃料气和空气的进入量都减小 (B)燃料气和空气的进入量都增大
(C)减小燃料气进入量或增大空气进入量 (D)增大燃料气进入量或减小空气进入量
31.某些科学家对3个互相联系的化学反应:①3FeCl+4HO FeO+6HCl+H
2 2 3 4 2
②FeO+3/2C1+6HCl 3FeCl+3HO+1/2O ,③3FeCl→3FeCl +3/2C1 很感兴趣,他们想
3 4 2 3 2 2 3 2 2
利用这三个反应来制取一种很有意义的物质是…………………………………………………( )
(A)H (B)O (C)Cl (D)HCl
2 2 2
二、填空题:
42.2001年11月,美军为打击躲藏在阿富汗山洞中的恐怖分子,使用了一种名叫BLU-82
的高效能燃料空气炸弹。这种炸弹爆炸时,除产生高温外,还可使山洞内氧气耗尽,使其中的
所有生物窒息死亡而山洞不致完全崩塌,以便后续军队进入山洞鉴别死者身份。燃料空气炸
弹的主装药之一是环氧乙烷( ),它的化学式可写作 。爆炸时,环氧
乙烷先成雾状分散在空气中,然后燃爆,反应的生成物为 。
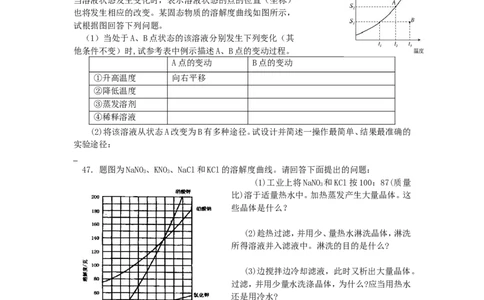
45.溶解度曲线中的任何一点都表示溶液的一种特定状态。
当溶液状态发生变化时,表示溶液状态的点的位置(坐标)
也将发生相应的改变。某固态物质的溶解度曲线如图所示,
试根据图回答下列问题。
(1)当处于A、B点状态的该溶液分别发生下列变化(其
他条件不变)时,试参考表中例示描述A、B点的变动过程。
A点的变动 B点的变动
①升高温度 向右平移
②降低温度
③蒸发溶剂
④稀释溶液
(2)将该溶液从状态A改变为B有多种途径。试设计并简述一操作最简单、结果最准确的
实验途径:
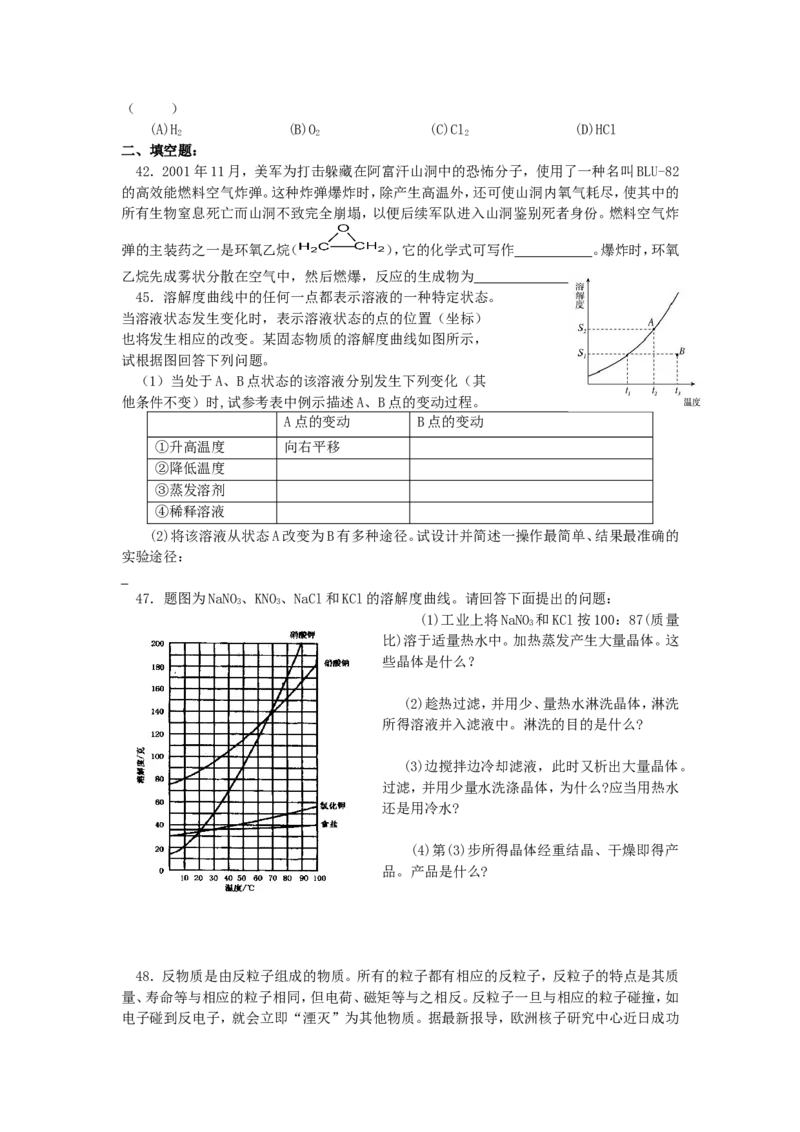
47.题图为NaNO、KNO、NaCl和KCl的溶解度曲线。请回答下面提出的问题:
3 3
(1)工业上将NaNO 和KCl按100:87(质量
3
比)溶于适量热水中。加热蒸发产生大量晶体。这
些晶体是什么?
(2)趁热过滤,并用少、量热水淋洗晶体,淋洗
所得溶液并入滤液中。淋洗的目的是什么?
(3)边搅拌边冷却滤液,此时又析出大量晶体。
过滤,并用少量水洗涤晶体,为什么?应当用热水
还是用冷水?
(4)第(3)步所得晶体经重结晶、干燥即得产
品。产品是什么?
48.反物质是由反粒子组成的物质。所有的粒子都有相应的反粒子,反粒子的特点是其质
量、寿命等与相应的粒子相同,但电荷、磁矩等与之相反。反粒子一旦与相应的粒子碰撞,如
电子碰到反电子,就会立即“湮灭”为其他物质。据最新报导,欧洲核子研究中心近日成功地制造出约555个低能量状态的反氢原子,这是人类首次在受控条件下大量制造的反物质。
试回答下列问题:
(1)你认为反氢原子结构示意图可表示为,图中代表各微粒的符号及其所表示的意义分别
是: 表示 ; 表示 。
(2)质子与反质子相碰撞而“湮灭”是化学变化吗? ,理由是
。
53.从物质所含元素的化合价是否发生变化(升高或降低)的角度看,CuO+H Cu+HO、
2 2
FeO+ 3CO 2Fe+3CO、Zn+HSO →ZnSO+H↑这三个化学反应可以划分为同一类型——氧
2 3 2 2 2 4 4 2
化还原反应。已知溴元素(Br)与氟元素(F)组成的一种液态化合物BrFx与水按分子个数比为
3:5发生氧化还原反应,其产物是溴酸(HBrO)、氢氟酸(HF)、单质溴(Br)和氧气。
3 2
(1)在化合物BrF 中,x的值是 ;
x
(2)写出有关反应化学方程式 ;
(3)该反应中,① 是还原剂,② 表现出氧化性。
54.减弱“温室效应”有效措施之一是大量植树造林,绿色植物在叶绿素存在下的光合作
用是完成二氧化碳循环的重要一环。已知叶绿素的相对分子质量小于 900,其分子含碳
73.8%(以下均指质量分数)、氢8.3%、氮6.3%、镁2.7%,其余为氧。试确定叶绿素的化学式。
答案
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16
AD D C D C AB AD B A A A D C D AB D
17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 32
D A A C C CD D AD A C C BC C AC A A
33.HO和CO,4CxHy+(4x+y)O 4xCO+2yHO
2 2 2 2 2
34.2AsH+3O→AsO+3HO
3 2 2 3 2
35.①ZnCO ZnO+CO↑②2ZnO+C 2Zn+CO↑③ 2CuO+C 4Cu+
3 2 2 2
CO↑
2
36.CH O 2CHOH+2CO↑;CH+2HO 4H+CO
6 12 6 2 5 2 4 2 2 2
37.2Cu+O+2HSO→2CuSO+2HO
2 2 4 4 2
38.3;2;单质;
39.HSO、HCO―;OH-、HCO-、NO―。
2 4 3 3 3
40.H+FeCl Fe+2HCl;防止生成的纳米Fe被氧化
2 高2温
41.停止乱挖滥采,改善水源;
Tl 2 SO 4 +Ba(OH) 2 →BaSO 4 ↓+2TlOH;2TlOH 高 温 Tl 2 O+H 2 O;Tl 2 O+H 2 高 温 2Tl+H 2 O42.C HO;CO、CO、HO
2 4 2 2
43.12,6,8;84
44.有水喷出;氢气分子质量小,运动速度快,因而在一定时间里进入容器A的氢气分子比
逸出的气体分子多,使容器A与盛水的瓶内气体的压强大于外界的大气压,因而有水喷出
45.
A点的变动 B点的变动
①升高温度 向右平移 向右平移
②降低温度 沿曲线下移 向左平移至曲线,再沿曲线下移
③蒸发溶剂 不动 垂直上移至曲线,不再变动
④稀释溶液 垂直下移 垂直下移
(2)将A状态的该溶液降温至t,过滤除去析出的该物质晶体后,将溶液升温至t。
1 3
46.A是Na,B是S,C是O,Z的化学式为NaSO。
2 4 6
47.(1)NaCl(2)减少KNO 的损失。(3)在洗掉氯化物的同时,可提高KNO 的产率;用冷
3 3
水。(4)KNO
3
48.(1) ,+1表示1个反电子;-1表示 反氢原子核且其中只有1个反质子(或1个
反质子)。(2)不是;化学变化是反应物中原子的重新组合,“湮灭”不是。
53. (1)3;(2)3BrF+5HO→HBrO+9HF+Br+O↑;(3)①HO和BrF ②BrF。
3 2 3 2 2 2 3 3
54.假设叶绿素中有一个镁原子
则叶绿素的相对分子质量为:24/2.7%=889<900 (2分)
由此说明叶绿素分子中仅含有一个镁原子,其相对分子质量为889。
叶绿素分子中含有碳原子的个数:894×73.8% /12 =55;
类推:H-74,O-5,N-4 (2分)
所以叶绿素的化学式为:C H ONMg (1分)
55 74 5 4
解法二:由题意知叶绿素中各元素原子的个数比:
碳﹕氢﹕氮﹕镁﹕氧= ﹕ ﹕ ﹕ ﹕
=6.15﹕8.3﹕0.45﹕0.1125﹕0.55625= 55﹕73﹕4﹕1﹕5
因为叶绿素的相对分子质量小于900。所以叶绿素的分子式为C H ONMg。
55 73 5 4