文档内容
2020-2021 学年上学期期末三校联考
高一化学
本试卷共8页,28小题,满分100分。考试用时75分钟。
可能用到的相对原于质量:N-14 0-16 Na-23 Mg-24 Si-28 C-35.5 Fe-56 Ba-137
一、选择题:本大题25小题, 每小题2分,共50分。
1. 下列成语或谚语中蕴含着一定的化学知识或原理,下列有关说法错误的是
A. 百炼成钢——通过反复锤炼,除去铁中部分杂质,使其转化为钢
B. 水滴石穿——CO+HO+CaCO===Ca(HCO)(以大理石为例)
2 2 3 3 2
C. 恨铁不成钢——钢的性能远优于铁
D. 真金不怕火炼——单质金的熔点很高
2. X、Y、Z、W各代表一种物质,若X+Y=Z+W,则X和Y的反应不可能是
A. 盐和盐的反应 B. 酸与碱的反应
C. 碱性氧化物和水的反应 D. 酸性氧化物和碱的反应
3. 下列表示物质结构的化学用语正确的是
A. H、D、T表示同一种核素
B. Cl-的结构示意图:
C. MgCl 的形成过程为:
2
D. NaCl的电子式: Na+Cl-
4. 中国科学技术大学的钱逸泰教授等以CCl 和金属钠为原料,在700℃时反应制造出纳米级金刚石粉末和
4
另一种化合物。该成果发表在世界权威的《科学》杂志上,被科学家们高度评价为“稻草变黄金”。下列
有关说法中,你认为错误的是( )
A. Na的还原性强于金刚石 B. 另一种化合物是NaCl
C. 纳米级金刚石粉末可以透过半透膜 D. 这个反应是置换反应
5. 对四组无色透明溶液进行离子检验,四位同学各鉴定一组,他们的实验报告的结论如下,其中可能正确
的是
A. MnO 、K+、S2-、Na+ B. Mg2+、NO 、OH-、Cl-
C. K+、H+、Cl-、CO D. Na+、OH-、Cl-、NO
学科网(北京)股份有限公司的
6. mg O 和 O 混合气体中含有n个O原子,则阿伏伽德罗常数N 可表示为
2 3 A
A. 40n/m mol-1 B. 16n/m mol-1
C. n/40m mol-1 D. n/16m mol-1
7. 下列关于元素周期表的叙述正确的是
A. 周期表中有七个主族,八个副族
B. 目前使用的元素周期表中,最长的周期含有32种元素
C. 短周期元素是指1~20号元素
D. 原子的最外层电子数都等于该元素所在的族序数
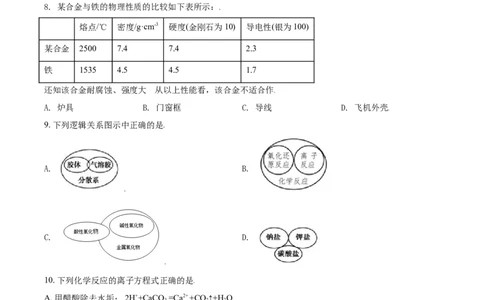
8. 某合金与铁的物理性质的比较如下表所示:
熔点/℃ 密度/g·cm-3 硬度(金刚石为10) 导电性(银为100)
某合金 2500 7.4 7.4 2.3
铁 1535 4.5 4.5 1.7
。
还知该合金耐腐蚀、强度大 从以上性能看,该合金不适合作
A. 炉具 B. 门窗框 C. 导线 D. 飞机外壳
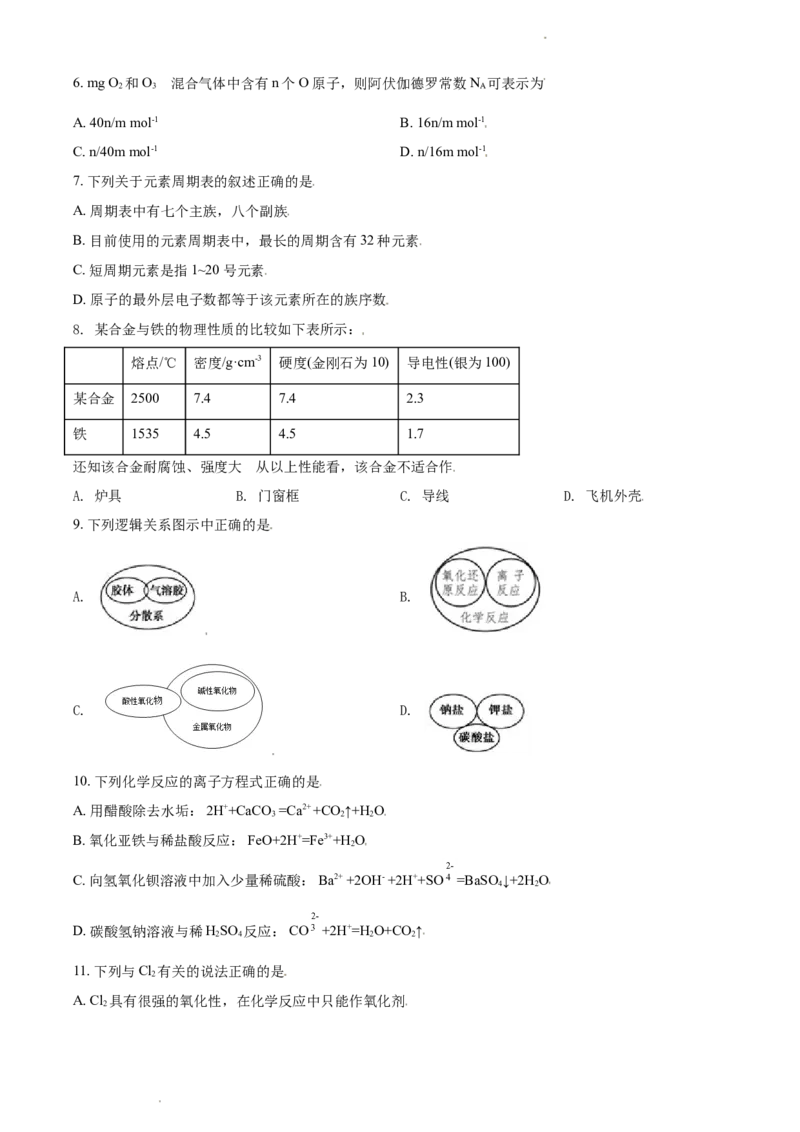
9. 下列逻辑关系图示中正确的是
A. B.
C. D.
10. 下列化学反应的离子方程式正确的是
A. 用醋酸除去水垢: 2H++CaCO =Ca2+ +CO ↑+H O
3 2 2
B. 氧化亚铁与稀盐酸反应: FeO+2H+=Fe3++H O
2
C. 向氢氧化钡溶液中加入少量稀硫酸: Ba2+ +2OH- +2H++SO =BaSO ↓+2H O
4 2
D. 碳酸氢钠溶液与稀HSO 反应: CO +2H+=H O+CO↑
2 4 2 2
11. 下列与Cl 有关的说法正确的是
2
A. Cl 具有很强的氧化性,在化学反应中只能作氧化剂
2
学科网(北京)股份有限公司B. 氯气作水的杀菌消毒剂时没有发生化学变化
C. 0.1molCl 与足量NaOH溶液反应,转移0.2mol电子
2
D. Cl 能使湿润的淀粉碘化钾试纸变蓝、说明Cl 具有氧化性
2 2
12. 下列有关钠的化合物说法正确的是
A. 灼烧某白色粉末,火焰呈黄色,证明原粉末中有Na元素,一定没有K元素
B. 将NaOH溶液滴加到饱和FeCl 溶液中制备Fe(OH) 胶体
3 3
C. 用加热法除去NaHCO 固体中混有的NaCO
3 2 3
D. 钠蒸气充入灯泡中制成钠灯,常用于公路照明
13. 对于温度、压强一定的气体,下列数值中与其物质的量无关的是
A. 质量 B. 体积 C. 分子数目 D. 气体摩尔体积
14. 下列说法中不正确的是
A. 离子化合物一定含有阴离子和阳离子的
B. 熔融状态下能导电的物质定是离子化合物
C. 两种元素形成离子化合物的过程中一定伴有电子得失
D. 原子序数为12和9的原子所对应的元素可形成离子化合物
15. 已知:①向KMnO 晶体滴加浓盐酸,产生黄绿色气体:
4
②向FeCl 溶液中通入少量实验①产生的气体,溶液变黄色:
2
③湿润的淀粉KI试纸遇到实验①生成的气体变蓝。下列判断正确的为
A. 上述实验可证明氧化性强弱: MnO >Cl>Fe3+>I
2 2
B. 上述实验中,共有两个氧化还原反应
C. 湿润的淀粉KI试纸可用于检验实验①生成的气体
D. 实验②证明Fe2+既有氧化性又有还原性
16. 某学生利用如图装置对电解质溶液导电性进行实验探究。下列说法中正确的是
A. 闭合开关K,电流表指针发生偏转,证明HCl溶液是电解质
B. 闭合开关K,向烧杯中加入NaCl固体,由于HCl与NaCl不反应,故电流表指针不发生变化
C. 闭合开关K,向溶液中加入CaCO 固体,电流表示数不变
3
D. 选取相同浓度的硫酸替换0.1mol·L-1的HCl溶液,电流表的示数相同
17. 三个相同的恒温恒容密闭容器中分别盛有等质量的H、CH、O,下列说法正确的是
2 4 2
学科网(北京)股份有限公司A. 三种气体的分子数目一定相等 B. 三种气体物质的量之比为16:2:1
C. 三种气体的密度之比为1:2:16 D. 三种气体的压强一定相等
18. 铬可用于制造不锈钢、汽车零件、工具、磁带和录像带等。铬的金属性位于锌和铁之间,根据元素周
期律的知识,下列有关铬的性质说法不正确的是
A. 铬能与硫酸铜溶液发生置换反应 B. Cr(OH) 属于强碱
3
C. 高温条件下,Al能与CrO 反应置换出Cr D. 铬能与稀盐酸发生反应
3
19. 实验室需要80mL 1 mol/L的稀硫酸,要用98%的浓硫酸(密度为1.84g·cm-3)来配制。现给出下列仪器(配
制过程中可能用到):①100mL量简②10mL量筒③50mL烧杯④托盘天平⑤100mL容量瓶 ⑥胶头滴管⑦
玻璃棒⑧80mL容量瓶。按使用仪器的先后顺序排列正确的是
A. ④③⑦⑧⑥ B. ②⑤⑦⑥ C. ①③⑧⑥⑦ D. ②⑥③⑦⑤⑥
20. 下列各组物质相互混合反应,既有气体生成最终又有沉淀生成的是
①金属钠投入MgCl 溶液中
2
②过量的NaOH溶液和FeCl 溶液
3
③过量的NaO 投入FeCl 溶液中
2 2 2
④过量NaOH和Ca(HCO) 溶液混合
3 2
A. ①④ B. ②③ C. ①③ D. ③④
21. W、X、Y 、Z为核电荷数依次增大的前20号主族元素,W的原子中只有1个电子,X与Y同族,Y的
一种单质在空气中易自燃,W与Z形成的二元化合物和水反应可生成W的单质。下列说法正确的是
A. W分别与Y、Z形成的化合物中化学键类型相同 B. 氢化物沸点: Y>X
C. Y的氧化物的水化物是强酸 D. 简单离子半径: Y>Z
22. ClO 是新一代饮用水的消毒剂,许多发达国家的自来水厂采用ClO 代替Cl 来进行自来水消毒。我国最
2 2 2
近成功研制出制取ClO 的新方法,其反应的微观过程如下所示:
2
下列有关该反应的叙述中正确的是
A. 该反应是复分解反应
B. 该反应的化学方程式为Cl+2NaClO =2ClO +2NaCl
2 2 2
C. 反应中Cl 既是氧化剂,又是还原剂
2
D. NaClO 和ClO 中Cl的化合价相同
2 2
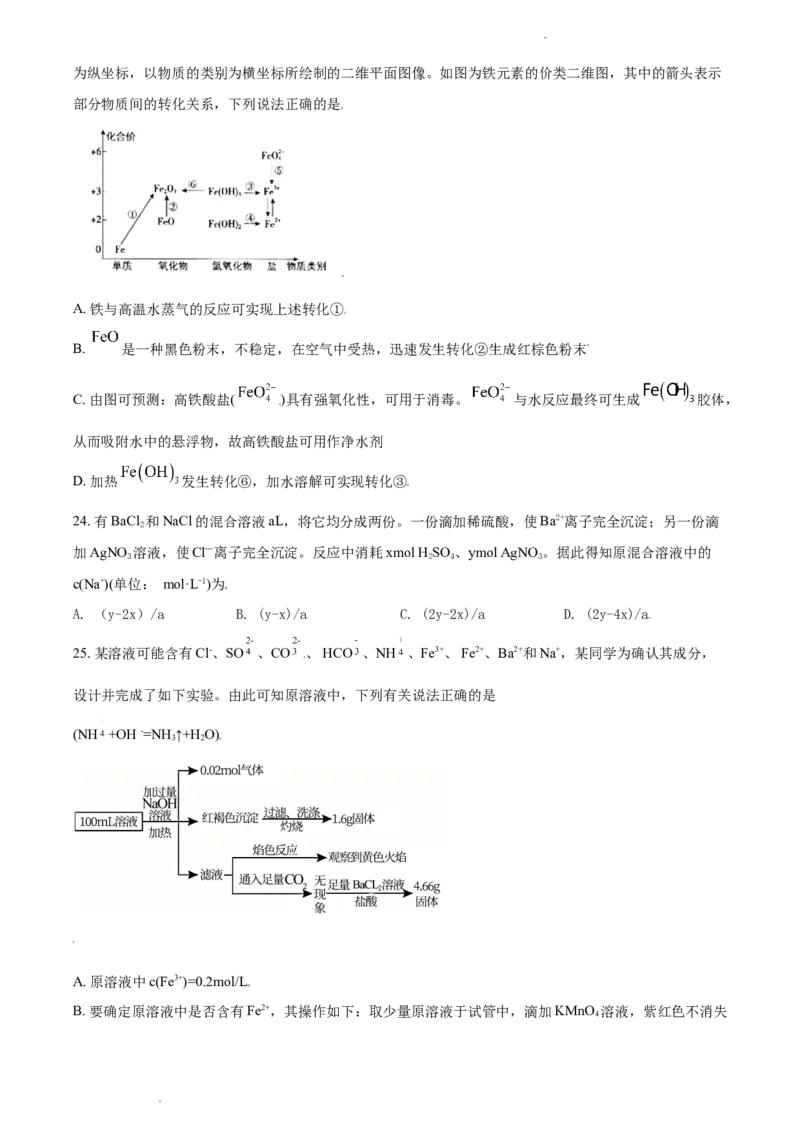
23. 元素的价类二维图是我们学习元素及其化合物相关知识的重要模型和工具,它指的是以元素的化合价
学科网(北京)股份有限公司为纵坐标,以物质的类别为横坐标所绘制的二维平面图像。如图为铁元素的价类二维图,其中的箭头表示
部分物质间的转化关系,下列说法正确的是
A. 铁与高温水蒸气的反应可实现上述转化①
B. 是一种黑色粉末,不稳定,在空气中受热,迅速发生转化②生成红棕色粉末
C. 由图可预测:高铁酸盐( )具有强氧化性,可用于消毒。 与水反应最终可生成 胶体,
从而吸附水中的悬浮物,故高铁酸盐可用作净水剂
D. 加热 发生转化⑥,加水溶解可实现转化③
24. 有BaCl 和NaCl的混合溶液aL,将它均分成两份。一份滴加稀硫酸,使Ba2+离子完全沉淀;另一份滴
2
加AgNO 溶液,使Cl—离子完全沉淀。反应中消耗xmol HSO 、ymol AgNO 。据此得知原混合溶液中的
3 2 4 3
c(Na+)(单位: mol·L-1)为
A. (y-2x)/a B. (y-x)/a C. (2y-2x)/a D. (2y-4x)/a
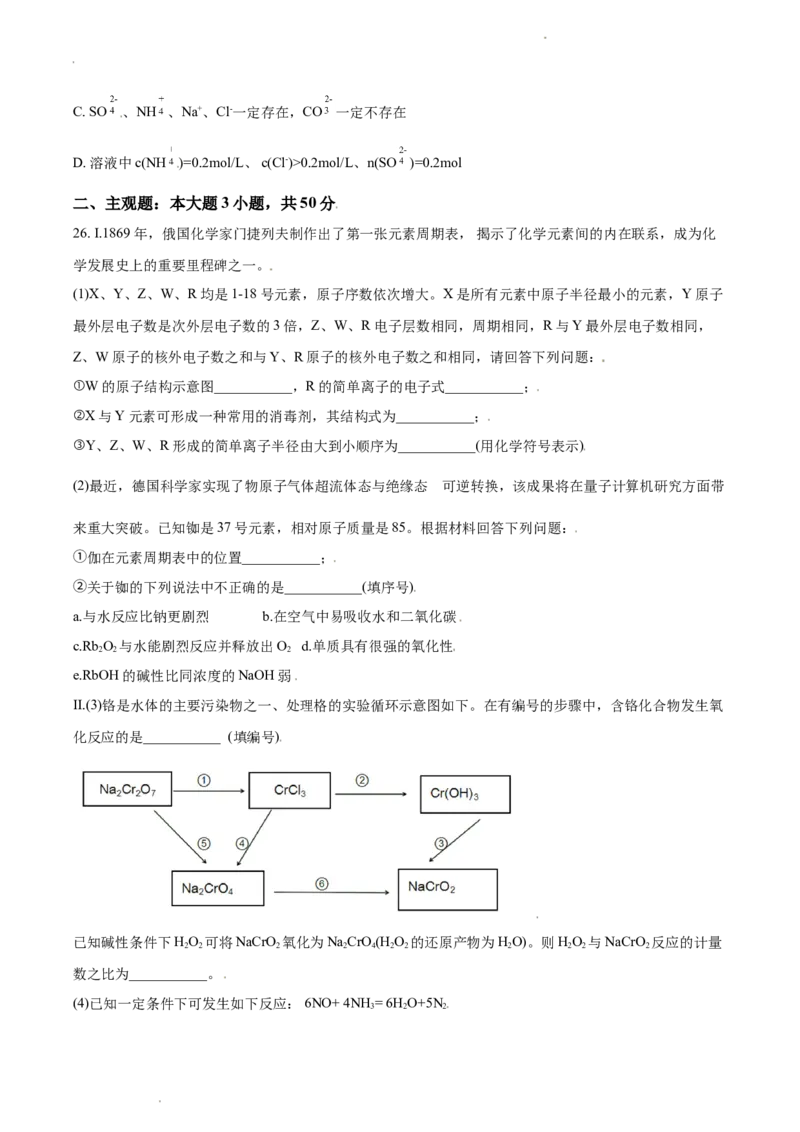
25. 某溶液可能含有Cl-、SO 、CO 、 HCO 、NH 、Fe3+、 Fe2+、Ba2+和Na+,某同学为确认其成分,
设计并完成了如下实验。由此可知原溶液中,下列有关说法正确的是
(NH +OH -=NH↑+H O)
3 2
A. 原溶液中c(Fe3+)=0.2mol/L
B. 要确定原溶液中是否含有Fe2+,其操作如下:取少量原溶液于试管中,滴加KMnO 溶液,紫红色不消失
4
学科网(北京)股份有限公司C. SO 、NH 、Na+、Cl-一定存在,CO 一定不存在
D. 溶液中c(NH )=0.2mol/L、 c(Cl-)>0.2mol/L、n(SO )=0.2mol
二、主观题:本大题3小题,共50分
26. I.1869 年,俄国化学家门捷列夫制作出了第一张元素周期表, 揭示了化学元素间的内在联系,成为化
学发展史上的重要里程碑之一。
(1)X、Y、Z、W、R均是1-18号元素,原子序数依次增大。X是所有元素中原子半径最小的元素,Y原子
最外层电子数是次外层电子数的3倍,Z、W、R电子层数相同,周期相同,R与Y最外层电子数相同,
Z、W原子的核外电子数之和与Y、R原子的核外电子数之和相同,请回答下列问题:
①W的原子结构示意图___________,R的简单离子的电子式___________;
②X与Y元素可形成一种常用的消毒剂,其结构式为___________;
③Y、Z、W、R形成的简单离子半径由大到小顺序为___________(用化学符号表示)
的
(2)最近,德国科学家实现了物原子气体超流体态与绝缘态 可逆转换,该成果将在量子计算机研究方面带
来重大突破。已知铷是37号元素,相对原子质量是85。根据材料回答下列问题:
①伽在元素周期表中的位置___________;
②关于铷的下列说法中不正确的是___________(填序号)
a.与水反应比钠更剧烈 b.在空气中易吸收水和二氧化碳
c.Rb O 与水能剧烈反应并释放出O d.单质具有很强的氧化性
2 2 2
e.RbOH的碱性比同浓度的NaOH弱
II.(3)铬是水体的主要污染物之一、处理格的实验循环示意图如下。在有编号的步骤中,含铬化合物发生氧
化反应的是___________ (填编号)
已知碱性条件下HO 可将NaCrO 氧化为NaCrO(H O 的还原产物为HO)。则HO 与NaCrO 反应的计量
2 2 2 2 4 2 2 2 2 2 2
数之比为___________。
(4)已知一定条件下可发生如下反应: 6NO+ 4NH = 6H O+5N
3 2 2
学科网(北京)股份有限公司①用双线桥法表示该反应中电子转移的方向和数目: ___________
②若有3.4g氨气发生反应,则反应所得还原产物与氧化产物的质量差为___________。
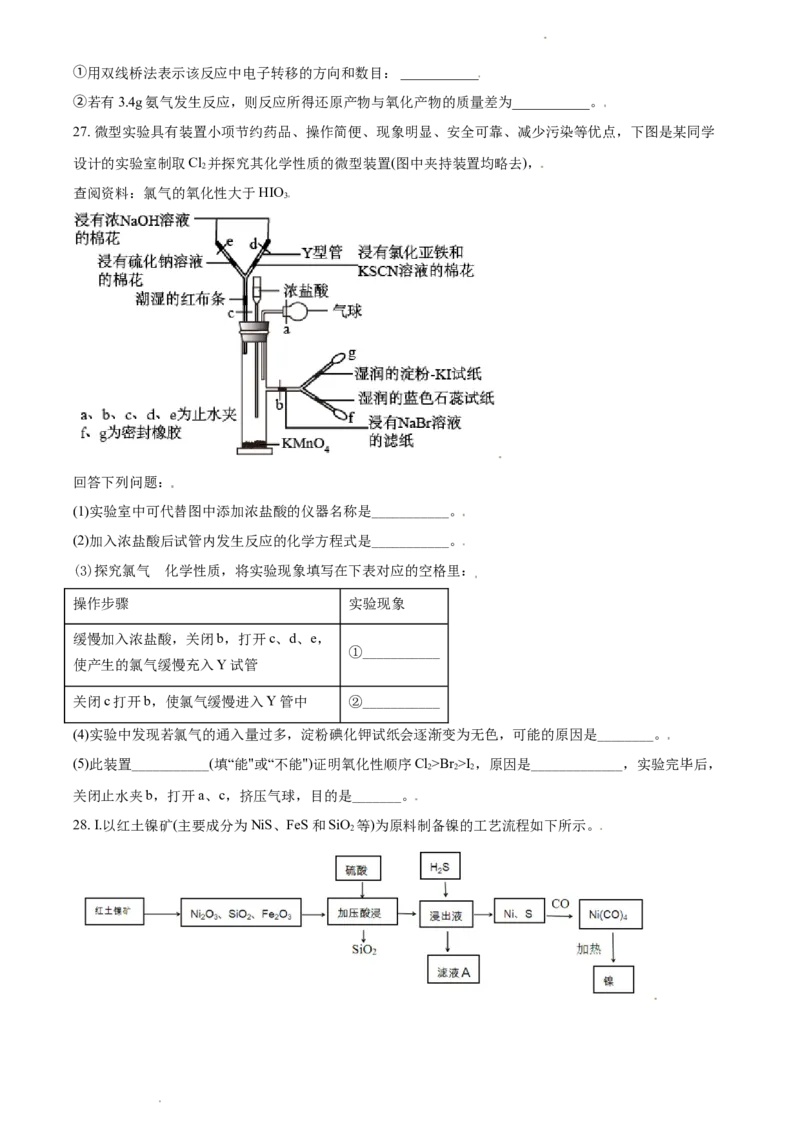
27. 微型实验具有装置小项节约药品、操作简便、现象明显、安全可靠、减少污染等优点,下图是某同学
设计的实验室制取Cl 并探究其化学性质的微型装置(图中夹持装置均略去),
2
查阅资料:氯气的氧化性大于HIO
3
回答下列问题:
(1)实验室中可代替图中添加浓盐酸的仪器名称是___________。
(2)加入浓盐酸后试管内发生反应的化学方程式是___________。
(3)探究氯气 的化学性质,将实验现象填写在下表对应的空格里:
操作步骤 实验现象
缓慢加入浓盐酸,关闭b,打开c、d、e,
①___________
使产生的氯气缓慢充入Y试管
关闭c打开b,使氯气缓慢进入Y管中 ②___________
(4)实验中发现若氯气的通入量过多,淀粉碘化钾试纸会逐渐变为无色,可能的原因是________。
(5)此装置___________(填“能"或“不能")证明氧化性顺序Cl>Br >I ,原因是_____________,实验完毕后,
2 2 2
关闭止水夹b,打开a、c,挤压气球,目的是_______。
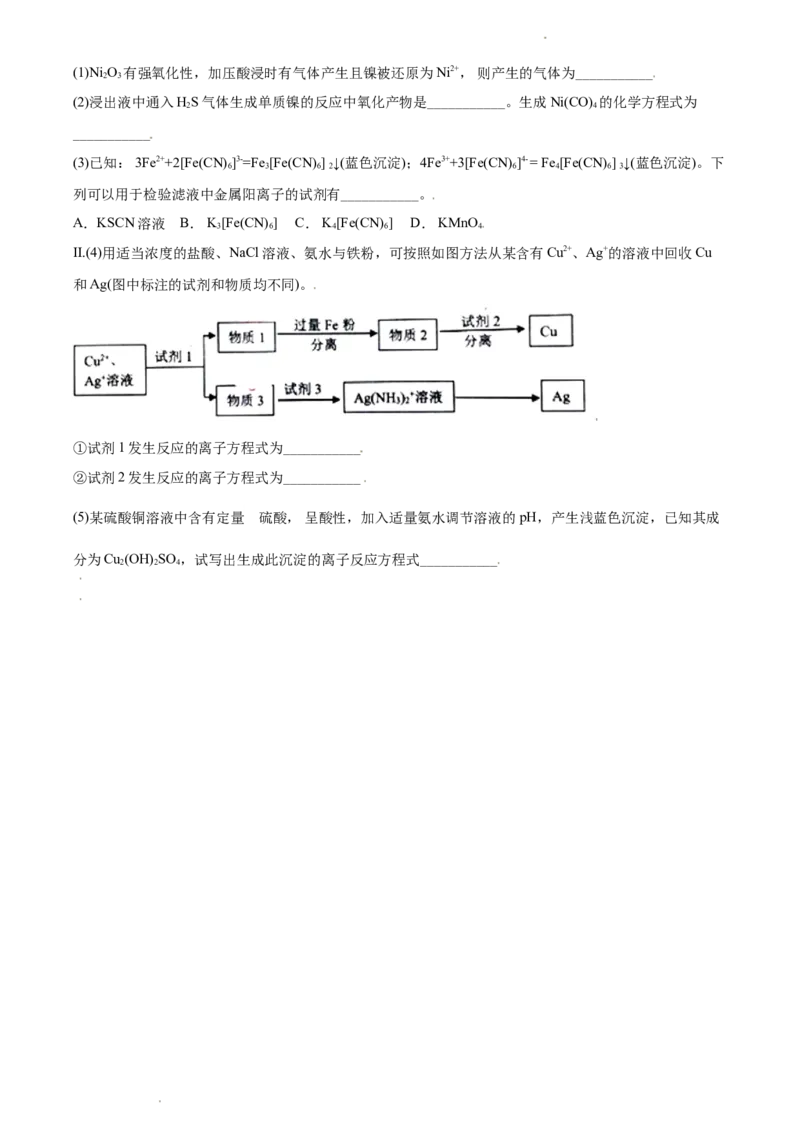
28. I.以红土镍矿(主要成分为NiS、FeS和SiO 等)为原料制备镍的工艺流程如下所示。
2
学科网(北京)股份有限公司(1)NiO 有强氧化性,加压酸浸时有气体产生且镍被还原为Ni2+, 则产生的气体为___________
2 3
(2)浸出液中通入HS气体生成单质镍的反应中氧化产物是___________。生成Ni(CO) 的化学方程式为
2 4
___________
(3)已知: 3Fe2++2[Fe(CN)]3-=Fe [Fe(CN) ] ↓(蓝色沉淀);4Fe3++3[Fe(CN)]4- = Fe [Fe(CN) ] ↓(蓝色沉淀)。下
6 3 6 2 6 4 6 3
列可以用于检验滤液中金属阳离子的试剂有___________。
A.KSCN溶液 B. K[Fe(CN) ] C. K[Fe(CN) ] D. KMnO
3 6 4 6 4
II.(4)用适当浓度的盐酸、NaCl溶液、氨水与铁粉,可按照如图方法从某含有Cu2+、Ag+的溶液中回收Cu
和Ag(图中标注的试剂和物质均不同)。
①试剂1发生反应的离子方程式为___________
②试剂2发生反应的离子方程式为___________
的
(5)某硫酸铜溶液中含有定量 硫酸, 呈酸性,加入适量氨水调节溶液的 pH,产生浅蓝色沉淀,已知其成
分为Cu (OH) SO ,试写出生成此沉淀的离子反应方程式___________
2 2 4
学科网(北京)股份有限公司学科网(北京)股份有限公司