文档内容
燃料电池及其它新型电池电极反应式的书写
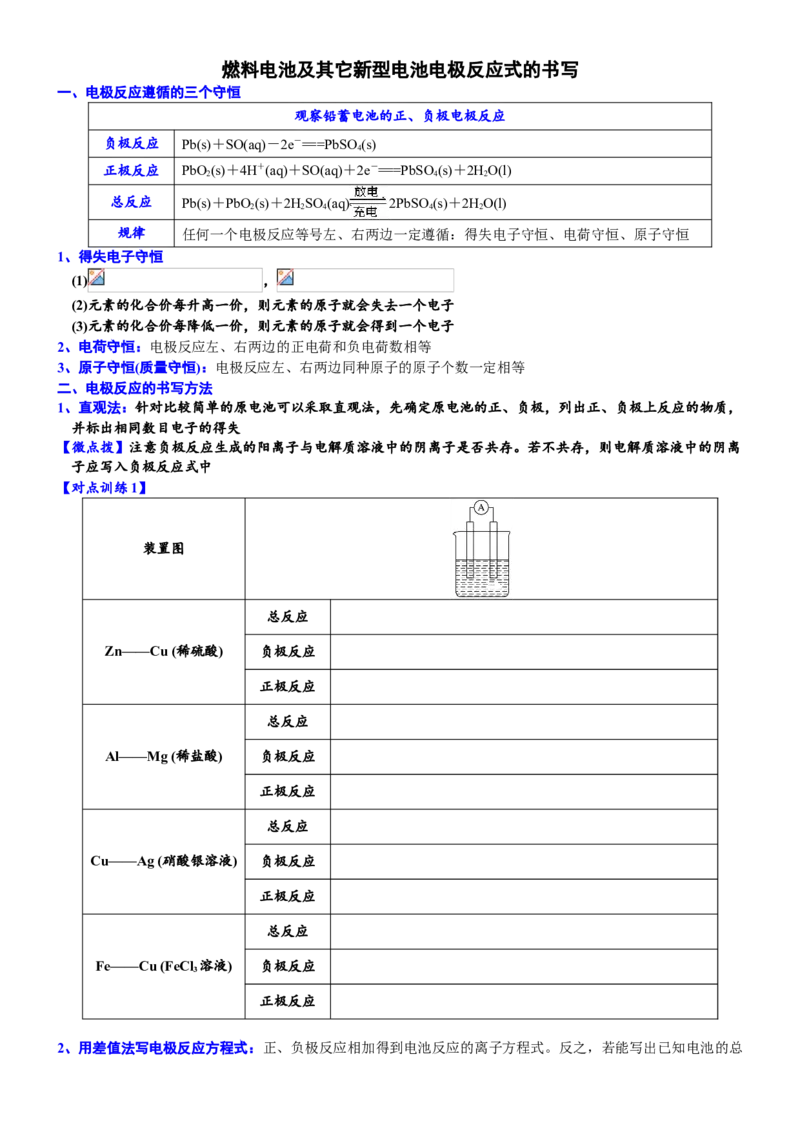
一、电极反应遵循的三个守恒
观察铅蓄电池的正、负极电极反应
负极反应 Pb(s)+SO(aq)-2e-===PbSO(s)
4
正极反应 PbO (s)+4H+(aq)+SO(aq)+2e-===PbSO(s)+2HO(l)
2 4 2
总反应 Pb(s)+PbO (s)+2HSO (aq) 2PbSO (s)+2HO(l)
2 2 4 4 2
规律 任何一个电极反应等号左、右两边一定遵循:得失电子守恒、电荷守恒、原子守恒
1、得失电子守恒
(1) ,
(2)元素的化合价每升高一价,则元素的原子就会失去一个电子
(3)元素的化合价每降低一价,则元素的原子就会得到一个电子
2、电荷守恒:电极反应左、右两边的正电荷和负电荷数相等
3、原子守恒(质量守恒):电极反应左、右两边同种原子的原子个数一定相等
二、电极反应的书写方法
1、直观法:针对比较简单的原电池可以采取直观法,先确定原电池的正、负极,列出正、负极上反应的物质,
并标出相同数目电子的得失
【微点拨】注意负极反应生成的阳离子与电解质溶液中的阴离子是否共存。若不共存,则电解质溶液中的阴离
子应写入负极反应式中
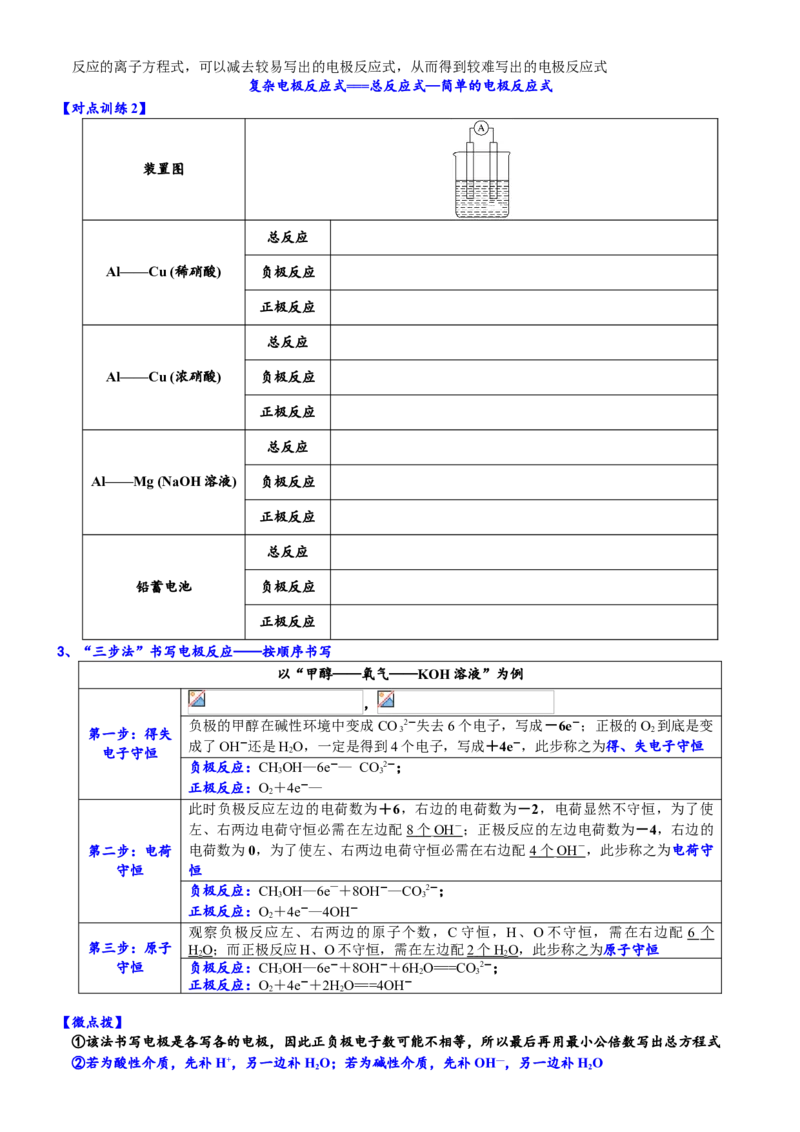
【对点训练1】
装置图
总反应
Zn——Cu (稀硫酸) 负极反应
正极反应
总反应
Al——Mg (稀盐酸) 负极反应
正极反应
总反应
Cu——Ag (硝酸银溶液) 负极反应
正极反应
总反应
Fe——Cu (FeCl 溶液) 负极反应
3
正极反应
2、用差值法写电极反应方程式:正、负极反应相加得到电池反应的离子方程式。反之,若能写出已知电池的总反应的离子方程式,可以减去较易写出的电极反应式,从而得到较难写出的电极反应式
复杂电极反应式===总反应式—简单的电极反应式
【对点训练2】
装置图
总反应
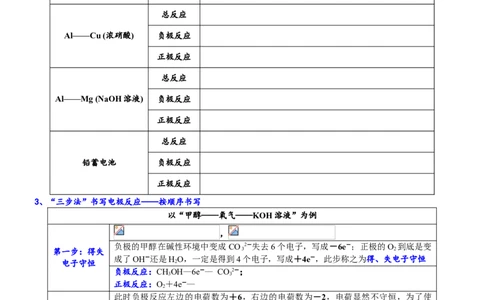
Al——Cu (稀硝酸) 负极反应
正极反应
总反应
Al——Cu (浓硝酸) 负极反应
正极反应
总反应
Al——Mg (NaOH溶液) 负极反应
正极反应
总反应
铅蓄电池 负极反应
正极反应
3、“三步法”书写电极反应——按顺序书写
以“甲醇——氧气——KOH溶液”为例
,
负极的甲醇在碱性环境中变成CO 2-失去6个电子,写成-6e-;正极的O 到底是变
第一步:得失 3 2
成了OH-还是HO,一定是得到4个电子,写成+4e-,此步称之为得、失电子守恒
电子守恒 2
负极反应:CHOH—6e-— CO2-;
3 3
正极反应:O+4e-—
2
此时负极反应左边的电荷数为+6,右边的电荷数为-2,电荷显然不守恒,为了使
左、右两边电荷守恒必需在左边配 8 个 OH - ;正极反应的左边电荷数为-4,右边的
第二步:电荷 电荷数为0,为了使左、右两边电荷守恒必需在右边配 4 个 OH - ,此步称之为电荷守
守恒 恒
负极反应:CHOH—6e—+8OH-—CO2-;
3 3
正极反应:O+4e-—4OH-
2
观察负极反应左、右两边的原子个数,C守恒,H、O不守恒,需在右边配 6 个
第三步:原子 HO;而正极反应H、O不守恒,需在左边配 2 个 H O,此步称之为原子守恒
2 2
守恒 负极反应:CHOH—6e-+8OH-+6HO===CO2-;
3 2 3
正极反应:O+4e-+2HO===4OH-
2 2
【微点拨】
①该法书写电极是各写各的电极,因此正负极电子数可能不相等,所以最后再用最小公倍数写出总方程式
②若为酸性介质,先补H+,另一边补HO;若为碱性介质,先补OH—,另一边补HO
2 2③有机物中化合价处理方法:“氧-2,氢+1,最后算碳化合价”,并且要注意溶液环境与产物之间的反应,
碱性环境下,C元素最终产物应为CO2-
3
④水溶液中不能出现O2-;碱性溶液反应物、生成物中均无H+;酸性溶液反应物、生成物中均无OH-,中性溶液反应物中无H+ 和OH-
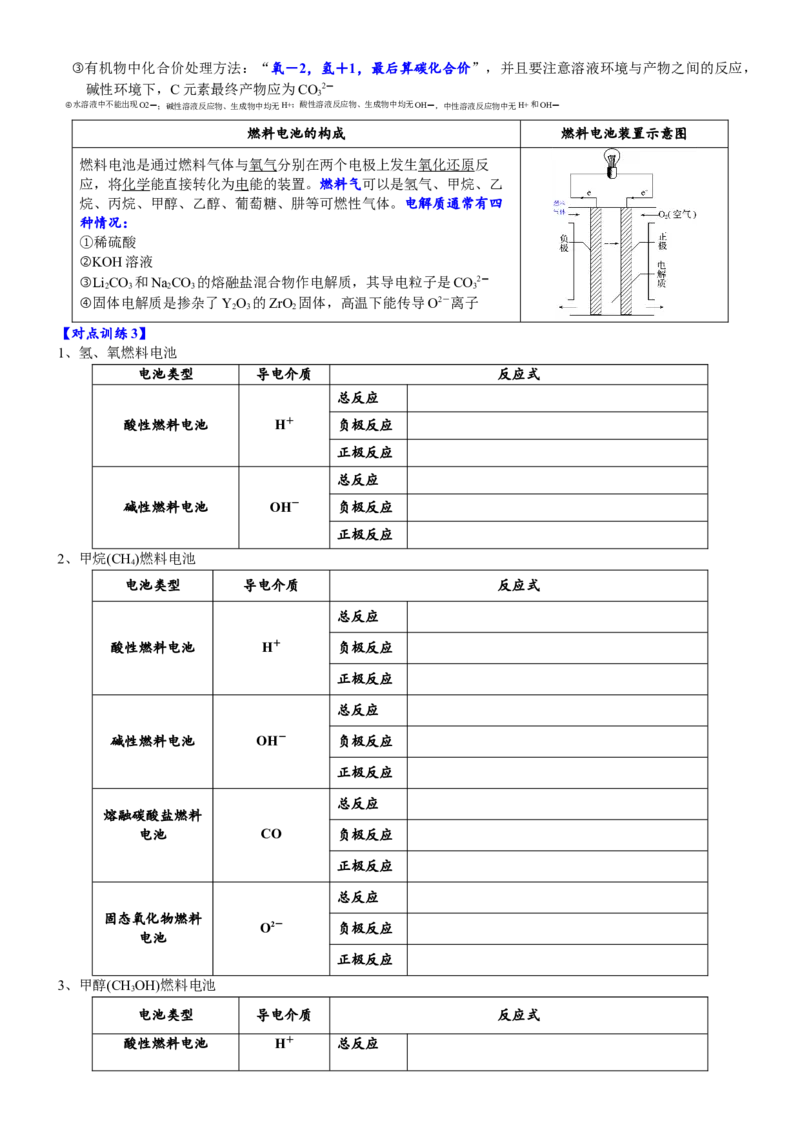
燃料电池的构成 燃料电池装置示意图
燃料电池是通过燃料气体与氧气分别在两个电极上发生氧化还原反
应,将化学能直接转化为电能的装置。燃料气可以是氢气、甲烷、乙
烷、丙烷、甲醇、乙醇、葡萄糖、肼等可燃性气体。电解质通常有四
种情况:
①稀硫酸
②KOH溶液
③LiCO 和NaCO 的熔融盐混合物作电解质,其导电粒子是CO2-
2 3 2 3 3
④固体电解质是掺杂了YO 的ZrO 固体,高温下能传导O2-离子
2 3 2
【对点训练3】
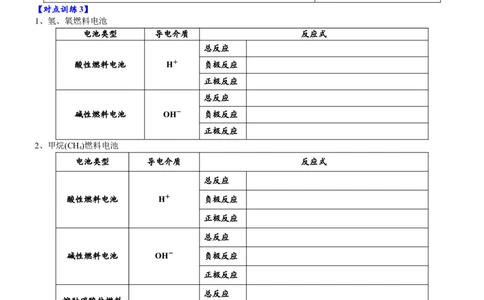
1、氢、氧燃料电池
电池类型 导电介质 反应式
总反应
酸性燃料电池 H+ 负极反应
正极反应
总反应
碱性燃料电池 OH- 负极反应
正极反应
2、甲烷(CH)燃料电池
4
电池类型 导电介质 反应式
总反应
酸性燃料电池 H+ 负极反应
正极反应
总反应
碱性燃料电池 OH- 负极反应
正极反应
总反应
熔融碳酸盐燃料
电池 CO 负极反应
正极反应
总反应
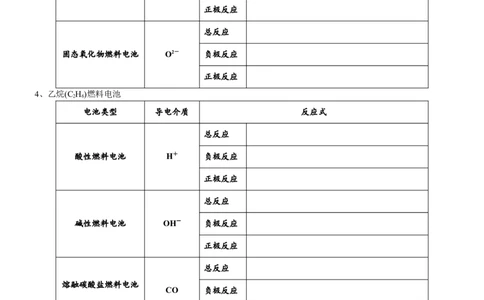
固态氧化物燃料
O2- 负极反应
电池
正极反应
3、甲醇(CHOH)燃料电池
3
电池类型 导电介质 反应式
酸性燃料电池 H+ 总反应负极反应
正极反应
总反应
碱性燃料电池 OH- 负极反应
正极反应
总反应
熔融碳酸盐燃料电池
CO 负极反应
正极反应
总反应
固态氧化物燃料电池 O2- 负极反应
正极反应
4、乙烷(C H)燃料电池
2 6
电池类型 导电介质 反应式
总反应
酸性燃料电池 H+ 负极反应
正极反应
总反应
碱性燃料电池 OH- 负极反应
正极反应
总反应
熔融碳酸盐燃料电池
CO 负极反应
正极反应
总反应
固态氧化物燃料电池 O2- 负极反应
正极反应
5、丙烷(C H)燃料电池
3 8
电池类型 导电介质 反应式
酸性燃料电池 H+ 总反应负极反应
正极反应
总反应
碱性燃料电池 OH- 负极反应
正极反应
总反应
熔融碳酸盐燃料电池
CO 负极反应
正极反应
总反应
固态氧化物燃料电池 O2- 负极反应
正极反应
6、乙醇(C HOH)燃料电池
2 5
电池类型 导电介质 反应式
总反应
酸性燃料电池 H+ 负极反应
正极反应
总反应
碱性燃料电池 OH- 负极反应
正极反应
总反应
熔融碳酸盐燃料电池
CO 负极反应
正极反应
总反应
固态氧化物燃料电池 O2- 负极反应
正极反应
7、葡萄糖(C H O)燃料电池
6 12 6
电池类型 导电介质 反应式
酸性燃料电池 H+ 总反应负极反应
正极反应
总反应
碱性燃料电池 OH- 负极反应
正极反应
总反应
熔融碳酸盐燃料电池
CO 负极反应
正极反应
总反应
固态氧化物燃料电池 O2- 负极反应
正极反应
8、CO燃料电池
电池类型 导电介质 反应式
总反应
酸性燃料电池 H+ 负极反应
正极反应
总反应
碱性燃料电池 OH- 负极反应
正极反应
总反应
熔融碳酸盐燃料电池
CO 负极反应
正极反应
总反应
固态氧化物燃料电池 O2- 负极反应
正极反应
9、肼(H N—NH)燃料电池:肼分子可以在氧气中燃烧生成氮气和水
2 2
电池类型 导电介质 反应式
酸性燃料电池 H+ 总反应负极反应
正极反应
总反应
碱性燃料电池 OH- 负极反应
正极反应
10、氨气燃料电池(生成无污染的气体)
电池类型 导电介质 反应式
总反应
酸性燃料电池 H+ 负极反应
正极反应
总反应
碱性燃料电池 OH- 负极反应
正极反应
四、其它新型电池电极反应式的书写
1、锂离子电池
锂离子电池通常都是锂做负极,平衡电荷的也是锂离子,因此可以先写出负极反应
书写技巧 (Li-e-===Li+,至于带x或者C 可以稍加变形加进去即可:LiC-xe-===xLi++
6 x 6
C),正极用总反应减去总反应即可
6
常见锂离子电池电极反应的书写
总反应 Li CoO +LiC LiCoO +C(x<1)
1-x 2 x 6 2 6
钴酸锂电池 负极反应
正极反应
总反应 FePO +Li LiFePO
4 4
磷酸铁锂电
负极反应
池
正极反应
总反应 Li C +Li NiCoMnO C +Li NiCoMnO
x 6 3-x 6 6 3 6
锰酸锂电池 负极反应
正极反应
总反应 xLi+LiV O===Li VO
3 8 1+x 3 8
锂钒氧化物
负极反应
电池
正极反应总反应 2Li+Cu O+HO===2Cu+2Li++2OH-
2 2
锂-铜
负极反应
电池
正极反应
2、高铁电池
高铁电池是一种新型可充电电池,与普通电池相比,该电池能较长时间保持稳定的放电电压。高铁电池的总
反应为3Zn+2KFeO+8HO===3Zn(OH) +2Fe(OH) +4KOH。请回答下列问题:
2 4 2 2 3
(1) 放 电 时 , 正 极 发 生 ________( 填 “ 氧 化 ” 或 “ 还 原 ” ) 反 应 , 则 负 极 反 应 式 为
________________________________,
正极反应式为_________________________________________
(2)放电时,________(填“正”或“负”)极附近溶液的碱性增强
3、镍氢电池
用吸收H 后的稀土储氢合金作为电池负极材料(用MH表示),NiO(OH)作为电池正极材料,KOH溶液作为电
2
解质溶液,可制得高容量、长寿命的镍氢电池。电池充放电时的总反应为:NiO(OH)+MH===Ni(OH) +M
2
电 池 放 电 时 , 负 极 的 电 极 反 应 式 为 _________________________ , 正 极 反 应 式 为
___________________________
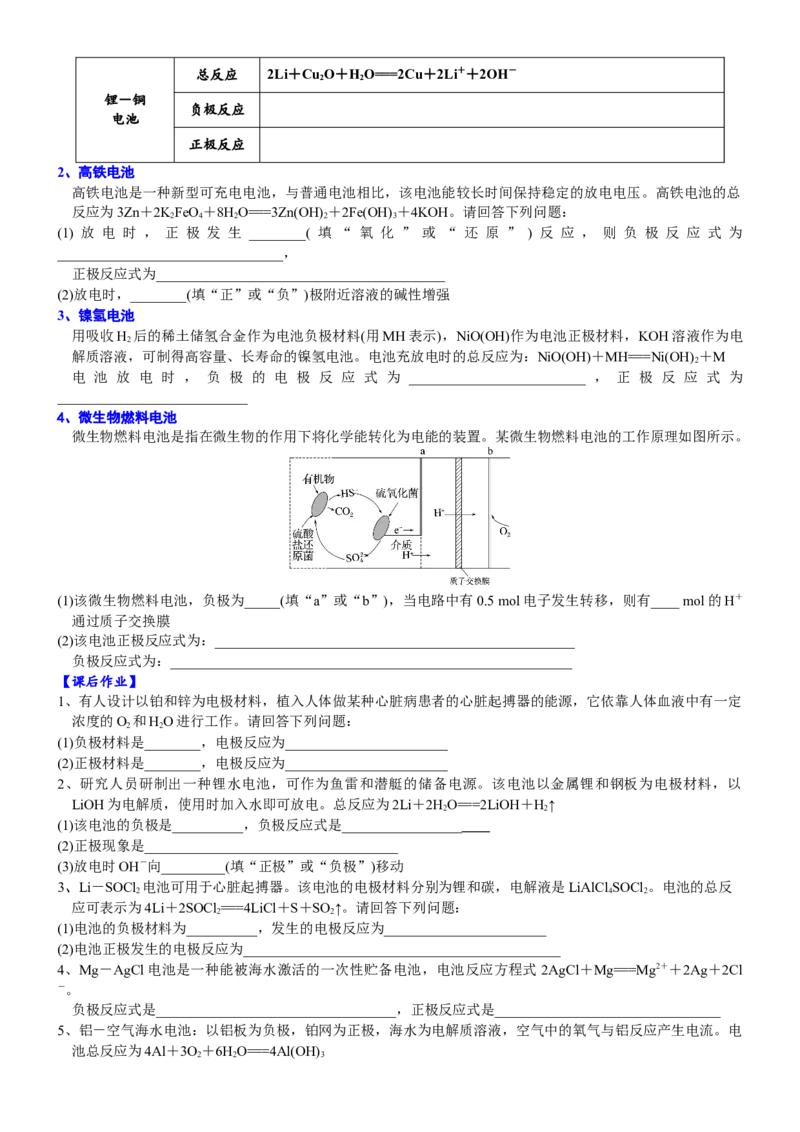
4、微生物燃料电池
微生物燃料电池是指在微生物的作用下将化学能转化为电能的装置。某微生物燃料电池的工作原理如图所示。
(1)该微生物燃料电池,负极为_____(填“a”或“b”),当电路中有0.5 mol电子发生转移,则有____ mol的H+
通过质子交换膜
(2)该电池正极反应式为:___________________________________________________
负极反应式为:_________________________________________________________
【课后作业】
1、有人设计以铂和锌为电极材料,植入人体做某种心脏病患者的心脏起搏器的能源,它依靠人体血液中有一定
浓度的O 和HO进行工作。请回答下列问题:
2 2
(1)负极材料是________,电极反应为_______________________
(2)正极材料是________,电极反应为_______________________
2、研究人员研制出一种锂水电池,可作为鱼雷和潜艇的储备电源。该电池以金属锂和钢板为电极材料,以
LiOH为电解质,使用时加入水即可放电。总反应为2Li+2HO===2LiOH+H↑
2 2
(1)该电池的负极是__________,负极反应式是_________________
(2)正极现象是____________________________________
(3)放电时OH-向_________(填“正极”或“负极”)移动
3、Li-SOCl 电池可用于心脏起搏器。该电池的电极材料分别为锂和碳,电解液是LiAlCl SOCl 。电池的总反
2 4 2
应可表示为4Li+2SOCl ===4LiCl+S+SO ↑。请回答下列问题:
2 2
(1)电池的负极材料为__________,发生的电极反应为_______________________
(2)电池正极发生的电极反应为_____________________________________________
4、Mg-AgCl电池是一种能被海水激活的一次性贮备电池,电池反应方程式 2AgCl+Mg===Mg2++2Ag+2Cl
-。
负极反应式是__________________________________,正极反应式是________________________________
5、铝-空气海水电池:以铝板为负极,铂网为正极,海水为电解质溶液,空气中的氧气与铝反应产生电流。电
池总反应为4Al+3O+6HO===4Al(OH)
2 2 3负极反应式是__________________________________,正极反应式是________________________________
6、肼分子(H N—NH)可以在氧气中燃烧生成氮气和水,利用肼、氧气与KOH溶液组成碱性燃料电池,请写出
2 2
该电池的负极反应式:_________________________________,正极反应式:
_____________________________,
总反应式:________________________________________
7、以甲醇(CHOH)为燃料,空气为氧化剂,以熔融KCO 为电解质环境的燃料电池,负极反应式为
3 2 3
_____________________________________,正极反应式为________________________________
8、科学家预言,燃料电池是21世纪获得电能的重要途径。甲醇燃料电池是采用铂或碳化钨作电极催化剂,在
硫酸电解质溶液中直接加入纯化后的甲醇,同时向一个电极通入空气。试回答以下问题:
(1)配平电池放电时发生的化学方程式:CHOH+____O―→____CO+____HO
3 2 2 2
(2)在硫酸电解质溶液中,CHOH失去电子,此电池的正极发生的反应是_____________________________,
3
负极发生的反应是____________________________________
(3)电解质溶液中的H+向________极移动,向外电路释放电子的电极是________极
9、酸性锌锰干电池是一种一次性电池,外壳为金属锌,中间是碳棒,其周围是由碳粉、MnO 、ZnCl 和NH Cl
2 2 4
等组成的糊状填充物。该电池放电过程产生MnOOH。回收处理该废电池可得到多种化工原料。该电池的正
极反应式为________________,电池反应的离子方程式为______________________________
10、二甲醚(CHOCH )直接燃料电池具有启动快、效率高等优点,其能量密度高于甲醇直接燃料电池(5.93
3 3
kW·h·kg-1)。若电解质为酸性,二甲醚直接燃料电池的负极反应为_________________________________
11、钴酸锂电池的正极采用钴酸锂(LiCoO ),负极采用金属锂和碳的复合材料,该电池充放电时的总反应式:
2
LiCoO +6C Li CoO+LiC ,写出放电时负极的电极反应____________________
2 1-x 2 x 6
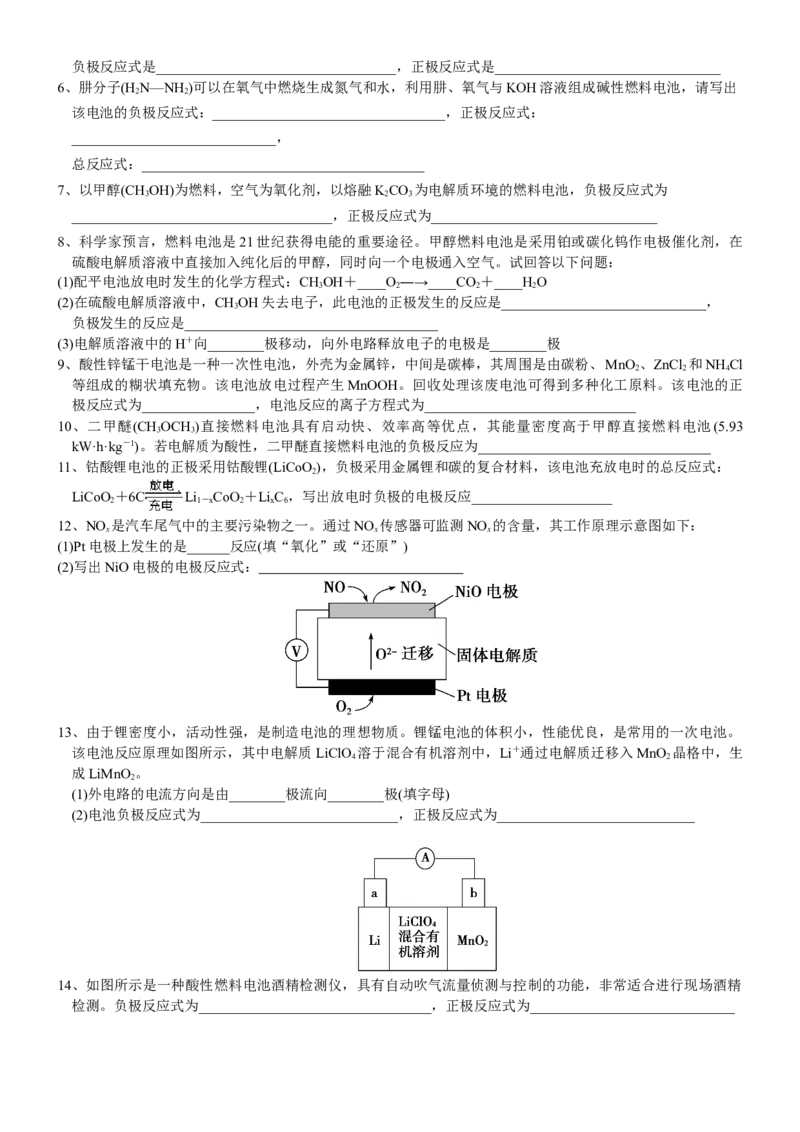
12、NO 是汽车尾气中的主要污染物之一。通过NO 传感器可监测NO 的含量,其工作原理示意图如下:
x x x
(1)Pt电极上发生的是______反应(填“氧化”或“还原”)
(2)写出NiO电极的电极反应式:
13、由于锂密度小,活动性强,是制造电池的理想物质。锂锰电池的体积小,性能优良,是常用的一次电池。
该电池反应原理如图所示,其中电解质LiClO 溶于混合有机溶剂中,Li+通过电解质迁移入MnO 晶格中,生
4 2
成LiMnO 。
2
(1)外电路的电流方向是由________极流向________极(填字母)
(2)电池负极反应式为____________________________,正极反应式为____________________________
14、如图所示是一种酸性燃料电池酒精检测仪,具有自动吹气流量侦测与控制的功能,非常适合进行现场酒精
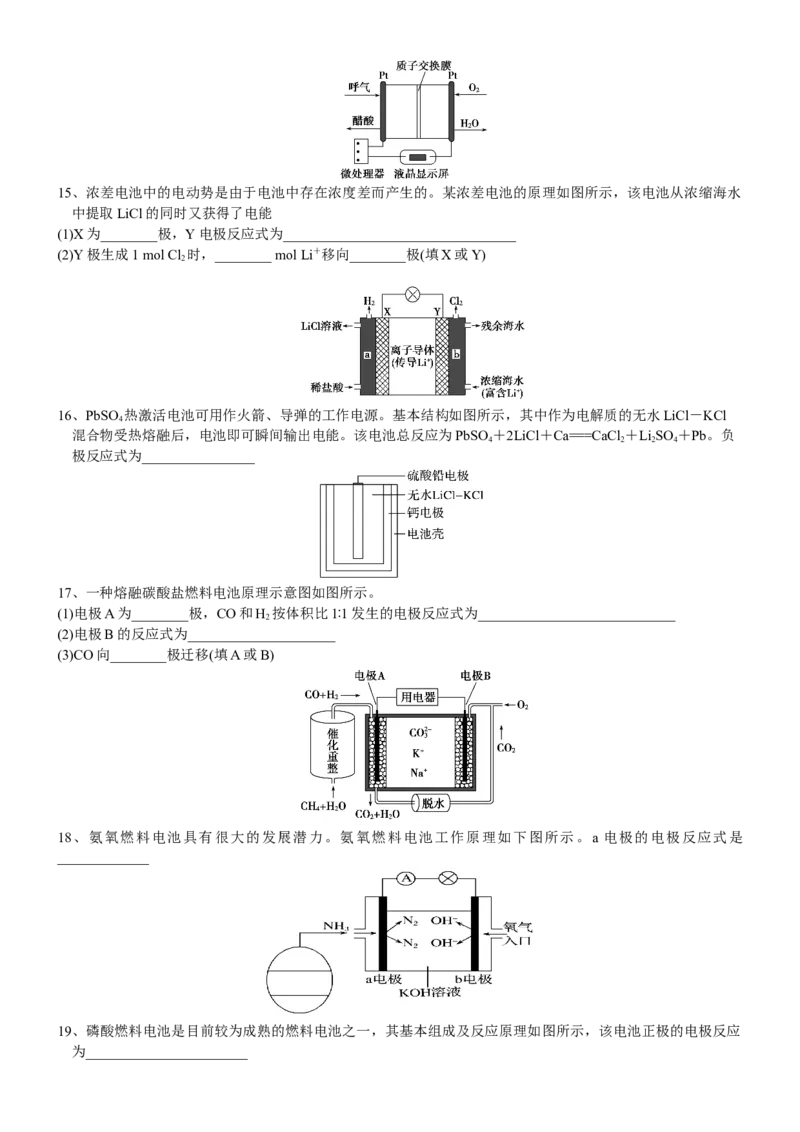
检测。负极反应式为_________________________________,正极反应式为_____________________________15、浓差电池中的电动势是由于电池中存在浓度差而产生的。某浓差电池的原理如图所示,该电池从浓缩海水
中提取LiCl的同时又获得了电能
(1)X为________极,Y电极反应式为_________________________________
(2)Y极生成1 mol Cl 时,________ mol Li+移向________极(填X或Y)
2
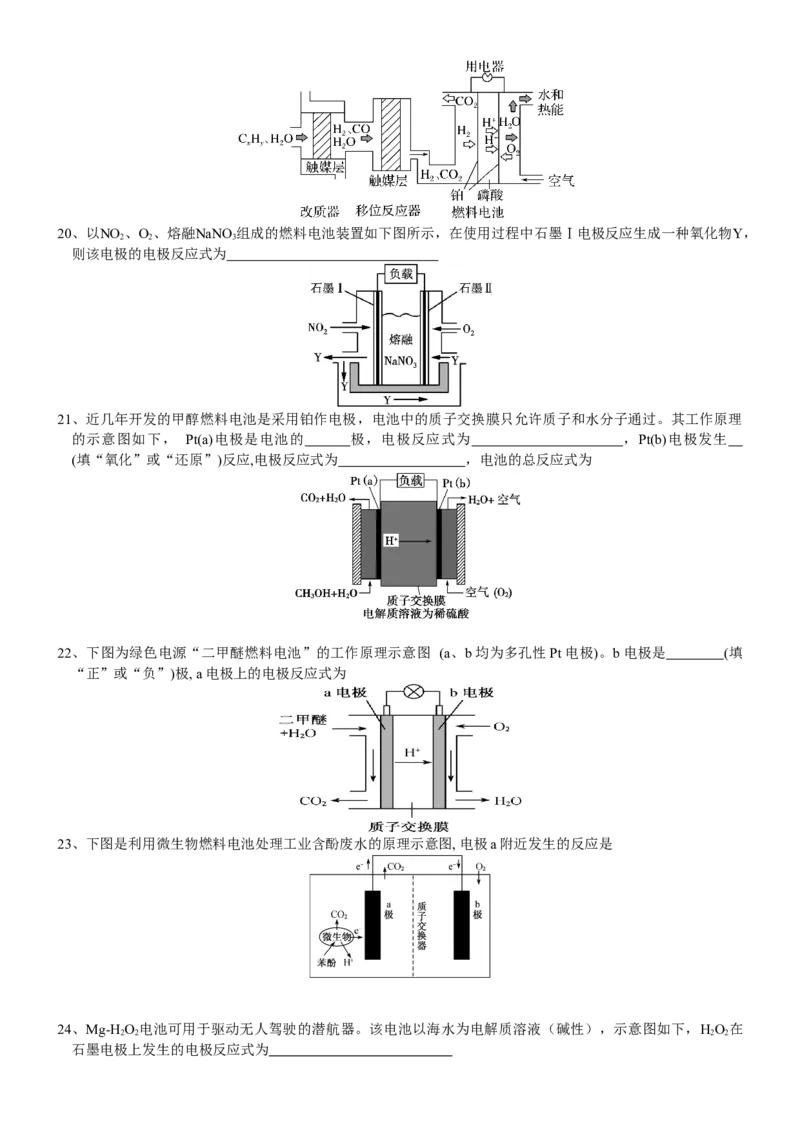
16、PbSO 热激活电池可用作火箭、导弹的工作电源。基本结构如图所示,其中作为电解质的无水LiCl-KCl
4
混合物受热熔融后,电池即可瞬间输出电能。该电池总反应为PbSO +2LiCl+Ca===CaCl +LiSO +Pb。负
4 2 2 4
极反应式为________________
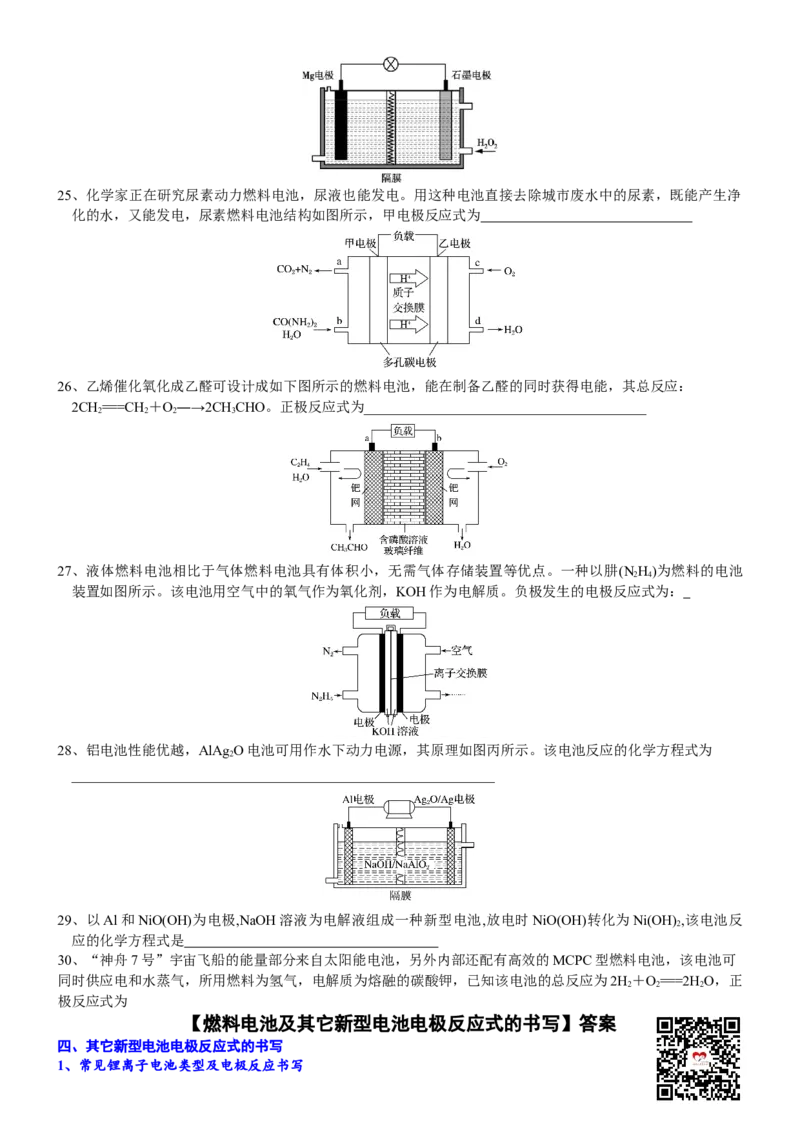
17、一种熔融碳酸盐燃料电池原理示意图如图所示。
(1)电极A为________极,CO和H 按体积比1∶1发生的电极反应式为____________________________
2
(2)电极B的反应式为_____________________
(3)CO向________极迁移(填A或B)
18、氨氧燃料电池具有很大的发展潜力。氨氧燃料电池工作原理如下图所示。a 电极的电极反应式是
_____________
19、磷酸燃料电池是目前较为成熟的燃料电池之一,其基本组成及反应原理如图所示,该电池正极的电极反应
为_______________________20、以NO 、O 、熔融NaNO 组成的燃料电池装置如下图所示,在使用过程中石墨Ⅰ电极反应生成一种氧化物Y,
2 2 3
则该电极的电极反应式为
21、近几年开发的甲醇燃料电池是采用铂作电极,电池中的质子交换膜只允许质子和水分子通过。其工作原理
的示意图如下, Pt(a)电极是电池的 极,电极反应式为 ,Pt(b)电极发生
(填“氧化”或“还原”)反应,电极反应式为 ,电池的总反应式为
22、下图为绿色电源“二甲醚燃料电池”的工作原理示意图 (a、b均为多孔性Pt电极)。b电极是 (填
“正”或“负”)极, a电极上的电极反应式为
23、下图是利用微生物燃料电池处理工业含酚废水的原理示意图, 电极a附近发生的反应是
24、Mg-H O 电池可用于驱动无人驾驶的潜航器。该电池以海水为电解质溶液(碱性),示意图如下,HO 在
2 2 2 2
石墨电极上发生的电极反应式为25、化学家正在研究尿素动力燃料电池,尿液也能发电。用这种电池直接去除城市废水中的尿素,既能产生净
化的水,又能发电,尿素燃料电池结构如图所示,甲电极反应式为
26、乙烯催化氧化成乙醛可设计成如下图所示的燃料电池,能在制备乙醛的同时获得电能,其总反应:
2CH===CH +O―→2CHCHO。正极反应式为________________________________________
2 2 2 3
27、液体燃料电池相比于气体燃料电池具有体积小,无需气体存储装置等优点。一种以肼(N H)为燃料的电池
2 4
装置如图所示。该电池用空气中的氧气作为氧化剂,KOH作为电解质。负极发生的电极反应式为:
28、铝电池性能优越,AlAg O电池可用作水下动力电源,其原理如图丙所示。该电池反应的化学方程式为
2
____________________________________________________________
29、以Al和NiO(OH)为电极,NaOH溶液为电解液组成一种新型电池,放电时NiO(OH)转化为Ni(OH) ,该电池反
2
应的化学方程式是
30、“神舟7号”宇宙飞船的能量部分来自太阳能电池,另外内部还配有高效的MCPC型燃料电池,该电池可
同时供应电和水蒸气,所用燃料为氢气,电解质为熔融的碳酸钾,已知该电池的总反应为2H+O===2H O,正
2 2 2
极反应式为
【燃料电池及其它新型电池电极反应式的书写】答案
四、其它新型电池电极反应式的书写
1、常见锂离子电池类型及电极反应书写锂离子电池通常都是锂做负极,平衡电荷的也是锂离子,因此可以先写出负极反应
书写技巧 (Li-e-===Li+,至于带x或者C 可以稍加变形加进去即可:LiC-xe-===xLi++
6 x 6
C),正极用总反应减去总反应即可
6
常见锂离子电池电极反应的书写
总反应 Li CoO +LiC LiCoO +C(x<1)
1-x 2 x 6 2 6
钴酸锂电池
负极反应 LiC-xe-===xLi++C
x 6 6
正极反应 Li CoO +xe-+xLi+===LiCoO
1-x 2 2
总反应 FePO +Li LiFePO
4 4
磷酸铁锂电
池 负极反应 Li-e-===Li+
正极反应 FePO +Li++e-===LiFePO
4 4
总反应 LixC6+Li3-xNiCoMnO6 C6+Li3NiCoMnO6
锰酸锂电池
负极反应 LiC-xe-===xLi++C
x 6 6
正极反应 Li3-xNiCoMnO6 +xe-+xLi+===Li3NiCoMnO6
总反应 xLi+LiV O===Li VO
3 8 1+x 3 8
锂钒氧化物
负极反应 xLi-xe-=== xLi+
电池
正极反应 xLi++LiV O+xe-===Li VO
3 8 1+x 3 8
总反应 2Li+Cu O+HO===2Cu+2Li++2OH-
2 2
锂-铜
负极反应 Li-e-===Li+
电池
正极反应 Cu O+HO+2e-===2Cu+2OH-
2 2
2、(1)还原 3Zn-6e-+6OH-===3Zn(OH)
2
2FeO2—+6e-+8HO===2Fe(OH) +10OH-
4 2 3
(2)正
解析:根据高铁电池放电时的总反应式可知,Zn为负极,负极反应为3Zn-6e-+6OH-===3Zn(OH) ,由电池
2
的总反应-负极反应=正极反应可知,正极反应为2FeO2—+6e-+8HO===2Fe(OH) +10OH-,正极区生成OH
4 2 3
-且消耗水,OH-浓度增大,故正极附近溶液的碱性增强。
3、MH-e-+OH-===M+HO NiO(OH)+HO+e-+OH-===Ni(OH)
2 2 2
解析:负极实际上是稀土储氢合金吸附的H 失去电子生成H+,H+再与OH-结合生成HO,所以负极的电极反
2 2
应式为MH-e-+OH-===M+HO。充电时阳极发生氧化反应,反应式为Ni(OH) -e-+OH-===NiO(OH)+
2 2
HO。
2
4、(1)a 0.5
(2)2O +8e-+8H+===4HO,HS-+4HO-8e-===SO+9H+
2 2 2
解析:(1)根据图示,在硫氧化菌作用下HS-转化为SO,发生氧化反应:HS-+4HO-8e-===SO+9H+;电极
2
a上发生氧化反应,电极a为负极,b为正极,正极上发生还原反应:2O +8e-+8H+===4HO,当电路中有0.5
2 2
mol电子发生转移,则有0.5 mol H+通过质子交换膜。
【课后作业】
1、(1)锌 2Zn-4e-===2Zn2+ (2)铂 O+2HO+4e-===4OH-
2 2
2、(1)锂 Li-e-===Li+ (2)有无色气体产生 (3)负极
3、(1)锂 4Li-4e-===4Li+ (2)2SOCl +4e-===4Cl-+S+SO ↑
2 2
4、负极:Mg-2e-===Mg2+ 正极:2AgCl+2e-===2Ag+2Cl-
5、4Al-12e-===4Al3+ 3O+6HO+12e-===12OH-
2 2
6、NH-4e-+4OH-===4HO+N O+4e-+2HO===4OH- NH+O===N+2HO
2 4 2 2 2 2 2 4 2 2 2
7、2CH OH-12e-+6CO===8CO +4HO 3O+12e-+3CO ===6CO
3 2 2 2 2
8、(1)2 3 2 4 (2)3O +12H++12e-===6HO 2CH OH+2HO-12e-===2CO +12H+ (3)正 负
2 2 3 2 2
9、MnO +H++e-===MnOOH 2MnO +Zn+2H+===2MnOOH+Zn2+
2 2
10、CH OCH -12e-+3HO===2CO+12H+
3 3 2 2
11、LiC-xe-===C +xLi+
x 6 612、①还原 ②NO+O2--2e-===NO
2
13、(1)b a (2)Li-e-===Li+ MnO +e-+Li+===LiMnO
2 2
14、CHOH-4e-+HO===CHCOOH+4H+ O+4e-+4H+===2H O
2 5 2 3 2 2
15、正 2Cl--2e-===Cl↑ 2 X
2
16、Ca+2Cl--2e-===CaCl
2
17、(1)负 CO+H-4e-+2CO===3CO+HO (2)O+4e-+2CO ===2CO (3)A
2 2 2 2 2
18、2NH -6e-+6OH-===N +6HO
3 2 2
19、O+4H++4e-===2H O
2 2
20、NO + NO 2--e-=N O
2 3 2 5
21、负 CH OH+H O-6e-=CO↑+6H+还原 O+4H++4e-=2H O 2CH OH+3O =2CO+4H O
3 2 2 2 2 3 2 2 2
22、正 CH OCH -12e-+3H O=2CO ↑+12H+
3 3 2 2
23、CHO-28e-+11HO 6CO ↑+28H+
6 6 2 2
24、HO+2e-=2OH-
2 2
25、CO(NH )+HO-6e-===CO+N+6H+
2 2 2 2 2
26、O+4H++4e-===2H O
2 2
27、NH+4OH--4e-===N +4HO
2 4 2 2
28、2Al+3Ag O+2NaOH===2NaAlO +6Ag+HO
2 2 2
29、Al+3NiO(OH)+NaOH+H O=NaAlO +3Ni(OH)
2 2 2
30、H+CO-2e-===CO↑+HO
2 2 2