文档内容
化学反应速率
【学习目标】
1、掌握化学反速率的概念及表示方法
2、掌握有关化学反应速率的计算方法
【主干知识梳理】
一、化学反应速率
1、意义:化学反应速率是用来衡量化学反应过程进行快慢程度的物理量
2、表示方法:通常用 单位时间内反应物浓度的减少量或生成物浓度的增加量 ( 均取正值 )来表示
3、表达式:v=或v=
式中:Δc为浓度的变化量,一般以 mol·L - 1 为单位;Δt为时间,一般以 s 或 min 为单位
如:某反应的反应物浓度在5 min内由6 mol/L变成了2 mol/L,则以该反应物浓度的变化表示的该反应在这
段时间内的平均反应速率为 0.8_mol/(L·min)
4、单位:mol/(L·s)、mol/(L·min)、mol/(L·h)
5、适用范围:所有的化学反应 (主要是气体和溶液)
如:在一个体积为2 L的密闭容器中发生反应2SO +O 2SO ,经过5 s后,测得SO 的物质的量为0.8
2 2 3 3
mol。填写下表:
有关反应物质 SO O SO
2 2 3
物质的量浓度变化 0.4 mol·L - 1 0.2 mol·L - 1 0.4 mol·L - 1
化学反应速率 0.08 mol·L - 1 ·s - 1 0.04 mol·L - 1 ·s - 1 0.08 mol·L - 1 ·s - 1
化学反应速率之比 2∶1∶2
【微点拨】
①对于一个具体的化学反应,反应物和生成物的物质的量的变化是按化学方程式中化学计量数之比进行的,
所以化学反应中各物质的反应速率之比等于化学方程式中各物质的化学计量数之比
对于反应aA+bB===cC+dD(A、B、C、D均不是固体或纯液体):
则:v(A)∶v(B)∶v(C)∶v(D)=Δn(A)∶Δn(B)∶Δn(C)∶Δn(D)=Δc(A)∶Δc(B)∶Δc(C)∶Δc(D)=a∶b∶c∶d
②在同一时间内的同一个化学反应里,虽然用不同物质表示的化学反应速率不一定相同,但它们表示的意义
相同,即一种物质的化学反应速率就代表了整个化学反应的反应速率
③表示化学反应速率时,必须指明具体的物质,因为同一化学反应,用不同的物质表示的反应速率,其数值
可能不同。如:化学反应N+3H 2NH ,用H 表示该反应的反应速率时应写成v(H )
2 2 3 2 2
④浓度是指物质的量浓度而不是物质的量或质量分数
⑤化学反应速率与时间和浓度有关,无论是用反应物浓度的减少还是用生成物浓度的增加来表示,都取正值
⑥化学反应速率有瞬时速率和平均速率之分。由于在中学里研究的是一段时间内的化学反应,因此化学反应
速率是指平均反应速率
⑦在一定温度下,对于固体和纯液体物质来说,其单位体积里的物质的量不会改变,即它们的物质的量浓度
为常数,即Δc=0(无意义),所以不用固体或纯液体表示反应速率
【对点训练1】
1、判断正误,正确的划“√”,错误的划“×”
(1)对于任何化学反应来说,反应速率越大,反应现象就越明显( )
(2)化学反应速率是指一定时间内任何一种反应物浓度的减少或任何一种生成物浓度的增加( )
(3)化学反应速率为0.8mol·L-1·s-1是指1s时某物质的浓度为0.8mol·L-1( )
(4)由v=计算平均速率,用反应物表示为正值,用生成物表示为负值( )
(5)同一化学反应,相同条件下用不同物质表示的反应速率,其数值可能不同,但表示的意义相同( )
(6)根据反应速率的大小可以判断化学反应进行的快慢( )
二、“三段式”法在化学反应速率计算中的应用
例:在一定条件下,向 2 L 密闭容器中充入 2 mol N 和 4 mol H 发生反应 N(g)+3H(g)
2 2 2 2
2NH (g),10 min时测定生成NH 1 mol,则用N、H、NH 表示的平均反应速率分别为多少?
3 3 2 2 3
N(g) + 3H(g) 2NH (g) 在“三段式”中,转化的部分是按照化学计量系
2 2 3
起始 2 mol 4 mol 0 数进行反应的转化 0.5 mol 1.5 mol 1 mol
末 1.5 mol 2.5 mol 1 mol
v(N )==0.025 mol/(L·min)
2
v(H )==0.075 mol/(L·min)
2
v(NH )==0.05 mol/(L·min)
3
1、反应的转化率(α):指已被转化的反应物的物质的量与其初始的物质的物质的量之比
N 的转化率= ,H 的转化率=
2 2
2、生成物的产率:指生成物的实际值与理论值(按照方程式计算的出来的)的比值
NH 的产率=
3
3、反应结束时各物质的浓度
c(N )= ,c(H)= ,c(NH )=
2 2 3
4、反应结束时各物质的百分含量(气体的体积分数、物质的量分数、质量分数)
N 的体积分数=
2
H 的体积分数=
2
NH 的体积分数=
3
5、恒温时,两种容器
恒温恒容 恒温恒压
恒温、恒容时: 恒温、恒压时:
【对点训练2】
1、恒温下,将1 mol N 和3 mol H 在体积为2 L的容器中混合,发生如下反应:N(g)+3H(g) 2NH (g),2 s
2 2 2 2 3
时测得NH 的体积分数为25%。则下列说法中不正确的是 ( )
3
A.用N 浓度的减少表示的平均反应速率为0.2 mol·L-1·s-1 B. 2 s时N 的转化率为40%
2 2
C.2 s时混合气体中n(N ):n(H ):n(NH )=3:9:4 D.2 s 时NH 的浓度为0.4 mol·L-1
2 2 3 3
三、化学反应速率的相关计算的常见题型
题型一、求化学反应速率
1、反应3X(g)+Y(g) 2Z(g)+2W(g)在2 L密闭容器中进行,5 min后Y减少了0.5 mol,则此反应的速率为(
)
A.v(X)=0.05 mol·L-1·min-1 B.v(Z)=0.10 mol·L-1·min-1
C.v(Y)=0.10 mol·L-1·min-1 D.v(W)=0.05 mol·L-1·min-1
2、反应2SO +O 2SO 经一段时间后,SO 的浓度增加了0.4 mol·L-1,在这段时间内用O 表示的反应速率
2 2 3 3 2
为0.04 mol·L-1·s-1,则这段时间为( )
A.0.1 s B.2.5 s C.5 s D.10 s题型二、化学反应反应速率快慢的比较
3、反应:3A(g)+B(g)===2C(g)+2D(g),在不同条件下,用不同物质表示其反应速率,①v(A)=0.6mol·L-1·min-
1 ②v(B)=0.45 mol·L-1·min-1 ③v(C)=0.015 mol·L-1·min-1 ④v(D)=0.45 mol·L-1·min-1。则此反应在不
同条件下进行最快的是( )
A.②③ B.①③ C.②④ D.②
4、对于可逆反应A(g)+3B(s) 2C(g)+2D(g),在不同条件下的化学反应速率如下,其中表示的反应速率最
快的是( )
A.v(A)=0.5mol·L-1·min-1 B.v(B)=1.2mol·L-1·s-1
C.v(D)=0.4mol·L-1·min-1 D.v(C)=0.1mol·L-1·s-1
【解法思路】同一化学反应速率用不同物质表示时数值可能不同,比较化学反应速率的快慢不能只看数值大小,
还要进行一定的转化
①看单位是否统一,若不统一,换算成相同的单位
②换算成同一物质表示的速率,再比较数值的大小
③比较化学反应速率与化学计量数的比值。如反应aA+bB cC,要比较v(A)与v(B)的相对大小,即:比
较的相对大小,若,则用v(A)表示的反应速率比用v(B)表示的反应速率大
题型三、根据各物质的反应速率之比写出化学方程式
5、在密闭容器中进行可逆反应,A与B反应生成C,其反应速率分别用v(A)、v(B)、v(C)(mol·L-1·s-1)表示,且
v(A)、v(B)、v(C)之间有如下所示的关系:v(B)=3v(A);3v(C)=2v(B)。则此反应可表示为( )
A.2A+3B 2C B.A+3B 2C C.A+3B 3C D.A+B C
6、已知某反应的各物质浓度数据如下:
aA(g)+bB(g) 2C(g)
起始浓度(mol·L-1) 3.0 1.0 0
2 s末浓度(mol·L-1) 1.8 0.6 0.8
据此可推算出上述反应化学方程式中,各物质的化学计量数之比是( )
A.9∶3∶4 B.3∶1∶2 C.2∶1∶3 D.3∶2∶1
题型四、化学反应速率的图像题
7、一定温度下,向容积为2 L的密闭容器中通入两种气体发生化学反应,反应中各物质的物质的量变化如图所
示,下列对该反应的推断合理的是( )
A.该反应的化学方程式为3B+4D 6A+2C
B.反应进行到6 s时B的转化率为40%
C.反应进行到6 s时,B的平均反应速率为0.05 mol·L-1·s-1
D.反应进行到6 s时,各物质的反应速率相等
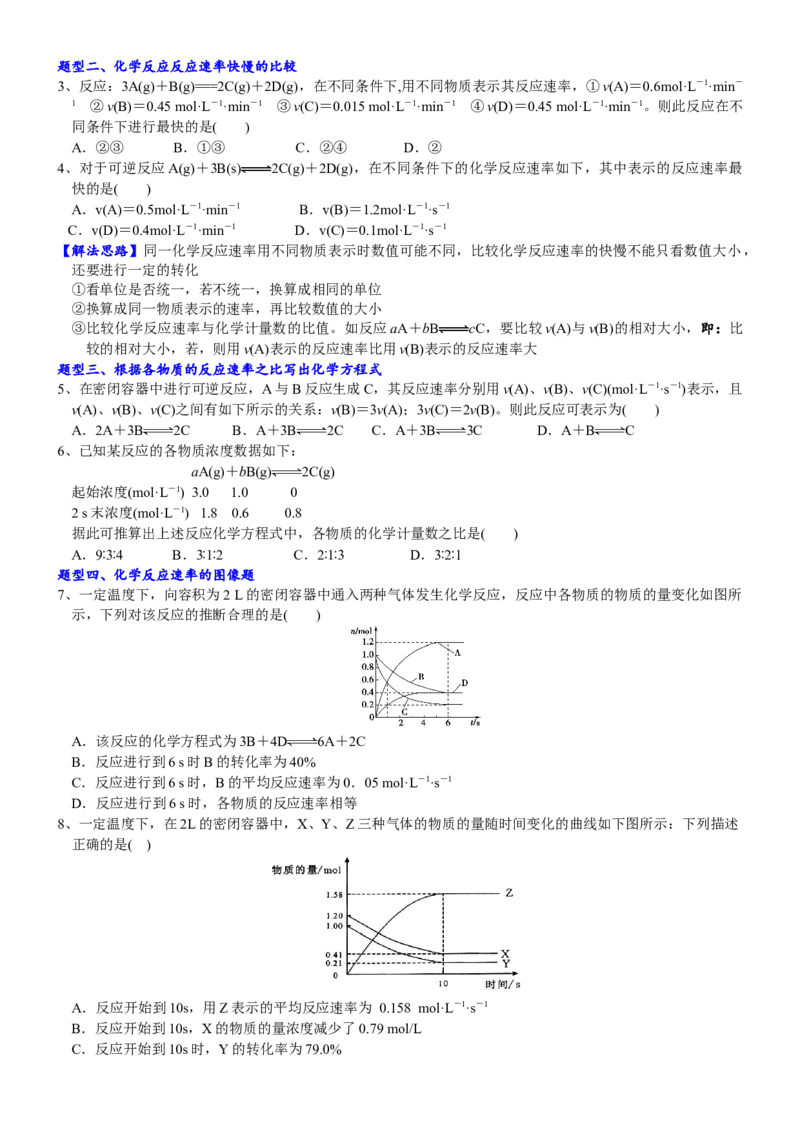
8、一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如下图所示:下列描述
正确的是( )
A.反应开始到10s,用Z表示的平均反应速率为 0.158 mol·L-1·s-1
B.反应开始到10s,X的物质的量浓度减少了0.79 mol/L
C.反应开始到10s时,Y的转化率为79.0%D.反应的化学方程式为:X(g)+Y(g) Z(g)
题型五、“三段式”法在化学反应速率计算中的妙用
9、将4 mol A气体和2 mol B气体在2 L的容器中混合并在一定条件下发生如下反应:2A(g)+B(g) 2C(g)。
若经2 s后测得C的浓度为0.6 mol·L-1,现有下列几种说法,其中正确的是( )
①用物质A表示的反应的平均速率为0.3 mol·L-1·s-1 ②用物质B表示的反应的平均速率为0.6 mol·L-1·s-1
③2 s时物质B的浓度为0.7 mol·L-1 ④2 s末,物质A的转化率为70%
A.①④ B.①③ C.②④ D.③④
10、可逆反应aA(g)+bB(g) cC(g)+dD(g),取amolA和bmolB置于VL的容器中,1min后,测得容器内A
的浓度为xmol·L-1。这时B的浓度为__________mol·L-1,C的浓度为__________mol·L-1。这段时间内反应
的平均速率若以物质A的浓度变化来表示,应为_____________
【课后作业】
1、下列关于化学反应速率的说法,不正确的是( )
A.化学反应速率是衡量化学反应进行快慢程度的物理量
B.化学反应速率的大小主要取决于反应物的性质
C.化学反应速率可以用单位时间内生成某物质的质量的多少来表示
D.化学反应速率常用单位有mol·L-1·s-1或mol·L-1·min-1
2、下列关于化学反应速率的说法正确的是( )
A.对于任何化学反应来说,反应速率越大,反应现象就越明显
B.化学反应速率通常表示一定时间内任何一种反应物浓度的减少或任何一种生成物浓度的增加
C.化学反应速率为0.8 mol·L-1·s-1是指1 s时某物质的浓度为0.8 mol·L-1
D.根据化学反应速率的大小可以知道化学反应进行的快慢
3、下列关于化学反应速率的说法中正确的是( )
A.化学反应速率可用某时刻生成物的物质的量来表示
B.在同一反应中,用反应物或生成物表示的化学反应速率的值是相等的
C.化学反应速率是指反应进行的时间内,反应物浓度的减少或生成物浓度的增加
D.可用单位时间内氢离子物质的量浓度的变化来表示氢氧化钠和硫酸的反应速率
4、已知合成氨反应的浓度数据如下:
N+3H 2NH
2 2 3
N H NH
2 2 3
起始浓度/mol·L-1 1.0 3.0 0
2 s末浓度/mol·L-1 0.6 1.8 0.8
当用氨气浓度的增加来表示该化学反应的速率时,其速率为( )
A.0.2 mol·L-1·s-1 B.0.4 mol·L-1·s-1 C.0.6 mol·L-1·s-1 D.0.8 mol·L-1·s-1
5、1 L的密闭容器中,发生反应4A(s)+3B(g)===2C(g)+D(g),经2 min后B的浓度减少0.6 mol·L-1。对此反应
速率的正确表示是( )
A.用A表示的反应速率是0.4 mol·L-1·min-1
B.用B、C、D分别表示反应的速率,其比值是3∶2∶1
C.在2 min末的反应速率用B表示是0.3 mol·L-1·min-1
D.在这2 min内用B表示的速率的值逐渐减小,用C表示的速率的值逐渐增大
6、对于反应2A(g)+B(g) 3C(g)+4D(g),下列表示的反应速率最快的是( )
A.v(A)=0.5 mol·L-1·s-1 B.v(B)=0.3 mol·L-1·s-1
C.v(C)=0.8 mol·L-1·s-1 D.v(D)=1 mol·L-1·s-1
7、已知4NH (g)+5O(g)=====4NO(g)+6HO(g),若反应速率分别用v(NH )、v(O )、v(NO)、v(H O)表示,则
3 2 2 3 2 2
正确的关系式为( )
A.4v(NH )=5v(O ) B.5v(O )=6v(H O) C.2v(NH )=3v(H O) D.4v(O )=5v(NO)
3 2 2 2 3 2 2
8、对于化学反应3W(g)+2X(g)===4Y(g)+3Z(g),下列反应速率关系中,正确的是( )A.v(W)=3v(Z) B.2v(X)=3v(Z) C.2v(X)=v(Y) D.3v(W)=2v(X)
9、温度不变的条件下,在恒容的密闭容器中进行反应NO(g) 2NO (g),若NO 的浓度由0.1 mol·L-1降到
2 4 2 2 4
0.07 mol·L-1需要15 s,那么NO 的浓度由0.07 mol·L-1降到0.05 mol·L-1反应所需时间为( )
2 4
A.等于5 s B.等于10 s C.大于10 s D.小于10 s
10、某温度下,浓度都是1 mol/L的两种气体X 和Y ,在密闭容器中反应生成气体Z。反应2 min后,测得参
2 2
加反应的X 为0.6 mol/L,用Y 的变化表示的反应速率v(Y )=0.1 mol/(L·min),生成的c(Z)为0.4 mol/L,则
2 2 2
该反应的化学方程式是( )
A.X+2Y 2XY B.2X+Y 2XY
2 2 2 2 2 2
C.3X+Y 2XY D.X+3Y 2XY
2 2 3 2 2 3
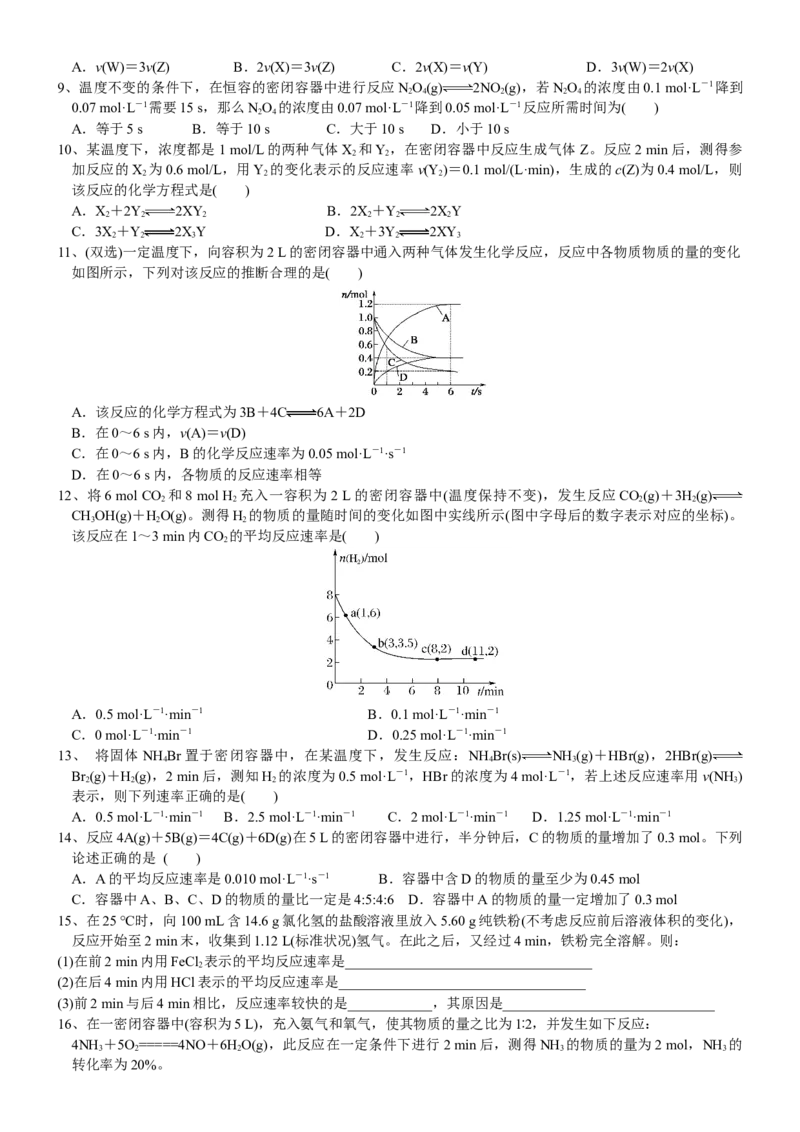
11、(双选)一定温度下,向容积为2 L的密闭容器中通入两种气体发生化学反应,反应中各物质物质的量的变化
如图所示,下列对该反应的推断合理的是( )
A.该反应的化学方程式为3B+4C 6A+2D
B.在0~6 s内,v(A)=v(D)
C.在0~6 s内,B的化学反应速率为0.05 mol·L-1·s-1
D.在0~6 s内,各物质的反应速率相等
12、将6 mol CO 和8 mol H 充入一容积为2 L的密闭容器中(温度保持不变),发生反应CO(g)+3H(g)
2 2 2 2
CHOH(g)+HO(g)。测得H 的物质的量随时间的变化如图中实线所示(图中字母后的数字表示对应的坐标)。
3 2 2
该反应在1~3 min内CO 的平均反应速率是( )
2
A.0.5 mol·L-1·min-1 B.0.1 mol·L-1·min-1
C.0 mol·L-1·min-1 D.0.25 mol·L-1·min-1
13、 将固体NH Br置于密闭容器中,在某温度下,发生反应:NH Br(s) NH (g)+HBr(g),2HBr(g)
4 4 3
Br (g)+H(g),2 min后,测知H 的浓度为0.5 mol·L-1,HBr的浓度为4 mol·L-1,若上述反应速率用v(NH )
2 2 2 3
表示,则下列速率正确的是( )
A.0.5 mol·L-1·min-1 B.2.5 mol·L-1·min-1 C.2 mol·L-1·min-1 D.1.25 mol·L-1·min-1
14、反应4A(g)+5B(g)=4C(g)+6D(g)在5 L的密闭容器中进行,半分钟后,C的物质的量增加了0.3 mol。下列
论述正确的是 ( )
A.A的平均反应速率是0.010 mol·L-1·s-1 B.容器中含D的物质的量至少为0.45 mol
C.容器中A、B、C、D的物质的量比一定是4:5:4:6 D.容器中A的物质的量一定增加了0.3 mol
15、在25 ℃时,向100 mL含14.6 g氯化氢的盐酸溶液里放入5.60 g纯铁粉(不考虑反应前后溶液体积的变化),
反应开始至2 min末,收集到1.12 L(标准状况)氢气。在此之后,又经过4 min,铁粉完全溶解。则:
(1)在前2 min内用FeCl 表示的平均反应速率是___________________________________
2
(2)在后4 min内用HCl表示的平均反应速率是___________________________________
(3)前2 min与后4 min相比,反应速率较快的是____________,其原因是______________________________
16、在一密闭容器中(容积为5 L),充入氨气和氧气,使其物质的量之比为1∶2,并发生如下反应:
4NH +5O=====4NO+6HO(g),此反应在一定条件下进行2 min后,测得NH 的物质的量为2 mol,NH 的
3 2 2 3 3
转化率为20%。(1)以NO的浓度变化表示该反应的平均反应速率是__________________________
(2)O 在2 min时的浓度是____________
2
17、在容积为2 L的密闭容器中进行如下反应:A(g)+2B(g) 3C(g)+nD(g),开始时A为4 mol,B为6 mol;
5 min末时测得C的物质的量为3 mol,用D表示的化学反应速率v(D)为0.2 mol·L-1·min-1。计算:
(1)5 min末A的物质的量浓度为_______________________________________
(2)前5 min内用B表示的化学反应速率v(B)为___________________________
(3)化学方程式中n值为_______________________________________________
(4)此反应在四种不同情况下的反应速率分别为:①v(A)=5 mol·L-1·min-1,②v(B)=6 mol·L-1·min-1,
③v(C)=4.5 mol·L-1·min-1,④v(D)=8 mol·L-1·min-1,其中反应速率最快的是______________
18、将等物质的量的A、B混合于2 L的密闭容器中,发生下列反应:3A(g)+B(g)=xC(g)+2D(g)。经4 min后
测知D的浓度为0.5 mol·L-1,c(A) :c(B)=3:5,C的平均反应速率是0.125 mol·L-1·min-1,此时A的物质的量
浓度为__________,B的平均反应速率为__________,x值是____________
19、(1)在反应A(g)+3B(g)===2C(g)中,若以物质A表示的该反应的化学反应速率为0.2 mol·L-1·min-1,则以物
质B表示此反应的化学反应速率为 mol·L-1·min-1
(2)在2 L的密闭容器中,充入2 mol N 和3 mol H ,在一定条件下发生反应,3 s后测得N 的物质的量为1.9
2 2 2
mol,则以H 的浓度变化表示的反应速率为____________
2
(3)将10 mol A和5 mol B放入容积为10 L的密闭容器中,某温度下发生反应:3A(g)+B(g)2C(g),在最初2
s 内,消耗A的平均速率为0.06 mol·L-1·s-1,则在2 s 时,容器中有 mol A,此时C的物质的量浓度为
____________
20、将0.1 mol MnO 粉末置于50 mL过氧化氢溶液(ρ=1.1 g·mL-1)中,在标准状况下放出气体的体积和时间的关
2
系如图所示
(1)实验时放出气体的总体积是________
(2)放出一半气体所需的时间为________,反应放出气体所需时间为________
(3)A、B、C、D各点反应速率快慢的顺序为________
【化学反应速率】答案
【对点训练1】
1、(1)× (2)× (3)× (4)× (5)√ (6)√
【对点训练2】
1、A
题型一、求化学反应速率
1、B。解析:根据v==,求出用Y表示的化学反应速率,再根据在同一化学反应中,不同物质的化学反应速
率之比等于化学计量数之比进行比较。v(Y)===0.05 mol·L-1·min-1。==,得v(X)=0.15 mol·L-1·min-1,A
错误;==,得v(Z)=0.10 mol·L-1·min-1,B正确;v(Y)=0.05 mol·L-1·min-1,C错误;==,得v(W)=0.10
mol·L-1·min-1,D错误。
2、C。解析:v(O )=0.04 mol·L-1·s-1,则v(SO )=0.08 mol·L-1·s-1,由Δt=Δc(SO )/v(SO ),代入数据计算得Δt
2 3 3 3
=5 s。故选C。
3、D。解析:各物质其反应速率单位相同时,用各反应速率除去化学计量数,比值大的反应速率大。
①=0.2 ②=0.45 ③=0.007 5 ④=0.225,②对应的反应最快,D正确。
4、D。解析:本题可以采用归一法进行求解,通过方程式的计量数将不同物质表示的反应速率折算成同一物质
表示的反应速率进行比较,B项中的B物质是固体,不能表示反应速率;C项中对应的v(A)=0.2mol·L-1·min-
1;D项中对应的v(A)=3mol·L-1·min-1。
5、B
6、B。解析:各物质的反应速率之比等于它们在化学方程式中的化学计量数之比。v(A)==0.6 mol·L-1·s-1,
v(B)==0.2 mol·L-1·s-1,v(C)==0.4 mol·L-1·s-1。化学计量数之比为0.6∶0.2∶0.4,即3∶1∶2。
7、C。解析:Δn(A)∶Δn(B)∶Δn(C)∶Δn(D)=(1.2-0)mol∶(1.0-0.4)mol∶(1.0-0.2)mol∶(0.4-0)mol=6∶3∶4∶2,所以化学方程式为3B+4C 6A+2D,A错误;B的转化率为×100%=60%,B错误;不论在什么时刻,用各物质表示
的速率之比等于化学计量数之比,D错误。
8、C
9、B
10、 -x v(A)=(-x)mol·L-1·min-1
解析 aA(g) +bB(g) cC(g) + dD(g)
起始量mol) a b 0 0
转化量mol(a-Vx) ·b ·c ·d
1min时molVx b-·b ·c ·d
所以此时c(B)=mol·L-1= mol·L-1,c(C)=mol·L-1=(-)mol·L-1,
v(A)==(-x)mol·L-1·min-1。
【课后作业】
1、C。解析:化学反应速率用单位时间内反应物或生成物的浓度变化来表示,而不采用物质的质量或物质的
量。]
2、D。解析:A项,化学反应速率越大,反应现象不一定越明显,如盐酸与氢氧化钠溶液的反应;B项,固体
或纯液体的浓度可视为常数,一般不用固体或纯液体表示化学反应速率;C项,0.8 mol·L-1·s-1表示1 s的时间
内,某物质的浓度变化了0.8 mol·L-1;D项,化学反应速率就是表示化学反应进行快慢的物理量。
3、D。解析:化学反应速率是用单位时间内反应物或生成物浓度的变化值来表示的平均速率,故 A、C两项错
误;因化学反应速率与各反应物、生成物的化学计量系数成正比,如果方程式中反应物与生成物的计量系数不
同,则反应速率的值不相同,B选项错误。
4、B。解析:v(NH )==0.4 mol·L-1·s-1,B项正确。
3
5、B。解析:A为固体,一般不用固体表示反应速率,所以A项错误;同一反应中,用不同物质表示的速率与
方程式中各物质的计量数成正比,B项正确;反应速率为平均值,并非2 min末的速率,所以C项错误;同一
时间段内,用反应物、生成物表示的速率的意义是相同的,变化趋势也是一样的,D项错误。
6、B。解析:正确的思路应是根据反应速率与化学方程式中化学计量数之间的关系将各物质的反应速率转化为
用同一种物质表示的速率。A项中据v(A)推知v(B)=0.25 mol·L-1·s-1,C项中据v(C)推出v(B)≈0.27 mol·L-1·s-
1,D项中据v(D)推出v(B)=0.25 mol·L-1·s-1,故反应速率最快的是B选项。
7、D。解析:在同一化学反应里,各物质的速率之比等于各物质的化学计量数之比。A选项应为5v(NH )=
3
4v(O );B选项应为6v(O )=5v(H O);C选项应为3v(NH )=2v(H O)。
2 2 2 3 2
8、C。解析:速率之比等于化学方程式中的化学计量数之比。A项,v(W)=v(Z);B项,3v(X)=2v(Z);C项,
2v(X)=v(Y);D项,2v(W)=3v(X)。]
9、C。解析:先求前15 s内的平均反应速率
v(N O)==0.002 mol·L-1·s-1,
2 4
根据隐含信息可知,随着反应的进行,15 s以后的平均反应速率减小,即v′(N O)=<0.002 mol·L-1·s-1,故
2 4
Δt>10 s。
10、C。解析:题目要求根据一定物质的浓度变化及物质的化学反应速率来确定物质反应的化学方程式。解题
时需要利用不同物质的化学反应速率与化学方程式计量数之间的关系进行逆向思维。参加反应的 X ,即为在反
2
应中X 物质的浓度变化,则X 表示的反应速率为:v(X )==0.3 mol/(L·min);用Z表示的化学反应速率v(Z)=
2 2 2
=0.2 mol/(L·min)。故X ,Y 和Z反应速率之比即化学方程式中物质的化学计量数之比为 v(X )v(Y )v(Z)=
2 2 2 2
0.3 mol/(L·min)0.1 mol/(L·min)0.2 mol/(L·min)=312。根据原子守恒,可确定Z的化学式为XY,故可得
3
出反应的化学方程式。
11、AC。解析:Δn(A)Δn(B)Δn(C)Δn(D)=(1.2-0) mol(1.0-0.4) mol(1.0-0.2) mol(0.4-0) mol=
6342,所以化学方程式为3B+4C 6A+2D,A正确;不论在什么时刻,用各物质表示的速率之比等于
化学计量数之比,B、D错误。
12、D。解析:由图可知,1~3 min内H 的物质的量的变化量是4.5 mol,则1~3 min内v(H )== mol·L-1·min
2 2
-1,根据化学反应速率之比等于化学计量数之比可知,v(CO)=v(H )=0.25 mol·L-1·min-1。
2 2
13、B
14、B。解析:C的物质的量增加了0.3 mol,也即消耗A为0.3 mol,D错;根据反应速率数学表达式:v(A)==0.002 mol·L-1·s-1,A错;生成D的物质的量为0.3 mol×=0.45 mol,故D的物质的量至少为0.45 mol,B正确;
根据计算容器中A、B、C、D的物质的量比不一定是4:5:4:6,C错。
15、(1)0.250 mol·L-1·min-1
(2)0.250 mol·L-1·min-1
(3)前2 min 随着反应的进行,反应物浓度减小,反应速率减慢
16、(1)0.05 mol·L-1·min-1 (2)0.875 mol·L-1
17、(1)1.5 mol·L-1
(2)0.2 mol·L-1·min-1
(3)2 (4)①
18、0.75 mol·L-1 0.0625 mol·L-1·min-1 2
解析:本题考查了化学反应速率有关计算的应用。由4 min内D的浓度变化量为0.5 mol·L-1,可以求出A、B、
C的浓度变化量分别为×0.5 mol·L-1、×0.5 mol·L-1、×0.5 mol·L-1。设A、B的起始浓度为n,则可以得到下列
关系:
3A(g)+ B(g)= xC(g)+ 2D(g)
n n 0 0
0.75 0.25 0.25x 0.5
(n-0.75) (n-0.25) 0.25x 0.5
由题意c(A) :c(B)=(n-0.75) : (n-0.25)=3:5,n=1.5 mol·L-1,c(A)=(n-0.75) mol·L-1=0.75 mol·L-1,根
据v(B)=或先求v(D),再根据v(B):v(D)=1:2求得v(B)=0.0625 mol·L-1·min-1,根据v(C)v(D)=x2,求得
x=2。
19、(1)0.6
(2)0.05 mol·L-1·s-1
(3)8.8 0.08 mol·L-1
解析:(1)根据化学方程式中的计量数关系:=,v(B)=3v(A)=3×0.2 mol·L-1·min-1=0.6 mol·L-1·min-1。
(2)解法一:3 s内消耗的N 的物质的量为2 mol-1.9 mol=0.1 mol,根据化学方程式N+3H2NH ,可以
2 2 2 3
计算出3 s内消耗的H 的物质的量为0.3 mol,根据化学反应速率的计算公式,v(H )==0.05 mol·L-1·s-1。
2 2
解法二:先计算出用N 表示的化学反应速率:v(N )== mol·L-1·s-1,再根据化学方程式的计量数关系,计算
2 2
出用H 表示的化学反应速率:v(H )=3v(N )=0.05 mol·L-1·s-1。
2 2 2
(3) 3A(g) + B(g) 2C(g)
起始浓度mol·L-1 1.0 0.5 0
转化浓度mol·L-1 0.06×2=0.12 0.04 0.08
2 s时浓度mol·L-1 1.0-0.12=0.88 0.5-0.04=0.46 0.08
则2 s时,n(A)=0.88 mol·L-1×10 L=8.8 mol,c(C)=0.08 mol·L-1。
20、(1)60 mL (2)1 min 2min (3)D>C>B>A