文档内容
关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
重难点突破 必考化学方程式汇总
目 录
必考化学方程式汇总 2
考法01 化学方程式分类训练 4
考法02 化学方程式变式训练 6
考法03 物质间转化关系系列 6
考法04 根据给定信息书写反应方程式 8
必考化学方程式汇总
1关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
1.澄清石灰水中通入二氧化碳气体(非复分解反应) (3)反应完全后,试管中的残余固体是氯化钾和二氧
Ca(OH) +CO=CaCO ↓+HO 化锰的混合物,进行分离的方法是:洗净、干燥、
2 2 3 2
现象:石灰水由澄清变浑浊。 称量。
相关知识点: ②加热高锰酸钾制氧气(分解反应)
可用来检验二氧化碳气体的存在。 2KMnO ====KMnO +MnO+O ↑
4 2 4 2 2
2.镁带在空气中燃烧(化合反应) 相关知识点:在试管口要塞上棉花,避免固体粉末
2Mg+O— \s\up6(点燃)2MgO 滑落堵塞导管。
2 —
③过氧化氢和二氧化锰制氧气(分解反应)
现象:镁在空气中剧烈燃烧,放热,发出耀眼的白
2HO=====2HO+O↑
光,生成白色粉末。 2 2 2 2
共同知识点:
相关知识点:
(1)这个反应中,镁元素从游离态转变成化合态:
(1)向上排空气法收集时导管要伸到集气瓶下方,收
集好后要正放在桌面上;
(2)物质的颜色由银白色转变成白色:
(2)实验结束要先撤导管,后撤酒精灯,避免水槽中
(3)镁可做照明弹:
水倒流炸裂试管;
(4)镁条的着火点高,火柴放热少,不能达到镁的着
(3)加热时试管要略向下倾斜,避免冷凝水回流炸裂
火点,不能用火柴点燃:
试管;
(5)镁很活泼,为了保护镁,在镁表面涂上一层黑色
(4)用排水集气法收集氧气要等到气泡连续均匀地冒
保护膜,点燃前要用砂纸打磨干净。
出再收集;
3.水通电分解(分解反应)
(5)用带火星的小木条放在瓶口验满,伸入瓶中检验
2HO— \s\up8(通电)2H↑+O↑
2 — 2 2
是否是氧气。
现象:通电后,电极上出现气泡,气体体积比约为
6.木炭在空气中燃烧(化合反应)
2 : 1
充分燃烧:C+O — \s\up8(点燃)CO
相关知识点: 2 — 2
不充分燃烧:2C+O — \s\up8(点燃)2CO
(1)正极产生氧气,负极产生氢气: 2 —
现象:
(2)氢气和氧气的 体积比为 2 : 1, 质量比为 1 : 8:
在空气中发出红光;
(3)电解水时,在水中预先加入少量氢氧化钠溶液或
在氧气中发出白光,放热,生成一种使澄清石灰水
稀硫酸,增强水的导电性:
变浑浊的无色气体。
(4)电源为直流电。
相关知识点:反应后的产物可用澄清的石灰水来进
4.生石灰和水反应(化合反应)
行检验。
CaO+HO=Ca(OH)
2 2 7.硫在空气(或氧气)中燃烧(化合反应)
现象:白色粉末溶解,放出大量的热。
S+O— \s\up8(点燃)SO
2 — 2
相关知识点:
现象:在空气中是发出微弱的淡蓝色火焰,在氧气
(1)最终所获得的溶液名称为氢氧化钙溶液,俗称澄
中是发出明亮的蓝紫色火焰,生成无色有刺激性气
清石灰水:
体。
(2)在其中滴入无色酚酞,酚酞会变成红色:
相关知识点:
(3)生石灰是氧化钙,熟石灰是氢氧化钙:
(1)应后的产物可用紫色的石蕊来检验(紫色变成红
(4)发出大量的热。
色);
5.实验室制取氧气
(2)在集气瓶底部事先放少量水或碱溶液(NaOH)以
①加热氯酸钾和二氧化锰的混合物制氧气(分解反 吸收生成的二氧化硫,防止污染空气。
应) 8.铁丝在氧气中燃烧(化合反应)
2KClO =====2KCl+3O↑
3 2 3Fe+2O — \s\up8(点燃)Fe O
2 — 3 4
相关知识点:
现象:铁丝在氧气中剧烈燃烧,火星四射,放热,
(1)二氧化锰在其中作为催化剂,加快氯酸钾的分解
生成黑色固体
速度或氧气的生成速度:
相关知识点:
(2)二氧化锰的质量和化学性质在化学反应前后没有
(1)铁丝盘成螺旋状是为了增大与氧气的接触面积;
改变:
2关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(2)在铁丝下方挂一根点燃的火柴是为了引燃铁丝; 碳酸钙;
(3)等火柴快燃尽在伸入集气瓶中,太早,火柴消耗 (2)不能用浓盐酸是因为浓盐酸有挥发性,挥发出
氧气,铁丝不能完全燃烧;太晚,不能引燃; HCl 气体 混入CO 中,使CO 不纯;
2 2
(4)事先在集气瓶底部放少量细沙,避免灼热生成物 (3)不能用稀硫酸是因为碳酸钙和硫酸反应,产生
溅落炸裂瓶底。 CaSO 微溶于水,覆盖在固体表面,使反应停止;
4
2Cu+O
2
====2CuO (4)不能用碳酸钙粉末是因为反应物接触面积大,反
9.红磷在氧气中燃烧(化合反应) 应速度太快。
4P+5O— \s\up8(点燃)2PO 14.工业制取二氧化碳气体(分解反应)
2 — 2 5
现象:产生大量白烟并放热。 高温煅烧石灰石
相关知识点:可用红磷来测定空气中氧气含量。 CaCO ==== +CO ↑
3 2
10.氢气在空气中燃烧(化合反应) 相关知识点:CaO
2H+O — \s\up8(点燃)2HO 15.一氧化碳在空气中燃烧(化合反应)
2 2 — 2
现象:产生淡蓝色的火焰,放热,有水珠生成 2 +O — \s\up8(点燃)2CO
2 — 2
相关知识点: 现象:产生
(1)氢气是一种常见的还原剂; 相关知识点:
(2)点燃前,一定要检验纯度。 (1)一氧化碳是一种常见的 ;
11.木炭还原氧化铜(置换反应) (2)点燃前,一定要 。
C+2CuO====2Cu+CO
2
↑ 16.一氧化碳还原氧化铜
现象:黑色粉末逐渐变成光亮的红色物质,放热 CO+CuO==== +CO
2
相关知识点: 现象: 逐渐变成光亮的 粉末,生
(1)把木炭粉和氧化铜铺放进试管,使受热面积大, 成气体使
反应快; 相关知识点:一氧化碳是还原剂,氧化铜是氧化剂
(2)导管通入澄清石灰水中,为了检验是否产生 17.甲烷在空气中燃烧
CO 2 ; +2O 2 — — \s\up8(点燃)CO 2 +2H 2 O
(3)在酒精灯上加网罩使火焰集中并提高温度; 现象: 呈浅蓝色
(4)先撤出导气管防止石灰水倒流炸裂试管; 相关知识点:甲烷是天然气(或 )的主要成
(5)试管冷却后在把粉末倒出,防止灼热的铜的氧气 分,是一种很好的燃料。
发生反应,生成CuO; 18.工业制造盐酸(化合反应)
(6)C是还原剂,CuO是氧化剂。 H
2
+Cl
2
—
—
\s\up8(点燃)2HCl
12.氢气还原氧化铜(置换反应) 相关知识点:
H+CuO====Cu+H O 该反应说明了在特殊条件下燃烧不一定需要氧气。
2 2
现象:黑色粉末逐渐变成光亮的红色物质,同时试 19.实验室制取氢气(置换反应)
管口有水滴生成。 Zn+H 2 SO 4 =ZnSO 4 +H 2 ↑
相关知识点: 相关知识点:
(1)实验开始时,应先通入一段时间氢气,目的是赶 (1)氢气是一种常见的还原剂;
走试管内的空气; (2)点燃前,一定要检验纯度。
(2)实验结束后,应 先 移去 酒精灯 ,后撤走氢气导 20.木炭和二氧化碳生成一氧化碳(化合反应)
管,目的是防止新生成的铜被氧化。 C+CO ====2CO
2
13.实验室制取二氧化碳气体(复分解反应) 相关知识点:
大理石(石灰石)和稀盐酸反应 (1)一氧化碳是一种常见的还原剂;
CaCO +2HCl=CaCl +H O+CO↑ (2)点燃前,一定要检验纯度。
3 2 2 2
现象:白色固体溶解,同时有大量气泡产生。 21.水和二氧化碳生成碳酸(化合反应)
相关知识点: CO+H O=HCO
2 2 2 3
(1)碳酸钙是一种白色难溶的固体,利用它能溶解在 现象:生成了能使紫色石蕊溶液变红的碳酸。
盐酸中的特性,可以用盐酸来除去某物质中混有的 22.碳酸不稳定分解(分解反应)
3关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
HCO=H O+CO↑ NaCO+2 =2NaCl+CO↑+H O
2 3 2 2 2 3 2 2
相关知识点: 现象: ,产生气泡。
(1)碳酸是一种不稳定的酸,受热易分解; 37.碳酸纳与氢氧化钙反应(复分解反应)
(2)分解时,二氧化碳从溶液中逸出,使红色石蕊溶 NaCO+ =CaCO ↓+2NaOH
2 3 3
液变成紫色。 38.硫酸纳与氯化钡反应(复分解反应)
23.灭火器的反应原理 NaSO + BaCl = ↓+2NaCl
2 4 2
Al (SO )+6NaHCO==3Na SO +2Al(OH) ↓+6CO ↑
2 4 3 3 2 4 3 2
灭火原理:灭火时,能喷射出大量二氧化碳及泡沫,
它们能粘附在可燃物上,使可燃物与空气隔绝,达到 考法 01 化学方程式分类训练
灭火的目的。
24.金属和水的反应(置换反应)
一、常见气体的实验室制取
①2Na+2HO=2NaOH+H ↑
2 2 (1)高锰酸钾分解制取氧气
②3Fe+4H O====Fe O+4H ↑
2 3 4 2
25.水与非金属的反应(置换反应)
(2)氯酸钾分解制取氧气
C+H O====CO+H
2 2
26.水与氧化物的反应(化合反应)
(3)过氧化氢分解制取氧气
①SO +H O=HSO
3 2 2 4
②NaO+ =2NaOH
2 (4)实验室制取二氧化碳
27.碳酸氢铵受热分解(分解反应)
NH HCO ====NH ↑+H O+CO↑
4 3 3 2 2 (5)实验室制取氢气
28.用盐(硫)酸来清除铁锈(复分解反应)
Fe O+6HCl=2FeCl +3H O
2 3 3 2
二、物质与氧气的反应
+3H SO =Fe (SO )+3H O
2 4 2 4 3 2
1. 非金属单质与氧气的反应
29.铁丝插入到硫酸铜溶液中(置换反应)
Fe+CuSO=FeSO +Cu
(1)木炭完全燃烧
4 4
现象:溶液由蓝色变成浅绿色,铁表面有红色固体
产生 (2)木炭不完全燃烧
30.硫酸铜溶液中滴加氢氧化钠溶液(复分解反
应) (3)硫在氧气中燃烧
CuSO
4
+2NaOH=Cu(OH)
2
↓+Na
2
SO
4
现象:产生蓝色沉淀 (4)磷在氧气中燃烧
31.二氧化硫与烧碱溶液反应
SO +2NaOH=Na SO +H O
2 2 3 2 (5)氢气在氧气中燃烧
SO +2NaOH= +H O
3 2
32.点燃酒精
2. 金属单质与氧气的反应
C HOH+3O — \s\up8(点燃)2 +3H O
2 5 2 — 2 (1)铁丝在氧气中燃烧
33.氯化钠溶液与硝酸银溶液反应生成不溶性沉淀
(复分解反应)
(2)镁条在氧气中燃烧
NaCl+AgNO =NaNO +AgCl↓
3 3
34.稀硫酸溶液与硝酸钡溶液反应生成不溶性沉淀
(3)铜丝在氧气中加热
HSO +Ba(NO)= ↓+2HNO
2 4 3 2 3
35.氯化铵固体和氢氧化钙固体混合加热(复分解
(4)铝在常温下雨氧气反应
反应)
2 +Ca(OH) ====2NH ↑+2H O+CaCl
2 3 2 2
3. 化合物与氧气的反应
36.碳酸纳与盐酸反应(复分解反应)
4关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(1)一氧化碳在氧气中燃烧 (1)铁与硫酸铜溶液反应
(2)甲烷在氧气中燃烧 (2)铝与硫酸铜溶液反应
(3)乙醇在氧气中加热 (3)锌与硝酸铜溶液反应
Zn+ Cu(NO ) = Zn(N O )+Cu
3 2 3 2
三、有二氧化碳参与的反应 (4)铜与硝酸银溶液反应
(1)二氧化碳与氢氧化钙反应(检验CO 气体)
2
六、金属的冶炼
(2)二氧化碳与氢氧化钠反应(NaOH变质的原 1. 铜的冶炼
因,吸收CO 气体) (1)氢气还原氧化铜
2
四、有水参与的反应 (2)木炭还原氧化铜
(1)电解水
(3)一氧化碳还原氧化铜
(2)氧化钙和水反应
2. 铁的冶炼
五、与金属有关的反应 (1)氢气还原氧化铁
1. 常见金属与酸的反应
(1)镁与稀盐酸反应 (2)木炭还原氧化铁
(2)镁与稀硫酸反应 (3)一氧化碳还原氧化铁
(3)铝与稀盐酸反应 (4)一氧化碳还原磁性氧化铁(四氧化三铁)
(4)铝与稀硫酸反应 七、酸、碱、盐之间的反应
1. 常见的酸和碱之间的反应
(5)锌与稀盐酸反应 (1)稀盐酸和氢氧化钠溶液反应
(6)铁与稀盐酸反应 (2)稀硫酸和氢氧化钠溶液反应
(7)铁与稀硫酸反应 (3)稀盐酸和氢氧化钙溶液反应
2. 常见金属氧化物与酸的反应 (4)稀硫酸和氢氧化钙溶液反应
(1)氧化铜与稀盐酸反应
(5)稀盐酸和氢氧化铜反应
(2)氧化铜与稀硫酸反应
(6)稀硫酸和氢氧化铜反应
(3)氧化铁与稀盐酸反应
(7)稀盐酸和氢氧化铝反应
(4)氧化铁与稀硫酸反应
(8)稀硫酸和氢氧化铝反应
3. 常见金属与盐的反应
5关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
2. 常见的酸和盐之间的反应
(1)稀盐酸和碳酸钠溶液反应 九、其他反应
(1)红热木炭和二氧化碳反应(典型的吸热反应)
(2)稀盐酸和碳酸氢钠溶液反应
(2)红热木炭和水反应(水煤气制法)
(3)稀盐酸和硝酸银溶液反应
(3)光合作用
(4)稀硫酸和碳酸钠溶液反应
(4)镁在二氧化碳气体中燃烧
(5)稀硫酸和氯化钡溶液反应
(6)稀硫酸和硝酸钡溶液反应
考法 02 化学方程式变式训练
3. 常见的碱和盐之间的反应
(1)氢氧化钠溶液和硫酸铜溶液反应
一、用化学方程式解释原理(或事实)
(1)实验室制氧气
(2)氢氧化钠溶液和氯化铁溶液反应
(3)氢氧化钠溶液和氯化镁溶液反应(海水提取镁)
(2)实验室制二氧化碳
(4)氢氧化钙溶液和硫酸铜溶液反应(波尔多液)
(3)实验室制氢气
(5)氢氧化钙溶液和碳酸钠溶液反应
(5)电解水
(6)氢氧化钡溶液和硫酸钠溶液反应
(5)氢氧化钠变质的原因,吸收CO 气体
2
4. 常见的盐和盐之间的反应
(1)氯化钠溶液和硝酸银溶液反应
(6)氢氧化钙变质
(2)氯化钙溶液和碳酸钠溶液反应
(7)生石灰作干燥剂
(3)氯化钡溶液和碳酸钠溶液反应
(8)一氧化碳还原赤铁矿
(4)氯化钡溶液和硫酸溶液反应
(9)稀盐酸(或稀硫酸)除铁锈
八、重要的分解反应
(1)碳酸分解 (10)铝制品内腐蚀的原因
(2)碳酸钙分解(高温煅烧石灰石) (11)不能用铁制品配制波尔多液的原因
(3)碳酸氢钠分解 (12)小苏打治疗胃酸过多
(4)氢氧化铜加热分解 (13)石灰浆涂抹墙壁,“流汗”现象
6关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(14)纯碱制取少量烧碱溶液
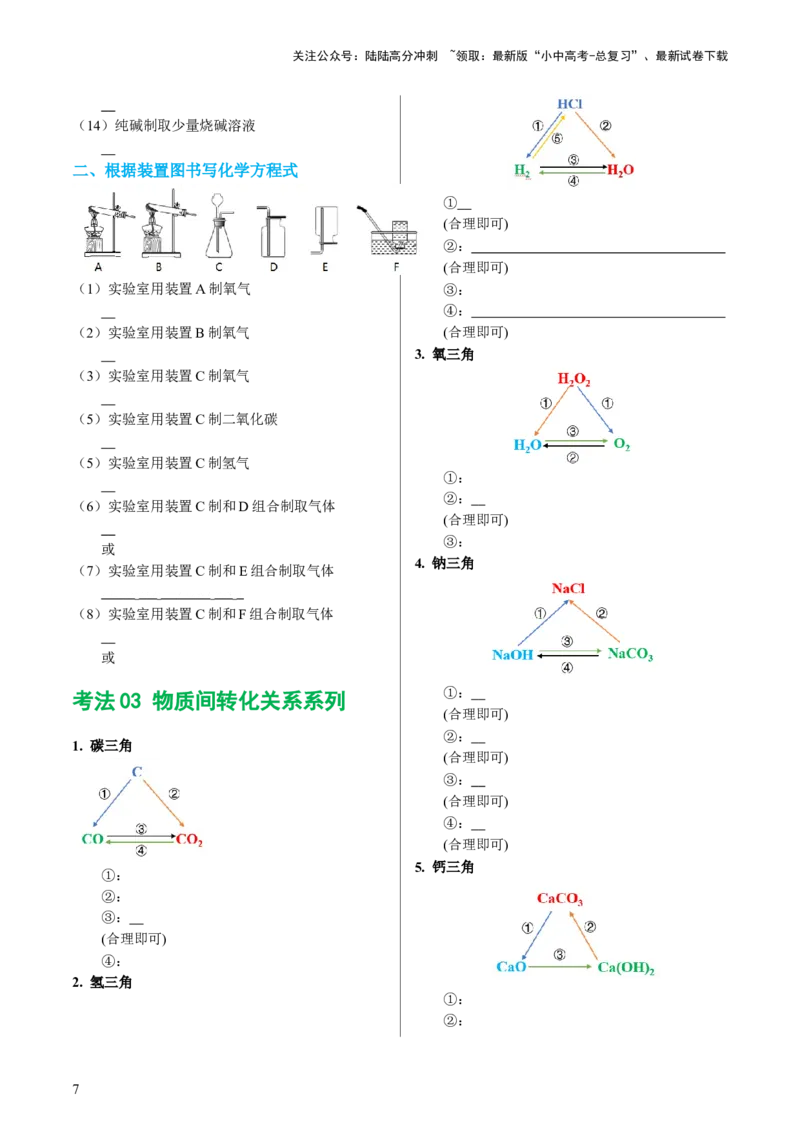
二、根据装置图书写化学方程式
①
(合理即可)
②:
(合理即可)
(1)实验室用装置A制氧气 ③:
④:
(2)实验室用装置B制氧气 (合理即可)
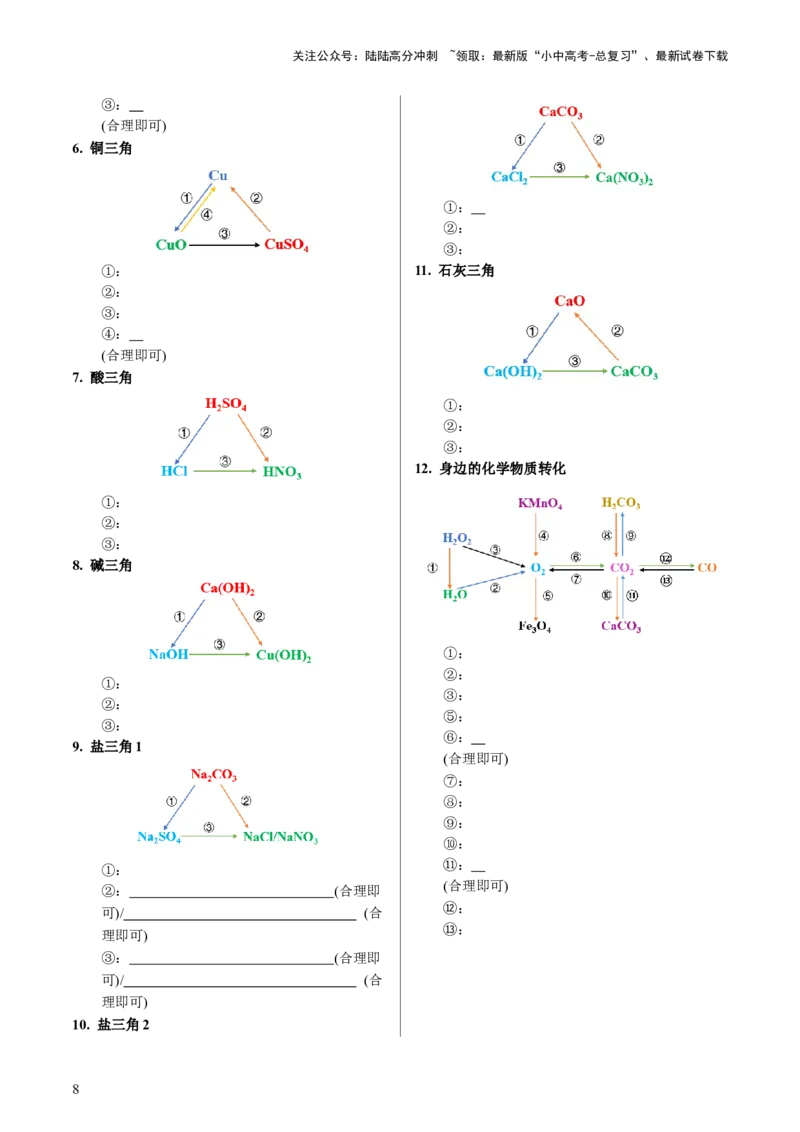
3. 氧三角
(3)实验室用装置C制氧气
(5)实验室用装置C制二氧化碳
(5)实验室用装置C制氢气
①:
②:
(6)实验室用装置C制和D组合制取气体
(合理即可)
③:
或
4. 钠三角
(7)实验室用装置C制和E组合制取气体
Zn+H SO = ZnSO +H ↑
2 4 4 2
(8)实验室用装置C制和F组合制取气体
或
考法 03 物质间转化关系系列 ①:
(合理即可)
②:
1. 碳三角
(合理即可)
③:
(合理即可)
④:
(合理即可)
5. 钙三角
①:
②:
③:
(合理即可)
④:
2. 氢三角
①:
②:
7关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
③:
(合理即可)
6. 铜三角
①:
②:
③:
①: 11. 石灰三角
②:
③:
④:
(合理即可)
7. 酸三角
①:
②:
③:
12. 身边的化学物质转化
①:
②:
③:
8. 碱三角
①:
②:
①:
③:
②:
⑤:
③:
⑥:
9. 盐三角1
(合理即可)
⑦:
⑧:
⑨:
⑩:
①:
⑪:
(合理即可)
②: (合理即
可)/ (合
⑫:
⑬:
理即可)
③: (合理即
可)/ (合
理即可)
10. 盐三角2
8关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
考法 04 根据给定信息书写反应
方程式
(1)氢氧化亚铁空气中逐渐由白色变成灰绿色,
最终变为红褐色
(2)氯化亚铁和氯气化合生成氯化铁
(3)过氧化钠和二氧化碳反应
(4)过氧化钠和水反应
(5)单质铝和烧碱溶液反应生成偏铝酸钠和氢气
9