文档内容
2008 年沈阳市中等学校招生统一考试(化 学)
可能用到的相对原子质量:H—1 C—12 O—16 Cl—35.5 Cu—64
一、选择题(本题包括13道小题。1~11小题,每题1分;12、 13小题,每题2分;共
15分。每小题有一个最符合题目要求的选项,请选出后将其序号填在题后的括号内。)
1.下列变化过程中包含化学变化的是 ( )
A.冰川消融 B.牛奶变酸 C.铜丝弯曲 D.汽油挥发
2.下列物质中属于氧化物的是 ( )
A. 氧化钙 B.氯化锌 C.金刚石 D.葡萄糖
3.人体中化学元素含量的多少直接影响人体的健康。如果人体内缺少钙元素,有可能引起
的疾病是( )
A.贫血症 B.夜盲症 C.佝偻病 D.甲状腺肿大
4. 豆腐是我国古代的一项重要发明,豆制品被视为中华饮食文化的瑰宝。下图是某豆腐干
标签的部分内容,配料中富含蛋白质的
是 ( ) X X 豆腐干
A.优质大豆 B.食盐 优质大豆、食盐、植物油、味
配料
C.植物油 D.辣椒 精、辣椒、山梨酸钾
5.生活中的下列物品由无机非金属材料制
成的是 ( )
A. 玻璃水杯 B. 塑料格尺
C. 不锈钢餐具 D. 自行车轮胎
6.水是我们生活、生产各方面都离不开的重要物质,下列有关水的说法错误的是 (
)
A.水是一种最常见的溶剂 B.自然界中的水都含有杂质
C.可用肥皂水鉴别硬水和软水 D.电解是一种常用的净水方法
7.下图所示的实验操作中正确的是 ( )
A.加热液体 B. 移走蒸发 C.倾倒液体 D. 读取液体体积
8.沈阳是2008年北京奥运会足球比赛的分赛场之一。兴奋剂检测是对足球运动员的一项
重要检测。诺龙是兴奋剂中的一种,其化学式是 C H O 。下列关于诺龙的说法正确的
18 26 2是( )
A.诺龙中含有氧分子 B.一个诺龙分子中含有46个原子
C.诺龙中碳、氢、氧元素质量比为9:13:1
D.诺龙由18个碳原子、26个氢原子、2个氧原子构成
9.下列化学反应中属于分解反应的是 ( )
点燃 高温
A.2H + O 2HO B.C + HO H + CO
2 2 2 2 2
高温
C.CaCO CaO + CO↑ D.Mg(OH) + HSO = MgSO + 2HO
3 2 2 2 4 4 2
10.用所学化学知识分析,下列做法正确的是 ( )
A. 家用电器着火时立即用水扑灭 B. 用食盐水除去热水瓶中的水垢
C. 用洗洁精洗去餐具上的油污 D. 经常用水冲洗自行车可防止生锈
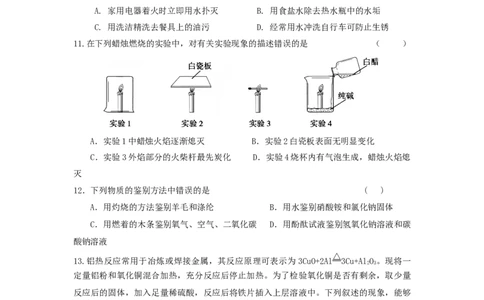
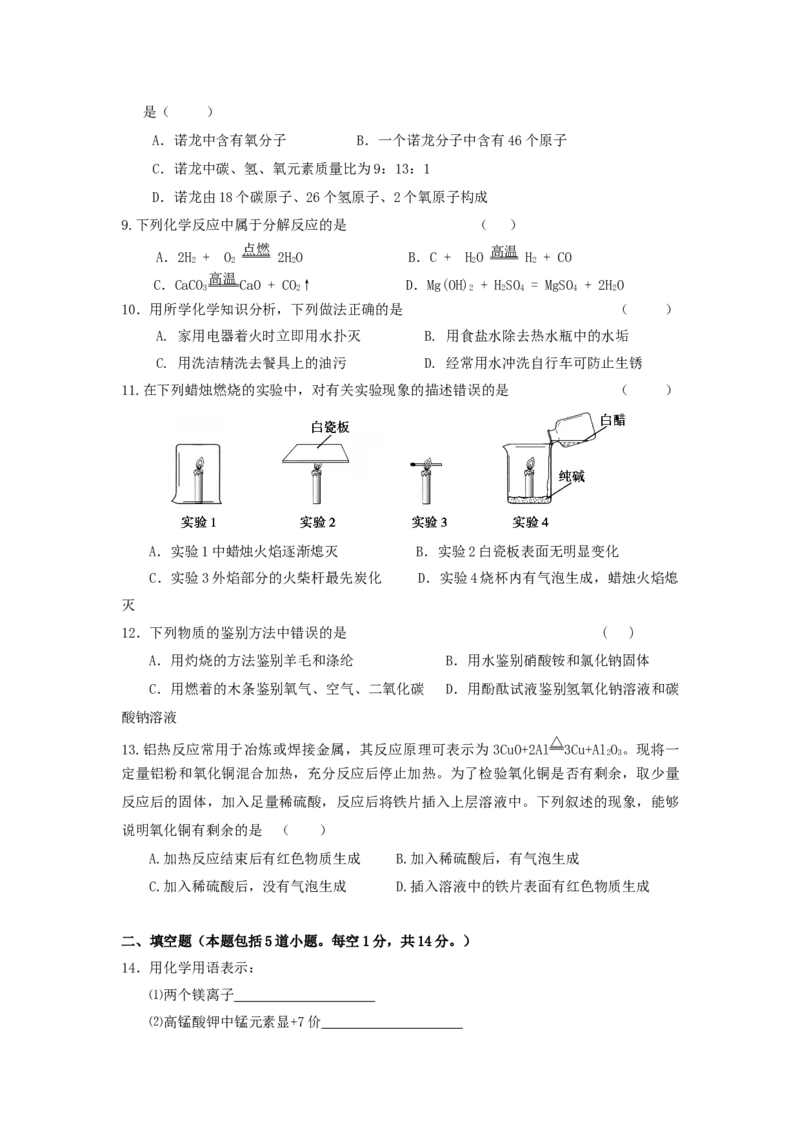
11.在下列蜡烛燃烧的实验中,对有关实验现象的描述错误的是 ( )
A.实验1中蜡烛火焰逐渐熄灭 B.实验2白瓷板表面无明显变化
C.实验3外焰部分的火柴杆最先炭化 D.实验4烧杯内有气泡生成,蜡烛火焰熄
灭
12.下列物质的鉴别方法中错误的是 ( )
A.用灼烧的方法鉴别羊毛和涤纶 B.用水鉴别硝酸铵和氯化钠固体
C.用燃着的木条鉴别氧气、空气、二氧化碳 D.用酚酞试液鉴别氢氧化钠溶液和碳
酸钠溶液
△
13.铝热反应常用于冶炼或焊接金属,其反应原理可表示为3CuO+2Al 3Cu+AlO 。现将一
2 3
定量铝粉和氧化铜混合加热,充分反应后停止加热。为了检验氧化铜是否有剩余,取少量
反应后的固体,加入足量稀硫酸,反应后将铁片插入上层溶液中。下列叙述的现象,能够
说明氧化铜有剩余的是 ( )
A.加热反应结束后有红色物质生成 B.加入稀硫酸后,有气泡生成
C.加入稀硫酸后,没有气泡生成 D.插入溶液中的铁片表面有红色物质生成
二、填空题(本题包括5道小题。每空1分,共14分。)
14.用化学用语表示:
⑴两个镁离子
⑵高锰酸钾中锰元素显+7价15.米饭、馒头中含有丰富的淀粉,淀粉属于 (填“无机物”或
“有机物” ),常用来检验淀粉的试剂是
。
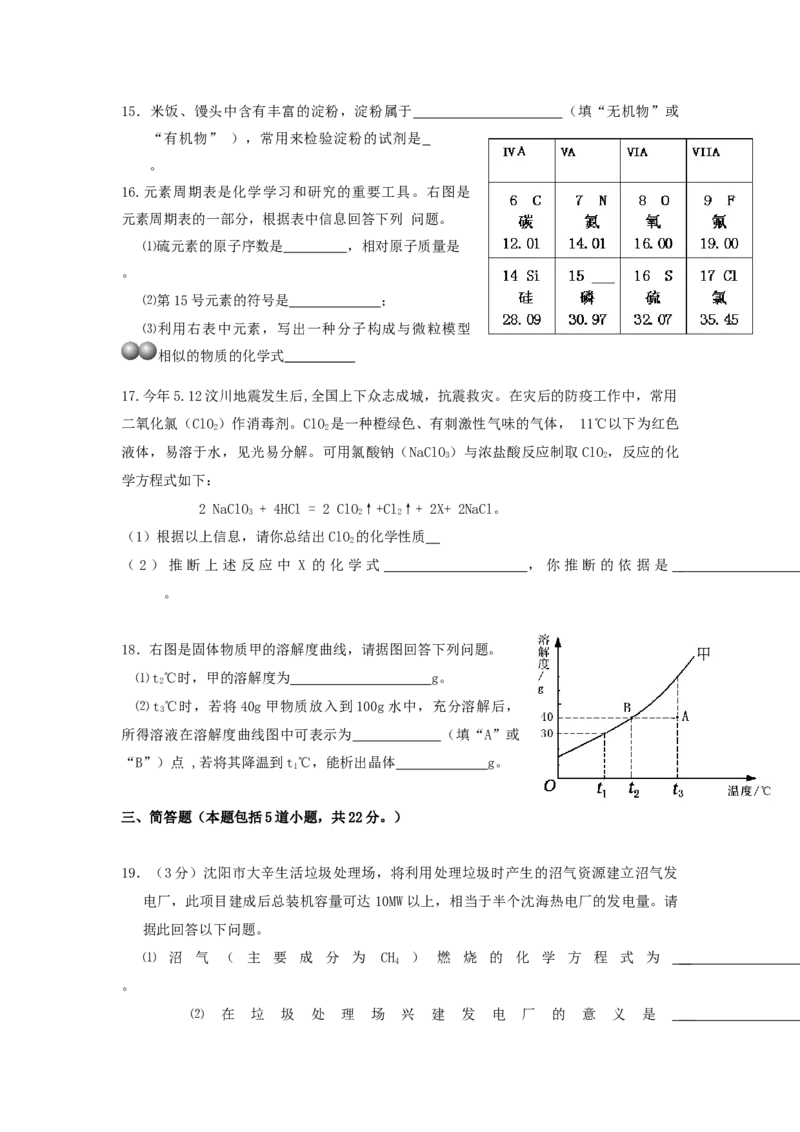
16.元素周期表是化学学习和研究的重要工具。右图是
元素周期表的一部分,根据表中信息回答下列 问题。
⑴硫元素的原子序数是 ,相对原子质量是
。
⑵第15号元素的符号是 ;
⑶利用右表中元素,写出一种分子构成与微粒模型
相似的物质的化学式
17.今年5.12汶川地震发生后,全国上下众志成城,抗震救灾。在灾后的防疫工作中,常用
二氧化氯(ClO )作消毒剂。ClO 是一种橙绿色、有刺激性气味的气体, 11℃以下为红色
2 2
液体,易溶于水,见光易分解。可用氯酸钠(NaClO )与浓盐酸反应制取ClO ,反应的化
3 2
学方程式如下:
2 NaClO + 4HCl = 2 ClO↑+Cl↑+ 2X+ 2NaCl。
3 2 2
(1)根据以上信息,请你总结出ClO 的化学性质
2
(2)推断上述反应 中 X 的化学式 ,你推断的依据是
。
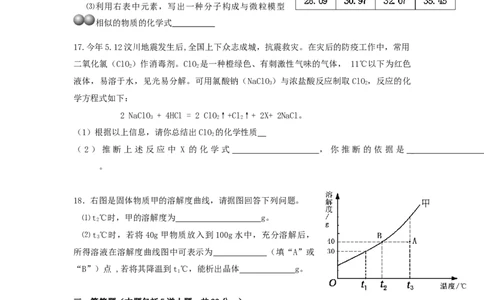
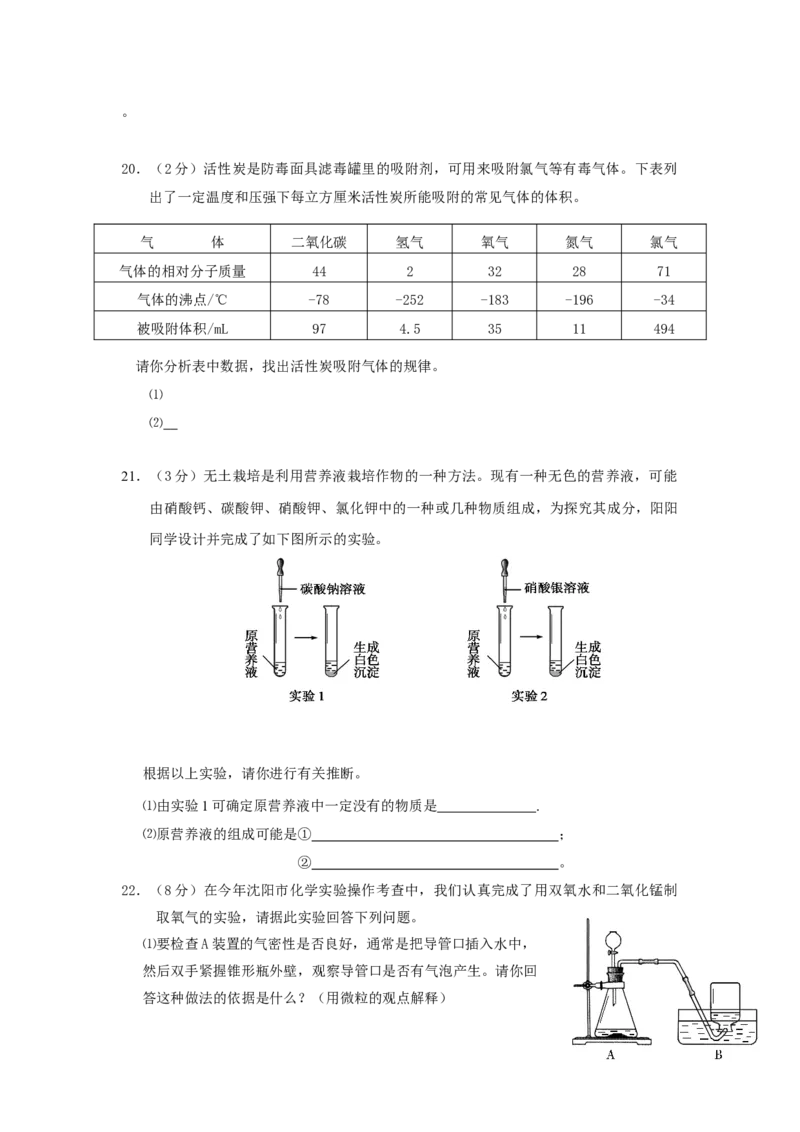
18.右图是固体物质甲的溶解度曲线,请据图回答下列问题。
⑴t℃时,甲的溶解度为 g。
2
⑵t℃时,若将40g甲物质放入到100g水中,充分溶解后,
3
所得溶液在溶解度曲线图中可表示为 (填“A”或
“B”)点 ,若将其降温到t℃,能析出晶体 g。
1
三、简答题(本题包括5道小题,共22分。)
19.(3分)沈阳市大辛生活垃圾处理场,将利用处理垃圾时产生的沼气资源建立沼气发
电厂,此项目建成后总装机容量可达10MW以上,相当于半个沈海热电厂的发电量。请
据此回答以下问题。
⑴ 沼 气 ( 主 要 成 分 为 CH ) 燃 烧 的 化 学 方 程 式 为
4
。
⑵ 在 垃 圾 处 理 场 兴 建 发 电 厂 的 意 义 是。
20.(2分)活性炭是防毒面具滤毒罐里的吸附剂,可用来吸附氯气等有毒气体。下表列
出了一定温度和压强下每立方厘米活性炭所能吸附的常见气体的体积。
气 体 二氧化碳 氢气 氧气 氮气 氯气
气体的相对分子质量 44 2 32 28 71
气体的沸点/℃ -78 -252 -183 -196 -34
被吸附体积/mL 97 4.5 35 11 494
请你分析表中数据,找出活性炭吸附气体的规律。
⑴
⑵
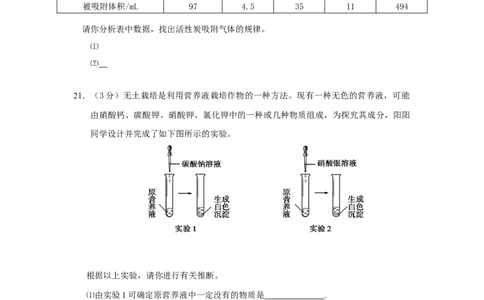
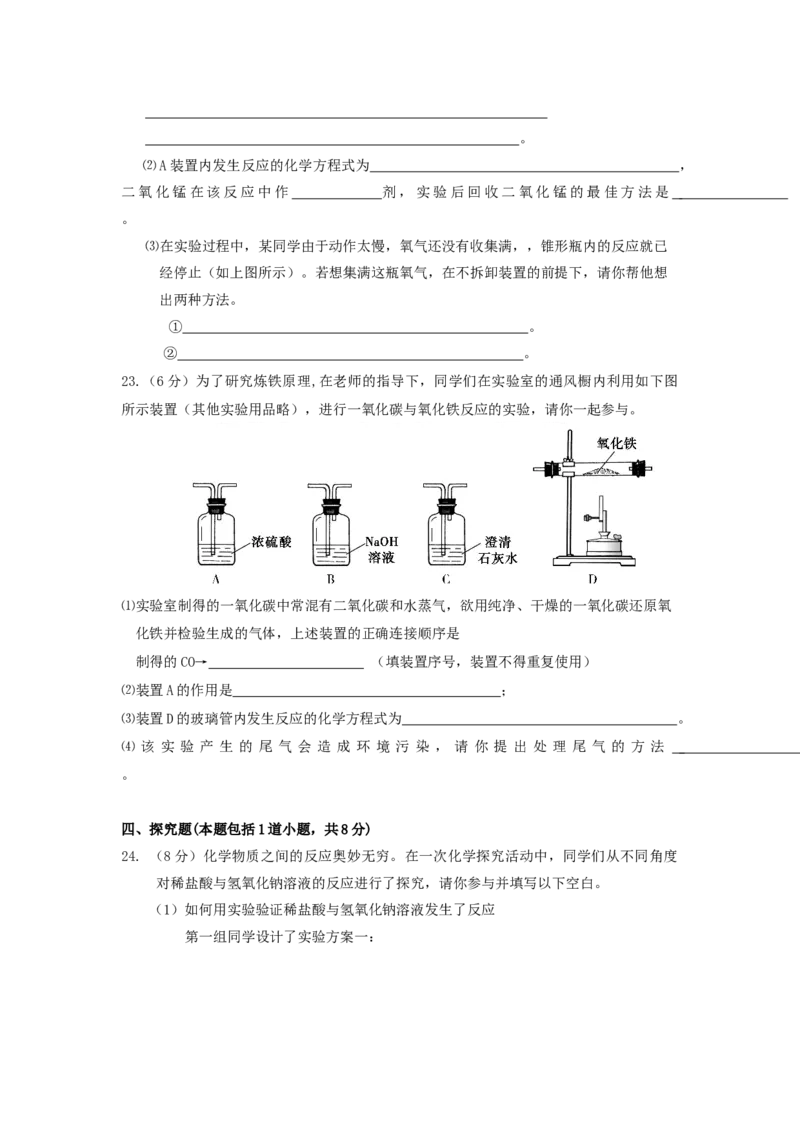
21.(3分)无土栽培是利用营养液栽培作物的一种方法。现有一种无色的营养液,可能
由硝酸钙、碳酸钾、硝酸钾、氯化钾中的一种或几种物质组成,为探究其成分,阳阳
同学设计并完成了如下图所示的实验。
根据以上实验,请你进行有关推断。
⑴由实验1可确定原营养液中一定没有的物质是 .
⑵原营养液的组成可能是① ;
② 。
22.(8分)在今年沈阳市化学实验操作考查中,我们认真完成了用双氧水和二氧化锰制
取氧气的实验,请据此实验回答下列问题。
⑴要检查A装置的气密性是否良好,通常是把导管口插入水中,
然后双手紧握锥形瓶外壁,观察导管口是否有气泡产生。请你回
答这种做法的依据是什么?(用微粒的观点解释)。
⑵A装置内发生反应的化学方程式为 ,
二氧化锰在该反应中作 剂,实验后回收二氧化锰的最佳方法是
。
⑶在实验过程中,某同学由于动作太慢,氧气还没有收集满,,锥形瓶内的反应就已
经停止(如上图所示)。若想集满这瓶氧气,在不拆卸装置的前提下,请你帮他想
出两种方法。
① 。
② 。
23.(6分)为了研究炼铁原理,在老师的指导下,同学们在实验室的通风橱内利用如下图
所示装置(其他实验用品略),进行一氧化碳与氧化铁反应的实验,请你一起参与。
⑴实验室制得的一氧化碳中常混有二氧化碳和水蒸气,欲用纯净、干燥的一氧化碳还原氧
化铁并检验生成的气体,上述装置的正确连接顺序是
制得的CO→ (填装置序号,装置不得重复使用)
⑵装置A的作用是 ;
⑶装置D的玻璃管内发生反应的化学方程式为 。
⑷ 该 实 验 产 生 的 尾 气 会 造 成 环 境 污 染 , 请 你 提 出 处 理 尾 气 的 方 法
。
四、探究题(本题包括1道小题,共8分)
24. (8分)化学物质之间的反应奥妙无穷。在一次化学探究活动中,同学们从不同角度
对稀盐酸与氢氧化钠溶液的反应进行了探究,请你参与并填写以下空白。
(1)如何用实验验证稀盐酸与氢氧化钠溶液发生了反应
第一组同学设计了实验方案一:①请你分析上述方案中为什么强调只有测得的 H≥7才能证明反应发生了?
P
实验步骤 实验现象 结论
先用 H试纸测定稀盐酸的 H, H逐渐变大, 稀盐酸与氢氧化钠溶液能
P P P
再逐渐滴加氢氧化钠溶液,并不断振 最后 H≥7 发生反应
P
荡,同时测定混合液的 H。
P
。
② 写 出 稀 盐 酸 与 氢 氧 化 钠 溶 液 反 应 的 化 学 方 程 式
。
(2)设计实验,探究稀盐酸与氢氧化钠溶液的反应是否放热
提供的实验仪器与药品:10%的盐酸、10%的氢氧化钠溶液、烧杯、温度计、玻璃棒、
胶头滴管。
实验步骤 实验现象 结论
稀盐酸与氢氧化
钠溶液反应放热
(3)探究稀盐酸与氢氧化钠溶液是否恰好完全反应请你完成实验方案设计:
第二组同学在做完稀盐酸与氢氧化钠溶液反应的实验后,为探究稀盐酸与氢氧化钠溶
液是否恰好完全反应,设计了实验方案二:
实验步骤 实验现象 结论
取少量上述反应后的溶液 若 氢氧化钠溶液过量于试管中,滴加硫酸铜溶 若没有明显现象 稀盐酸与氢氧化钠溶液恰好完
液。 全反应
此时有同学提出方案二不能证明稀盐酸与氢氧化钠溶液恰好完全反应,其原因是
。为此,还需要选择 (填一种试剂),再进行实验即可。
五、计算题(本题包括1道小题,共6分。)
25.(6分)化学小组的同学为了测定某铜矿中碱式碳酸铜[化学式为Cu(OH)CO ,相
2 2 3
对分子质量为222]的质量分数,称取该铜矿样品30g,加入132.2g稀盐酸时恰好完
全反应,共生成CO 气体4.4g。反应的化学方程式如下:
2
Cu(OH)CO +4HCl=2CuCl+3HO +CO↑
2 2 3 2 2 2
请你计算:
⑴铜矿样品中碱式碳酸铜的质量是多少克?其质量分数是多少?
⑵反应后所得溶液中溶质质量分数是多少?
(假设铜矿中的杂质不与稀盐酸反应,也不溶于水。)2008年沈阳市中等学校招生统一考试化学试题参考答案及评分标准
一、选择题(1~11小题每题1分;12、13小题每题2分;共15分。)
1.B 2.A 3.C 4.A 5.A 6.D 7.C 8.B 9.C 10.C 11.B 12.D 13.D
二、填空题(本题包括5道小题,每空1分,共14分。)
+7
14.⑴2Mg2+ ⑵
KMnO4
15. 有机物 碘酒(或碘水)
16.⑴16 32.07 ⑵P ⑶O(或Cl、N、F)
2 2 2 2
17.⑴见光易分解 ⑵HO 质量守恒定律
2
18.⑴40 ⑵A 10
三、简答题(本题包括5道小题,共22分。)
点 燃
19.⑴ CH + 2O CO + 2HO
4 2 2 2
(2分)
⑵变废为宝(或废物利用、、保护环境、充分利用资源等) (1
分)
20.⑴相同条件下,气体的沸点越高,越易被活性炭吸附
⑵相同条件下,气体的相对分子质量越大,越易被活性炭吸附 (各 1
分)
21.⑴碳酸钾(或KCO)
2 3
⑵①硝酸钙、氯化钾 [或Ca(NO ) 、KCl]②硝酸钙、氯化钾、硝酸钾 [或Ca(NO )
3 2 3
、KCl、KNO](各1分)
2 3
22.⑴手握锥形瓶,使瓶内气体受热,微粒运动速率增大,间隔变大,气体体积膨胀,能
从导管口逸出。
MnO2
⑵2HO 2HO+O ↑ 催化 过滤
2 2 2
⑶①再加入适量的双氧水使反应继续进行
②从分液漏斗向锥形瓶内加水,将锥形瓶内的氧气压入集气瓶中
[(1) 、方程式各2分,其他各1分]
23.⑴B、 A、 D 、C
⑵干燥CO气体(或吸收水蒸气)
高温
⑶3CO+FeO 2Fe+3CO
2 3 2⑷用酒精灯点燃尾气(或用气球、集气瓶收集尾气)
[(1) 、(3)各2分,其他各1分]
四、探究题(本题包括1道小题,共8分)
24.⑴①排除因氢氧化钠溶液的加入,稀释盐酸而引起 H变大(或只有 H≥7才能说明盐
P P
酸已经反应掉了)
② NaOH+HCl=NaCl+HO
2
⑵
实验步骤 实验现象
取一定量10%的氢氧化钠溶液于烧杯, 温度计是示数上升
插入温度计测温度;加入适量10%的盐酸, (或温度升高)
用玻璃棒搅拌,再测温度。
⑶生成蓝色沉淀
若盐酸过量,加入硫酸铜溶液时也无明显现象(或盐酸可能有剩余)
紫色石蕊试液(或锌粒、碳酸钠、氧化铜、氢氧化铜、pH试纸等)
(方程式各2分,其他各1分)
五、计算题(本题包括1道小题,共6分。)
25.解:设铜矿中碱式碳酸铜的质量是为x,生成氯化铜的质量为y。
Cu(OH)CO +4HCl=2CuCl + 3HO+ CO↑
2 2 3 2 2 2
222 270 44
x y 4.4g (1分)
222 x
44 4.4g
= x =22.2g (1分)
270 y
44 4.4g
= y =27g (1分)
22.2g
30g
铜矿样品中碱式碳酸铜的质量分数为 ×100%=74% (1分)
反应后所得氯化铜溶液的质量为 22.2g+132.2g-4.4g=150g (1分)
27g
150g
反应后所得氯化铜溶液中溶质的质量分数为 ×100%=18% (1分)
答:铜矿样品中碱式碳酸铜的质量是 22.2g ,其质量分数是74%。反应后所得氯化铜溶液
中溶质的质量分数是18%。