文档内容
化学
可能用到的相对原子质量:H-1 C-12 N-14 O-16
一、单项选择题(每小题1分,共10分)
1.1956年,在吉林省诞生了新中国第一辆解放牌汽车。生产汽车的材料中,属于金属材
料的是
A.合金 B.橡胶 C.塑料 D.玻璃
2.空气是一种宝贵的资源。下列空气中的成分,由植物光合作用产生的是
A.二氧化碳 B.稀有气体 C.氧气 D.氮气
3.在下列物质的用途中,主要利用其化学性质的是
A.用盐酸除铁锈 B.利用液氮进行冷冻
C.用铜丝作导线 D.干冰用于人工增雨
4.配制100g质量分数为16%的氯化钠溶液进行选种时,下列相关内容错误的是
A.相关图标 B.量取
C.溶解 D.装瓶贴签
探索物质组成和结构的历程,凝结了许多人的辛勤劳动和智慧,使人们对物质的组成和结
构的认识不断深入。运用所学知识完成下面小题。
5.【微观解释】气体可压缩储存于钢瓶中的原因是
A.分子种类改变 B.分子不断运动
C.分子之间有间隔 D.分子数目增多
6.【宏观组成】用电解水实验探究水的组成,下列说法正确的是
A.电解水的变化过程中没有能量转化
B.用燃着的木条检验负极产生的气体
C.水分子是该化学变化中的最小粒子
D.水是由氢气和氧气组成
试卷第1页,共3页7.【探索历程】下列人物与其贡献不相符的是
A.道尔顿——提出原子论 B.拉瓦锡——发现元素周期律
C.徐寿——新造元素中文名称 D.张青莲——测定相对原子质量
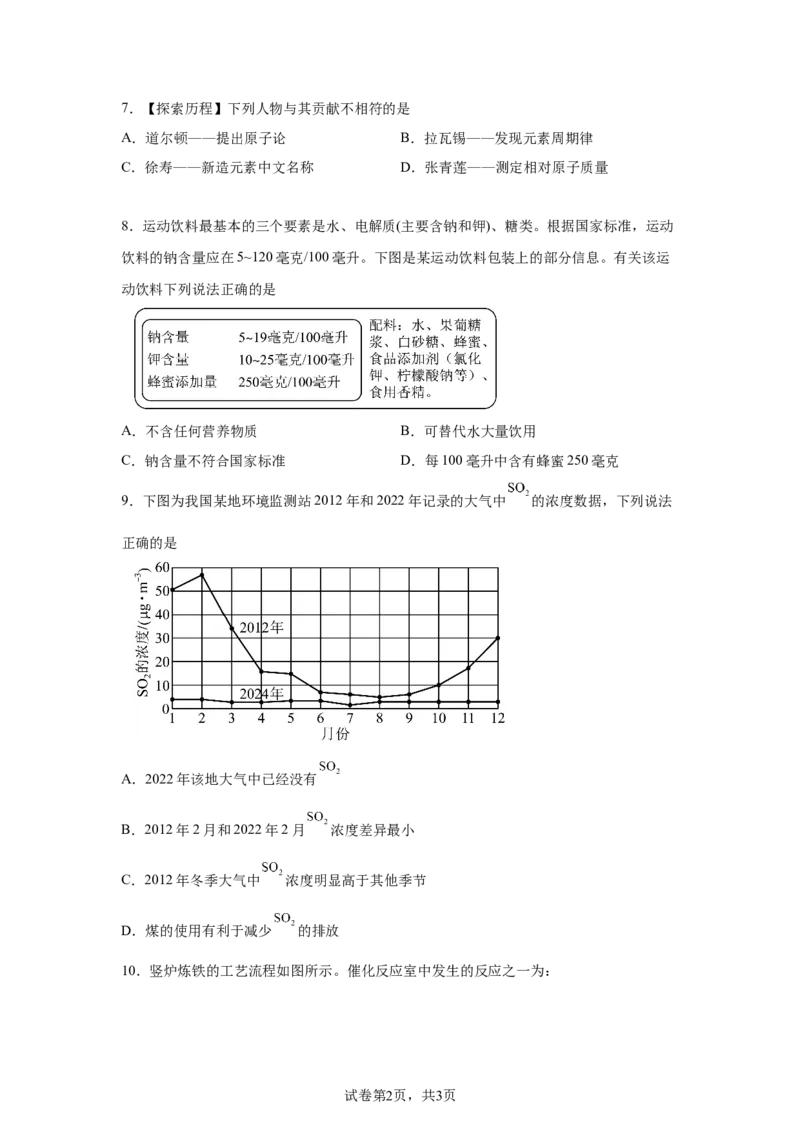
8.运动饮料最基本的三个要素是水、电解质(主要含钠和钾)、糖类。根据国家标准,运动
饮料的钠含量应在5~120毫克/100毫升。下图是某运动饮料包装上的部分信息。有关该运
动饮料下列说法正确的是
A.不含任何营养物质 B.可替代水大量饮用
C.钠含量不符合国家标准 D.每100毫升中含有蜂蜜250毫克
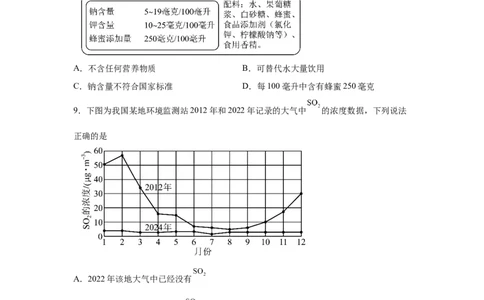
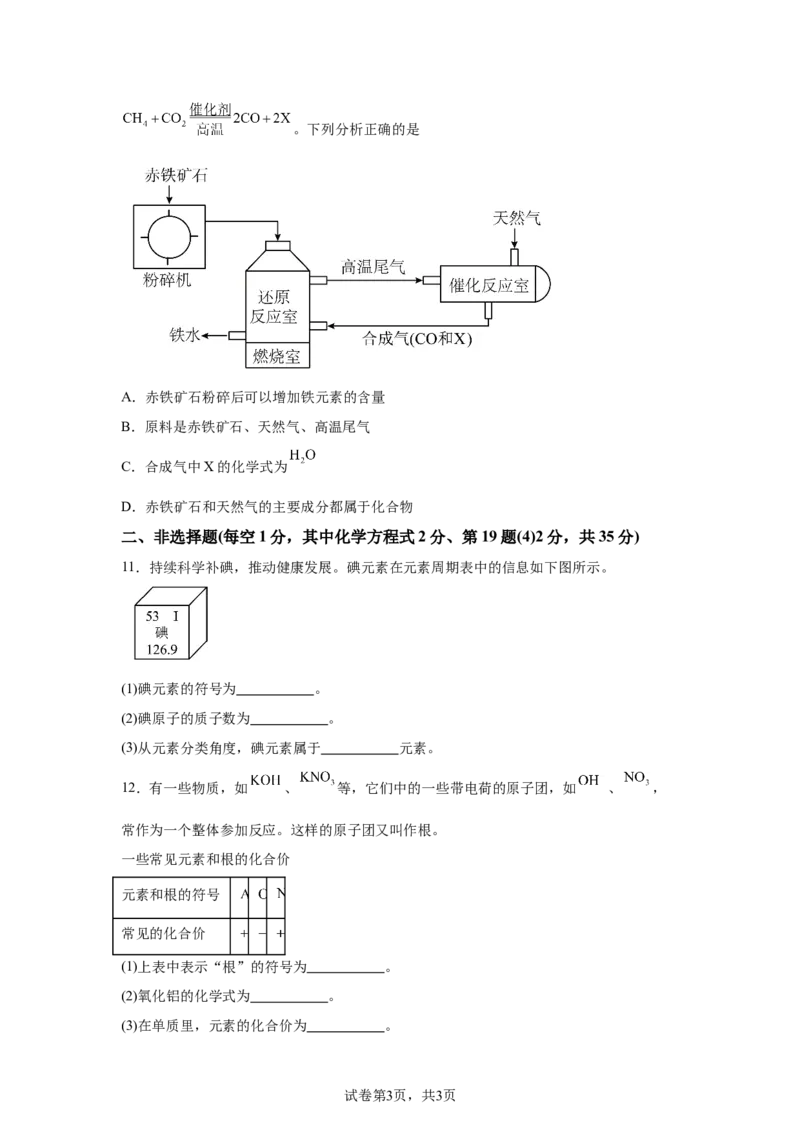
9.下图为我国某地环境监测站2012年和2022年记录的大气中 的浓度数据,下列说法
正确的是
A.2022年该地大气中已经没有
B.2012年2月和2022年2月 浓度差异最小
C.2012年冬季大气中 浓度明显高于其他季节
D.煤的使用有利于减少 的排放
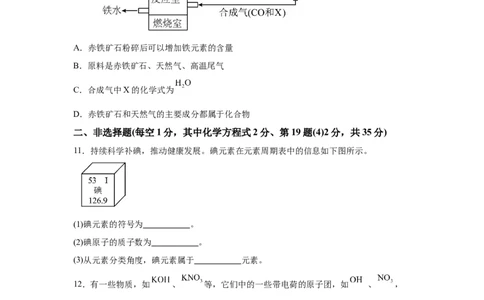
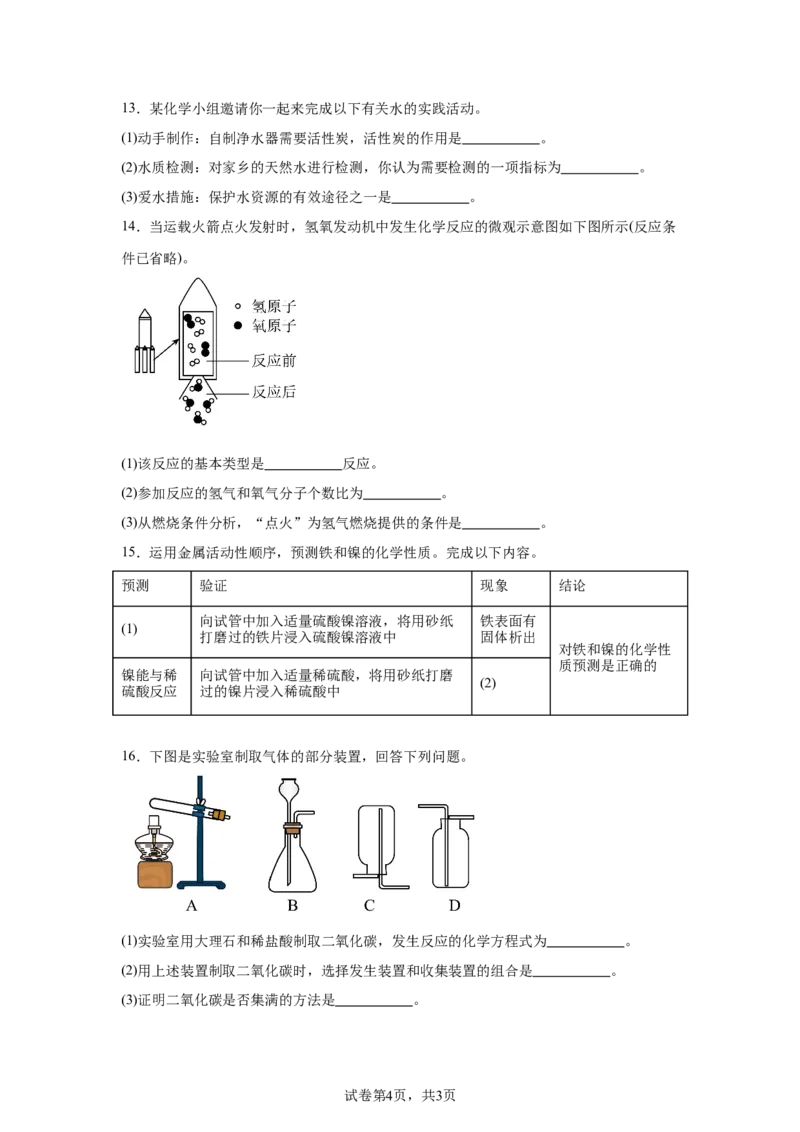
10.竖炉炼铁的工艺流程如图所示。催化反应室中发生的反应之一为:
试卷第2页,共3页。下列分析正确的是
A.赤铁矿石粉碎后可以增加铁元素的含量
B.原料是赤铁矿石、天然气、高温尾气
C.合成气中X的化学式为
D.赤铁矿石和天然气的主要成分都属于化合物
二、非选择题(每空1分,其中化学方程式2分、第19题(4)2分,共35分)
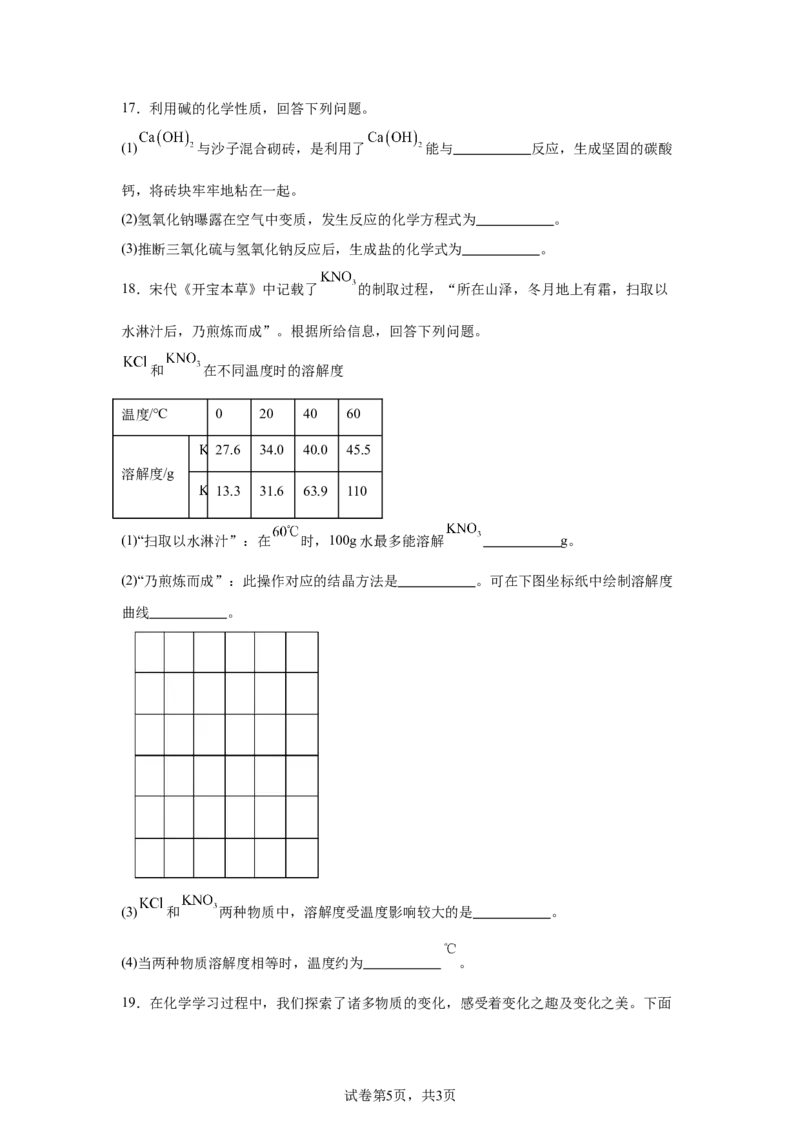
11.持续科学补碘,推动健康发展。碘元素在元素周期表中的信息如下图所示。
(1)碘元素的符号为 。
(2)碘原子的质子数为 。
(3)从元素分类角度,碘元素属于 元素。
12.有一些物质,如 、 等,它们中的一些带电荷的原子团,如 、 ,
常作为一个整体参加反应。这样的原子团又叫作根。
一些常见元素和根的化合价
元素和根的符号
常见的化合价
(1)上表中表示“根”的符号为 。
(2)氧化铝的化学式为 。
(3)在单质里,元素的化合价为 。
试卷第3页,共3页13.某化学小组邀请你一起来完成以下有关水的实践活动。
(1)动手制作:自制净水器需要活性炭,活性炭的作用是 。
(2)水质检测:对家乡的天然水进行检测,你认为需要检测的一项指标为 。
(3)爱水措施:保护水资源的有效途径之一是 。
14.当运载火箭点火发射时,氢氧发动机中发生化学反应的微观示意图如下图所示(反应条
件已省略)。
(1)该反应的基本类型是 反应。
(2)参加反应的氢气和氧气分子个数比为 。
(3)从燃烧条件分析,“点火”为氢气燃烧提供的条件是 。
15.运用金属活动性顺序,预测铁和镍的化学性质。完成以下内容。
预测 验证 现象 结论
向试管中加入适量硫酸镍溶液,将用砂纸 铁表面有
(1)
打磨过的铁片浸入硫酸镍溶液中 固体析出
对铁和镍的化学性
质预测是正确的
镍能与稀 向试管中加入适量稀硫酸,将用砂纸打磨
(2)
硫酸反应 过的镍片浸入稀硫酸中
16.下图是实验室制取气体的部分装置,回答下列问题。
(1)实验室用大理石和稀盐酸制取二氧化碳,发生反应的化学方程式为 。
(2)用上述装置制取二氧化碳时,选择发生装置和收集装置的组合是 。
(3)证明二氧化碳是否集满的方法是 。
试卷第4页,共3页17.利用碱的化学性质,回答下列问题。
(1) 与沙子混合砌砖,是利用了 能与 反应,生成坚固的碳酸
钙,将砖块牢牢地粘在一起。
(2)氢氧化钠曝露在空气中变质,发生反应的化学方程式为 。
(3)推断三氧化硫与氢氧化钠反应后,生成盐的化学式为 。
18.宋代《开宝本草》中记载了 的制取过程,“所在山泽,冬月地上有霜,扫取以
水淋汁后,乃煎炼而成”。根据所给信息,回答下列问题。
和 在不同温度时的溶解度
温度/℃ 0 20 40 60
27.6 34.0 40.0 45.5
溶解度/g
13.3 31.6 63.9 110
(1)“扫取以水淋汁”:在 时,100g水最多能溶解 g。
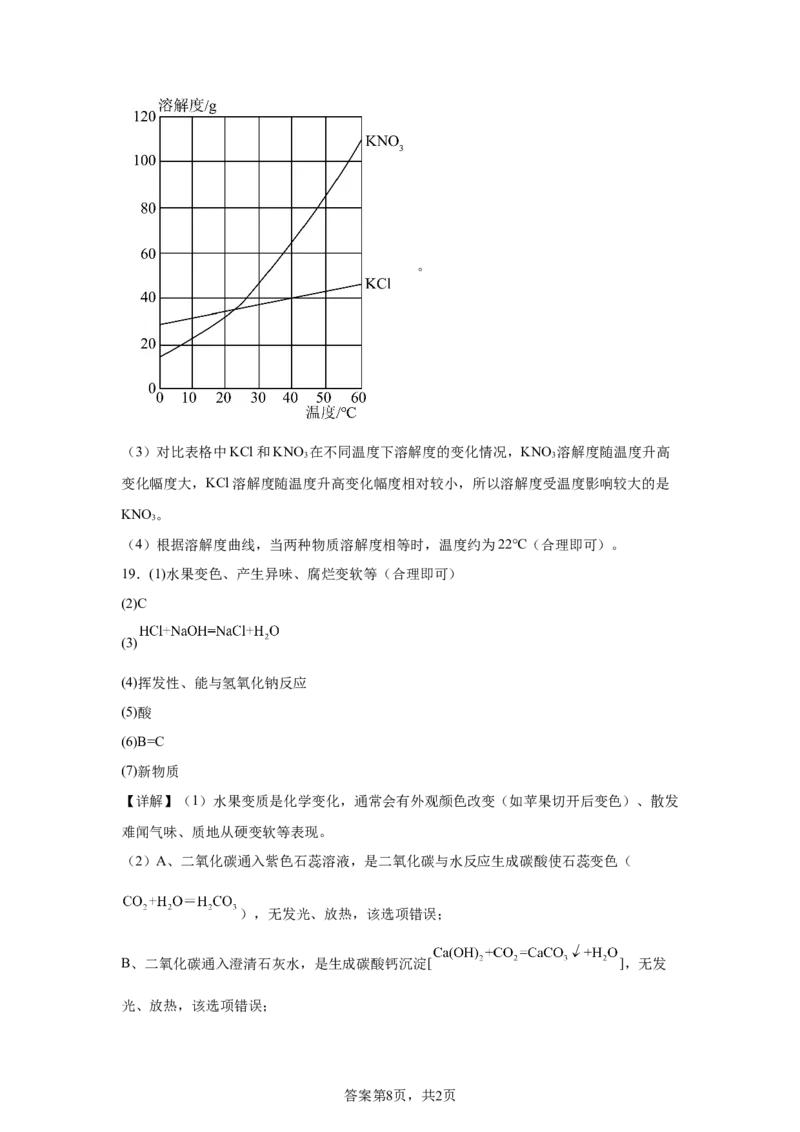
(2)“乃煎炼而成”:此操作对应的结晶方法是 。可在下图坐标纸中绘制溶解度
曲线 。
(3) 和 两种物质中,溶解度受温度影响较大的是 。
(4)当两种物质溶解度相等时,温度约为 。
19.在化学学习过程中,我们探索了诸多物质的变化,感受着变化之趣及变化之美。下面
试卷第5页,共3页我们将对物质的化学变化进行项目式学习。
【项目主题】通过现象识别物质的化学变化
【任务设计与实施】
任务一 感知化学变化
观察思考:
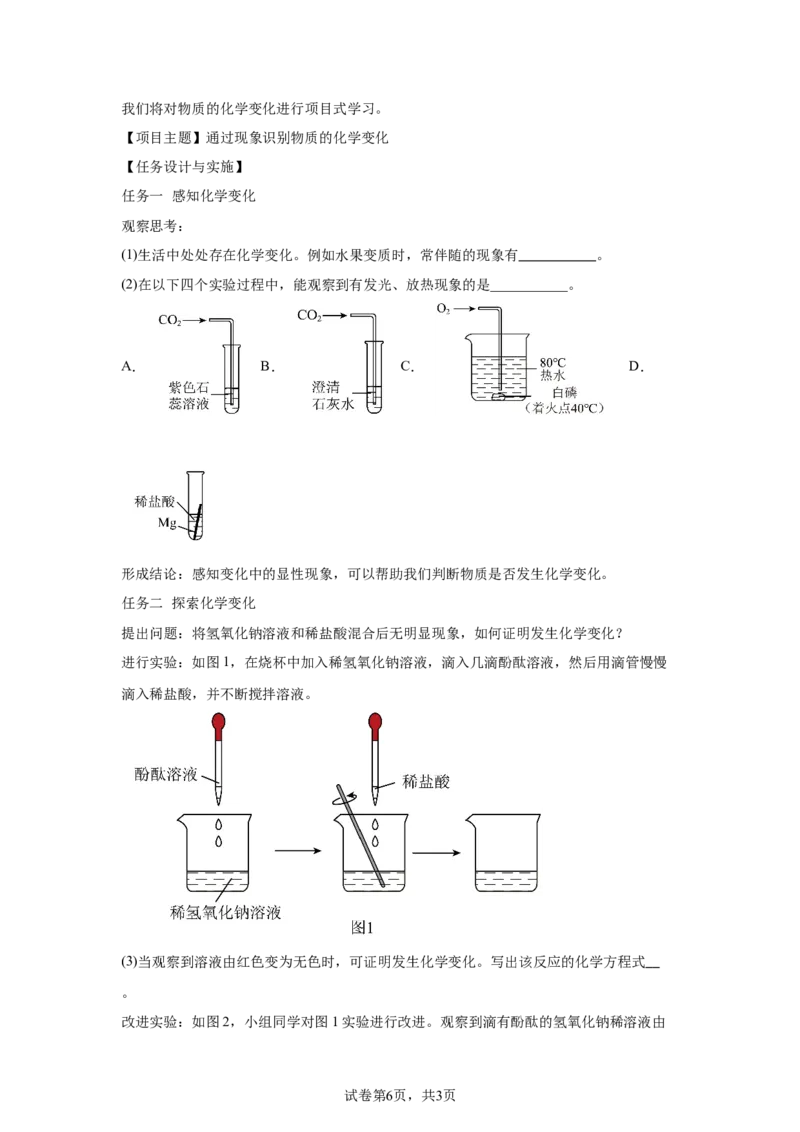
(1)生活中处处存在化学变化。例如水果变质时,常伴随的现象有 。
(2)在以下四个实验过程中,能观察到有发光、放热现象的是___________。
A. B. C. D.
形成结论:感知变化中的显性现象,可以帮助我们判断物质是否发生化学变化。
任务二 探索化学变化
提出问题:将氢氧化钠溶液和稀盐酸混合后无明显现象,如何证明发生化学变化?
进行实验:如图1,在烧杯中加入稀氢氧化钠溶液,滴入几滴酚酞溶液,然后用滴管慢慢
滴入稀盐酸,并不断搅拌溶液。
(3)当观察到溶液由红色变为无色时,可证明发生化学变化。写出该反应的化学方程式
。
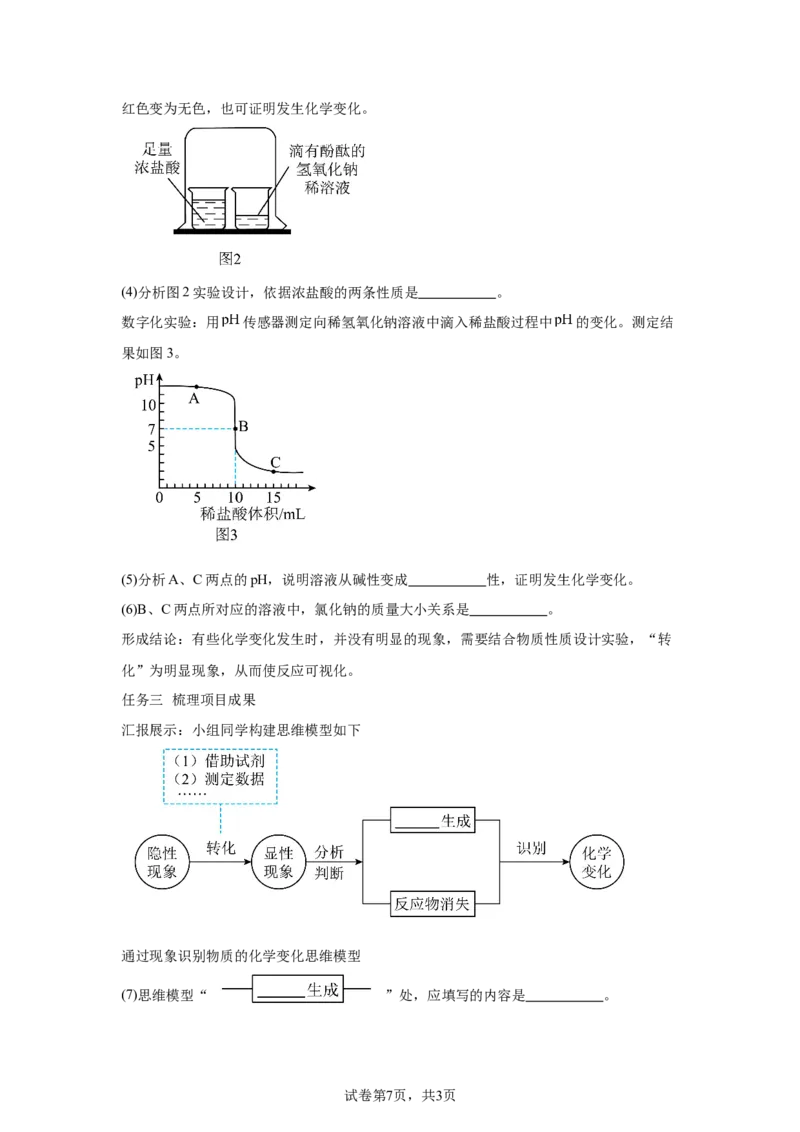
改进实验:如图2,小组同学对图1实验进行改进。观察到滴有酚酞的氢氧化钠稀溶液由
试卷第6页,共3页红色变为无色,也可证明发生化学变化。
(4)分析图2实验设计,依据浓盐酸的两条性质是 。
数字化实验:用 传感器测定向稀氢氧化钠溶液中滴入稀盐酸过程中 的变化。测定结
果如图3。
(5)分析A、C两点的pH,说明溶液从碱性变成 性,证明发生化学变化。
(6)B、C两点所对应的溶液中,氯化钠的质量大小关系是 。
形成结论:有些化学变化发生时,并没有明显的现象,需要结合物质性质设计实验,“转
化”为明显现象,从而使反应可视化。
任务三 梳理项目成果
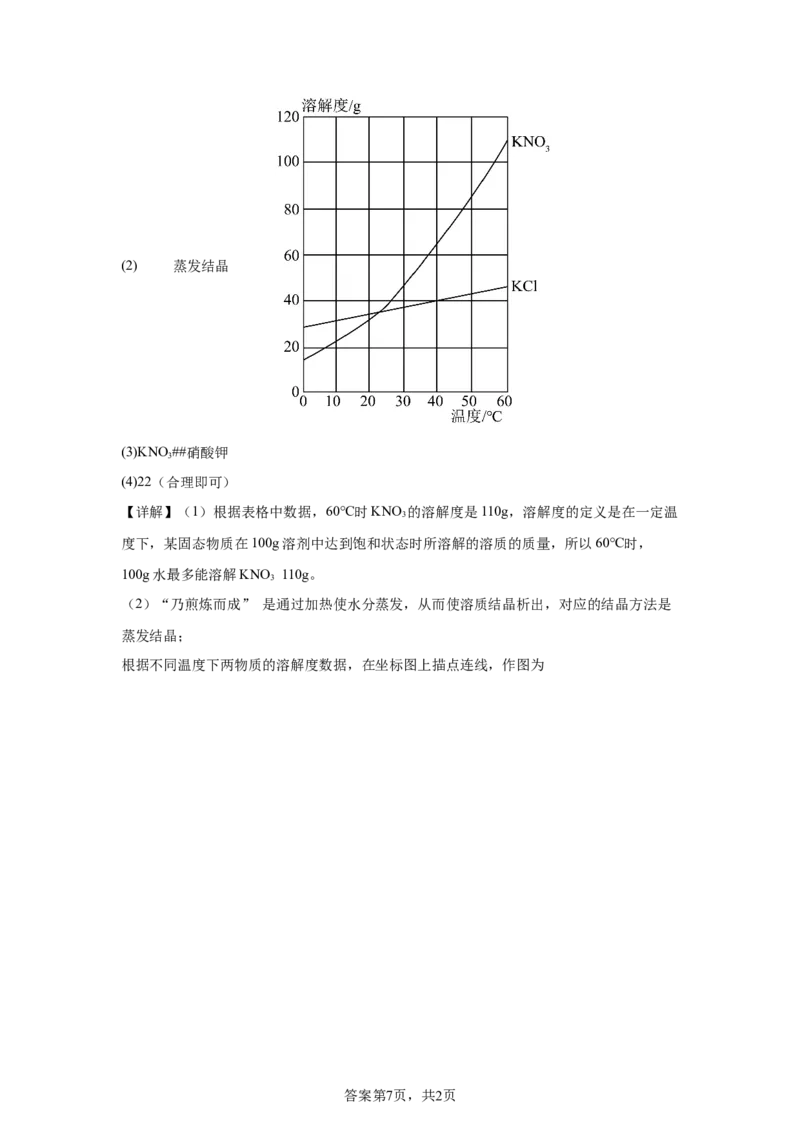
汇报展示:小组同学构建思维模型如下
通过现象识别物质的化学变化思维模型
(7)思维模型“ ”处,应填写的内容是 。
试卷第7页,共3页通过对现象的观察、分析,可以帮助我们更好地识别物质的化学变化。
三、计算题(共5分)
20.吉林省位于黄金玉米带上。提高粮食产量,需要合理施用化肥。尿素是氮肥中最主要
的一种,合成尿素的原理是 。回答下列问题。
(1) 中氮元素和氢元素质量的最简整数比为 。
(2)利用上述化学方程式计算:44吨 能与多少吨 恰好完全反应?
试卷第8页,共3页1.A
【详解】A、合金是由一种金属跟其他金属(或非金属)熔合形成的具有金属特性的物质,
属于金属材料,汽车很多关键部件如发动机、车架等会用到合金材料,A 选项正确;
B、橡胶是有机高分子材料,分为天然橡胶和合成橡胶,常用于汽车轮胎、密封件等,但
不属于金属材料,B 选项错误;
C、塑料是有机合成材料,具有质轻、耐腐蚀等特点,可用于汽车内饰等部件,并非金属
材料,C 选项错误;
D、玻璃属于无机非金属材料,在汽车上主要用于车窗等部位,不属于金属材料,D 选项
错误。
故选A。
2.C
【详解】A、二氧化碳是植物光合作用的原料,植物通过光合作用吸收二氧化碳,而不是
产生二氧化碳,A 选项错误;
B、稀有气体在空气中含量相对稳定,其来源与植物光合作用没有关系,B 选项错误;
C、植物光合作用的过程是在叶绿体里,利用光能,将二氧化碳和水转化成储存能量的有
机物,并且释放出氧气,所以氧气是植物光合作用产生的,C 选项正确;
D、氮气在空气中含量最多,它的产生和植物光合作用无关,D 选项错误。
故选C。
3.A
【详解】A、用盐酸除铁锈,是因为盐酸能与铁锈(主要成分是Fe O)发生化学反应,化
2 3
学方程式为 ,通过化学反应体现性质,利用的是盐酸的化学性
质,A 选项正确;
B、利用液氮进行冷冻,是利用液氮汽化吸热,使周围温度降低,这一过程没有新物质生
成,利用的是液氮的物理性质(汽化吸热),B 选项错误;
C、用铜丝作导线,是利用铜的导电性,导电性不需要发生化学变化就能表现出来,属于
物理性质,C 选项错误;
D、干冰用于人工增雨,是利用干冰升华吸热,使周围水蒸气凝结成水滴,升华是物理变
化,利用的是干冰的物理性质,D 选项错误。
故选A。
4.D
答案第1页,共2页【详解】A、图标分别是佩戴护目镜和洗手,在配制溶液过程中,为避免溶液溅入眼睛,
需佩戴护目镜,实验后需要洗手,以保持手部清洁,该选项正确;
B、配制100g质量分数为16%的氯化钠溶液,需要氯化钠的质量为 ,需要
水的质量为 ,水的密度是1g/mL,则水的体积为84mL,用量筒量取84mL
水时,读数正确,该选项正确;
C、溶解氯化钠时在烧杯中进行,并用玻璃棒搅拌加速溶解,该选项正确;
D、装瓶时应使用细口瓶,方便倾倒液体,广口瓶一般用于存放固体药品;另外,标签应
写上溶液名称和溶质质量分数,图中标签缺少溶液名称,该选项错误。
故选D。
5.C 6.B 7.B
【解析】5.气体可压缩储存于钢瓶中,是因为分子之间有间隔,在受压的情况下,分子间
间隔变小 。分子种类在压缩过程中不会改变;分子不断运动与气体可压缩储存无关;压缩
过程中分子数目也不会增多。
故选C。
6.A、电解水过程中,电能转化为化学能,存在能量转化,A 错误;
B、电解水时,负极产生的气体是氢气,氢气具有可燃性,可用燃着的木条检验,若气体
能燃烧,产生淡蓝色火焰,则是氢气,B 正确;
C、在化学变化中,分子可分,原子不可分,原子是化学变化中的最小粒子,电解水的化
学变化中最小粒子是氢原子和氧原子,C 错误;
D、电解水生成氢气和氧气,根据化学反应前后元素种类不变,说明水是由氢元素和氧元
素组成,而不是由氢气和氧气组成,D 错误。
故选B。
7.A、道尔顿提出了原子论 ,该选项人物与贡献相符,A 不符合题意;
B、发现元素周期律并编制出元素周期表的是门捷列夫 ,拉瓦锡通过实验得出空气是由氮
气和氧气组成等重要结论,该选项人物与贡献不相符,B 符合题意;
C、徐寿新造了许多元素中文名称 ,该选项人物与贡献相符,C 不符合题意;
D、张青莲为测定相对原子质量作出了卓越贡献,该选项人物与贡献相符,D 不符合题意。
故选B。
8.D
答案第2页,共2页【详解】A、该运动饮料配料中有糖类(果葡糖浆、白砂糖、蜂蜜)、水,它们属于营养
物质,所以该饮料含有营养物质,A 选项错误;
B、运动饮料虽能补充电解质等,但不能替代水大量饮用,大量饮用可能会导致体内电解
质失衡等问题,B 选项错误;
C、国家标准规定运动饮料钠含量应在5~120毫克 /100毫升,该饮料钠含量为5~19毫克
/100毫升,符合国家标准,C 选项错误;
D、从包装信息可知,该运动饮料蜂蜜添加量为250毫克/100毫升,即每100毫升中含有蜂
蜜250毫克,D 选项正确。
故选D。
9.C
【详解】A、从图中可以看到,2022 年大气中SO 浓度数值不为 0 ,说明大气中是有SO
2 2
存在的,A 选项错误;
B、观察图中数据,对比 2012 年 2 月和 2022 年 2 月SO 浓度,二者差异较大,并非差
2
异最小,B 选项错误;
C、冬季一般指 12、1、2 月,从图中明显看出 2012 年这几个月SO 浓度值较高,明显高
2
于其他季节,C 选项正确;
D、煤中往往含有硫元素,燃烧煤会产生SO ,会增加SO 的排放,而不是减少,D 选项错
2 2
误。
故选C。
10.D
【详解】A.赤铁矿石粉碎后可以增大反应物的接触面积,使反应更充分,并不能增加铁元
素的含量,故A错误;
B.由流程图可知,原料是赤铁矿石、天然气,高温尾气可循环使用,但不是原料,故B错
误;
C.根据质量守恒定律,化学反应前后原子的种类和数目不变,反应物中C、H、O原子的个
数分别为2、4、2,生成物中C、O原子的个数分别为2、2,所以2X中应有4个氢原子,
X的化学式为H,故C错误;
2
D.赤铁矿石的主要成分氧化铁( ),天然气的主要成分是甲烷( ),它们都是
由不同种元素组成的纯净物,都属于化合物,故D正确。
故选:D。
答案第3页,共2页11.(1)I
(2)53
(3)非金属
【详解】(1)元素周期表信息示意图中,右上角的字母为元素符号,由图可知碘元素的符
号是I。
(2)元素周期表信息示意图中,左上角的数字表示原子序数,由图可知碘的原子序数为
53。在原子中,原子序数=质子数,所以碘原子的质子数为53。
(3)碘元素名称带 “石” 字旁,从元素分类角度,属于非金属元素。
12.(1)
(2)AlO
2 3
(3)0##零
【详解】(1)根据文中对 “根” 的定义,Al是铝元素,O是氧元素, 是铵根离子,
是带电荷的原子团,所以表示 “根” 的符号为 。
(2)氧化铝中铝元素化合价为+3价,氧元素化合价为−2价。设氧化铝化学式为Al O,
x y
根据化合物中各元素化合价代数和为零的原则,有 ,解得 ,所以
氧化铝化学式为Al O。
2 3
(3)在单质里,元素的化合价规定为0。
13.(1)
吸附水中的色素和异味
(2)
硬度(或酸碱度、可溶性杂质含量、微生物含量等,合理即可)
(3)
节约用水(或防治水体污染,合理即可)
【详解】(1)活性炭具有疏松多孔的结构,这种结构使其具有很强的吸附性,能吸附水中
的色素和异味。
(2)硬度是衡量水中钙、镁离子含量的指标,硬度高的水可能会对生活和生产产生不利影
响;酸碱度(pH)反映水的酸碱性,合适的酸碱度对水生生物和人类用水很重要;检测可
溶性杂质含量、微生物含量等也能反映水质情况,这些指标都可以用来评估天然水的水质。
(3)节约用水,比如随手关闭水龙头、使用节水器具等,可以减少水资源的浪费,提高水
答案第4页,共2页资源的利用率;防治水体污染,例如工业废水处理达标后排放、合理使用农药化肥等,能
防止水资源受到污染,保障水资源的质量,这两者都是保护水资源的有效途径。
14.(1)化合
(2)2:1
(3)温度达到着火点
【详解】(1)从微观示意图可知,该反应是氢气和氧气反应生成水,该反应是由两种物质
生成一种物质的反应,基本反应类型属于化合反应。故填:化合。
(2)氢气和氧气在点燃条件下反应生成水,该反应的化学方程式为: ,
化学计量数之比等于参加反应的分子个数比,所以参加反应的氢气和氧气分子个数比为
2:1。故填:2:1。
(3)燃烧需要同时满足三个条件:可燃物、与氧气(或空气)接触、温度达到着火点,所
以从燃烧条件分析,“点火”为氢气燃烧提供的条件是温度达到着火点。故填:温度达到
着火点。
15.
铁的活动性比镍强(或铁能置换硫酸镍中的镍)
镍片表面有气泡产生
【详解】根据实验操作 “向试管中加入适量硫酸镍溶液,将用砂纸打磨过的铁片浸入硫酸
镍溶液中” 以及现象 “铁表面有固体析出” ,结合金属活动性顺序相关知识,可知铁能
与硫酸镍溶液发生置换反应,所以预测内容是铁的活动性比镍强(或铁能置换硫酸镍中的
镍);
已知预测是 “镍能与稀硫酸反应” ,镍是比较活泼的金属,在金属活动性顺序中位于氢
之前,能与稀硫酸发生置换反应,生成氢气和相应的盐。所以当把用砂纸打磨过的镍片浸
入稀硫酸中时,会观察到镍片表面有气泡产生。
16.(1)
(2)BD
(3)将燃着的木条放在集气瓶口,若木条熄灭,说明二氧化碳已集满
【详解】(1)大理石主要成分是碳酸钙,它与稀盐酸反应生成氯化钙、水和二氧化碳,化
学方程式为 。
答案第5页,共2页(2)实验室用大理石和稀盐酸制取二氧化碳,该反应是固体和液体在常温下进行,不需要
加热,所以发生装置应选 B;二氧化碳密度比空气大,能溶于水,只能用向上排空气法收
集,所以收集装置选 D,组合为 BD。
(3)因为二氧化碳不燃烧也不支持燃烧,所以将燃着的木条放在集气瓶口,如果木条熄灭,
就表明集气瓶内二氧化碳已充满。
17.(1)
二氧化碳##CO
2
(2)
(3)
NaSO
2 4
【详解】(1)Ca(OH) (氢氧化钙)能与空气中的二氧化碳(CO)反应,化学方程式为
2 2
,生成的碳酸钙是坚硬的物质,可将砖块粘结在一起。
(2)氢氧化钠(NaOH)暴露在空气中,会与空气中的二氧化碳反应生成碳酸钠和水(
),所以变质。
(3)三氧化硫(SO )属于非金属氧化物,氢氧化钠(NaOH)属于碱,非金属氧化物与
3
碱反应生成盐和水。三氧化硫与氢氧化钠反应时,硫元素化合价不变,三氧化硫中硫元素
为+6价,反应生成的盐中硫元素也为+6价,该盐是硫酸钠,化学式为NaSO ,反应的化
2 4
学方程式为 。
18.(1)110
答案第6页,共2页(2) 蒸发结晶
(3)KNO##硝酸钾
3
(4)22(合理即可)
【详解】(1)根据表格中数据,60℃时KNO 的溶解度是110g,溶解度的定义是在一定温
3
度下,某固态物质在100g溶剂中达到饱和状态时所溶解的溶质的质量,所以60℃时,
100g水最多能溶解KNO 110g。
3
(2)“乃煎炼而成” 是通过加热使水分蒸发,从而使溶质结晶析出,对应的结晶方法是
蒸发结晶;
根据不同温度下两物质的溶解度数据,在坐标图上描点连线,作图为
答案第7页,共2页。
(3)对比表格中KCl和KNO 在不同温度下溶解度的变化情况,KNO 溶解度随温度升高
3 3
变化幅度大,KCl溶解度随温度升高变化幅度相对较小,所以溶解度受温度影响较大的是
KNO。
3
(4)根据溶解度曲线,当两种物质溶解度相等时,温度约为22℃(合理即可)。
19.(1)水果变色、产生异味、腐烂变软等(合理即可)
(2)C
(3)
(4)挥发性、能与氢氧化钠反应
(5)酸
(6)B=C
(7)新物质
【详解】(1)水果变质是化学变化,通常会有外观颜色改变(如苹果切开后变色)、散发
难闻气味、质地从硬变软等表现。
(2)A、二氧化碳通入紫色石蕊溶液,是二氧化碳与水反应生成碳酸使石蕊变色(
),无发光、放热,该选项错误;
B、二氧化碳通入澄清石灰水,是生成碳酸钙沉淀[ ],无发
光、放热,该选项错误;
答案第8页,共2页C、白磷在80℃热水且通入氧气条件下燃烧( ),会发光、放热,该选
项正确;
D、镁与稀盐酸反应会放热( ),但不会发光,该选项错误。
故选C。
(3)酚酞遇碱性物质变红,遇中性物质或酸性物质不变色。氢氧化钠溶液呈碱性,能使酚
酞溶液变红,溶液由红色变为无色,是因为氢氧化钠(NaOH)与盐酸(HCl)发生中和反
应,生成氯化钠(NaCl)和水(HO),化学方程式为 。
2
(4)浓盐酸具有挥发性,挥发出的氯化氢气体扩散到氢氧化钠溶液中,与氢氧化钠发生反
应,使溶液碱性减弱,酚酞褪色,从而证明发生了化学变化。
(5)A 点pH大于 7,溶液呈碱性;C 点pH小于 7,溶液呈酸性,说明随着稀盐酸加入,
溶液从碱性变为酸性,证明氢氧化钠和盐酸发生了反应。
(6)B 点pH等于7,稀盐酸与氢氧化钠恰好完全反应,B 点到 C 点,稀盐酸过量,反
应不再发生,没有氯化钠生成,所以 B 点对应溶液中氯化钠质量等于 C 点。
(7)化学变化的本质特征是有新物质生成,通过判断是否有新物质生成,结合反应物是否
消失等情况,来识别化学变化。
20.(1)
(2)解:设所需NH 的质量为x
3
x=34t
答:44吨CO 能与34吨NH 恰好完全反应。
2 3
【详解】(1) 中氮元素和氢元素质量的最简整数比为 。
(2)根据CO 的质量计算,见答案。
2
答案第9页,共2页