文档内容
绝密★启用前 试卷类型:A
山东省泰安市二〇一四年初中学生学业考试
化 学 试 题
本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分,第Ⅰ卷1至4页,第Ⅱ卷5至10
页。满分100分,考试时间90分钟。
注意事项:
1.答卷前,请考生仔细阅读答题卡上的注意事项,并务必按照相关要求作答。
2.考试结束后,监考人员将本试卷和答题卡一并收回。
相对原子质量:H 1 C 12 O 16 Na 23 S 32 Cl 35.5 Ca 40 Fe 56 Cu 64
第Ⅰ卷(选择题 共40分)
一、选择题(本题包括20小题,每小题2分,共40分。每小题只有一个选项符合题意。)
1.元素在自然界里分布并不均匀,如智利富藏铜矿、澳大利亚多铁矿、我国山东富含黄金,
但从整个地壳中元素的含量来看,最丰富的金属元素是
A.O B.Si C.Al D.Fe
[来源:Zxxk.Com]
2.“节能减排,低碳生活”的主题旨在倡导节约能源和利用清洁能源,减少温室气体二氧化
碳的排放。下列措施中不符合该主题的是
A.广泛使用太阳能和风能等清洁能源
B.回收利用废旧金属
C.多使用一次性塑料制品
D.减少使用私家车次数、多乘公交车或骑自行车
3.下列变化一定属于化学变化的是
A.石油分离出汽油、煤油和柴油等
B.煤焦化产生焦炭、煤焦油、焦炉气等
C.工业上分离空气制取氧气、氮气
D.膜法和热法淡化海水
4.分类是化学学习、研究的重要方法。下列有关物质的分类,错误的是A.水属于氧化物 B.干冰属于单质
C . 硝 酸 铵 属 于 盐 D . 乙 醇 属 于 有 机
物
5.下列实验操作中错误的是
A.蒸发结晶 B.稀释浓硫酸 C.滴管用后不洗插回原瓶 D.用力塞紧橡皮塞
6.下列有关实验现象的描述,正确的是
A.铁丝在氧气中剧烈燃烧、火星四射、生成白色固体
B.分别点燃一小块棉纤维和羊毛纤维,都产生了烧焦羽毛的气味
C.测定空气中氧气含量的实验里,铜粉加热变黑
D.一氧化碳高温还原氧化铁时,红色粉末逐渐变为银白色
7.过多的植物营养物质如尿素CO(NH) 等进入水体会恶化水质,导致“水华”现象。尿素
2 2
属于
A.氮肥 B.磷肥 C.钾肥 D.复合肥
8.今年5月,南京某公司丢失一枚探伤用放射源铱-192,经过多方寻找终于放回安全箱。右
下图所是元素周期表提供的铱元素的部分信息,下列说法正确的是
A.铱的原子序数为70
B.铱原子的核电荷数为77
C.铱原子的相对原子量质量为192.2 g
D.铱元素为非金属元素
9.溶洞中存在的化学反应:CaCO +CO +H O === Ca(HCO ),此反应属于
3 2 2 3 2
A.化合反应 B.分解反应
C.置换反应 D.复分解反应
10.实验室中利用过氧化氢、氯酸钾、高锰酸钾都可以制取氧气,其原因是
A.都属于氧化物 B.都含有氧气
C . 都 含 有 氧 气 分 子
D.都含有氧元素11.稀土元素铕(Eu)是激光及原子能应用的重要材料。已知氯化铕的化学式为EuCl ,则氧
3
化铕的化学式为
A.EuO B. Eu O
2 3
C.Eu O D.EuO
3 2 3
12.关于分子和原子两种粒子的叙述正确的是
A.物质只能由分子、原子构成 B.分子质量一定大于原子质量
C.化学变化中分子数目一定发生变化 D.同种原子可能构成不同的分子
13.据探测卫星发回的数据分析,火星大气中95%是二氧化碳,其余为少量的氮气、氢气,还
找到了有液态水存在的证据。根据以上信息,某同学作出如下推断:①火星大气是混合物;
②火星大气与地球大气成分相似;③火星上钢铁不容易生锈;④火星环境适宜人类生存;
⑤火星上温室效应显著。你认为正确的是
A.①③⑤ B.②③⑤
C.②③④ D.①④⑤
1 4.化学上常用元素符号左下角的数
字表示原子的质子数,左上角的数字表示原子的中子数与质子数之和,如 13C表示核内有
6
6个质子和7个中子的碳原子。下列关于 131I和 127I的说法中错误的是
53 53
A.各一个原子相比较,质子数相同
B.各一个原子相比较,中子数相同
C.各一个原子相比较,核外电子数相同
D.属于同种元素
15.关于下列事实的解释不正确的是
选项 事实 解释
A 10mL酒精和10mL 水混合后体积小于20mL 分子之间有间隔
溶液中都含有H+,也存在不同
B 稀硫酸和稀盐酸化学性质相似也存在差异
的SO 2- 、Cl-离子
4
C 化学反应中都易得到1个电子
F 、Cl原子化学性质相似
D 化肥硫酸铵不能和熟石灰混放或混用 硫酸铵与熟石灰发生中和反应
16 . 掌 握 化 学 用 语 是 学 好 化 学 的 关 键 。 下 列 化 学 用 语 与 所 表 述 的 意义相符合的是
+1
①FeCl —氯化亚铁 ②2Ca2+—-2个钙离子 ③O—2个氧原子 ④Na —钠离子
2 2
0
⑤HO—1个水分子 ⑥2H—2个氢元素 ⑦ N —-氮气中氮元素的化合价为0
2 2
A.①④⑤⑦ B.②③④⑥ C.①②⑤⑦ D.②⑤⑥⑦
17.化学兴趣小组的同学利用废铜制取硫酸铜,设计了如下两个方案:
O 稀硫酸
方案一:Cu 2 CuO CuSO
△
△4
方案二:Cu 浓硫酸 CuSO [Cu + 2H SO (浓)===△= CuSO + SO↑ + 2H O]
4 2 4 4 2 2
△
比较上述两个方案,你认为方案一的优点是
①节约能源 ②不产生污染大气的二氧化硫 ③提高硫酸的利用率 ④提高铜的利用率
A.②③ B.①②③
C.①③④ D.①②③④
18.取一滤纸条,等间距滴10滴紫色石蕊试液,然后装入玻璃管中(如图所示),两端管口同时
放入分别蘸有浓氨水和浓盐酸的棉球,几秒后观察到图示现象。下列说法不正确的是
A.氨水的pH大于7, 盐酸的pH小于7
B.浓氨水和浓盐酸都具有挥发性
C.氨分子和氯化氢分子的运动速率相等
D.酸、碱能使紫色石蕊试液显示不同颜色
19.某化学兴趣小组,为验证Ag、Fe、Cu三种金属的活动性顺序,设计了如图所示的实验操
作,其中可以达到实验目的的组合是
A .①②或②③或②④⑤
B.②④或①③或②④⑤
C.①③或②③或①④⑤ D.①②或②③或③④⑤
20.现有a、b、c、d四种无色溶液,分别是碳酸钾溶液、硫酸溶液、氯化钡 溶液、盐酸中的一种,两两混
合后出现右图所示的现象,试确定a、b、c、d的顺序分别为
A.硫酸溶液、碳酸钾溶液、氯化钡溶液、盐酸,
B.氯化钡溶液、盐酸、碳酸钾溶液、硫酸溶液
C.碳酸钾溶液、硫酸溶液、盐酸、氯化钡溶液
D.盐酸、硫酸溶液、碳酸钾溶液、氯化钡溶液
第Ⅱ卷(非选择题 共60分)
二、(本题包括6小题,共26分)
21.(5分) 从化学的视角认识厨房中蕴含的丰富化学知识。
(1)下列食物中富含蛋白质的是 (填字母序号,下同);
A . 米 饭 B . 西 红 柿 C . 牛 肉
D.花生油
(2)下列厨房用品所使用的主要材料,属于金属材料的是 ;A.紫砂锅 B.陶瓷碗 C.不锈钢水瓢 D.塑料盆
(3)天然气是主要的家用燃气。天然气的主要成分是 ;
(4)炒菜时油锅着火,盖上锅盖即可灭火,原因是 ;
( 5 ) 洗 涤 剂 可 清 洗 餐 具 上 的 油 污 , 这 是 因 为 洗
涤剂具有__ ___功能。
22.(3分)2014年4月2日~4日发生了清华学生PX词条“保卫战”,最终在百度百科上锁
定“PX”为“低毒化合物”的准确描述,向国人揭示了尊重事实的科
学态度。PX是“对二甲苯”,其组成和结构如右图所示,相关性质如
下:
①无色透明液体,有芳香气味 ②熔点13.2℃、沸点138.5℃
③密度0.86g/cm3 ④可燃 ⑤有挥发性,但比汽油低
[来源:学,科,网]
⑥遇火可爆炸,但爆炸性比汽油低 ⑦低毒,毒性与汽油相当。
根据上述信息,请你回答下列问题:
(1)上表中属于PX物理性质的是(填数字序号) ;
(2)试写出PX在空气中完全燃烧反应的化学方程式 ;
(3)根据PX的性质,从防止环境污染和安全的角度,应如何保存和储运PX? 。
23.(5分)KNO 和NaCl在不同温度时的溶解度如下表所示。请回答下列问题:
3
温度/℃ 0 10 20 30 40 50 60 70
溶 度 解 /g KNO 3 13.3 20.9 Z 源科X] : X网学 [来 K 31.6 Z学,X,科 [ ,X 来 ,,网K 源 ] : 45.8 63.9 85.5 110 138
+科+网] [来源:学 NaCl 35.7 35.8 36.0 36.3 36.6 37.0 37.3 37.8
(1)依据上表数据,绘制出KNO 和NaCl的溶解度曲线如右图所示,图中能表示KNO 溶
3 3
解度曲线的是 (填“A”或“B”);
(2)由表中数据分析可知, KNO 和NaCl在某一温度时具有相同的
3
溶解度,则温度的取值范围是 ;
(3)某兴趣小组做了以下实验:20℃ 100 g水
上述实验过程中得到的溶液一定属于不饱和溶液的是 (填数字序号),将
⑤继续冷却至10℃,过滤,共可回收得到KNO 固体 g;
3
(4)硝酸钾中含有少量氯化钠时,可通过 (填“蒸发结晶”或“降
温结晶”)的方法提纯。
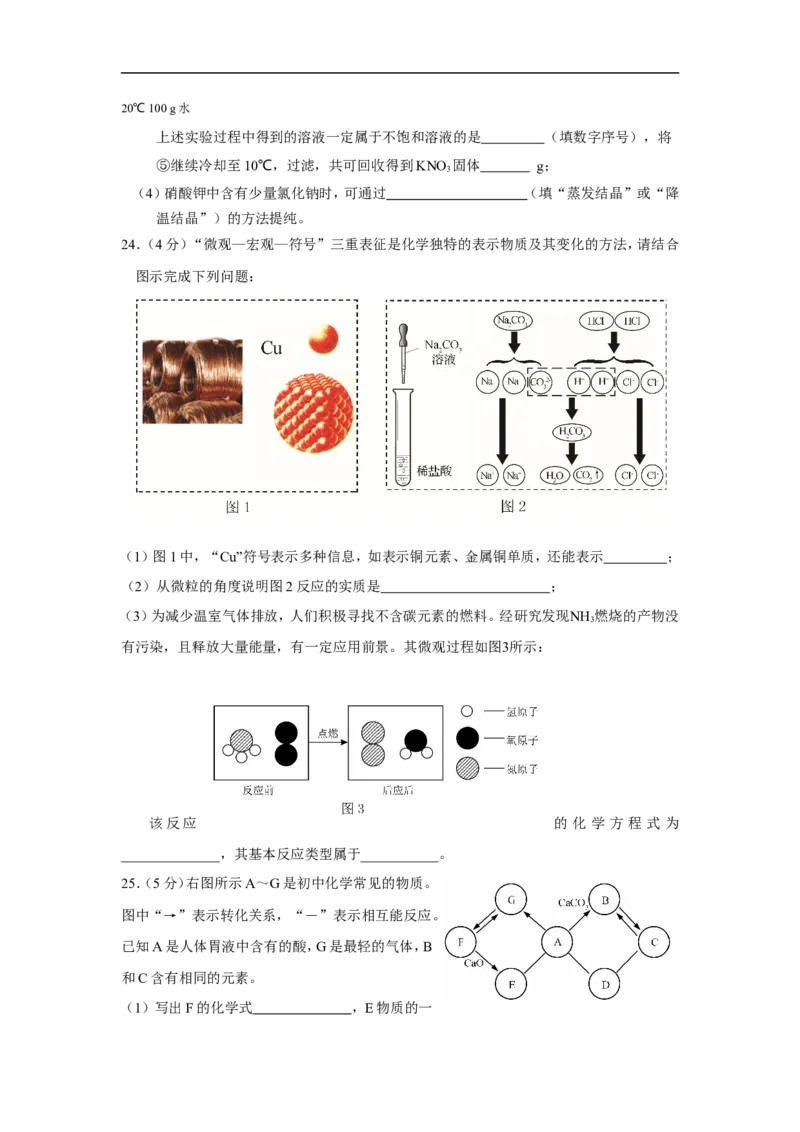
24.(4分)“微观—宏观—符号”三重表征是化学独特的表示物质及其变化的方法,请结合
图示完成下列问题:
(1)图1中,“Cu”符号表示多种信息,如表示铜元素、金属铜单质,还能表示 ;
(2)从微粒的角度说明图2反应的实质是 ;
(3)为减少温室气体排放,人们积极寻找不含碳元素的燃料。经研究发现NH 燃烧的产物没
3
有污染,且释放大量能量,有一定应用前景。其微观过程如图3所示:
该反应 的 化 学 方 程 式 为
______________,其基本反应类型属于___________。
25.(5分)右图所示A~G是初中化学常见的物质。
图中“→”表示转化关系,“―”表示相互能反应。
已知A是人体胃液中含有的酸,G是最轻的气体,B
和C含有相同的元素。
(1)写出F的化学式 ,E物质的一种用途 ,C物质的一条化学性质 ;
(2)C和D反应需要高温,写出他们发生反应的化学方程式 ;
(3)A→B反应的化学方程式是 。
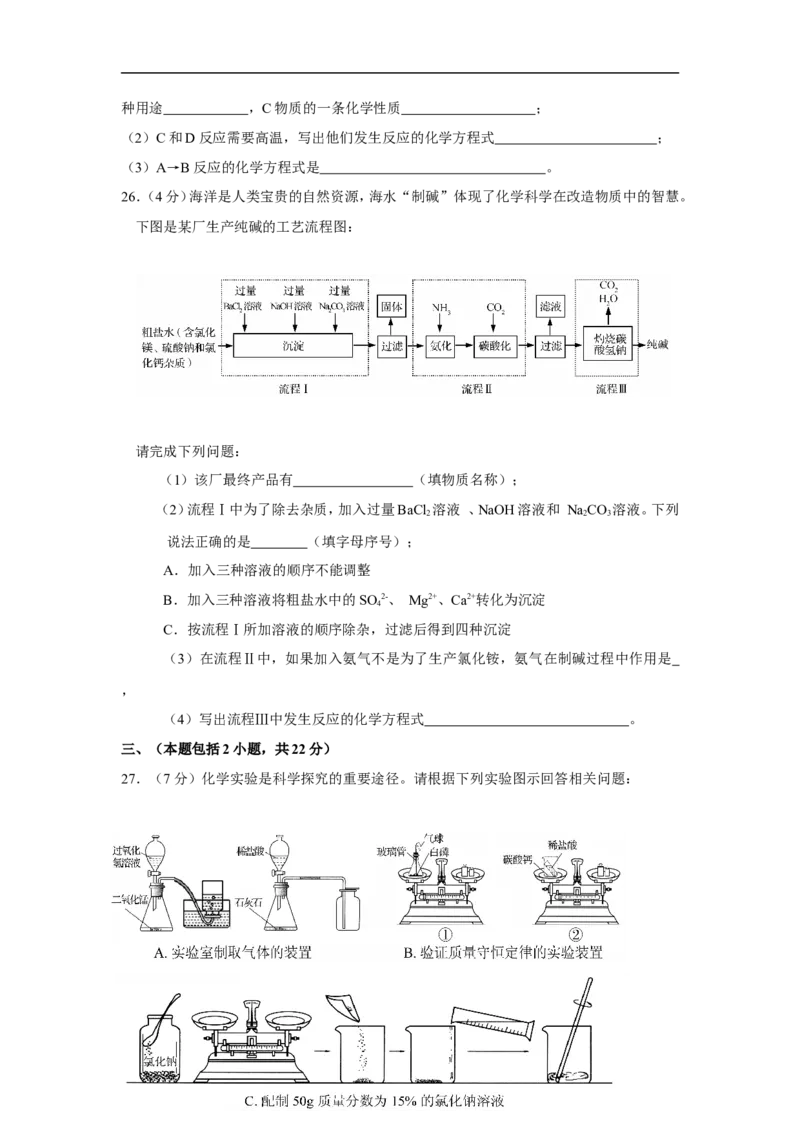
26.(4分)海洋是人类宝贵的自然资源,海水“制碱”体现了化学科学在改造物质中的智慧。
下图是某厂生产纯碱的工艺流程图:
请完成下列问题:
(1)该厂最终产品有 (填物质名称);
(2)流程Ⅰ中为了除去杂质,加入过量BaCl 溶液 、NaOH溶液和 NaCO 溶液。下列
2 2 3
说法正确的是 (填字母序号);
A.加入三种溶液的顺序不能调整
B.加入三种溶液将粗盐水中的SO 2-、 Mg2+、Ca2+转化为沉淀
4
C.按流程Ⅰ所加溶液的顺序除杂,过滤后得到四种沉淀
(3)在流程Ⅱ中,如果加入氨气不是为了生产氯化铵,氨气在制碱过程中作用是
,
(4)写出流程Ⅲ中发生反应的化学方程式 。
三、(本题包括2小题,共22分)
27.(7分)化学实验是科学探究的重要途径。请根据下列实验图示回答相关问题:(方1)A是实验室制备气体的发生与收集装置。用过氧化氢溶液与二氧化锰制取氧气的化
学程式为 ,制取氧气、二氧化碳可用同样的发生装置,原因
是 ,选择收集装置的依据是 ;
(2)B实验中设计合理的是 (填“①”或“②”);另一装置设计中存在的问
题是
;
(3)C是定量实验,选择仪器不恰当或操作不规范都会导致实验结果有误差。实验时选择
量筒规格应为 (填“50mL”或“100 mL”),称量时砝码与药品位置放反
了(1g以下使用游码),所得溶液的质量分数 15%(填“大于”、“等于”或
“小于”)。
28.(15分)实验室有一瓶长期暴露在空气中的氢氧化钠固体样品,观察发现,样品表面有白
色粉末。某兴趣小组的同学对该样品的成分及含量进行了探究。
【提出问题1】该样品中含有哪些物质?
【提出猜想】通过分析,提出如下猜想:
猜想Ⅰ:已完全变质,该样品中只含NaCO;
2 3
猜想Ⅱ:部分变质,该样品中含有NaOH和NaCO。
2 3
则NaOH变质反应的化学方程式为________________________________;
【查阅资料】
①碱性的NaCO 溶液可以与中性的CaCl 溶液发生复分解反应;
2 3 2
②CO 在饱和的碳酸氢钠溶液中几乎不溶解。
2
【实验探究1】
为确定该样品的成分,小明设计了如下实验方案,请你一起完成下列实验报告。
实验操作 实验现象 实验结论
白色沉
(1)取少量样品溶于水,加入 该反应的化学方程式为
;
淀产生
(2)将上述反应后的混合液过滤,取
证明猜想Ⅱ成立
滤液加入 ;【提出问题2】如何测量该部分变质样品中碳酸钠的质量分数?
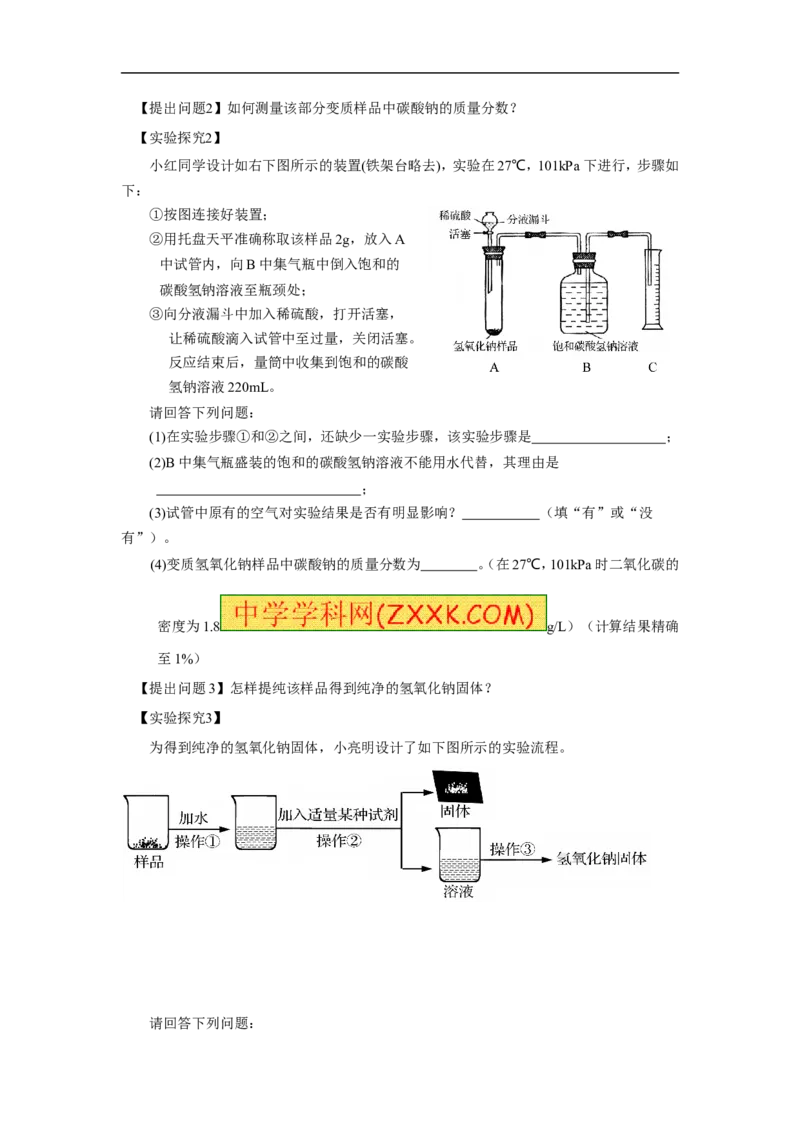
【实验探究2】
小红同学设计如右下图所示的装置(铁架台略去),实验在27℃,101kPa 下进行,步骤如
下:
①按图连接好装置;
②用托盘天平准确称取该样品2g,放入A
中试管内,向B中集气瓶中倒入饱和的
碳酸氢钠溶液至瓶颈处;
③向分液漏斗中加入稀硫酸,打开活塞,
让稀硫酸滴入试管中至过量,关闭活塞。
反应结束后,量筒中收集到饱和的碳酸
氢钠溶液220mL。
请回答下列问题:
(1)在实验步骤①和②之间,还缺少一实验步骤,该实验步骤是 ;
(2)B中集气瓶盛装的饱和的碳酸氢钠溶液不能用水代替,其理由是
;
(3)试管中原有的空气对实验结果是否有明显影响? (填“有”或“没
有”)。
(4)变质氢氧化钠样品中碳酸钠的质量分数为 。(在27℃,101kPa时二氧化碳的
密度为1.8 g/L)(计算结果精确
至1%)
【提出问题3】怎样提纯该样品得到纯净的氢氧化钠固体?
【实验探究3】
为得到纯净的氢氧化钠固体,小亮明设计了如下图所示的实验流程。
请回答下列问题:(1)操作①、②、③分别是 ,为了使样品充分溶解,操作①中还要用
到的玻璃仪器是 ;
(2)该实验中发生反应的化学方程式为 ;
(3)最终所得氢氧化钠固体质量 变质后样品中氢氧化钠的质量(填“大于”、
“等于”或“小于”)。
【实验反思】
( 1)通过本题,你学会了定性检验
氢氧化钠的变质、定量测定变质后某成分的含量,以及除杂提纯物质。为了得到可靠
的实验结果,探究过程中你需要思考问题有
(填数字序号);
①选择试剂种类 ②确定试剂用量 ③试剂产地
④实验装置与步骤的设计 ⑤实验安全环保 ⑥测量中减少误差
(2)实验探究1中的检验和实验探究3中的除杂都将碳酸钠进行了转化,但二者目的不同,
分别是 。
四、(本题包括2小题,共12分)
29.(5分)钙是维持人体正常功能所必需的元素,有时需要服用补钙剂满足人体需求。下图
分别为两种补钙剂说明书的一部分。
葡萄糖酸钙片 金钙尔奇
【主要成分】每片含葡萄糖酸钙 【主要原料】碳酸钙(CaCO )氧化镁 硫酸锌 硫酸铜、
3
(C H O Ca)0.5g 维生素等
12 22 14
【用法】口服 【含量】每片含 钙280mg 镁99.7mg 锌3.08mg 铜
【用量】每日3次,一次 片 0.51 mg 等
【用量】每日2次,一次1片
请根据图示中的信息回答下列问题:
(1)钙是人体必须的常量元素,每日要摄取足够量的钙,才能避免 (填字母序号);
A. 佝偻病或骨质疏松症
B. 贫血症 C. 甲状腺肿大
(2)葡萄糖酸钙(C H O Ca)的化学式量是 ;
12 22 14
(3)碳酸钙(化学式CaCO )中钙元素的质量分数为 ;
3
(4)每片金钙尔奇中含碳酸钙的质量为 mg;
(5)按照金钙尔奇说明书每日的补钙量,若改用葡萄糖酸钙,一日3次,一次应服用几片? 。
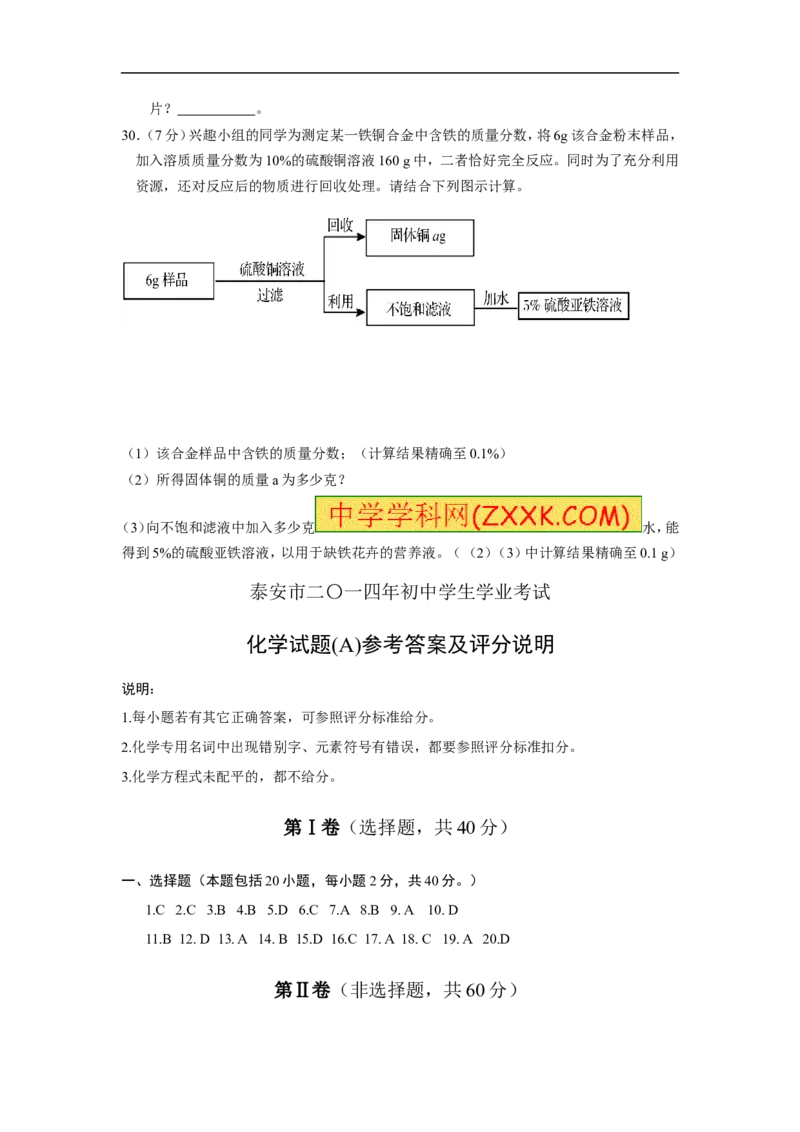
30.(7分)兴趣小组的同学为测定某一铁铜合金中含铁的质量分数,将6g该合金粉末样品,
加入溶质质量分数为10%的硫酸铜溶液160 g中,二者恰好完全反应。同时为了充分利用
资源,还对反应后的物质进行回收处理。请结合下列图示计算。
(1)该合金样品中含铁的质量分数;(计算结果精确至0.1%)
(2)所得固体铜的质量a为多少克?
(3)向不饱和滤液中加入多少克 水,能
得到5%的硫酸亚铁溶液,以用于缺铁花卉的营养液。((2)(3)中计算结果精确至0.1 g)
泰安市二〇一四年初中学生学业考试
化学试题(A)参考答案及评分说明
说明:
1.每小题若有其它正确答案,可参照评分标准给分。
2.化学专用名词中出现错别字、元素符号有错误,都要参照评分标准扣分。
3.化学方程式未配平的,都不给分。
第Ⅰ卷(选择题,共40分)
一、选择题(本题包括20小题,每小题2分,共40分。)
1.C 2.C 3.B 4.B 5.D 6.C 7.A 8.B 9. A 10. D
11.B 12. D 13. A 14. B 15.D 16.C 17. A 18. C 19. A 20.D
第Ⅱ卷(非选择题,共60分)二、(本题包括6小题,共26分)
21.(5分)
(1)C(1分)
(2)C(1分)
(3)甲烷(或CH)(1分)
4
(4)隔绝空气(1分)
(5)乳化(1分)
22.(3分)
(1)①②③⑤(1分)
点燃
(2)2C H +21O ===16CO +10H O(1分)
8 10 2 2 2
(3)密封保存、严禁烟火(1分)
23.(5分)
(1)A(1分)
(2)20℃~30℃(1分)
(3)①③④(1分) 59.1(1分)
(4)降温结晶(1分)
24.(4分)
(1)一个铜原子(1分)
(2)氢离子与碳酸根离子结合生成水和二氧化碳(或H+和CO2-结合生成HO和CO)(1分)
3 2 2
点燃
(3)4NH +3O ====2N +6H O(1分) 置换反应(1分)
3 2 2 2
25.(5分)
(1)HO(1分)
2
建筑材料(或改良酸性土壤或生产农药、漂白粉、烧碱等,1分)
可燃性(或毒性或还原性,1分)
(2)Fe O+3CO == 高 = 温 ==Fe +3CO(1分)(Fe O、CuO等均可)
2 3 2 2 3 4
(3)CaCO +2HCl===CaCl +HO+CO ↑(1分)
3 2 2 2
26.(4分)
(1)纯碱、氯化铵(或碳酸钠、氯化铵)(1分)
(2)B C(1分)
通电
(3)使溶液显碱性,有利于二氧化碳的吸收(1分)
(4)2NaHCO △ N aCO+H O+CO ↑(1分)
3 2 3 2 2三、(本题包括2小题,共22分)
27.(7分)
MnO
(1)2HO====22H O+ O ↑(1分)
2 2 2
反应物状态及反应条件相同(或都是固体与液体反应,且不需加热,1分)
气体的密度和溶解性(1分)
(2)①(1分)
②中装置不密闭生成的二氧化碳逸散空气中,没有称量计入反应后的总质量(1分)
(3)50mL(1分) 小于(1分)
28.(15分)
【提出猜想】CO+2NaOH===Na CO+ H O(1分)
2 2 3 2
【实验探究1】
实验操作 实验现象 实验结论
NaCO+ CaCl = 2NaCl+CaCO
2 3 2
过量CaCl 溶液(1分)
2
或BaCl 溶液
2 ↓(1分)
3
或 NaCO+ BaCl = 2NaCl+BaCO ↓
2 3 2 3
酚酞试液(1分) 溶液变红色(1分)
【实验探究2】
(1)检查装置的气密性(1分)
(2)避免二氧化碳溶解在水中而损耗,导致测定结果偏低(1分)
(3)没有(1分)
(4)48%(1分)
【提出问题3】
(1)溶解、过滤、蒸发(1分) 玻璃棒(1分)
(2)NaCO+Ca(OH) ==CaCO↓+2NaOH(或NaCO+Ba(OH) ==BaCO↓+2NaOH,1
2 3 2 3 2 3 2 3
分)
(3)大于(1分)
【实验反思】
(1)①②④⑤⑥(1分)
(2)检验中将NaCO 转化为NaCl,以排除对NaOH检验的干扰;除杂中是将NaCO
2 3 2 3
转化为产品NaOH (1分)
四、(本题包括2小题,共12分)29.(5分)
(1)A(1分) (2)430(1分) (3)40%(1分)
(4)700(1分) (5)4(1分)
30.(7分)
解: 设样品中铁的质量为x,生成铜的
质量为y,生成硫酸亚铁的质量为z。
[
Fe + CuSO = FeSO + Cu ····················
4 4
·······1 分
56 160 152 64
x 160g×10% z y
56/160= x/160g×10% x = 5.6g ···························1 分
160/64=160g×10%/ y y = 6.4g ···························1 分
160/152=160g×10%/ z z = 15.2g ···························1 分
⑴样品中含铁的质量分数=5.6 g/6g× 100%=93.3% ····················1 分
⑵ a=6.4g+(6g-5.6g)=6.8g ······················1 分
⑶要得到5%的硫酸亚铁溶液,需要向不饱和滤液中加入水质量为m。
15.2g /(5.6g + 160g – 6.4g + m)× 100% = 5%
m =144.8g ···························1 分
答:略
说明:1.计算题只写出最后结果而无运算过程的不给分。
2.计算题解题过程不符合法定单位制(设未知数不符合要求或运算过程不带单位)和
计算结果不符合要求者共扣1分。