文档内容
试卷类型A
济宁市二O一四年高中段学校招生考试
化学试题
注意事项(略)(共5条)
第I卷(选择题 共16分)
可能用到的相对原子质量:
N-14 O-16 S-32 Cl-35.5 Na-23 Ag-108
一、选择题(下列各题只有一个正确选项。其中1~4小题各1分,5~10小题各2分,本大题共
16分)
1.(2014年山东济宁,1题,1分)物质的性质决定了物质的用途。下列几种常见物质的性质、
用途不一致的是
A.氮气 性质稳定 保护气
B.酒精 可燃性 消毒剂
C.食醋 酸性 除水垢
D.干冰 升华吸热 人工降雨
2 . ( 2014 年 山 东 济 宁 , 2 题 , 1 分 ) 日 常 生 活 中 的 许 多 做 法 都 蕴 含
化学知识的运用。其中,运用
不正确的是
A.低温冷藏有助于减缓食品腐败
B.保鲜膜可保持水果水分、隔离空气,延长保质期
C.烹调绿叶蔬菜焖烂煮透,营养更加丰富
D.食用碱可消除面粉发酵产生的酸味
3.(2014 年山东济宁,3题,1
分)“水是生命的源泉”。下面对水化学式(HO)意义的理解,错误的是
2
A.水是一种氧化物
B.水是由氢、氧两种元素组成的
C.水分子中含有氢、氧两种原子
D.水分子中含有两个氢原子、一个氧原子
4.(2014年山东济宁,4题,1分)对下面一些实验现象的描述,正确的是
A.氢气在空气中点燃 发出黄光、放出热量
B.铁粉在空气中加热 剧烈燃烧、生成黑色固体
C.浓硫酸敞口放置 溶液的颜色、质量不变
D.烧碱固体放入水中 迅速溶解、溶液温度升高
5.(2014年山东济宁,5题,2分)对下面符号或示意图的理解,正确的是
[来源:学.科.网]
A.Fe2+、Fe3+都属于铁元素,是同一种离子
B.NO 、NO 中氮元素的化合价都是+4价,是同一化合物
2 2 4
C.NH NO 中氮元素有两种不同的化合价,分别是-3、+5
4 3D. 两种粒子的电子排布情况相同,属于同一元素
6.(2014年山东济宁,6题,2分)依据不同化学反应的特点,可将某些反应归于同一类型。下
面几组分类结果最合理的一组是
点燃
①2CO+O 2CO
2 2
△
②CuO+CO Cu+CO
2
③NaO+2HCl=2NaCl+HO
2 2
④NaO+2HO=2NaOH+HO
2 2 2 2 2
A.①③ B.②③ C.③④ D.②④
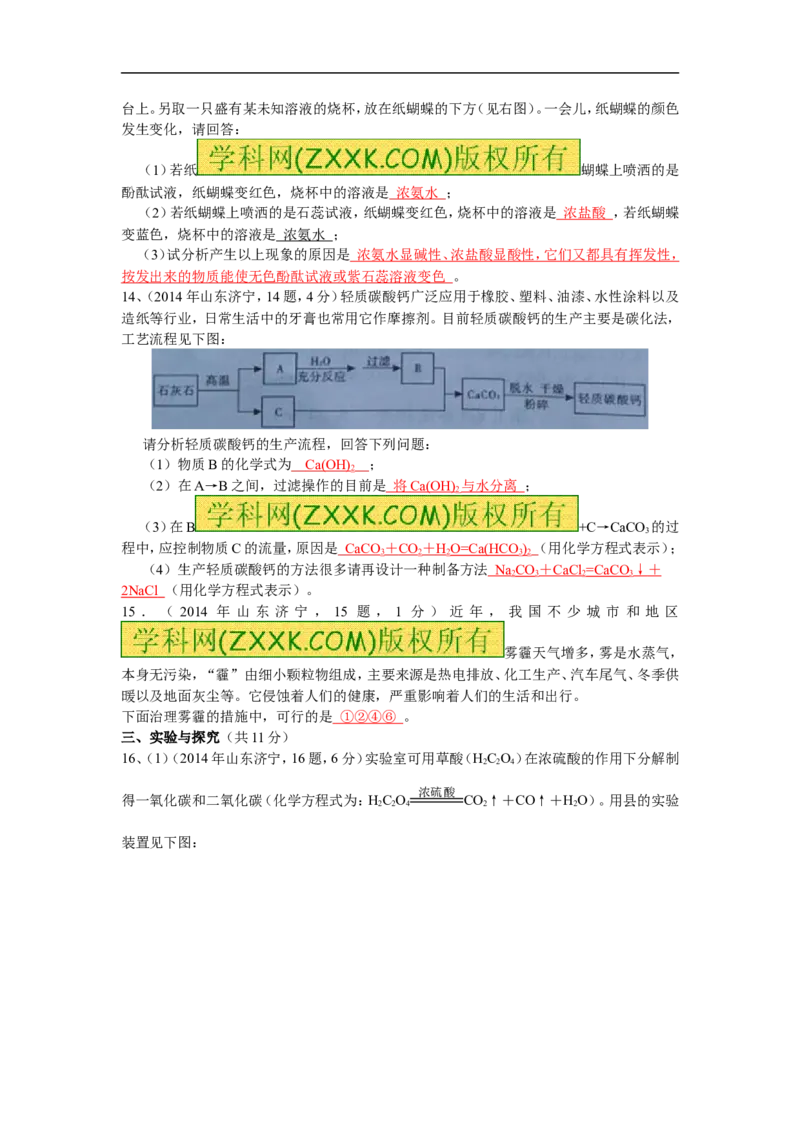
7.(2014年山东济宁,7题,2分)右图为硝酸钾和氯化钠两种物质的饱和溶液的质量分数随
温度变化的曲线,M、N分别是50℃时硝酸钾和氯化钠质量分数随温度变化曲线上的点。分
析曲线得到的以下结论中,正确的是
A.50℃时,M、N之间任一点表示的溶液一定是肖酸钾和氯化钠的饱和溶液
B.50℃时,其他条件不变,升温至60℃,M点向右平移,硝酸钾的溶解度增大
C.50℃时,其他条件不变,降温至40℃,N点向右平移,氯化钠的溶解度减小
D.50℃时,向两饱和溶液添加溶质,M 点不动,硝酸钾和氯化钠的溶
解度增大
8.(2014 年山东济宁,8 题,2 分)某无色气体可能由 H 、CH 、CO、CO 中的
2 4 2
几种组成。将些混合气体通
过过量的澄清石灰水,出现白色浑浊;将剩余气体导出,经干燥后点燃,罩在火焰上方的干燥
烧杯内壁有水珠生成。该混合气体的可能组成是
A.H、CH
2 4
B.H、CO
2
C.H、CH、CO
2 4D.CH、CO、CO
4 2[来源:学科网]
9.(2014年山东济宁,9题,2分)“电子垃圾”中含有金属铜和少量贵金属金、银等,直接废
弃将严重污染环境且造成金属资源浪费。社会实践小组为回收这些金属,设计了以下操作步
骤:
①分拆、灼烧:把废弃电子产品分拆后灼烧,将部分金属转化为氧化物;
②酸洗:用硝酸溶解灼烧得到的混合物,过滤,收集残渣中的金;
③回收:利用合适的金属提炼出滤液中的铜和银。
为达到分别提炼金属铜、银的目的,下列方案合理的是
A.用金属铁同时提炼出铜和银
B.先用金属铜提炼出银,再用金属铁提炼出铜
C.用金属铁提炼出金属铜
D.用金属铜提炼出金属银
10.(2014年山东济宁,10题,2分)有甲、乙、丙、丁四种无色溶液,它们分别是HCl、HSO 、
2 4
BaCl 、NaCO 溶液中的一种。为区别这四种溶液,现将它们两两混合并得到下面现象:
2 2 3
溶液 甲+乙 乙+丙 丙+丁 甲+丁
现象 无明显现象 白色沉淀 白色沉淀 无色气体
[来源:学科网]
根据对上述现象的分析,可推知甲、乙、丙、丁四种溶液的顺序依次是
A.HCl 、BaCl 、HSO 、
2 2 4
NaCO
2 3
B.HSO 、HCl、BaCl 、NaCO
2 4 2 2 3
C.HCl、HSO 、BaCl 、NaCO
2 4 2 2 3
D.HSO 、NaCO、HCl、BaCl
2 4 2 3 2
第II卷(非选择题 共34分)
二、填空与简答(共17分)
11.(2014年山东济宁,11题,4分)分子、原子和离子都是构成物质的粒子。请按要求用符号
完成下面问题(每题答案不唯一,请务必写全)
(1)五氧化二磷分子中的原子 O 、 P ;
(2)氯化镁中溶液中的离子 M g 2 + 、 C l - ;
( 3 ) 化 肥 硫 酸 铵 中 的 原 子 团 N
H + 、 SO 2- ;
4 4
(4)二氧化碳溶液中的分子 H O 、 H CO ;
2 2 3
12.(2014年山东济宁,12题,4分)今年5月,吴王夫差剑重返苏州。吴王夫差剑为春秋末期
制造的青铜剑,时隔2500年,虽表面有一层蓝色薄锈,但仍寒光逼人,刃锋极锋利,堪称削铁
如泥,吹毛断发。
仔细阅读上面文字,完成下面问题:
( 1 ) 青 铜 是 金 属 材 料 中 合 金 , 其 主 要 成 分 是 Cu 、 Zn ( 填 符 号
);
(2)从文中信息可以看出,青铜具有 A 、 C ;
(3)吴王夫差剑表面的蓝色薄锈,其主要成分为碱式碳酸铜[化学式:Cu (OH) CO],这
2 2 3
层蓝色薄锈形成的可能原因是 铜与空气中的氧气、水分、二氧化碳等物质发生反应反应 。
13、(2014年山东济宁,13题,4分)用滤纸折成蝴蝶并喷洒某种溶液或试剂后,悬挂于铁架台上。另取一只盛有某未知溶液的烧杯,放在纸蝴蝶的下方(见右图)。一会儿,纸蝴蝶的颜色
发生变化,请回答:
[来源:学,科,网Z,X,X,K]
(1)若纸 蝴蝶上喷洒的是
酚酞试液,纸蝴蝶变红色,烧杯中的溶液是 浓氨水 ;
(2)若纸蝴蝶上喷洒的是石蕊试液,纸蝴蝶变红色,烧杯中的溶液是 浓盐酸 ,若纸蝴蝶
变蓝色,烧杯中的溶液是 浓氨水 ;
(3)试分析产生以上现象的原因是 浓氨水显碱性、浓盐酸显酸性,它们又都具有挥发性,
按发出来的物质能使无色酚酞试液或紫石蕊溶液变色 。
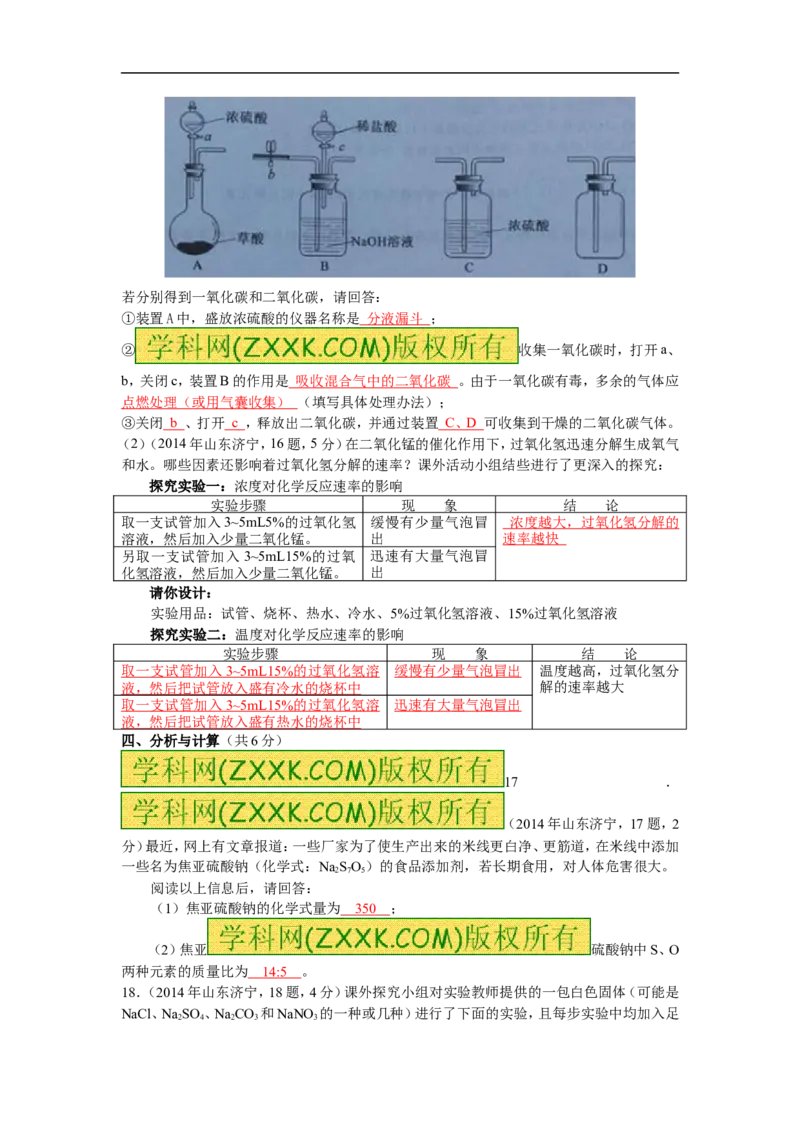
14、(2014年山东济宁,14题,4分)轻质碳酸钙广泛应用于橡胶、塑料、油漆、水性涂料以及
造纸等行业,日常生活中的牙膏也常用它作摩擦剂。目前轻质碳酸钙的生产主要是碳化法,
工艺流程见下图:
请分析轻质碳酸钙的生产流程,回答下列问题:
(1)物质B的化学式为 Ca(OH ) ;
2
(2)在A→B之间,过滤操作的目前是 将 Ca(OH ) 与水分离 ;
2
(3)在B +C→CaCO 的过
3
程中,应控制物质C的流量,原因是 CaCO + CO + H O=Ca(HCO ) (用化学方程式表示);
3 2 2 3 2
(4)生产轻质碳酸钙的方法很多请再设计一种制备方法 N aCO + CaC l =CaCO ↓ +
2 3 2 3
2 NaCl (用化学方程式表示)。
15 . ( 2014 年 山 东 济 宁 , 15 题 , 1 分 ) 近 年 , 我 国 不 少 城 市 和 地 区
雾霾天气增多,雾是水蒸气,
本身无污染,“霾”由细小颗粒物组成,主要来源是热电排放、化工生产、汽车尾气、冬季供
暖以及地面灰尘等。它侵蚀着人们的健康,严重影响着人们的生活和出行。
下面治理雾霾的措施中,可行的是 ①②④⑥ 。
三、实验与探究(共11分)
16、(1)(2014年山东济宁,16题,6分)实验室可用草酸(HC O)在浓硫酸的作用下分解制
2 2 4
浓硫酸
得一氧化碳和二氧化碳(化学方程式为:HC O CO↑+CO↑+HO)。用县的实验
2 2 4 2 2
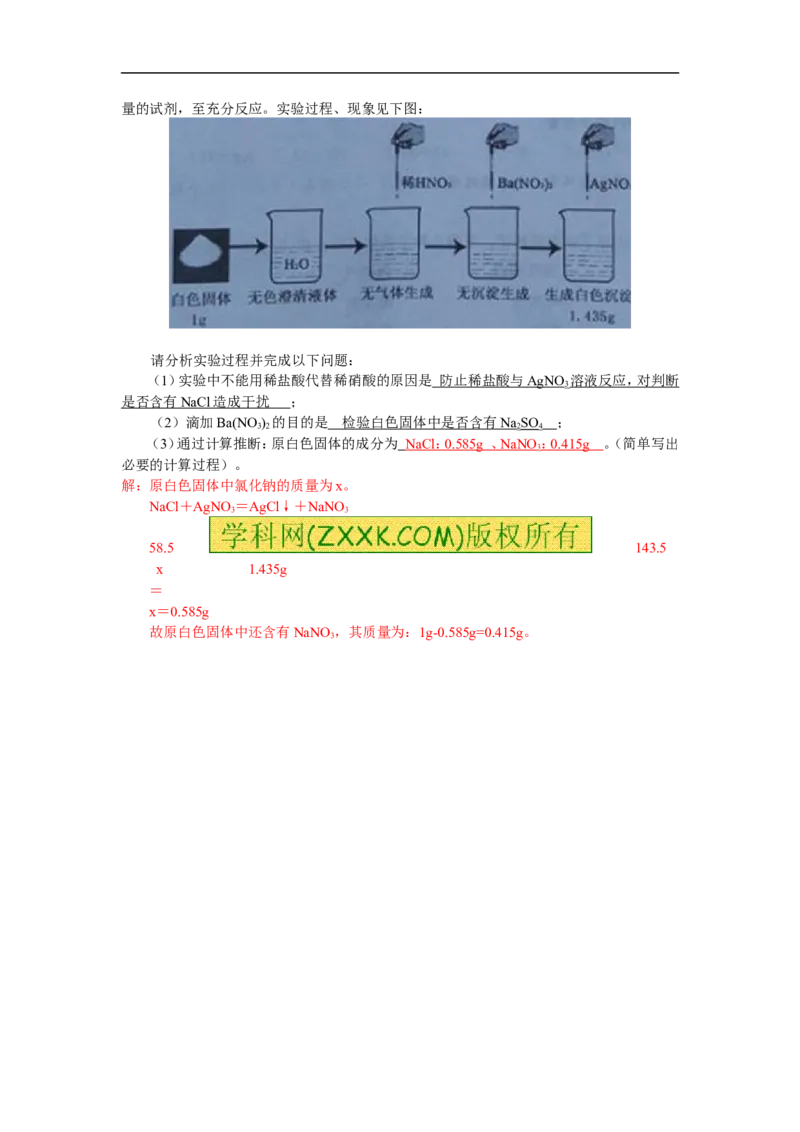
装置见下图:若分别得到一氧化碳和二氧化碳,请回答:
①装置A中,盛放浓硫酸的仪器名称是 分液漏斗 ;
② 收集一氧化碳时,打开a、
b,关闭c,装置B的作用是 吸收混合气中的二氧化碳 。由于一氧化碳有毒,多余的气体应
点燃处理(或用气囊收集) (填写具体处理办法);
③关闭 b 、打开 c ,释放出二氧化碳,并通过装置 C 、 D 可收集到干燥的二氧化碳气体。
(2)(2014年山东济宁,16题,5分)在二氧化锰的催化作用下,过氧化氢迅速分解生成氧气
和水。哪些因素还影响着过氧化氢分解的速率?课外活动小组结些进行了更深入的探究:
探究实验一:浓度对化学反应速率的影响
实验步骤 现 象 结 论
取一支试管加入3~5mL5%的过氧化氢 缓慢有少量气泡冒 浓度越大,过氧化氢分解的
溶液,然后加入少量二氧化锰。 出 速率越快
另取一支试管加入 3~5mL15%的过氧 迅速有大量气泡冒
化氢溶液,然后加入少量二氧化锰。 出 [来源:Zxxk.Com]
请你设计:
实验用品:试管、烧杯、热水、冷水、5%过氧化氢溶液、15%过氧化氢溶液
探究实验二:温度对化学反应速率的影响
实验步骤 现 象 结 论
取一支试管加入 3~5mL15% 的过氧化氢溶 缓慢有少量气泡冒出 温度越高,过氧化氢分
液,然后把试管放入盛有冷水的烧杯中 解的速率越大
取一支试管加入 3~5mL15% 的过氧化氢溶 迅速有大量气泡冒出
液,然后把试管放入盛有热水的烧杯中
四、分析与计算(共6分)
17 .
(2014年山东济宁,17题,2
分)最近,网上有文章报道:一些厂家为了使生产出来的米线更白净、更筋道,在米线中添加
一些名为焦亚硫酸钠(化学式:NaSO)的食品添加剂,若长期食用,对人体危害很大。
2 7 5
阅读以上信息后,请回答:
(1)焦亚硫酸钠的化学式量为 35 0 ;
(2)焦亚 硫酸钠中S、O
两种元素的质量比为 14: 5 。
18.(2014年山东济宁,18题,4分)课外探究小组对实验教师提供的一包白色固体(可能是
NaCl、NaSO 、NaCO 和NaNO 的一种或几种)进行了下面的实验,且每步实验中均加入足
2 4 2 3 3量的试剂,至充分反应。实验过程、现象见下图:
请分析实验过程并完成以下问题:
(1)实验中不能用稀盐酸代替稀硝酸的原因是 防止稀盐酸与 AgNO 溶液反应,对判断
3
是否含有 NaC l 造成干扰 ;
(2)滴加Ba(NO ) 的目的是 检验白色固体中是否含有 N aSO ;
3 2 2 4
(3)通过计算推断:原白色固体的成分为 NaC l : 0.585 g 、 NaNO : 0.415 g 。(简单写出
3
必要的计算过程)。
解:原白色固体中氯化钠的质量为x。
NaCl+AgNO=AgCl↓+NaNO
3 3
58.5 143.5
x 1.435g
=
x=0.585g
故原白色固体中还含有NaNO ,其质量为:1g-0.585g=0.415g。
3