文档内容
2024 年中考第二次模拟考试(徐州卷)
化 学
(考试时间:60分钟 试卷满分:60分)
注意事项:
1.答卷前,考生务必将自己的姓名、准考证号填写在答题卡上。
2.回答选择题时,选出每小题答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡
皮擦干净后,再选涂其他答案标号。写在本试卷上无效。
3.回答非选择题时,将答案写在答题卡上。写在本试卷上无效。
4.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Na-23 Mg-24 Cl-35.5 K-39
一、选择题(本大题共10小题,每小题2分,共20分。每小题给出的四个选项中,只有一个选项最符合
题目的要求)
1.下列变化属于化学变化的是
A.氢氧化钠的潮解 B.石油的分馏
C.活性炭净化水 D.熟石灰变质
【答案】D
【解析】A、氢氧化钠的潮解是吸收空气中的水蒸气,没有新物质生成,属于物理变化;
B、石油的分馏是利用各成分的沸点不同将其一一分离出来,没有新物质生成,属于物理变化;
C、活性炭净化水是利用活性炭的吸附性,除去水中的部分杂质,没有新物质生成,属于物理变化;
D、熟石灰变质是因为熟石灰和空气中的二氧化碳反应生成碳酸钙和水,有新物质生成,属于化学变
化。
故选:D。
2.《周礼》中记载沿海古人“煤饼烧蛎房(蛎房即牡蛎壳,主要成分和石灰石的主要成分相同)成
灰”,并把这种灰称为“蜃”。下列有关说法错误的是
A.较多“蜃”加入水中温度无明显变化 B.“蛎房”的主要成分是CaCO
3
C.“煤饼”的主要作用是提供高温环境 D.“蛎房成灰”的基本反应类型是分解反应
【答案】A
【解析】A、蛎房即牡蛎充,主要成分和石灰石的主要成分相同,都是碳酸钙,烧蛎房成灰时,即碳酸
钙高温分解生成氧化钙和二氧化碳,灰称为“蜃”,即为氧化钙,氧化钙和水反应生成氢氧化钙,该
反应放出大量热,所以较多“蜃”加入水中温度升高,故A说法错误;
B、石灰石的主要成分是碳酸钙,蛎房即牡蛎充,主要成分和石灰石的主要成分相同,都是碳酸钙,故
B说法正确;
C、“煤饼”的主要作用是提供高温环境 ,为碳酸钙分解提供高温环境,故C说法正确;
D、“蛎房成灰”,即碳酸钙高温分解生成氧化钙和二氧化碳,该反应符合“一变多”的特点,属于分
解反应,故D说法正确;故选:A。
3.盐水洗鼻法是防治感冒的手段之一,某同学用50.0g水配制0.9%的洗鼻液(NaCl溶液),以下关于该
溶液配制的说法正确的是
A.需称取NaCl的质量为4.5g
B.用100mL量筒量取50mL水
C.溶解时玻璃棒作用是加速溶解
D.装瓶时溶液洒落会导致浓度偏低
【答案】C
【解析】A、用50.0g水配制0.9%的氯化钠溶液,设需要氯化钠的质量为x,则 ,
x=0.45g,说法错误;
B、选择量筒遵循大而近的原则,用50mL量筒量取50mL水,说法错误;
C、溶解时玻璃棒作用是搅拌,加速溶解,说法正确;
D、溶液具有均一性,装瓶时溶液有部分溅出,不影响所配制的溶液溶质质量分数,说法错误。
故选C。
4.我国科学家成功实现了用CO 和CH 合成醋酸,其反应的微观示意图如下。下列说法错误的是
2 4
A.反应物、生成物均含有机物 B.反应中的最小微粒是原子
C.醋酸可使紫色石蕊溶液变成红色 D.醋酸的化学式为C HO
2 3 2
【答案】D
【分析】由图可知,该反应为甲烷和二氧化碳在催化剂的作用下转化为醋酸,该反应的化学方程式
为: 。
【解析】A、由分析可知,反应物为二氧化碳和甲烷,其中二氧化碳为无机物,甲烷为有机物,生成物
为醋酸,其为有机物,说法正确,不符合题意;
B、在化学反应中分子可分,原子不可分,故反应中的最小微粒是原子,说法正确,不符合题意;
C、醋酸是酸,其溶液显酸性,可使紫色石蕊溶液变红色,说法正确,不符合题意;
D、根据分析可知,醋酸的化学式为C HO,说法错误,符合题意;
2 4 2
故选D。
5.下列有关物质性质与用途的说法不正确的是
A.活性炭可用于净水,利用其具有吸附性
B.水可以灭火,利用水可以降低可燃物的着火点
C.石墨可以做电极,利用石墨具有导电性
D.熟石灰可以中和酸性土壤,利用熟石灰呈碱性【答案】B
【解析】A、活性炭具有吸附性,可以吸附水中的色素和异味,因此可用活性炭来净化水,故说法正
确;
B、水可以灭火,利用水可以降低可燃物的温度至着火点以下,故说法错误;
C、石墨可以做电极,利用石墨具有导电性,故说法正确;
D、熟石灰可以中和酸性土壤,利用熟石灰呈碱性,故说法正确。
故选B。
6. 和NaCl的溶解度曲线如图所示,下列说法正确的是
A. 的溶解度为36.2g
B. ℃时,NaCl和 溶液的质量分数相等
C. ℃时18g 加入到50g水中充分溶解,降温到 ℃析出10g晶体
D.若NaCl中混有少量 ,可采取降温结晶的方法提纯得到NaCl
【答案】C
【解析】A、没有指明是何种温度下碳酸钠的溶解度,无法判断,故A不正确;
B、t ℃时,NaCl和NaCO 饱和溶液的溶质质量分数相等,未说明溶液状态,无法确定,故B不正
2 2 3
确;
C、t℃时,碳酸钠的溶解度是36.2g,所以50g水中能溶解18.1g碳酸钠固体,t℃时,碳酸钠的溶解度
2 1
是16g,所以50g水中能溶解8g碳酸钠固体,故降温到 t ℃析出10g晶体,故C正确;
1
D、因为氯化钠的溶解度受温度的影响较小,所以若NaCl中混有少量NaCO,可采取蒸发结晶的方法
2 3
提纯得到NaCl,故D不正确。
故选C。
7.下列客观事实的微观解释正确的是
选
客观事实 微观解释
项
A 水通电生成氢气和氧气 水由氢分子和氧分子构成
B 酸碱盐溶液都能导电 因为酸碱盐都由离子构成
C 酸具有相似的化学性质 酸溶液中都含有酸根离子D Na、Na+化学性质不同 微粒中最外层电子数不同
【答案】D
【解析】A、水通电生成氢气和氧气,是因为水分子分成了氢原子和氧原子,然后氢原子、氧原子分别
重新组合形成氢分子、氧分子,水中不含氢分子和氧分子,故选项解释错误;
B、溶液能导电的原因是物质在溶解的过程中会形成能自由移动的离子,酸碱盐溶液都能导电,是因为
酸碱盐溶液中都存在能自由移动的离子,故选项解释错误;
C、酸具有相似的化学性质,是因为酸溶液中都含有氢离子,故选项解释错误;
D、Na、Na+化学性质不同,是因为微粒中最外层电子数不同,故选项解释正确。
故选D。
8.唐宋时期人们已能从柿子中提取具有利尿功效的甘露醇,其化学式为C H O。下列说法正确的是
6 14 6
A.甘露醇中氢元素的质量分数最高 B.甘露醇与碳酸所含元素种类相同
C.甘露醇中C、O元素质量比为1:1 D.甘露醇完全燃烧会生成有毒气体
【答案】B
【解析】A、甘露醇中C、H、O元素的质量比为: ,氧元素的质量分数最
高,不符合题意;
B、碳酸的化学式为:HCO,由化学式可知,碳酸和甘露醇均是由C、H、O三种元素组成,符合题
2 3
意;
C、甘露醇中C、O元素的质量比为: ,不符合题意;
D、根据质量守恒定律,化学反应前后,元素的种类不变,甘露醇由C、H、O三种元素组成,故甘露
醇完全燃烧生成二氧化碳和水,不会生成有毒气体,不符合题意。
故选B。
9.分离、检验、鉴别、除杂是最基本的实验技能,下列实验设计能达到实验目的的是
选项 实验目的 实验设计
A 除去二氧化锰中的氯化钾 加水溶解、过滤、蒸发、结晶
B 除去N 中混有的少量O 将气体缓缓通过足量的灼热铜网
2 2
C 检验NaCO 溶液中混有的NaSO 取样、滴加BaCl 溶液,观察现象
2 3 2 4 2
D 分离CaO和CaCO 的固体混合物 加适量水溶解、过滤、洗涤固体并烘干
3
【答案】B
【解析】A、KCl易溶于水,MnO 难溶于水,可采取加水溶解、过滤、洗涤、干燥的方法进行分离除
2
杂,故选项不能达到实验目的;
B、将混合气体通过足量灼热铜网,N 不与铜反应,Cu与O 加热能发生反应生成CuO固体,符合除杂
2 2
原则,故选项能达到实验目的;
C、碳酸钠和氯化钡反应生成碳酸钡沉淀和氯化钠,硫酸钠和氯化钡反应生成硫酸钡沉淀和氯化钠,取
样,滴加BaCl 溶液,碳酸钠和硫酸钠均会与氯化钡反应产生白色沉淀,故选项不能达到实验目的;
2D、CaO和CaCO 的固体混合物加水后CaO与HO反应发生反应产生Ca(OH),原物质被消耗,不
3 2 2
能达到分离目的,故选项不能达到实验目的;
故选:B。
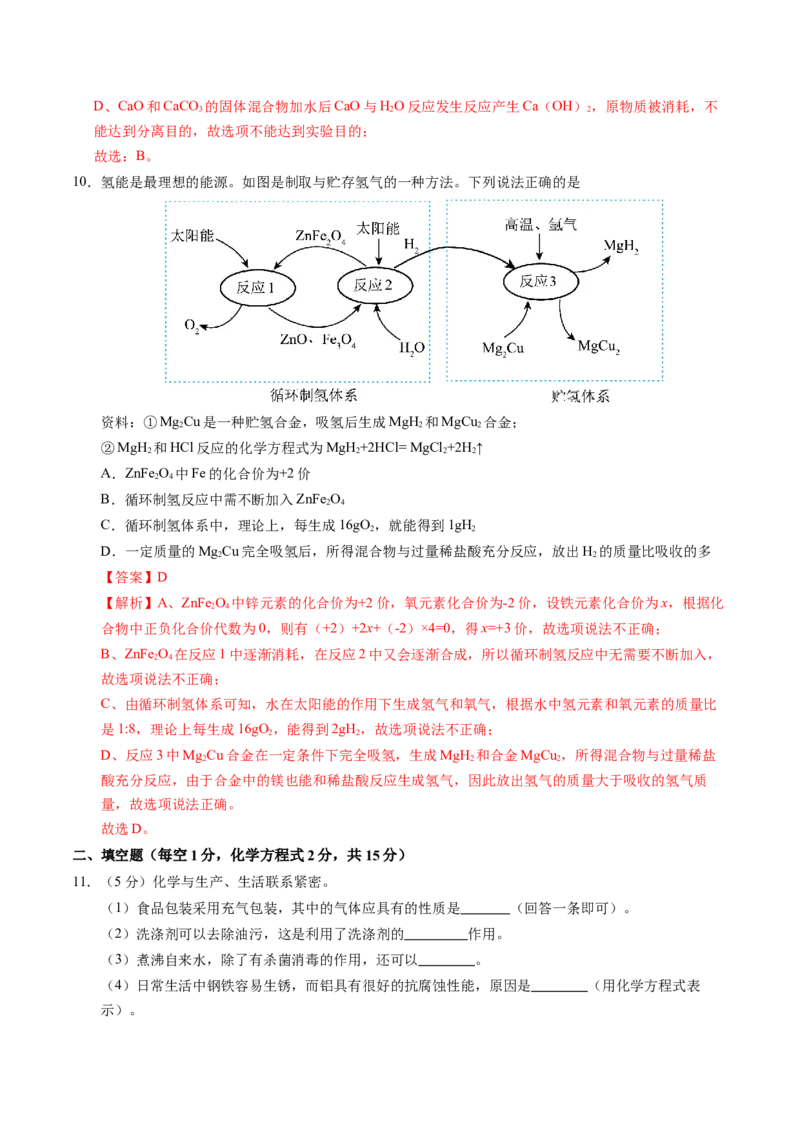
10.氢能是最理想的能源。如图是制取与贮存氢气的一种方法。下列说法正确的是
资料:①MgCu是一种贮氢合金,吸氢后生成MgH 和MgCu 合金;
2 2 2
②MgH 和HCl反应的化学方程式为MgH +2HCl= MgCl +2H ↑
2 2 2 2
A.ZnFe O 中Fe的化合价为+2价
2 4
B.循环制氢反应中需不断加入ZnFe O
2 4
C.循环制氢体系中,理论上,每生成16gO,就能得到1gH
2 2
D.一定质量的MgCu完全吸氢后,所得混合物与过量稀盐酸充分反应,放出H 的质量比吸收的多
2 2
【答案】D
【解析】A、ZnFe O 中锌元素的化合价为+2价,氧元素化合价为-2价,设铁元素化合价为x,根据化
2 4
合物中正负化合价代数为0,则有(+2)+2x+(-2)×4=0,得x=+3价,故选项说法不正确;
B、ZnFe O 在反应1中逐渐消耗,在反应2中又会逐渐合成,所以循环制氢反应中无需要不断加入,
2 4
故选项说法不正确;
C、由循环制氢体系可知,水在太阳能的作用下生成氢气和氧气,根据水中氢元素和氧元素的质量比
是1:8,理论上每生成16gO,能得到2gH,故选项说法不正确;
2 2
D、反应3中MgCu合金在一定条件下完全吸氢,生成MgH 和合金MgCu ,所得混合物与过量稀盐
2 2 2
酸充分反应,由于合金中的镁也能和稀盐酸反应生成氢气,因此放出氢气的质量大于吸收的氢气质
量,故选项说法正确。
故选D。
二、填空题(每空1分,化学方程式2分,共15分)
11.(5分)化学与生产、生活联系紧密。
(1)食品包装采用充气包装,其中的气体应具有的性质是 (回答一条即可)。
(2)洗涤剂可以去除油污,这是利用了洗涤剂的 作用。
(3)煮沸自来水,除了有杀菌消毒的作用,还可以 。
(4)日常生活中钢铁容易生锈,而铝具有很好的抗腐蚀性能,原因是 (用化学方程式表
示)。【答案】(1)无毒或化学性质稳定
(2)乳化
(3) 降低水的硬度
(4) 4Al+3O =2Al O
2 2 3
【解析】(1)食品包装采用充气包装,其中的气体应具有无毒、化学性质稳定的性质;
(2)洗涤剂可以去除油污,这是利用了洗涤剂对油污的乳化作用;
(3)自来水煮沸后有较多水垢出现,推测自来水为硬水,可在自来水中加入肥皂水进行检验,煮沸
自来水,除了有杀菌消毒的作用,还可以降低水的硬度;
(4)日常生活中钢铁容易生锈,铁生锈是因为铁与HO、O 同时接触而导致;铝具有很好的抗腐蚀
2 2
性能,是因为铝在空气中与氧气反应,其表面生成一层致密的氧化铝薄膜,从而阻止铝进一步被氧化,
化学方程式为4Al+3O =2Al O。
2 2 3
12.某品牌新能源电动汽车使用磷酸铁锂电池,该电池具有容量大、续航能力强的特点,其反应原理为:
。
(1)推广新能源汽车可减少因燃烧化石燃料造成的酸雨,酸雨指pH< 的雨水。
(2)该电池充电时发生的化学反应属于 (填基本反应类型);放电时电池将
能转化为电能。
(3)LiFePO 中铁元素与氧元素的质量比为 。
4
(4)某些电动汽车的蓄电池是铅酸电池,报废后要回收处理的原因是 。
【答案】(1)5.6
(2) 分解反应 化学
(3)7:8
(4)防止污染土壤和水源
【解析】(1)雨水呈弱酸性,酸雨是指pH<5.6的雨水。
(2)该电池充电时发生的反应由一种物质生成了两种物质,该反应属于分解反应。放电时,电池将
化学能转化电能。
(3)LiFePO 中铁元素与氧元素的质量比为56:(16×4)=7:8。
4
(4)铅酸电池含有的汞、镉等重金属和酸性废液会污染土壤和水源,所以某些电动汽车的蓄电池报
废后要回收处理。
13.钛和钛合金被认为是21世纪的重要金属材料,被广泛应用于航天、医疗等领域。工业上以金红石(主
要成分为TiO)为原料生产钛金属的工艺流程如图所示。
2
(1)金红石属于 (选填“纯净物”或“混合物”)。
(2)反应①的化学方程式为 。(3)反应②的基本反应类型是 。
(4)制造航天飞机常用钛合金材料,是因为钛合金具有很多优良性能,如 (写出一点即
可)。
【答案】(1)混合物
(2)
(3)置换反应
(4)硬度大(或抗腐蚀性强、密度小等,合理即可)
【解析】(1)金红石主要成分为TiO,此外还含有其它杂质,属于混合物;
2
(2)由流程图可知,反应①为二氧化钛、氯气和碳在高温下反应生成四氯化钛和一氧化碳,反应的
化学方程式为 。
(3)反应②为四氯化钛和镁在高温、隔绝氧气条件下反应生成钛和氯化镁,该反应是一种单质和化
合物生成另外一种单质和化合物的反应,属于置换反应;
(4)合金具有硬度大、抗腐蚀性好等优点;钛合金具备很多优良性能,如耐高温(硬度大、耐腐
蚀、密度小等)。
三、实验与探究题(每空1分,化学方程式2分,共25分)
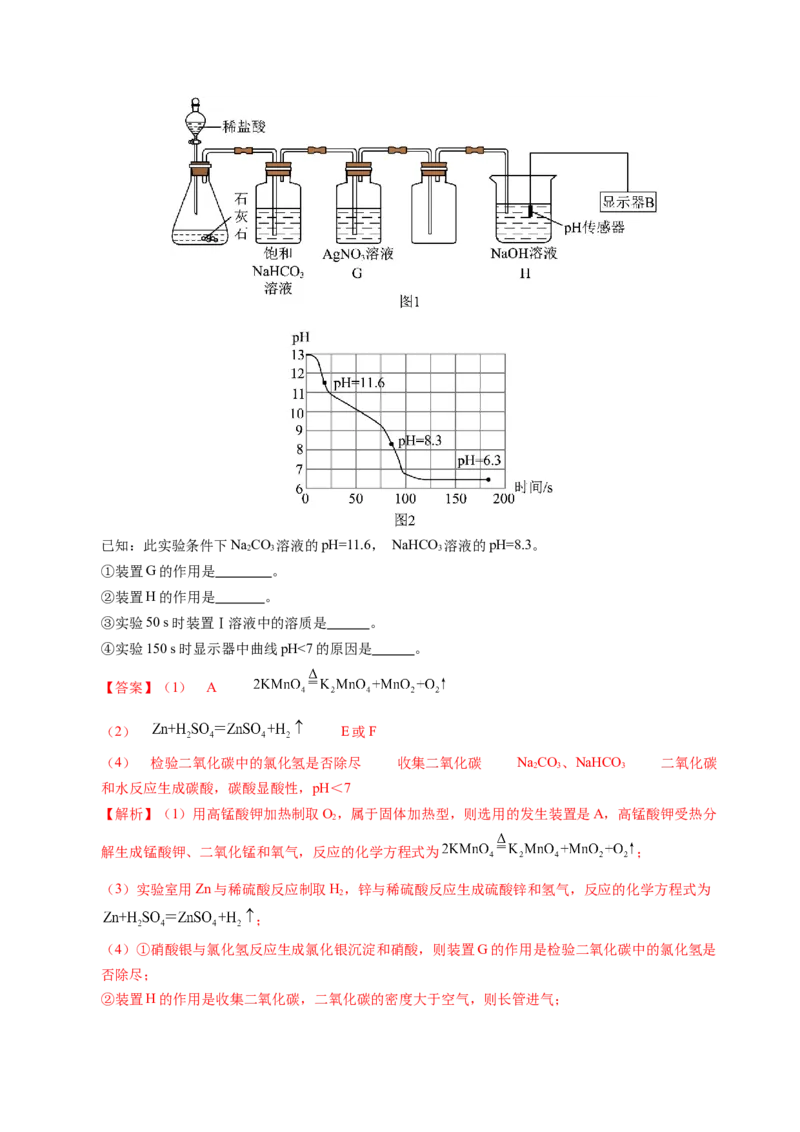
14.(10分)结合下图回答问题。
(1)用高锰酸钾制取O,选用的发生装置是 (填序号)。反应的化学方程式为 。
2
(2)实验室用Zn与稀硫酸反应制取H,反应的化学方程式为 ,收集装置可选择 。
2
(3)用图1装置制取CO 并探究其性质。图2表示装置Ⅰ中溶液的pH与实验时间的变化关系曲线。
2已知:此实验条件下NaCO 溶液的pH=11.6, NaHCO 溶液的pH=8.3。
2 3 3
①装置G的作用是 。
②装置H的作用是 。
③实验50 s时装置Ⅰ溶液中的溶质是 。
④实验150 s时显示器中曲线pH<7的原因是 。
【答案】(1) A
(2) E或F
(4) 检验二氧化碳中的氯化氢是否除尽 收集二氧化碳 NaCO、NaHCO 二氧化碳
2 3 3
和水反应生成碳酸,碳酸显酸性,pH<7
【解析】(1)用高锰酸钾加热制取O,属于固体加热型,则选用的发生装置是A,高锰酸钾受热分
2
解生成锰酸钾、二氧化锰和氧气,反应的化学方程式为 ;
(3)实验室用Zn与稀硫酸反应制取H,锌与稀硫酸反应生成硫酸锌和氢气,反应的化学方程式为
2
;
(4)①硝酸银与氯化氢反应生成氯化银沉淀和硝酸,则装置G的作用是检验二氧化碳中的氯化氢是
否除尽;
②装置H的作用是收集二氧化碳,二氧化碳的密度大于空气,则长管进气;③分析图像信息可知,50s时溶液的pH=10,实验条件下碳酸钠溶液的pH≈11.6,碳酸氢钠溶液的
pH≈8.3,则实验50s时装置H溶液中的溶质是NaCO、NaHCO ;
2 3 3
④实验150s时氢氧化钠已反应完,二氧化碳和水反应生成碳酸,碳酸显酸性,pH<7。
15.(15分)纯碱是一种重要的化工原料,广泛用于玻璃、造纸、纺织和洗涤剂的生产。某化学兴趣小组
对纯碱的制备、性质及用途等开展项目式学习。
任务一:了解纯碱的制备——“侯氏制碱法”
“侯氏制碱法”主要化学原理是利用饱和氯化钠溶液吸收两种气体,生成碳酸氢钠和氯化铵( NH Cl
4
),再加热碳酸氢钠即可制得纯碱。
(1)纯碱属于 (填“酸”“碱”或“盐”)。
(2)饱和氯化钠溶液吸收的两种气体是 (填字母序号)。
A.Cl B.NH C.SO D.CO
2 3 2 2
任务二:探究纯碱的性质——NaCO 溶液呈碱性
2 3
【查阅资料】①溶液呈碱性,是因为溶液中存在较多的 。②NaCO 在水中全部解离出 和
2 3
。 ③CaCl 溶液呈中性, 、 对溶液的酸碱性没有影响。
2
【提出猜想】
(3)猜想一:HO单独起作用,产生较多的 ,使溶液呈碱性。
2
猜想二: 与HO作用,产生较多的 ,使溶液呈碱性。
2
猜想三: 。
【实验探究】
(4)
实验操作 实验现象 实验结论
(1)向试管中加入一定量的蒸馏水,滴入2滴酚酞溶 猜想一不成
溶液无明显变化
液 立
(2)向试管中加入一定量的NaCl溶液,滴入2滴酚 猜想二不成
溶液无明显变化
酞溶液 立
(3)①向试管中加入一定量的NaCO 溶液,滴入2 ①
2 3
滴酚酞溶液 ②有白色沉淀生成溶液由红 猜想三成立
②往①所得溶液中逐滴加入CaCl 溶液至过量 色变无色
2
【交流与讨论】
(5)实验操作(3)中加入CaCl 溶液至过量后,溶液由红色变为无色的原因是 (用化学
2
方程式解释);
【解释与结论】同学们和老师交流,得知 和HO作用,产生较多的 和另一种阴离子。
2
【拓展与延伸】(6)结合任务二的所有信息和结论,运用初中化学所学知识,经过分析推理可得出:NaCO 溶液中
2 3
含有的阴离子是 、 、 。
任务三:探究市售纯碱样品成分。市售纯碱主要成分是碳酸钠,还含少量氧化钠等杂质。
已知:①部分银盐的溶解性如下表:
Ag+ 溶 不 不
②氯化银不溶于稀硝酸。
验证样品中含有氯化钠 实验Ⅰ、取纯碱样品,加水溶解得溶液X,测得溶液pH约为12。
实验Ⅱ、取溶液X,滴加过量试剂Y,产生能使澄清石灰水变浑浊的气体。
实验Ⅲ、向实验Ⅱ后所得溶液中滴加硝酸银溶液,有白色沉淀生成。
结论:样品中含有氯化钠。
(7)测定溶液pH的操作:用玻璃棒蘸取溶液滴在pH试纸上,与 相比较。
(8)实验Ⅱ中所加的试剂Y应选用 (填字母)。
a.稀盐酸 b.稀硝酸 c.氢氧化钠溶液 d.氯化钙溶液
任务四:测定样品中碳酸钠含量
准确称取2g干燥纯碱样品,加水溶解,逐滴加入溶质质量分数为3.65%的稀盐酸,边滴加边搅拌,当
两者恰好完全反应时(含碳物质全部转化为CO ),消耗盐酸体积为37.00mL。(该盐酸的密度近似
2
等于1g/mL,杂质不与盐酸反应)
无水碳酸钠等级规定如下:
优等品 一等 合格品
碳酸钠质量分数 ≥99.2% ≥98.8% ≥98.0%
(9)通过计算判断该纯碱样品的等级 (写出计算过程)(5分)。
【答案】(1)盐
(2)BD
(3)碳酸根离子( )和水作用,产生较多的OH-,使溶液呈碱性
(4)溶液变红色
(5)NaCO+CaCl =CaCO ↓+2NaCl;
2 3 2 3
(6) OH-或 或OH-(与前一空对应,不能写成相同)
(7)标准比色卡
(8)b
(9)消耗氯化氢的质量=1g/ml×37.00ml×3.65%=1.3505g;
设纯碱中碳酸钠的质量为x;x=1.961g
纯碱中碳酸钠的质量分数= ;
根据表格知,该纯碱样品的等级为合格品。
答:该纯碱样品的等级为合格品。
【解析】(1)纯碱是碳酸钠的俗称,碳酸钠是由钠离子和碳酸根离子组成的化合物,属于盐;
(2)氯化钠溶液吸收两种气体生成碳酸氢钠和氯化铵,根据质量守恒定律知,化学变化前后元素种
类不变,生成物中多出了氮元素、碳元素,故吸收的两种气体中一定含有氮元素和碳元素,故选
BD;
(3)碳酸钠在水中全部电离生成钠离子和碳酸根离子,则猜想三为碳酸根离子( )和水作用,
产生较多的OH-,使溶液呈碱性;
(4)猜想三成立,则是碳酸根离子和水作用,产生较多的OH-,向试管中加入一定量的NaCO 溶液
2 3
滴入2滴酚酞溶液,由于碳酸钠溶液呈碱性,加入酚酞后溶液变红,继续滴加入CaCl 溶液,氯化钙
2
会与碳酸钠反应生成碳酸钙沉淀和氯化钠,则现象为产生白色沉淀,溶液红色消失。
(5)实验操作(3)中加入CaCl 溶液至过量后,氯化钙与碳酸钠反应生成碳酸钙沉淀和氯化钠,碳
2
酸钠完全消耗,碱性消失,反应的化学方程式为:NaCO+CaCl =CaCO ↓+2NaCl;
2 3 2 3
(6)由题目信息知,碳酸根和水作用,产生较多的氢氧根和另一种阴离子,根据所学知识,另一种
阴离子为碳酸氢根,故推理可得出:NaCO 溶液中含有的阴离子是 、OH-、 ;
2 3
(7)测溶液的pH时,应用玻璃棒待测溶液滴到试纸上,再与标准比色卡对比;
(8)取纯碱样品,加水溶解,滴加过量试剂Y,产生能使澄清石灰水变浑浊的气体,则气体为二氧化
碳,发生的反应为碳酸钠和酸反应,为避免对氯离子的检验的干扰,不能用盐酸,用稀硝酸。
故选b。
(9)见答案。