文档内容
2026届高三年级上学期期末质量检测
化 学
本试卷共8页,共19题。满分100分,考试用时75分钟。
注意事项:
1.答题前,考生务必将自己的姓名、准考证号填写在答题卡指定位置。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑。
如需改动,用橡皮擦擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题
卡上。写在本试卷上无效。
3.考试结束,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H1 C12 016 Na 23
一、选择题:本题共15小题,每小题3分,共45分。在每小题给出的四个选项中,只有一项
是符合题目要求的。
1.2025年九三阅兵展示了我国多种高科技材料。下列材料中属于金属材料的是
A.战机发动机的钛合金部件 B.卫星通信车的碳纤维复合材料
C.地面装备传动系统的氮化硅陶瓷 D.柔性电路基材的聚酰亚胺薄膜
2.化学与生活息息相关。下列物质不能用作净水混凝剂的是
A.硫酸亚铁 B.硫酸铝 C.聚合氯化铝 D.硫酸铜
3.一种用于合成染料和药物的中间体结构如图,下列说法正确的是
CH,o—NHCOCH,
A.有3种官能团
B.有1个手性碳原子
C.名称为对甲氧基乙酰苯胺
D.可与4 mol H?发生加成反应
4.在电解氯化铜溶液的实验中,未涉及下列图标的操作或警示的是
A. B. C. D.
5.化学用语是学好化学的基石。下列化学用语表述正确的是
N::
A.N?H?的电子式:
B.N?O的中心原子杂化轨道示意图:
高三年级化学试卷 第1页 共8页C.氨气和水形成的占比最大的氢键示意图:
D.Mg?N?的水解方程式:Mg?N?+6H?O—3Mg(OH)?+2NH?↑
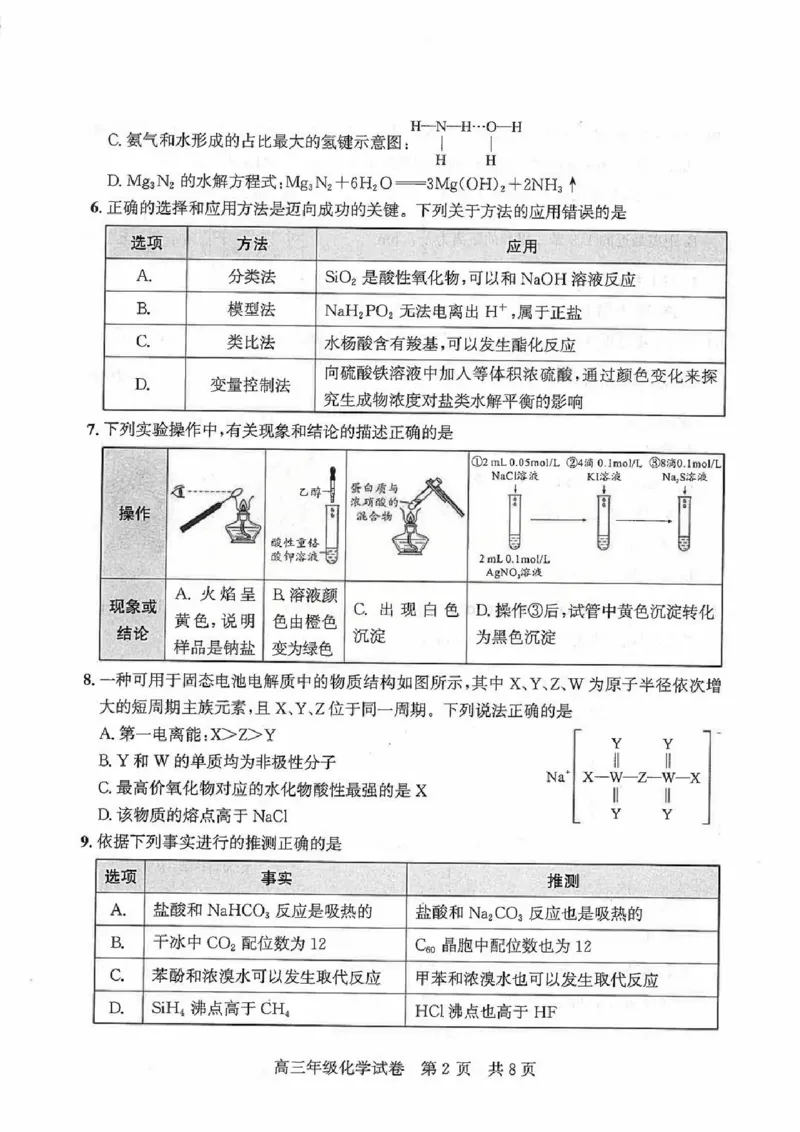
6.正确的选择和应用方法是迈向成功的关键。下列关于方法的应用错误的是
选项 方法 应用
A.
分类法 SiO?是酸性氧化物,可以和NaOH溶液反应
B.
模型法 NaH?PO?无法电离出H+,属于正盐
C.
类比法 水杨酸含有羧基,可以发生酯化反应
向硫酸铁溶液中加入等体积浓硫酸,通过颜色变化来探
D.
变量控制法
究生成物浓度对盐类水解平衡的影响
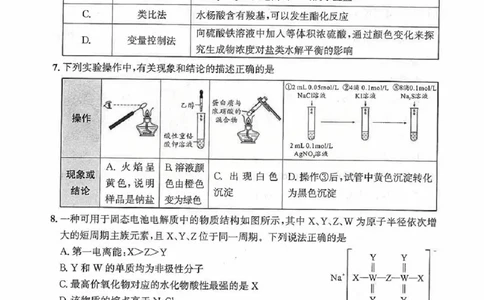
7.下列实验操作中,有关现象和结论的描述正确的是
①2mL0.05mol/L ②4滴0.1mol/L③8滴0.1mol/L
NaCl溶液 KI溶液 Na,S溶液
重 乙醇- 蛋白质与 燃
浓硝酸的 8 日
操作
混合物 A
酸性重铬
酸钾溶波臣 2mL0.1mol/L
AgNO,溶液
A.火焰呈 B溶液颜
现象或 C.出现白色 D.操作③后,试管中黄色沉淀转化
黄色,说明 色由橙色
结论 沉淀 为黑色沉淀
样品是钠盐 变为绿色
8.一种可用于固态电池电解质中的物质结构如图所示,其中X,Y、Z、W为原子半径依次增
4+
大的短周期主族元素,且X、Y、Z位于同一周期。下列说法正确的是
A.第一电离能:X>Z>Y
B.Y和W的单质均为非极性分子
C.最高价氧化物对应的水化物酸性最强的是X
D.该物质的熔点高于NaCl
9.依据下列事实进行的推测正确的是
选项 事实 推测
A. 盐酸和NaHCO?反应是吸热的 盐酸和Na?CO?反应也是吸热的
B.
干冰中CO?配位数为12 C?o晶胞中配位数也为12
C.
苯酚和浓溴水可以发生取代反应 甲苯和浓溴水也可以发生取代反应
D. SiH?沸点高于CH? HCl沸点也高于HF
高三年级化学试卷 第2页 共8页-
10.MOFs材料具有无机材料的刚性和有机材料的柔性特征,可用于存储甲烷和氢气等燃料
气。一种MOFs材料的晶胞结构如图,晶胞参数为a pm。下列说法错误的是
A.基态Zn原子的价电子排布式为3d1?4s2 O A
2a pm o锌簇[OZn.]
点
Q
bo
B.距离最近的1,3-苯二甲酸的距离为 Qi O ● 1,3-苯二甲酸
6 9
C.与1个锌簇等距且最近的1,3-苯二甲酸有4个
D.该材料存储甲烷和氢气是通过范德华力实现的
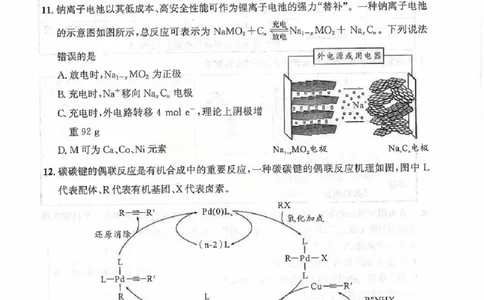
11.钠离子电池以其低成本、高安全性能可作为锂离子电池的强力“替补”。一种钠离子电池
的示意图如图所示,总反应可表示为NaMO?+c。Na-MO?+Na?C。下列说法
错误的是 外电源或用电器
A.放电时,Na-MO?为正极
B.充电时,Na+移向Na?C,电极
f86
C.充电时,外电路转移4 mol e,理论上阴极增
重92g
D.M可为Ca、Co、Ni元素 NaMO?电极 Na,C,电极
12.碳碳键的偶联反应是有机合成中的重要反应,一种碳碳键的偶联反应机理如图,图中L
代表配体、R代表有机基团、X代表卤素。
RX
R-=R′
Pd(0)L =
氧化加成
还原消除
L
(n-2)L
R—Pd一X F7
L1
L
RR'
Cu-
Cux
下列说法错误的是
A.PdL。是该反应的催化剂
B.R"N在反应中起到了碱的作用
C.整个过程中Pd的化合价发生了变化
D.若用 R'C=CR′代替 HC=CR′,也会生成 R'C=CR
高三年级化学试卷 第3页 共8页13.如图所示的物质转化关系中,其中有机物I(M=30g·mol?1)的核磁共振氢谱显示为一
组峰,K为金属单质,J既可以和酸、也可以和碱反应。下列说法错误的是
A.G和J为离子化合物 E
G
J
B.E和F相互滴加现象不同 F
O2. K
C.常温下,J的水溶液pH<7 H 1
D.每生成-1 mol K,转移2 mole
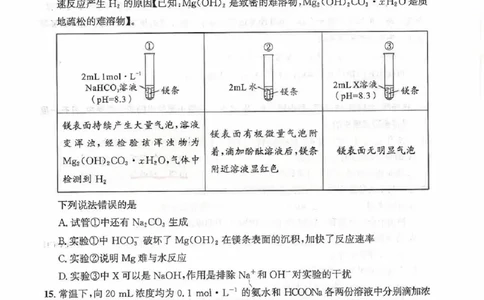
14.室温下,用质量和表面积均相同的镁条(已用砂纸打磨),探究Mg与NaHCO?溶液能快
速反应产生H?的原因【已知:Mg(OH)?是致密的难溶物,Mg?(OH)?CO?·xH?O是质
地疏松的难溶物】。
① ② ③
2mL1mol·L?1
NaHCO?溶液 2mL水 2mLX溶液、
镁条 镁条 镁条
(pH=8.3)
(pH=8.3)
镁表面持续产生大量气泡,溶液
镁表面有极微量气泡附
变浑浊,经检验该浑浊物为
着,滴加酚酞溶液后,镁条 镁表面无明显气泡
Mg?(OH)?CO?·xH?O,气体中
附近溶液显红色
检测到H?
下列说法错误的是
A.试管①中还有Na?CO?生成
B.实验①中HCO?破坏了Mg(OH)?在镁条表面的沉积,加快了反应速率
C.实验②说明Mg难与水反应
D.实验③中X可以是NaOH,作用是排除Na+和OH?对实验的干扰
15.常温下,向20 mL浓度均为0.1mol·L?1的氨水和HCOONa各两份溶液中分别滴加浓
度均为0.1 mol·L?1的NH?Cl溶液和HCOOH溶液, HCOOH溶液V/mL
a
11.12
-lgc水(H+)随加入溶液体积的变化如图所示【c水(H+)表
b
((HH))
示由水电离的氢离子浓度】。下列说法中正确的是 7 C
一一11ggGG
A.NH?·H?O的K。为10-4-76 d
N
B.N点处b、d曲线的溶质恰好相同
0 20 V/mL
C.c曲线恰为中性时,V>20mL
NH?Cl溶液V/mL
D.V=40mL时,d曲线中存在c(NH)+c(H+)=c(HCOO-)+c(OH-)
高三年级化学试卷 第4页 共8页二、非选择题,本题共4小题,共55分。
16.(14分)
钼镍催化剂是石油裂解工业的重要催化剂,其通常使用Al?O?作为催化剂载体。从废弃
钼镍催化剂中回收钼元素与镍元素的工艺流程如下图所示。
①H?SO?
②75℃H?S(g)
提纯MoS,
沉钼
H?SO、HF、NaOH
H?O? (pH≈5.5) NaOH 废液1
废弃钼镍
焙烧 酸浸 调pH 调pH? ①HCI、
催化剂
②NH?·H?O、
H?O?
滤渣 ③Na?S
NiSO
洗渣 沉淀转化
已知:
废液2
①25℃时,K?[Ni(OH)?]=2×10?1?,lg2=0.3;
②pH>6时,钼元素常以MoO?形式存在;
③加沉淀剂使一种金属离子浓度小于等于10??mol·L?1,即认为沉淀完全。
回答下列问题:
(1)“焙烧”的目的是除去固态碳沉积物和_____。
(2)已知F的配位能力极强,滤渣主要成分的晶体结构中阴阳离子之比为1:3,其化学
式为________。
(3)“调pH?”后的过滤操作选用漏斗的材质可为_______(填标号)。
①塑料 ②铁 ③陶瓷
(4)“调pH?”中控制溶液的pH范围为_____。
(5)“沉钼”中②的离子方程式为______。
(6)“沉淀转化”中发生的化学方程式为______。
(7)“废液1”与“废液2”可先混合再处理,这样操作比直接分别处理的优势是______。
17.(13分)
某研究小组探究硫酸铜溶液与硫化钠溶液反应的产物。
实验 实验操作 实验现象
向2 mL0.02 mol·L?1 CuSO?溶液中加入
工
立即产生黑色沉淀
2 mL0.02 mol·L?1 Na?S溶液
向2mL饱和CuSO?溶液中加入2mL饱和
Ⅱ
产生棕黑色沉淀
Na?S溶液
Ⅲ
向I的上层清液滴加浓氨水 无明显现象
IV 溶液显浅蓝色,放置一段时间
向Ⅱ的上层清液滴加浓氨水
后溶液蓝色加深
高三年级化学试卷 第5页 共8页已知:CuS、Cu?S均为黑色沉淀;Cu?S可溶于浓氨水形成无色的[Cu(NH?)?]+,在空气
中易被氧化为[Cu(NH?)?]2+。
回答下列问题:
(1)实验Ⅲ的现象说明了实验I中发生了____反应(选填“氧化还原”或“复分解”)。
(2)实验IV中溶液蓝色加深的离子方程式为_____。
(3)为探究实验Ⅱ棕黑色沉淀的成分,取洗涤后的棕黑色沉淀进行如下实验操作:
试剂X白色沉淀稀盐酸。沉淀溶解稀硝酸
上层清液- 白色沉淀
浓NaOH
棕黑色溶液,加热
沉淀 稀硫酸
离心分离 无现象
均分三份
稀硫酸
有气泡生成,溶液变蓝
H?O?
仔细观边缘有红色固体
蔡颜色 ________。
①通过“白色沉淀”判断上层清液中SO2,则试剂X是___。
②棕黑色沉淀在NaOH溶液中部分溶解的化学方程式为_
(4)结合以上实验,得出结论:实验Ⅱ中棕黑色沉淀成分为_____ _(填化学式)。
(5)某小组设计如下原电池.装置,研究pH对反应的影响:
向Na?S溶液中滴加NaOH溶液,测得电压升高,从化 盐桥
学平衡角度解释原因为___。
石墨 石墨
(6)综合上述实验可知:影响硫酸铜溶液与硫化钠溶液反
应的产物的因素有____。
饱和CuSO?饱和Na?S
18.(14分)
溶液 溶液
一种可用于治疗类风湿性关节炎的药物重要中间体H的合成路线如图。
+
>D=0
L
NF
Boc
F UH
高三年级化学试卷 第6页 共8页已知:Boc-NH?结构式:
回答下列问题:
(1)B中官能团的名称为______。
(2)C→D的反应方程式为_____。
(3)G的结构简式为_______。
(4)F→G的反应类型为______。
(5)判断并解释E的a-H具有活泼性的原因是______。
(6)D→F的反应分为两步,第二步反应生成F和另一种产物的结构简式为___。
(7)A的同分异构体中既含有羧基(一COOH)、又含有氨基(一NH?)的有____种。
19.(14分)
°0),存在以下反应:
1,4-丁二醇在铜锌复合催化剂上制备γ-丁内酯(
OH
I. HO
(B)一°?(g)+2H?⑧)△H?>0
OH
(g)一°)+2ZH?(g)△H?>0
Ⅱ. HO
°0(g)+2H?(g)一°(g)+H?Og)△H?
Ⅲ.
(1)298 K,101kPa下部分物质的燃烧热如下表:
?(⑧) O
(g) H?(g)
1868 2325 285.8
燃烧热(kJ·mol?1)
已知H?Og)——H?O(1) △H=—40.7kJ·mol?1,则△H?=_____kJ·mol?1。
(2)向一密闭容器中充人·γ-丁内酯和H?,仅发生反应Ⅲ,改变下列条件,能同时增大反应
速率和γ-丁内酯平衡转化率的有____(填标号)。
d.更换高效催化剂
a.升高温度 b.充人γ-丁内酯 c.压缩容器体积
(3)已知该催化剂中起实际催化作用的是Cu(O),且Cu越分散,活性催化点位就越多。
实际使用时,将复合催化剂xCuO·yZnO在氢气氛围下使用,而不直接使用Cu单
质作为催化剂的原因是______。
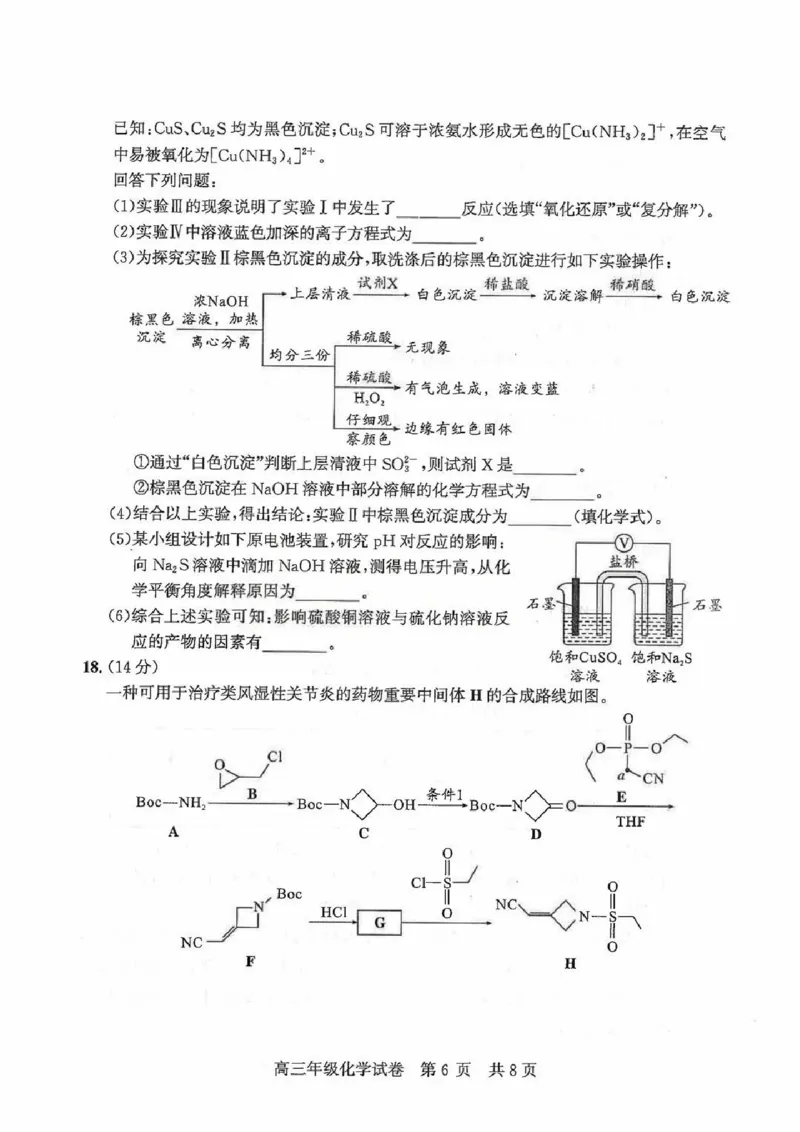
高三年级化学试卷 第7页 共8页(4)在一定压强下,将氢气与1,4-丁二醇混合后,以恒定流速通过催化剂,发生反应I、
Ⅱ、Ⅲ。维持体系温度不变,在相同时间,γ-丁内酯的产量随氢醇比的变化如下图所
示。随着氢醇比的增大,y-丁内酯的产量先升高后降低的原因是_____。
1.3
1.2
1.1
1.0
产量
0.9
0.8
0.7
0.6
1 234567
n(H?):n(1,4-乙二醇)
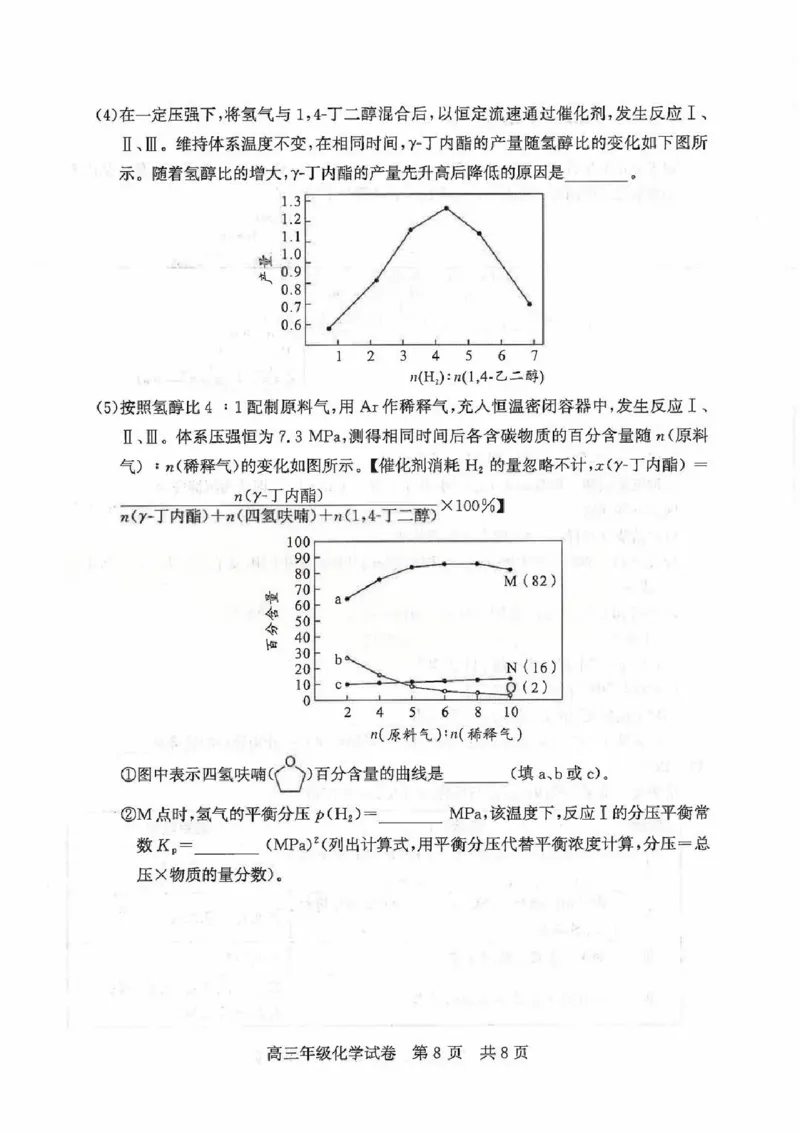
(5)按照氢醇比4:1配制原料气,用Ar作稀释气,充入恒温密闭容器中,发生反应I、
Ⅱ、Ⅲ。体系压强恒为7.3 MPa,测得相同时间后各含碳物质的百分含量随n(原料
气):n(稀释气)的变化如图所示。【催化剂消耗H?的量忽略不计,x(y-丁内酯)=
(Y-T内酚)+n(四红实喃》+(1,4-T二醇×100%)
100
90
80
M(82)
70 a
百分含量
60
50
40
30
ba
20 N(16)
c
10
Q(2)
0
2 4 5 6 8 10
n(原料气):n(稀释气)
°>百分含量的曲线是____(填a、b或c)。
①图中表示四氢呋喃(
②M点时,氢气的平衡分压p(H?)=_______MPa,该温度下,反应I的分压平衡常
数Kp=____(MPa)2(列出计算式,用平衡分压代替平衡浓度计算,分压=总
压×物质的量分数)。
高三年级化学试卷 第8页 共8页