文档内容
本试卷共10页,100分。考试时长90分钟。考生务必将答案写在答题卡上,在试
卷上作答无效。考试结束后,将本试卷和答题纸一并交回。
可能用到的相对原子质量:H1 C12 O16 Na23 Fe56 Pb207
第一部分
本部分共14小题,每题3分,共42分,在每题列出的4个选项中,选出最符合题目
要求的一项。
1.我国科研团队通过高温高压技术成功合成新型超导材料 MgB₂,其临界温度远高于
传统超导材料,在新能源、医疗设备等领域具有广阔应用前景。下列说法正确的是
A.MgB₂ 中镁元素的化合价为 +2价,硼元素为 −3价
B.合成MgB₂ 的过程中,原子的种类和数目均发生改变
C.MgB₂ 的超导性属于物质的化学性质
D.镁原子的结构示意图中,最外层电子数为2
2.下列化学用语或图示表达正确的是
A.乙炔的球棍模型:
B.SO2- 的 VSEPR 模型:平面三角形
3
C.基态 Cr原子的价层电子排布式:3d54s1
24
D.次氯酸的结构式:H−Cl−O
3.下列说法不
.
正
.
确
.
的是
A.淀粉、纤维素和蛋白质均属于天然有机高分子
B.麦芽糖在稀硫酸催化下发生水解反应,产物能与新制氢氧化铜悬浊液反应生
成砖红色沉淀
C.油脂在碱性条件下的水解反应称为皂化反应,可用于生产肥皂
D.向蛋白质溶液中加入饱和硫酸铵溶液,蛋白质发生变性,出现白色沉淀
高三化学 第 1 页 共 10 页4.物质的微观结构决定其宏观性质。乙胺(CH CH NH )是一种无色、有强烈氨味的
3 2 2
液体,能与水、乙醇、乙醚等有机溶剂混溶。下列说法不正确的是
...
A.乙胺的电子式:
B.乙胺分子中,乙基中的碳原子和氨基中的氮原子均为 sp3 杂化
C.乙胺分子中的氨基可与水形成氢键
D.乙胺可与盐酸发生反应,生成CH CH NH Cl
3 2 3
5.下列叙述对应的反应中,能体现SO2-还原性的是
3
A.向亚硫酸钠溶液中加入稀盐酸,产生能使澄清石灰水变浑浊的气体
B.向酸性高锰酸钾溶液中滴加亚硫酸钠溶液,溶液紫红色逐渐褪去
C.向亚硫酸钠溶液中通入二氧化碳,无明显实验现象
D.向氯化钡溶液中滴加亚硫酸钠溶液,生成白色沉淀
6.下列化学方程式或离子方程式与所给事实不
.
相
.
符
.
的是
A.实验室用大理石与稀盐酸制取二氧化碳:CaCO +2H+===Ca2++CO ↑+H O
3 2 2
△
B.铜与浓硫酸在加热条件下反应:Cu+2H SO (浓)===CuSO +SO ↑+2H O
2 4 4 2 2
C.向溴化亚铁溶液中通入过量氯气:2Fe2++Cl ===2Fe3++2Cl−
2
D.用 CuSO 溶液除去乙炔中的 H S:Cu2++H S===CuS↓+2H+
4 2 2
7.下列实验的相应操作中,不
.
正
.
确
.
的是
中和滴定 配制溶液 蒸馏 制备并检验 SO
2
A.用NaOH标准溶 B.向容量瓶中 C.冷却水从冷凝管 D.为防止有害气体
液滴定HCl溶液 转移溶液 ②口通入,①口流出 逸出,先放置浸 NaOH
溶液的棉团,再加热
高三化学 第 2 页 共 10 页8.二溴甲烷是无色透明液体,微溶于水,可溶于乙醇、乙醚等有机溶剂,在工业、医
药等领域应用广泛,其结构如下图所示。下列关于二溴甲烷的说法不正确的是
...
A.分子中不含手性碳原子
B.是非极性分子
C.电负性:Br > C > H
D.一定条件下能与 NaOH 溶液发生反应
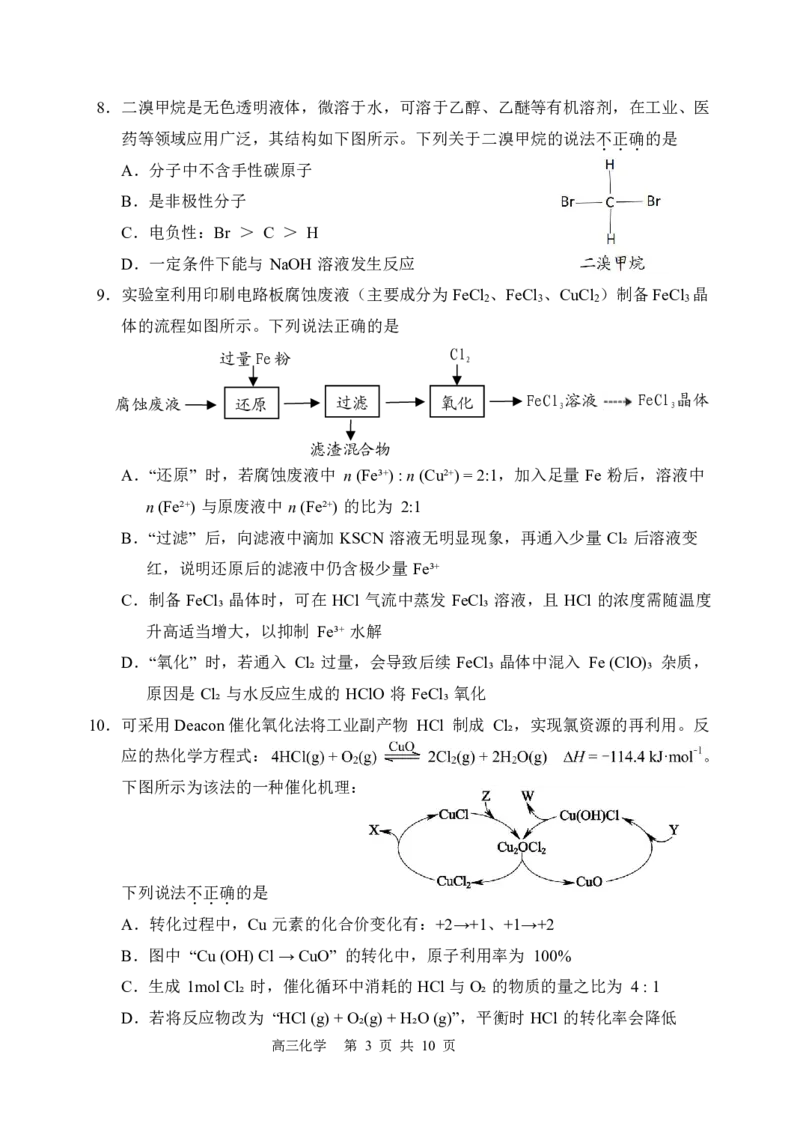
9.实验室利用印刷电路板腐蚀废液(主要成分为FeCl 、FeCl 、CuCl )制备FeCl 晶
2 3 2 3
体的流程如图所示。下列说法正确的是
过量Fe粉 Cl
2
腐蚀废液 还原 过滤 氧化 FeCl 3 溶液 FeCl 3 晶体
滤渣混合物
A.“还原” 时,若腐蚀废液中 n(Fe³⁺):n(Cu²⁺)=2:1,加入足量 Fe 粉后,溶液中
n(Fe²⁺) 与原废液中 n(Fe²⁺) 的比为 2:1
B.“过滤” 后,向滤液中滴加 KSCN 溶液无明显现象,再通入少量 Cl₂ 后溶液变
红,说明还原后的滤液中仍含极少量 Fe³⁺
C.制备 FeCl₃ 晶体时,可在 HCl 气流中蒸发 FeCl₃ 溶液,且 HCl 的浓度需随温度
升高适当增大,以抑制 Fe³⁺ 水解
D.“氧化” 时,若通入 Cl₂ 过量,会导致后续 FeCl₃ 晶体中混入 Fe(ClO)₃ 杂质,
原因是 Cl₂ 与水反应生成的 HClO 将 FeCl₃ 氧化
10.可采用Deacon催化氧化法将工业副产物 HCl 制成 Cl₂,实现氯资源的再利用。反
应的热化学方程式:
下图所示为该法的一种催化机理:
下列说法不正确的是
...
A.转化过程中,Cu 元素的化合价变化有:+2→+1、+1→+2
B.图中 “Cu(OH)Cl→CuO” 的转化中,原子利用率为 100%
C.生成 1molCl₂ 时,催化循环中消耗的HCl与O₂ 的物质的量之比为 4:1
D.若将反应物改为 “HCl(g)+O₂(g)+H₂O(g)”,平衡时 HCl 的转化率会降低
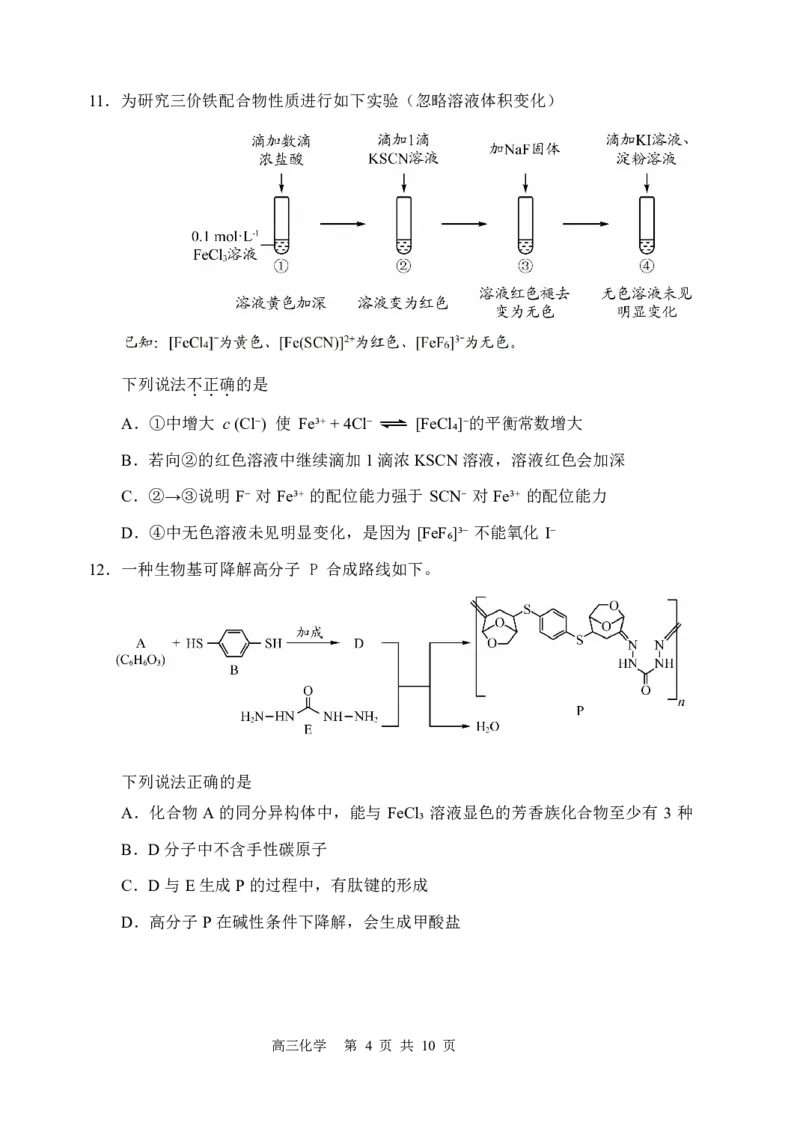
高三化学 第 3 页 共 10 页11.为研究三价铁配合物性质进行如下实验(忽略溶液体积变化)
下列说法不正确的是
...
A.①中增大 c(Cl⁻) 使 Fe³⁺+4Cl⁻ [FeCl₄]⁻的平衡常数增大
B.若向②的红色溶液中继续滴加1滴浓KSCN溶液,溶液红色会加深
C.②→③说明 F⁻ 对 Fe³⁺ 的配位能力强于 SCN⁻ 对 Fe³⁺ 的配位能力
D.④中无色溶液未见明显变化,是因为 [FeF₆]³⁻ 不能氧化 I⁻
12.一种生物基可降解高分子 P 合成路线如下。
下列说法正确的是
A.化合物A的同分异构体中,能与 FeCl₃ 溶液显色的芳香族化合物至少有 3 种
B.D分子中不含手性碳原子
C.D与E生成P的过程中,有肽键的形成
D.高分子P在碱性条件下降解,会生成甲酸盐
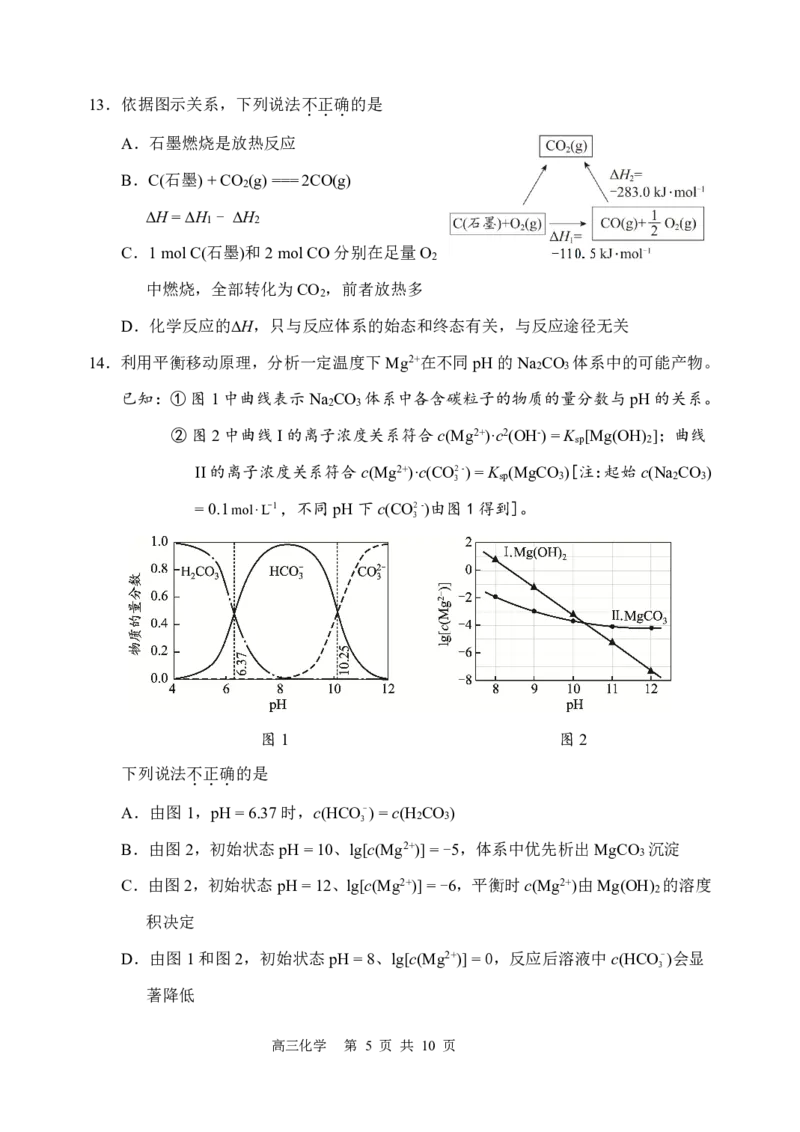
高三化学 第 4 页 共 10 页13.依据图示关系,下列说法不
.
正
.
确
.
的是
A.石墨燃烧是放热反应
B.C(石墨)+CO (g)===2CO(g)
2
H=H - H
1 2
C.1molC(石墨)和2molCO分别在足量O
2
中燃烧,全部转化为CO ,前者放热多
2
D.化学反应的H,只与反应体系的始态和终态有关,与反应途径无关
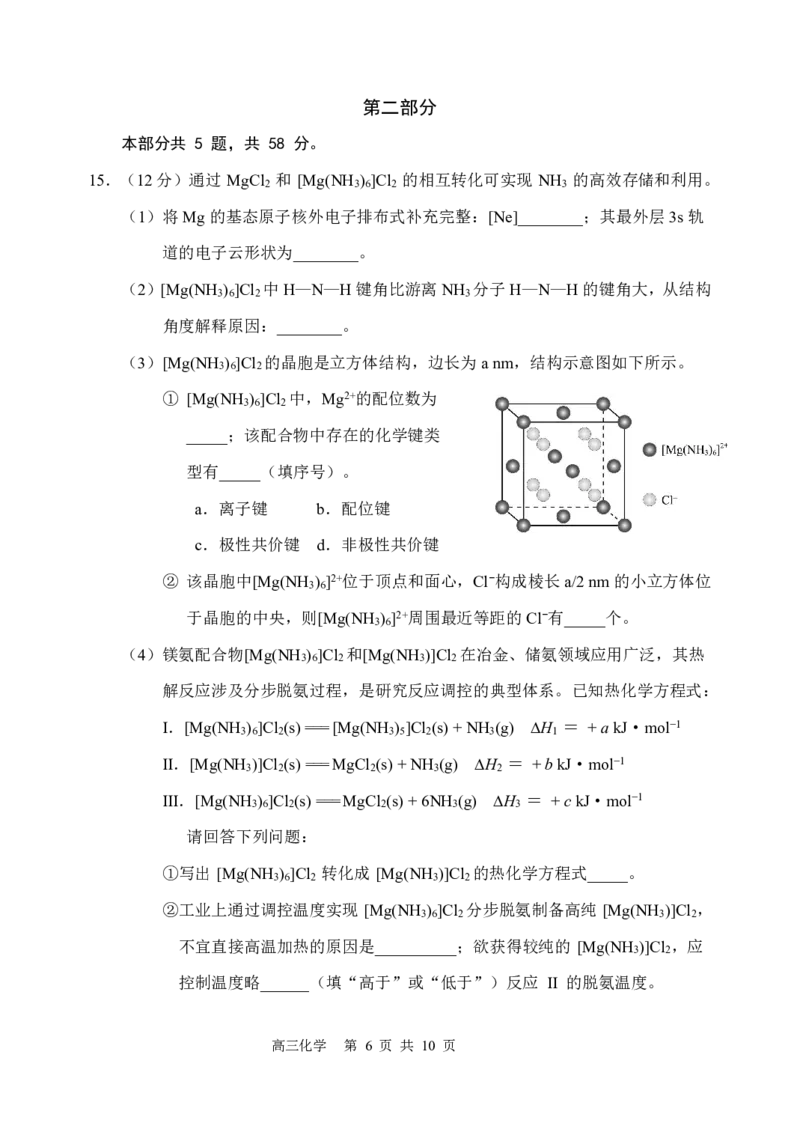
14.利用平衡移动原理,分析一定温度下Mg2+在不同pH的Na CO 体系中的可能产物。
2 3
已知:①图1中曲线表示Na CO 体系中各含碳粒子的物质的量分数与pH的关系。
2 3
②图2中曲线I的离子浓度关系符合c(Mg2+)·c2(OH-)=K [Mg(OH) ];曲线
sp 2
II的离子浓度关系符合c(Mg2+)·c(CO2-)=K (MgCO )[注:起始c(Na CO )
3 sp 3 2 3
=0.1molL-1,不同pH下c(CO2-)由图1得到]。
3
图1 图2
下列说法不正确的是
...
A.由图1,pH=6.37时,c(HCO-)=c(H CO )
3 2 3
B.由图2,初始状态pH=10、lg[c(Mg2+)]=-5,体系中优先析出MgCO 沉淀
3
C.由图2,初始状态pH=12、lg[c(Mg2+)]=-6,平衡时c(Mg2+)由Mg(OH) 的溶度
2
积决定
D.由图1和图2,初始状态pH=8、lg[c(Mg2+)]=0,反应后溶液中c(HCO-)会显
3
著降低
高三化学 第 5 页 共 10 页第二部分
本部分共 5 题,共 58 分。
15.(12分)通过 MgCl 和 [Mg(NH ) ]Cl 的相互转化可实现 NH 的高效存储和利用。
2 3 6 2 3
(1)将Mg的基态原子核外电子排布式补充完整:[Ne]________;其最外层3s轨
道的电子云形状为________。
(2)[Mg(NH ) ]Cl 中H—N—H键角比游离NH 分子H—N—H的键角大,从结构
3 6 2 3
角度解释原因:________。
(3)[Mg(NH ) ]Cl 的晶胞是立方体结构,边长为anm,结构示意图如下所示。
3 6 2
① [Mg(NH ) ]Cl 中,Mg2+的配位数为
3 6 2
_____;该配合物中存在的化学键类
型有_____(填序号)。
a.离子键 b.配位键
c.极性共价键 d.非极性共价键
② 该晶胞中[Mg(NH ) ]2+位于顶点和面心,Cl−构成棱长a/2nm的小立方体位
3 6
于晶胞的中央,则[Mg(NH ) ]2+周围最近等距的Cl−有_____个。
3 6
(4)镁氨配合物[Mg(NH ) ]Cl 和[Mg(NH )]Cl 在冶金、储氨领域应用广泛,其热
3 6 2 3 2
解反应涉及分步脱氨过程,是研究反应调控的典型体系。已知热化学方程式:
I.[Mg(NH ) ]Cl (s)===[Mg(NH ) ]Cl (s)+NH (g) ∆H = +akJ·mol−1
3 6 2 3 5 2 3 1
II.[Mg(NH )]Cl (s)===MgCl (s)+NH (g) ∆H = +bkJ·mol−1
3 2 2 3 2
III.[Mg(NH ) ]Cl (s)===MgCl (s)+6NH (g) ∆H = +ckJ·mol−1
3 6 2 2 3 3
请回答下列问题:
①写出 [Mg(NH ) ]Cl 转化成 [Mg(NH )]Cl 的热化学方程式_____。
3 6 2 3 2
②工业上通过调控温度实现 [Mg(NH ) ]Cl 分步脱氨制备高纯 [Mg(NH )]Cl ,
3 6 2 3 2
不宜直接高温加热的原因是__________;欲获得较纯的 [Mg(NH )]Cl ,应
3 2
控制温度略______(填“高于”或“低于”)反应 II 的脱氨温度。
高三化学 第 6 页 共 10 页16.(13分)铅酸电池是用途广泛并不断发展的化学电源。
(1) 十九世纪,铅酸电池工作原理初步形成并延续至今。
铅酸电池工作原理:
PbO +Pb+2H SO 2PbSO +2H O
2 2 4 4 2
① 放电时,当外电路通过2mol电子时,理论上电解质溶液中H+的物质的量
_____(填 “增加” 或 “减少”)_____mol。
② 充电时,若将铅酸电池与外接电源连接,正极应与外接电源的_____极相连,
充电时阳极发生的电极反应为______。
③SO2-参与电极反应并有利于保持电压稳定,SO2-的VSEPR模型名称为___。
4 4
④ 铅酸电池储存过程中,存在化学能的缓慢消耗:PbO 电极在H SO 作用下
2 2 4
产生的O 可将Pb电极氧化。若储存过程中消耗标准状况下2.24LO ,则理
2 2
论上被氧化的Pb的质量为______g。
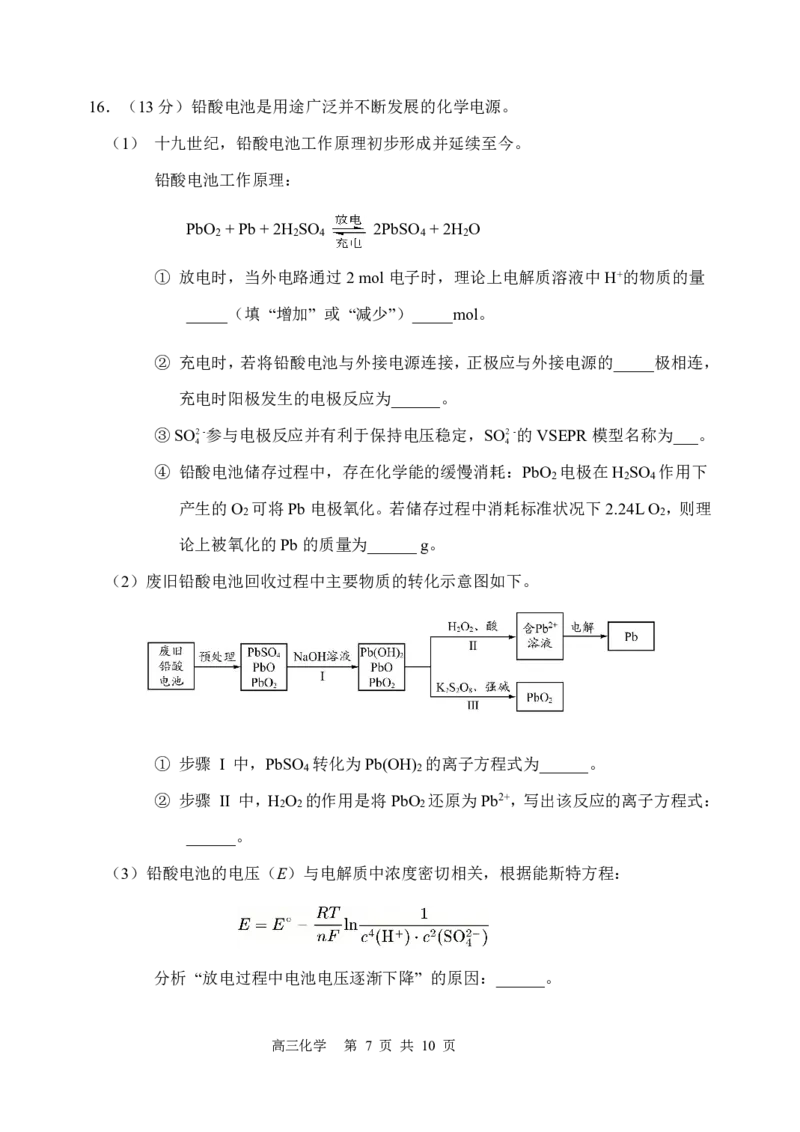
(2)废旧铅酸电池回收过程中主要物质的转化示意图如下。
① 步骤 Ⅰ 中,PbSO 转化为Pb(OH) 的离子方程式为______。
4 2
② 步骤 Ⅱ 中,H O 的作用是将PbO 还原为Pb2+,写出该反应的离子方程式:
2 2 2
______。
(3)铅酸电池的电压(E)与电解质中浓度密切相关,根据能斯特方程:
分析 “放电过程中电池电压逐渐下降” 的原因:______。
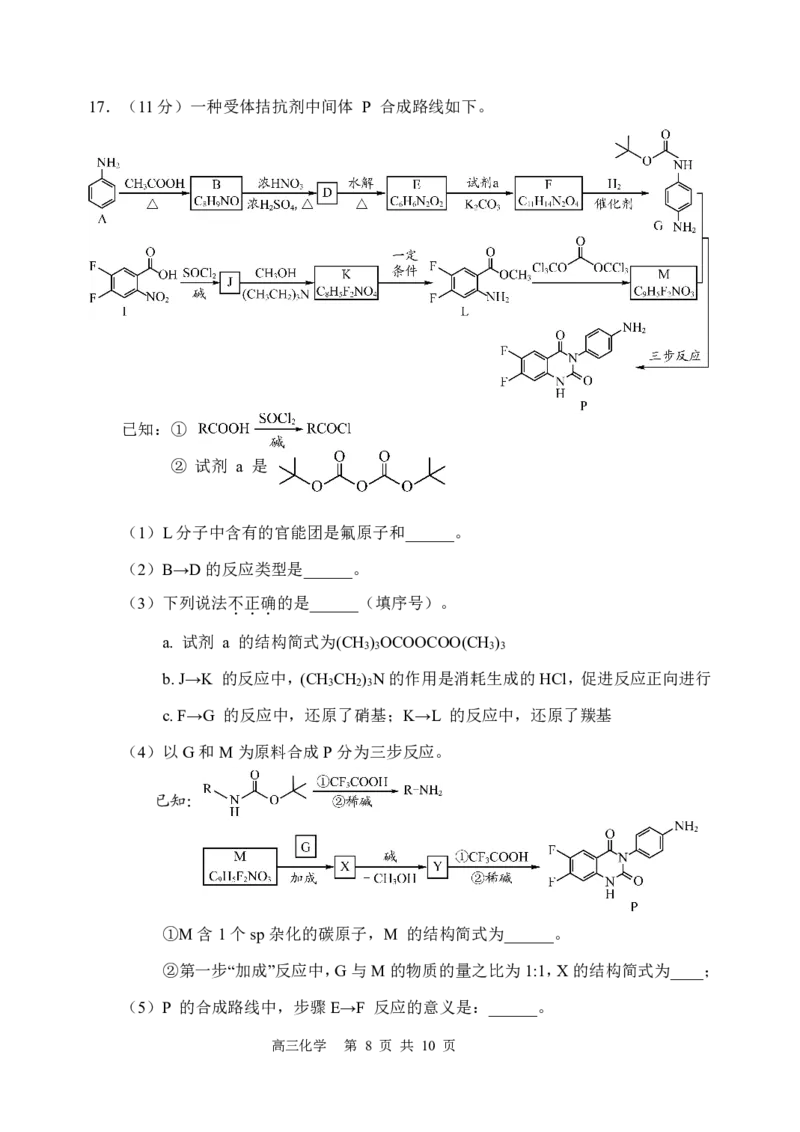
高三化学 第 7 页 共 10 页17.(11分)一种受体拮抗剂中间体 P 合成路线如下。
已知:①
② 试剂 a 是
(1)L分子中含有的官能团是氟原子和______。
(2)B→D的反应类型是______。
(3)下列说法不
.
正
.
确
.
的是______(填序号)。
a. 试剂 a 的结构简式为(CH ) OCOOCOO(CH )
3 3 3 3
b.J→K 的反应中,(CH CH ) N的作用是消耗生成的HCl,促进反应正向进行
3 2 3
c.F→G 的反应中,还原了硝基;K→L 的反应中,还原了羰基
(4)以G和M为原料合成P分为三步反应。
已知:
①M含1个sp杂化的碳原子,M 的结构简式为______。
②第一步“加成”反应中,G与M的物质的量之比为1:1,X的结构简式为____;
(5)P 的合成路线中,步骤E→F 反应的意义是:______。
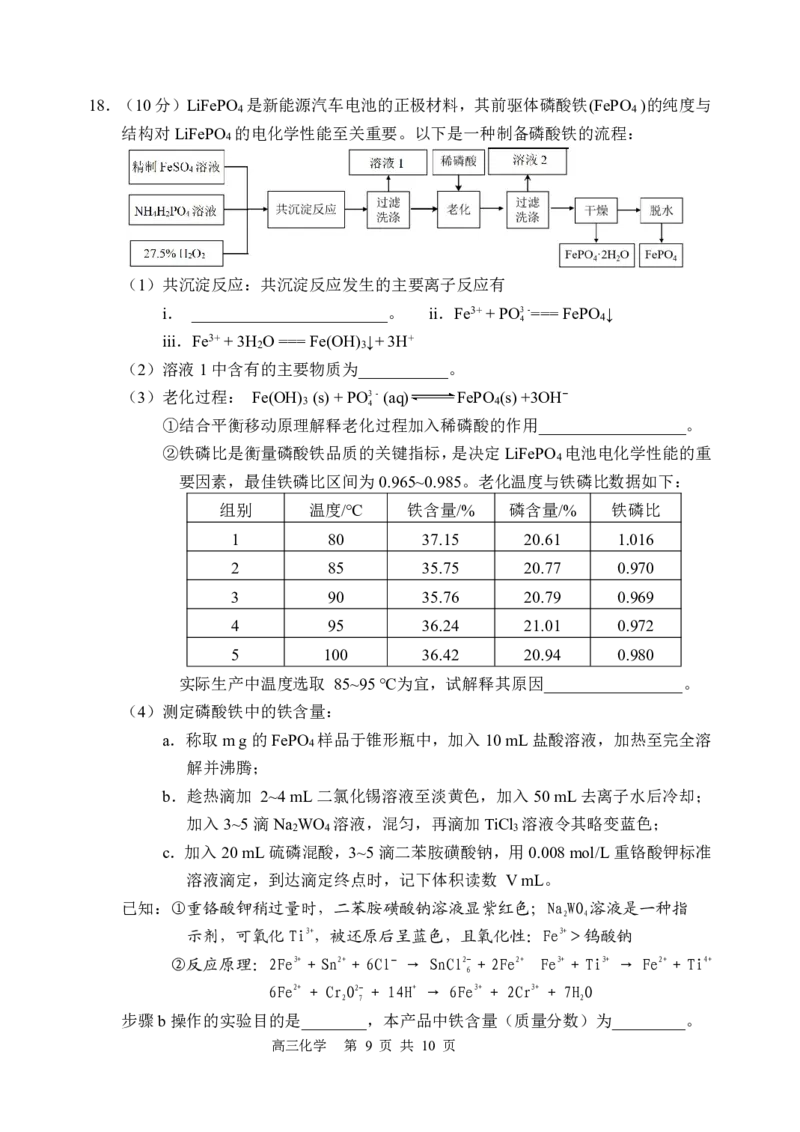
高三化学 第 8 页 共 10 页18.(10分)LiFePO 是新能源汽车电池的正极材料,其前驱体磷酸铁(FePO )的纯度与
4 4
结构对LiFePO 的电化学性能至关重要。以下是一种制备磷酸铁的流程:
4
(1)共沉淀反应:共沉淀反应发生的主要离子反应有
i. ________________________。 ii.Fe3++PO3-===FePO ↓
4 4
iii.Fe3++3H O===Fe(OH) ↓+3H+
2 3
(2)溶液1中含有的主要物质为___________。
(3)老化过程: Fe(OH) (s)+PO3-(aq) FePO (s)+3OH−
3 4 4
①结合平衡移动原理解释老化过程加入稀磷酸的作用__________________。
②铁磷比是衡量磷酸铁品质的关键指标,是决定LiFePO 电池电化学性能的重
4
要因素,最佳铁磷比区间为0.965~0.985。老化温度与铁磷比数据如下:
组别 温度/℃ 铁含量/% 磷含量/% 铁磷比
1 80 37.15 20.61 1.016
2 85 35.75 20.77 0.970
3 90 35.76 20.79 0.969
4 95 36.24 21.01 0.972
5 100 36.42 20.94 0.980
实际生产中温度选取 85~95℃为宜,试解释其原因_________________。
(4)测定磷酸铁中的铁含量:
a.称取mg的FePO 样品于锥形瓶中,加入10mL盐酸溶液,加热至完全溶
4
解并沸腾;
b.趁热滴加 2~4mL二氯化锡溶液至淡黄色,加入50mL去离子水后冷却;
加入3~5滴Na WO 溶液,混匀,再滴加TiCl 溶液令其略变蓝色;
2 4 3
c.加入20mL硫磷混酸,3~5滴二苯胺磺酸钠,用0.008mol/L重铬酸钾标准
溶液滴定,到达滴定终点时,记下体积读数 VmL。
已知:①重铬酸钾稍过量时,二苯胺磺酸钠溶液显紫红色;NaWO 溶液是一种指
2 4
示剂,可氧化Ti3+,被还原后呈蓝色,且氧化性:Fe3+>钨酸钠
②反应原理:2Fe3+ + Sn2+ + 6Cl− → SnCl2− + 2Fe2+ Fe3+ + Ti3+ → Fe2+ + Ti4+
6
6Fe2+ + CrO2− + 14H+ → 6Fe3+ + 2Cr3+ + 7HO
2 7 2
步骤b操作的实验目的是________,本产品中铁含量(质量分数)为_________。
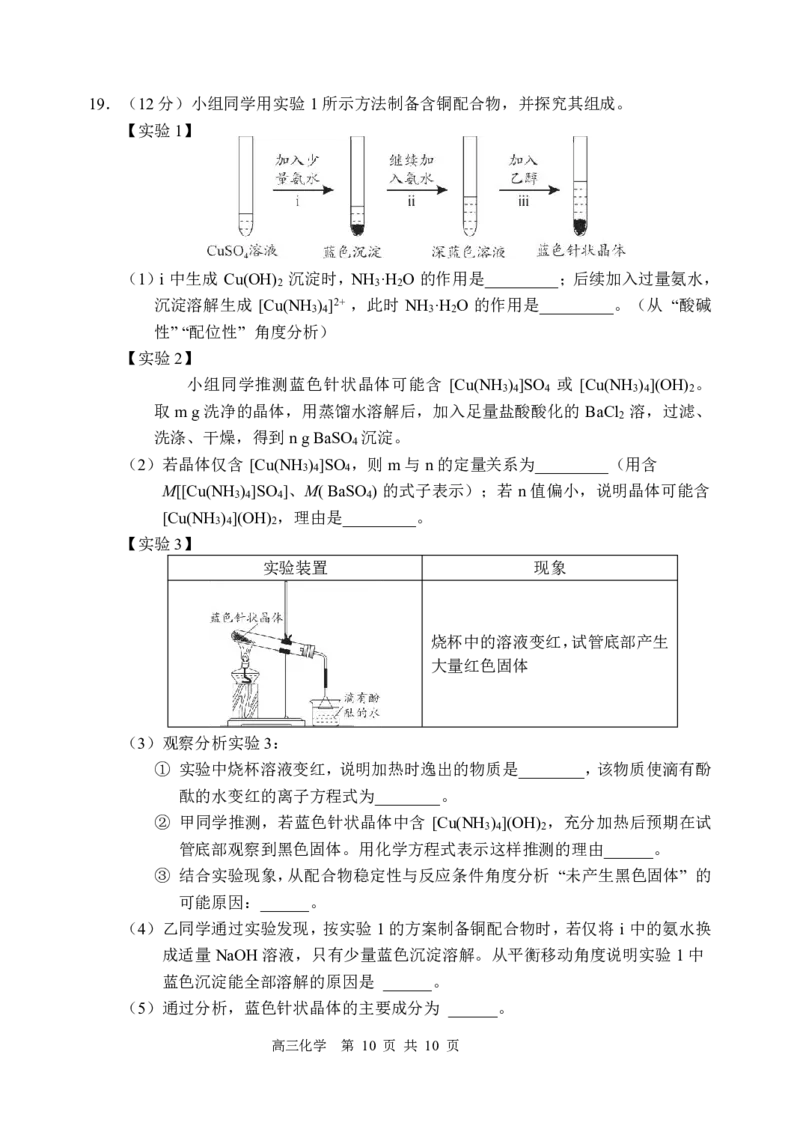
高三化学 第 9 页 共 10 页19.(12分)小组同学用实验1所示方法制备含铜配合物,并探究其组成。
【实验1】
(1)ⅰ 中生成 Cu(OH) 沉淀时,NH ·H O 的作用是_________;后续加入过量氨水,
2 3 2
沉淀溶解生成 [Cu(NH ) ]2+ ,此时 NH ·H O 的作用是_________。(从 “酸碱
3 4 3 2
性”“配位性” 角度分析)
【实验2】
小组同学推测蓝色针状晶体可能含 [Cu(NH ) ]SO 或 [Cu(NH ) ](OH) 。
3 4 4 3 4 2
取mg洗净的晶体,用蒸馏水溶解后,加入足量盐酸酸化的 BaCl 溶,过滤、
2
洗涤、干燥,得到ngBaSO 沉淀。
4
(2)若晶体仅含 [Cu(NH ) ]SO ,则m与n的定量关系为_________(用含
3 4 4
M[[Cu(NH ) ]SO ]、M(BaSO ) 的式子表示);若n值偏小,说明晶体可能含
3 4 4 4
[Cu(NH ) ](OH) ,理由是_________。
3 4 2
【实验3】
实验装置 现象
烧杯中的溶液变红,试管底部产生
大量红色固体
(3)观察分析实验3:
① 实验中烧杯溶液变红,说明加热时逸出的物质是________,该物质使滴有酚
酞的水变红的离子方程式为________。
② 甲同学推测,若蓝色针状晶体中含 [Cu(NH ) ](OH) ,充分加热后预期在试
3 4 2
管底部观察到黑色固体。用化学方程式表示这样推测的理由______。
③ 结合实验现象,从配合物稳定性与反应条件角度分析 “未产生黑色固体” 的
可能原因:______。
(4)乙同学通过实验发现,按实验1的方案制备铜配合物时,若仅将 ⅰ 中的氨水换
成适量NaOH溶液,只有少量蓝色沉淀溶解。从平衡移动角度说明实验1中
蓝色沉淀能全部溶解的原因是 ______。
(5)通过分析,蓝色针状晶体的主要成分为 ______。
高三化学 第 10 页 共 10 页高三化学参考答案
第一部分(共14题,每小题3分,答对给3分,答错、空答、多答为0分,满分42分)
题号 1 2 3 4 5 6 7
答案 D C D A B C A
题号 8 9 10 11 12 13 14
答案 B C B A A C B
第二部分(共5题,满分58分)
15.(12分)
(1)3s2(1分) 球形 (1分)
(2)NH3 与Mg2+形成配位键时,孤
.
电
.
子
.
对
.
参
.
与
.
成
.
键
.
,孤电子对与成键电子对的斥
.
力
.
减
.
弱
.
,成
键电子对之间的斥力相对增大,故键角变大(2分)
(3) ①6(1分) abc(2分,填对2个得1分,填对3个得2分,有错不得分)
②8(1分)
(4) ①[Mg(NH3)6]Cl2(s)===[Mg(NH3)]Cl2(s)+5NH3(g) ∆H1 = +(c−b)kJ·mol−1
(数值对1分,共2分)
②[Mg(NH3)6]Cl2 直接高温加热会导致进一步分解为MgCl2 ,无法得到目标产物(1分);
低于(1 分)
16.(13分)
(1)① 减少4(2分)
② 正(1分) PbSO4−2e−+2H2O ====PbO2+SO2
4
-+4H+ (物质对1分,共2分)
③ 正四面体(1分)
④41.4(2分)
(2)①PbSO4 +2OH−====Pb(OH)2+SO2
4
-(1分,有错不得分)
②PbO2+H2O2+2H+==== Pb2++O2+2H2O(物质1分,2分)
(3)放电过程中,H2SO4 不断被消耗,c(H+)、c(SO2
4
-)降
.
低
.
,根据能斯特方程,
的值增大,E. 减
.
小
.
,故电池电压逐渐下降。(2分)
117.(11分)
(1)氨基、酯基(2分,填化学式亦可)
(2)取代反应(1分)
(3)ac(2分)
(4)① (2分) ② (2分)
(5)E中氨基与试剂a 形成酰胺键,避免后续G 与M反应中氨基全部反应,最终通过 “稀碱”
脱除保护基(2分);保护氨基(1分),防止全部与M反应(1分)
18.(10分)
(1)2Fe2++H2O2+2H+===2Fe3++2H2O (物质对1分,共2分)
(2)硫酸铵或(NH4)2SO4 (1分)
(3)
① 老化过程存在平衡 Fe(OH)3(s)+PO3
4
-(aq) FePO4(s)+3OH−,加入磷酸,H+与OH−
发生中和反应同时生成PO3
4
-,均使平衡正向移动,促使Fe(OH)3 溶解,生成 FePO4 (2
分)
②温度低于 85℃时铁磷比偏高(超过 0.985),温度高于 95℃时铁磷比无明显优化,但
高温会增加能耗、溶剂挥发或可能导致产物分解等,故选择 85~95℃。(1 分)
(4) 将Fe3+恰
.
好
.
全
.
部
.
转化为Fe2+(2 分)
(2 分)
19.(12分)
(1)提供OH-,表现碱性(1 分);提供NH3 作为配体,表现配位性(1 分)
(2) m/M[[Cu(NH3)4]SO4]=n/M(BaSO4)(1 分)
晶体中含[Cu(NH3)4](OH)2 时,SO2
4
-的物质的量减少,生成的BaSO4 沉淀质量小。(1 分)
(3)①NH3 (1 分);NH3+H2O NH3·H2O NH
4
+ + OH-(1 分)
△
②[Cu(NH3)4](OH)2===CuO + 4NH3↑ +H2O (物质对1分,共2 分)
③分解生成的CuO与未逸出的NH3 发生反应,生成了非黑色物质(铜单质或氧化亚
铜)(1 分)。
(4)Cu(OH)2(s) Cu2+(aq)+2OH-(aq),加入NH3·H2O后,Cu2+可以与NH3 形成
[Cu(NH3)4]2+,且ⅰ中反应Cu2++2NH3·H2O===Cu(OH)2↓+2NH4 +产生的N.H.4. +.能
.
与
.
溶
.
解 . 平 . 衡 . 中 . 的 .O.H..-的 . 结 . 合 . 生 . 成 .N.H.3..·H.2. O. ,均使沉淀溶解平衡正向移动。(2分)
(5) [Cu(NH3)4]SO4 (1 分)
2