文档内容
名校联盟
s schan uagn
绝密★考试结束前
Z20名校联盟(浙江省名校新高考研究联盟)2026届高三第二次联考
化学试题
命题:宁海中学 朱孙燕、周丰琦
磨题:嘉善高级中学 耿晓冬 平湖中学 李燕 嵊州中学裘丹丽 校稿:苏艳丽、王雪莲
1.本试题卷分选择题和非选择题两部分,共8页,满分100分,考试时间90分钟。
2.可能用到的相对原子质量:H:1 C:12 N:14 O:16
选择题部分
一、选择题(本大题共16题,每小题3分,共48分。每小题只有一个选项符合题目要求,不选、
多选、错写均不得分。)
1.下列物质属于电解质的是
A. SO? C. CH?COONa D. Cu
B.漂白粉
2.下列物质的性质能说明其用途的是
A. SO?具有氧化性,因此加入葡萄酒中起杀菌和抗氧化作用
B. NaClO溶液水解呈酸性,因此可作漂白剂
C.植物油可通过催化加氢提高饱和度,因此可用于制取肥皂
H cH OH oH oB
D.木糖醇( 不属于糖类,但甜味与蔗糖相当,因此可用作糖尿病患者适用的
甜味剂
3.下列表示不正确的是
A.质量数为18的氧原子:8o B. BCl?的电子式:
:Ci:B:Ci:
C. Cl?中σ键的电子云轮廓图:α D. SO?的价层电子对互斥(VSEPR)模型:
。
。
4.利用下列仪器、装置及药品能达到实验目的的是
温度计、
玻璃 4mL0.01 mol/L 4mL0.02 mol/L
搅拌器
KMnO?溶液 KMnO?溶液
SO?(HCI)
浓HNO?
a 内筒、
饱和 杯盖
Na?SO? KI-淀粉 隔热层、 中 2 mL0.2 mol/L h 2mL0.2 mol/L
b 图
溶液 外壳 H?C?O4溶液 H?C?O4溶液
① ② ③ ④
A.图①用来除去SO?气体中的HCl杂质
B.图②装置b中溶液变蓝能够说明浓HNO?分解生成NO?
C.图③装置可用于测定中和热
D.图④依据褪色时间的长短,能证明反应物浓度对反应速率的影响
5.下列说法不正确的是
A.汽车尾气排放的氮氧化合物主要来自汽油的不充分燃烧
B.煤的干馏是指将煤隔绝空气加强热使之分解的过程,工业上也叫煤的焦化
C.多糖、蛋白质、油脂在一定条件下均可水解
D.医学上常用体积分数为75??乙醇溶液杀菌消毒6.过二硫酸钠Na?S?Os(n |08°。N)
是工业上常用的强氧化剂,下列说法正确的是
A.过二硫酸钠中硫的化合价为+7价
B.过二硫酸钠氧化性比双氧水更强
C. Mn2++S?O3+H?O→MnO?+H++SO2,该反应中氧化剂与还原剂的物质的量之比为2:5
D.电解硫酸氢钠溶液制备1mol过二硫酸钠,则电路中转移2个电子
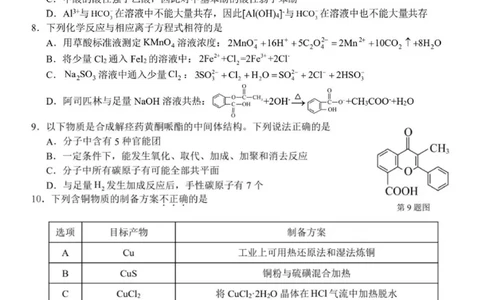
7.类比或推理是重要的学习方法,下列类比或推理不合理的是
A.常温下,K.(NH?·H?O)=1.8×10??K(HF)=6.3×10?,因此NH?F溶液显酸性
B. KH?PO?是正盐,因此H?PO?是一元酸
C.甲酸的酸性强于乙酸,因此对甲基苯酚的酸性弱于苯酚
D. Al3+与HCO?在溶液中不能大量共存,因此[Al(OH)4]与HCO?在溶液中也不能大量共存
8.下列化学反应与相应离子方程式相符的是
A.用草酸标准液测定KMnO?溶液浓度:2MnO?+16H++5C?O2-=2Mn2++10CO?↑+8H?O
B.将少量Cl?通入Fel?的溶液中:2Fe2?+Cl?=2Fe3+2Cl
C. Na?SO?溶液中通入少量Cl?:3SO2-+Cl?+H?O=SO2-+2CI?+2HSO?
o+0co rcncoHo
D.阿司匹林与足量NaOH溶液共热:
9.以下物质是合成解痉药黄酮哌酯的中间体结构。下列说法正确的是 0
A.分子中含有5种官能团
CH?
B. 一定条件下,能发生氧化、取代、加成、加聚和消去反应
C.分子中所有碳原子有可能全部共平面
D.与足量H?发生加成反应后,手性碳原子有7个
COOH
10.下列含铜物质的制备方案不正确的是
第9题图
选项 目标产物 制备方案
A Cu
工业上可用热还原法和湿法炼铜
B CuS
铜粉与硫磺混合加热
C CuCl?
将CuCl?·2H?O晶体在HCl气流中加热脱水
向硫酸铜溶液中逐滴加入氨水至沉淀溶解,再
D
[Cu(NH?)4]SO?·H?O
加入适量95??醇,过滤、洗涤、干燥
11.我国多条高压直流电线路的瓷绝缘子出现铁帽腐蚀现象,在铁帽上加锌 锌环
湿润的绝
环能有效防止铁帽的腐蚀,防护原理如图所示。下列说法不正确的是 铁帽、
缘子表面
A.该保护铁帽的方法是牺牲阳极法
B.正极上的电极反应式为O?+2H?O+4e?=40H- 第11题图
C.若用外加电流法保护铁帽,可使铁帽表面的腐蚀电流降至零或接近零而受到保护
D.把锌环换成锡环后,仍能防止铁帽被腐蚀
Z20名校联盟(浙江省名校新高考研究联盟)2026届高三第二次联考 化学试题卷 第2 页 共8页12.一定条件下,三个体积均为IL的密闭容器中发生反应:
CH?(g)+2NO?(g)=N?(8)+CO?(g)+2H?O(g)在Ti、T?(Ti>T?)两个不同温度下实验,测得
有关数据如下表。
起始时物质的量/mol 平衡时物质的量/mol
容器编号 温度/K
CH? NO? N? CO? H?O NO?
I T? 1.16 3.0 0 0 0 1.0
Ⅱ T? 1.0 2.0 0.5 0.5 2.5 X
Ⅲ T? 0.16 1.0 1.0 1.0 2.0 0.80
下列说法正确的是
A.该反应只有在高温下才能自发进行
B.实验II中,x=0.5
C.若实验Ⅲ中反应起始时通入2.32mol CH?和6.0 mol NO?,达到平衡时 c(NO?)>1.60 mol/L
D.其他条件不变,增大c(CH?):c(NO?)的比值,能提高CH?的平衡转化率
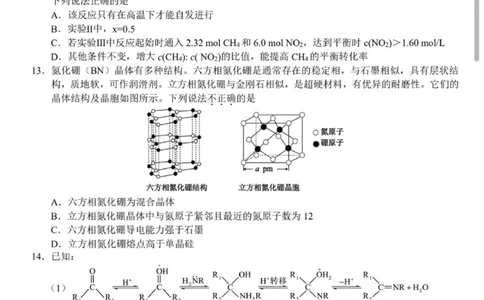
13.氮化硼(BN)晶体有多种结构。六方相氮化硼是通常存在的稳定相,与石墨相似,具有层状结
构,质地软,可作润滑剂。立方相氮化硼与金刚石相似,是超硬材料,有优异的耐磨性。它们的
晶体结构及晶胞如图所示。下列说法不正确的是
O氮原子
O ●硼原子
a pm
六方相氮化硼结构 立方相氮化硼晶胞
A.六方相氮化硼为混合晶体
B.立方相氮化硼晶体中与氮原子紧邻且最近的氮原子数为12
C.六方相氮化硼导电能力强于石墨
、一”-m:nu
D.立方相氮化硼熔点高于单晶硅
14.已知:
(2)同一个C原子连接着一个-OH和的物质不稳定,会失去一个H?O分子。
下列说法不正确的是
A.与
按以上机理反应生成的有机产物仅有
B.将水从反应体系中蒸出可使反应正向进行程度增大
C. H+是该反应的催化剂,溶液酸性越强,但催化效果不一定越好
D.以HCHO和NH?为原料合成乌洛托品( )的过程中涉及π键的断裂
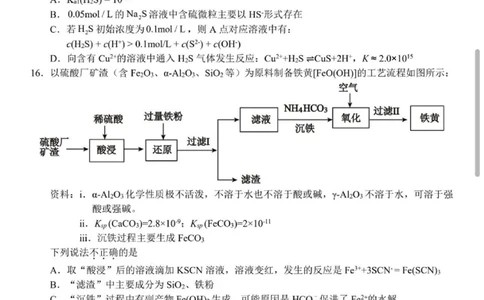
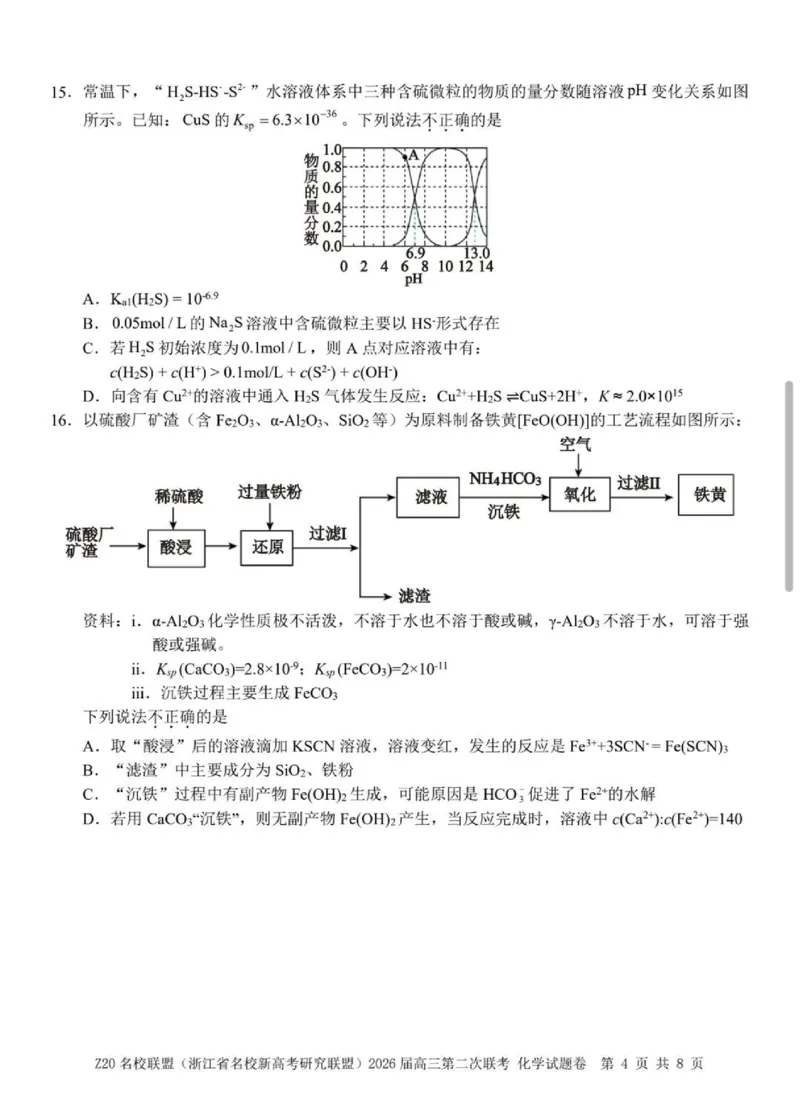
Z20名校联盟(浙江省名校新高考研究联盟)2026届高三第二次联考 化学试题卷 第3页 共8页15.常温下,“H?S-HS-S2”水溶液体系中三种含硫微粒的物质的量分数随溶液pH变化关系如图
所示。已知:CuS的Ks=6.3×10?3?。下列说法不正确的是
1.0
A
物质的量分数
0.8
0.6
0.4
0.2
0.0
6.9 13.0
024 68 10 12 14
pH
A.Kai(H?S)=10-6.9
B. 0.05mol/L的Na?S溶液中含硫微粒主要以HS-形式存在
C.若H?S初始浓度为0.1mol/L,则A点对应溶液中有:
c(H?S)+c(H+)>0.1mol/L+c(S2-)+c(OH)
D.向含有Cu2+的溶液中通入H?S气体发生反应:Cu2++H?S=CuS+2H+,K≈2.0×101?
16.以硫酸厂矿渣(含Fe?O?、α-Al?O?、SiO?等)为原料制备铁黄[FeO(OH)]的工艺流程如图所示:
空气
NH?HCO?
过滤Ⅱ
稀硫酸 过量铁粉 滤液 氧化 铁黄
沉铁
硫酸厂 过滤I
酸浸 还原
矿渣
滤渣
资料:i.α-Al?O?化学性质极不活泼,不溶于水也不溶于酸或碱,γ-Al?O?不溶于水,可溶于强
酸或强碱。
ii. Ksp(CaCO?)=2.8×10-?;Ksp(FeCO?)=2×10-11
iii.沉铁过程主要生成FeCO?
下列说法不正确的是
A.取“酸浸”后的溶液滴加 KSCN溶液,溶液变红,发生的反应是Fe3++3SCN·=Fe(SCN)?
B.“滤渣”中主要成分为SiO?、铁粉
C.“沉铁”过程中有副产物Fe(OH)?生成,可能原因是HCO?促进了Fe2+的水解
D.若用CaCO?“沉铁”,则无副产物Fe(OH)?产生,当反应完成时,溶液中c(Ca2+):c(Fe2+)=140
Z20名校联盟(浙江省名校新高考研究联盟)2026届高三第二次联考 化学试题卷 第4 页 共8页非选择题部分
二、非选择题(52分)
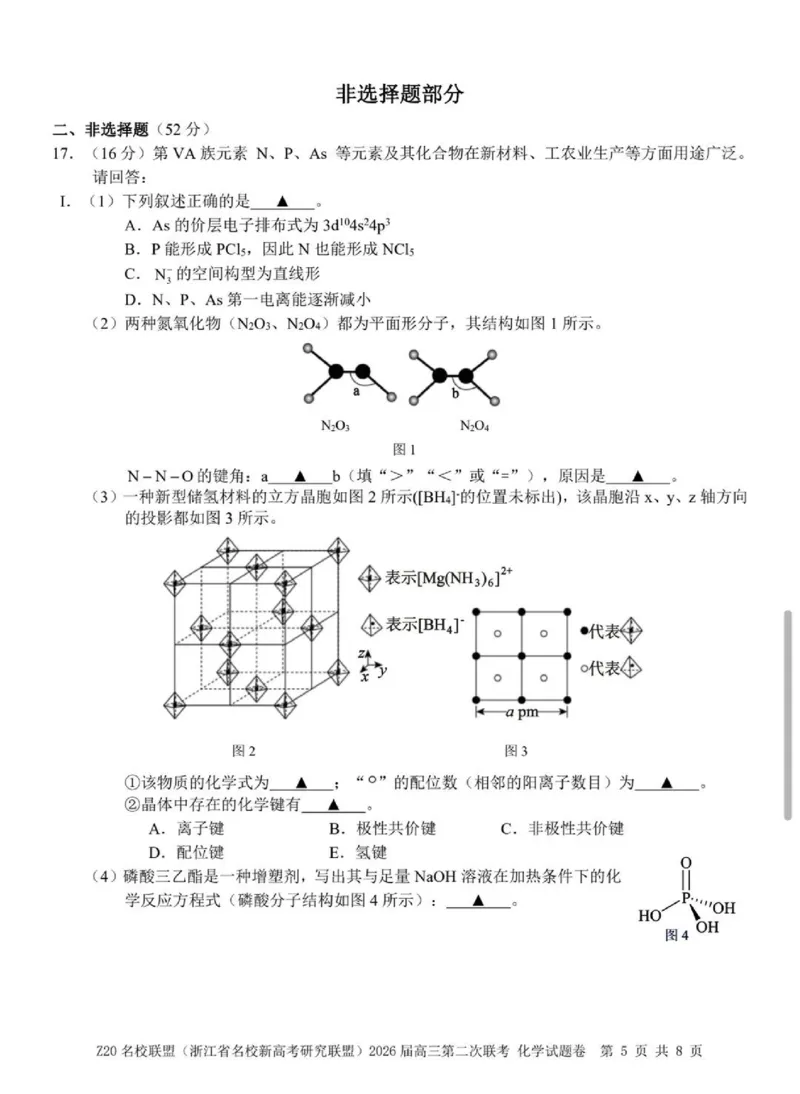
17.(16分)第VA族元素N、P、As等元素及其化合物在新材料、工农业生产等方面用途广泛。
请回答:
I.(1)下列叙述正确的是▲_。
A. As的价层电子排布式为3d104s24p3
B. P能形成PCls,因此N也能形成NCl?
C. N?的空间构型为直线形
D. N、P、As第一电离能逐渐减小
(2)两种氮氧化物(N?O?、N?O?)都为平面形分子,其结构如图1所示。
O
a
b
0
N?O?
N?O?
图1
N-N-O的键角:a ▲_b(填“>”“<”或“=”),原因是▲_。
(3)一种新型储氢材料的立方晶胞如图2所示([BH4]的位置未标出),该晶胞沿x、y、z轴方向
的投影都如图3所示。
表示[Mg(NH?)?]2+
表示[BH?] o o
●代表
Zx个
o o
○代表
y
a pm-
图2 图3
①该物质的化学式为 ▲;“○”的配位数(相邻的阳离子数目)为▲。
②晶体中存在的化学键有 ▲。
A.离子键 B.极性共价键 C.非极性共价键
D.配位键 E.氢键 O=
(4)磷酸三乙酯是一种增塑剂,写出其与足量NaOH溶液在加热条件下的化 oB
学反应方程式(磷酸分子结构如图4所示):▲。
HO
Z20名校联盟(浙江省名校新高考研究联盟)2026届高三第二次联考 化学试题卷 第5 页 共8页IⅡ.砷盐净化工艺成功应用于冶炼锌工业,加快了我国锌冶炼技术改造步伐。从砷盐净化渣(成分为
Cu、As?O?、Zn、ZnO、Co、SiO?等)中回收有价值的金属具有重要意义。
稀H?SO?H?O?、H?SO? Na?AsO? X NaOH
砷盐 选择 氧化
调节pH 沉铜 Cu?H?(AsO?)4·2H?O→碱浸→Cu(OH)?
净化渣 浸Zn 浸出
操作!coc?0?
滤液- 沉钴
浸Zn液 浸渣
Na?C?O?
(5)“氧化浸出”时,As?O?被氧化为H?AsO?4的化学方程式为▲_。
(6)“碱浸”时,除回收得到Cu(OH)?外,还得到物质X,且X在该工艺流程中可循环利用,
X的化学式为▲。
(7) 如何检验“操作1”得到的沉淀已洗涤干净_▲。
18.(12分)氯气、二氧化氯常用于漂白、杀菌,有重要的应用价值。
请回答:
I.(1)氯水中存在以下平衡 Cl?+H?O=HCl+ HCIO,其平衡常数表达式K=▲_。氯水中加
入CaCO?会增大c(HCIO),用平衡移动原理解释其原因▲_。
(2)常温下,将0.1 mol Cl?通入100 mL2 mol/L NaOH溶液中充分吸收,则溶液pH=▲_
(已知 Ka(HCIO)=4.0×10?,1g2≈0.3)
Ⅱ.工业上采用RuO?催化氧化法处理HCI废气,同时实现氯资源循环利用:
2HCI(g)+O2(⑧)—CL(8)+H?O(g)AH?=57.2kJ·mol1,将HCI和02分别以不同起始
流速通入反应器中,在360℃、400℃和440℃下反应,通过检测流出气成分绘制HCl转化率(α)
曲线,如下图1所示,其中较低流速时(≤0.10mol/h)转化率可近似为平衡转化率。
90
HCI的转化率/%
O O
80
甲 Q
N
(0.10,80)
70
T?
O O-T?
n(HCD):n(O?)=4:4
60 -T?
0.18 0.14 0.10 0.06
NaCIO?、H?SO?溶液
HCl流速/(mol/h)
图1 图2
(3)T?= ▲℃。
(4)下列措施可提高N点HC1转化率的是▲(填字母)。
A.增大n(HCl):n(O?) B.将温度适当降低
C.使用更高效的催化剂 D.用分子筛分离H?O(g)
(5)图中较高流速时,α(T?)小于α(T?)和α(T?),原因是▲_。
Ⅲ.(6)含氯化合物二氧化氯CIO?是一种高效安全的消毒剂,其可由图2所示装置制备(电极不反
应)。写出生成CIO?的电极反应方程式为▲。
Z20名校联盟(浙江省名校新高考研究联盟)2026届高三第二次联考 化学试题卷 第6页 共8页19.(12分)氨基甲酸铵(H?NCOONH?)是一种重要的化工原料,可用于药物合成、制备化学肥料、
灭火剂或洗涤剂等。该物质是一种易水解、受热易分解的白色固体,可通过氨气和二氧化碳反
应制备,方程式为:2NH?(g)+CO?(g)—H?NCOONH?(S) △H<0。某化学兴趣小组用如图
所示装置制取氨基甲酸铵。
甲
电动搅拌棒
活塞 a
多孔隔板
而
8
i CCl?-
妻
一冰水
2 6 7
4
1 3 液体石蜡鼓泡瓶 5
实验过程:
I.制备氨基甲酸铵:将干燥的氨气和二氧化碳气体按一定比例通入四氯化碳试剂中,不断搅拌。
控制反应温度在30~40℃,反应生成白色固体。待反应结束后,过滤并干燥产物。
IⅡ.测定产品中氨基甲酸铵的纯度:称取 2.000g的氨基甲酸铵样品。加入 50.00 mL1.000 mol/L
的盐酸(过量),使氨基甲酸铵完全反应。用0.5000 mol/L NaOH标准溶液滴定剩余的盐酸,
消耗NaOH标准溶液的体积为 20.00ml。通过计算确定氨基甲酸铵的纯度。(不考虑杂质
与盐酸和NaOH溶液的反应。)
请回答:
(1)装置甲的名称▲_,装置6中盛放的试剂是▲。
(2)1装置能制备以下哪些气体▲_。
A. CO?(CaCO?+盐酸) B. H?(锌粒+盐酸)
C. C?H?(电石+饱和食盐水) D. Cl?(MnO?+浓盐酸)
(3)液体石蜡鼓泡瓶的作用是▲_。
(4)实验中要控制温度在30~40℃的原因是▲。
(5)下列说法正确的是▲。
A.I中为了得到较干燥的产物,可采用低温烘干的方法
B.Ⅱ滴定过程所加指示剂为酚酞,最后半滴溶液加入后溶液由浅红色变无色且半分钟不
变色,则达到滴定终点
C.Ⅱ滴定读数时,滴定前平视,滴定后仰视可能导致样品纯度测定结果偏低
D. a口只需连接装有碱石灰的干燥管,用于吸收空气中的H?O
(6)制备的氨基甲酸铵的纯度为▲。
Z20名校联盟(浙江省名校新高考研究联盟)2026届高三第二次联考 化学试题卷 第7页 共8页-
一
P
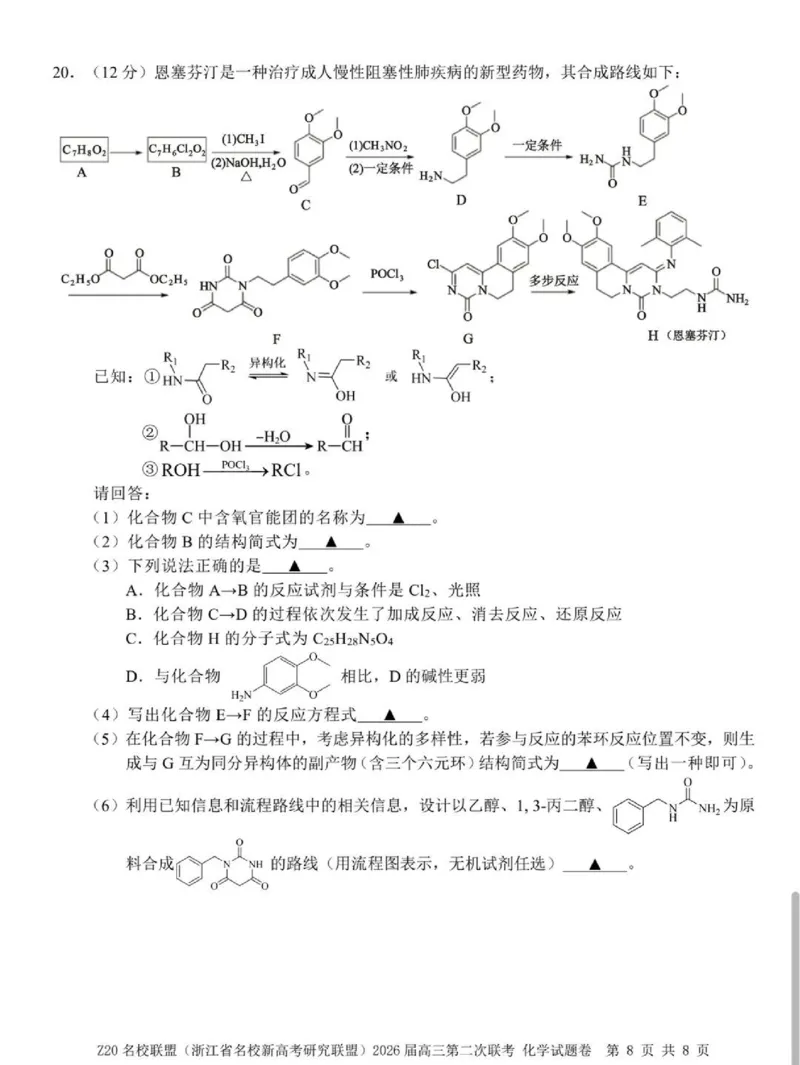
20.(12分)恩塞芬汀是一种治疗成人慢性阻塞性肺疾病的新型药物,其合成路线如下:
p
D E
G H(恩塞芬汀)
已知: 或
②R-CH-0oR-
③ROHPOCl?→RCl。
请回答:
(1)化合物C中含氧官能团的名称为▲_。
(2)化合物B的结构简式为▲。
(3)下列说法正确的是▲_。
A.化合物A→B的反应试剂与条件是Cl?、光照
B.化合物C→D的过程依次发生了加成反应、消去反应、还原反应
C.化合物H的分子式为C??H??N?O?
D.与化合物 相比,D的碱性更弱
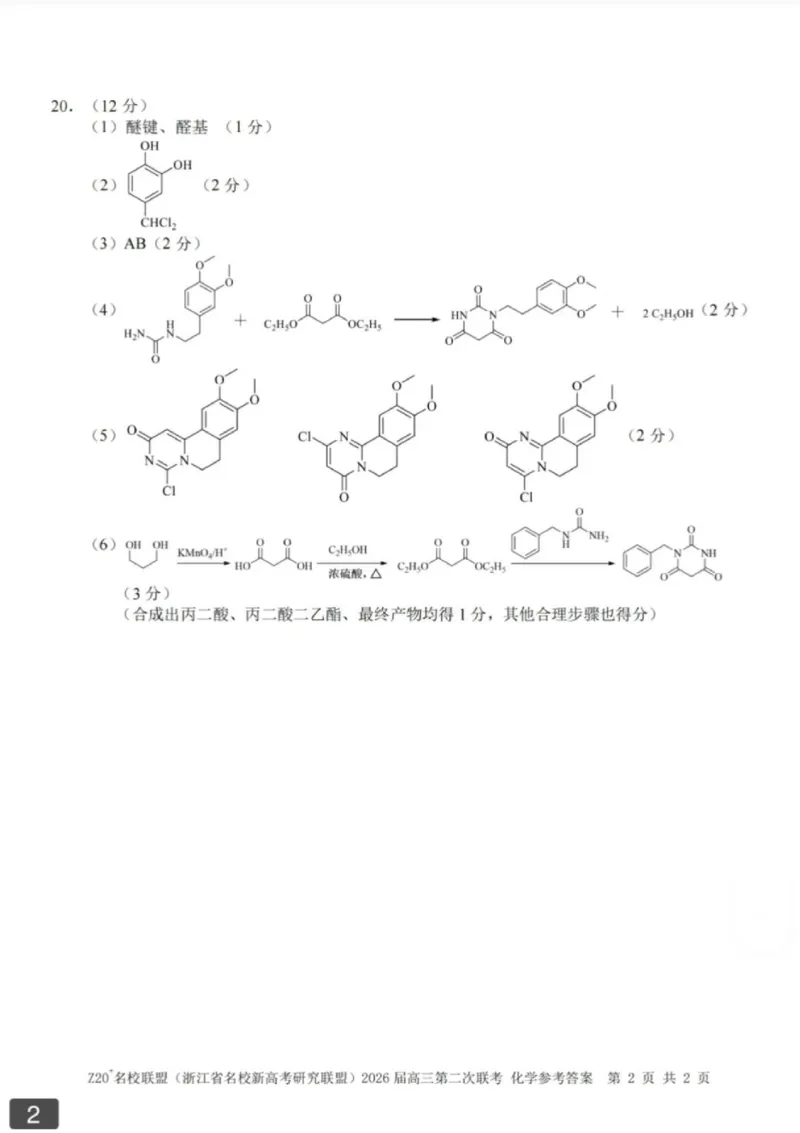
(4)写出化合物E→F的反应方程式 ▲。
(5)在化合物F→G的过程中,考虑异构化的多样性,若参与反应的苯环反应位置不变,则生
成与G互为同分异构体的副产物(含三个六元环)结构简式为▲(写出一种即可)。
(6)利用已知信息和流程路线中的相关信息,设计以乙醇、1,3-丙二醇、 为原
点
料合成 的路线(用流程图表示,无机试剂任选)▲。
Z20名校联盟(浙江省名校新高考研究联盟)2026届高三第二次联考 化学试题卷 第8页 共8页名校联盟
Z20+名校联盟(浙江省名校新高考研究联盟)2026届高三第二次联考
化学参考答案
一、选择题(48分)
1 2 3 4 5 6 7 8
题号
C D B C A B D C
答案
题号 9 10 11 12 13 14 15 16
C B D C C A C B
答案
二、非选择题(共52分)
17.(16分)
(1)CD(2分)
(2)<(1分) 中心原子N 均为sp2杂化,但N?O?中心原子N存在1 对孤对电子,
而N?O?中心原子N无孤对电子,由于孤电子对对成键电子对的斥力较大,故键角a