文档内容
科目:化 学
(试题卷)
注意事项:
1.答题前,考生务必将自己的姓名、准考证号写在答
题卡和本试题卷的封面上,并认真核对答题卡条形码上的
姓名、准考证号和科目。
2.选择题和非选择题均须在答题卡上作答,在本试题
卷和草稿纸上作答无效。考生在答题卡上按答题卡中注意
事项的要求答题。
3.本试卷共 6 页。如缺页,考生须及时报告监考老师,
否则后果自负。
4.考试结束,将本试题卷和答题卡一并交回。
姓 名
准考证号
祝 你 考 试 顺 利 !
化学试卷 第0页 共6页2026 年常德市高三年级模拟考试
化 学
可能用到的相对原子质量:H-1 C-12 O-16 Co-59 Sm-150
一、选择题:本小题共14题,每小题3分,共42分。在每小题给出的四个选项中,只
有一项符合题目要求。
1.2025年我国科技在各领域取得突破性成果。下列说法不正确的是
A.第12届世运会引导员的蜀绣服饰由蚕丝制成,蚕丝的主要成分为蛋白质
B.钍基熔盐实验堆首次实现钍铀燃料转换,钍、铀属于短周期元素
C.高精度模拟计算机芯片的主要成分是Si
D.“福建舰”的舰体材料是合金钢,其硬度高于纯铁
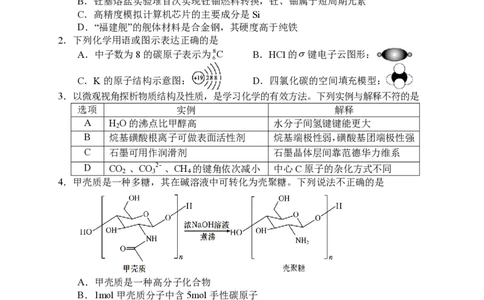
2.下列化学用语或图示表达正确的是
A.中子数为8的碳原子表示为8C B.HCl的σ键电子云图形:
6
C.K的原子结构示意图: D.四氯化碳的空间填充模型:
3.以微观视角探析物质结构及性质,是学习化学的有效方法。下列实例与解释不符的是
选项 实例 解释
A H O的沸点比甲醇高 水分子间氢键键能更大
2
B 烷基磺酸根离子可做表面活性剂 烷基端极性弱,磺酸基团端极性强
C 石墨可用作润滑剂 石墨晶体层间靠范德华力维系
D CO 、CO 2- 、CH 的键角依次减小 中心C原子的杂化方式不同
2 3 4
4.甲壳质是一种多糖,其在碱溶液中可转化为壳聚糖。下列说法不正确的是
A.甲壳质是一种高分子化合物
B.1mol甲壳质分子中含5mol手性碳原子
C.壳聚糖在酸中的溶解性比在水中的强
+
D.壳聚糖与Ag 配位后的产物有抑菌作用
5.新型串联催化剂(Cu-ZSM-5@Ru/S-1)可催化氧化含氯挥发性有机物 CH Cl ,其反应
2 2
原理为2CH Cl +3O 2CO +2H O+2Cl ,N 为阿伏加德罗常数的值。下列有
2 2 2 2 2 2 A
关说法正确的是
A.标准状况下,2.24L CH Cl 含有的分子数为0.1N
2 2 A
B.反应中氧化产物只有CO ,还原产物只有H O
2 2
C.该反应每生成3.6gH O转移的电子数为1.2N
2 A
D.Cu-ZSM-5@Ru/S-1可降低反应的反应热,加快反应速率
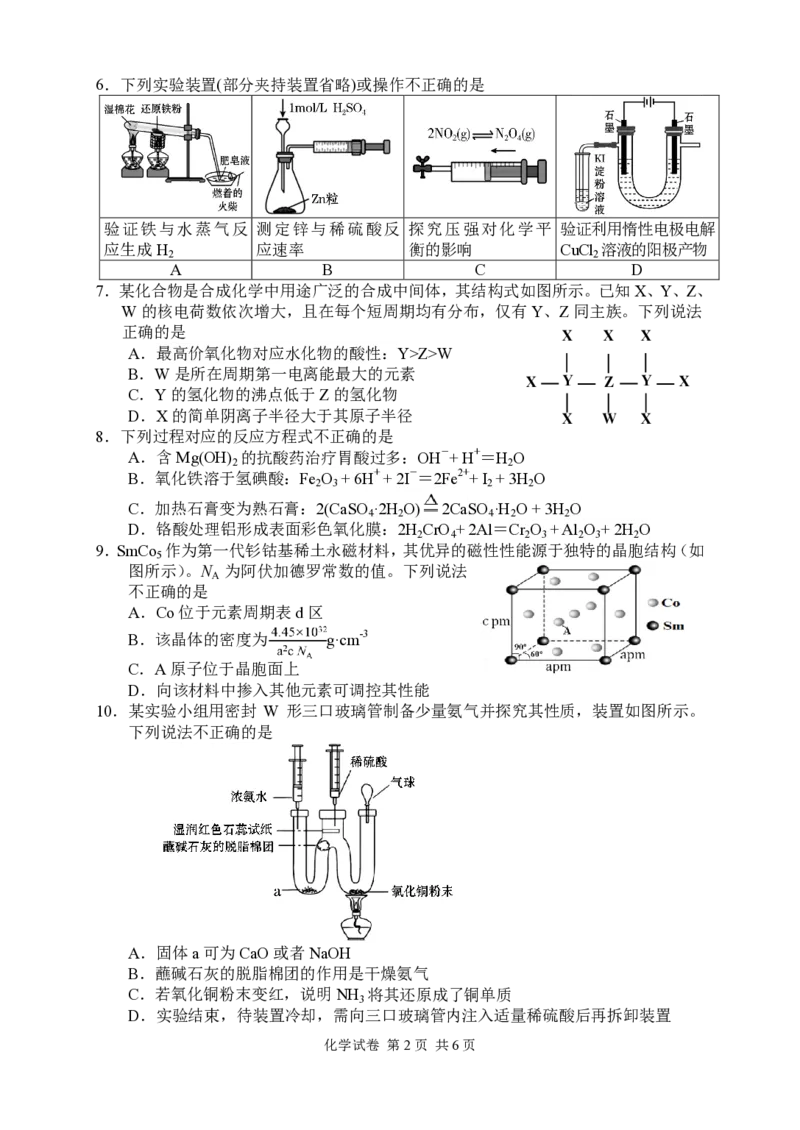
化学试卷 第1页 共6页6.下列实验装置(部分夹持装置省略)或操作不正确的是
验证铁与水蒸气反 测定锌与稀硫酸反 探究压强对化学平 验证利用惰性电极电解
应生成H 应速率 衡的影响 CuCl 溶液的阳极产物
2 2
A B C D
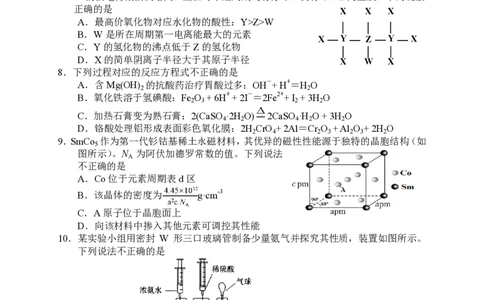
7.某化合物是合成化学中用途广泛的合成中间体,其结构式如图所示。已知X、Y、Z、
W的核电荷数依次增大,且在每个短周期均有分布,仅有Y、Z同主族。下列说法
正确的是
X X X
A.最高价氧化物对应水化物的酸性:Y>Z>W
B.W是所在周期第一电离能最大的元素
X Y Z Y X
C.Y的氢化物的沸点低于Z的氢化物
D.X的简单阴离子半径大于其原子半径
X W X
8.下列过程对应的反应方程式不正确的是
A.含Mg(OH) 的抗酸药治疗胃酸过多:OH-+ H+=H O
2 2
B.氧化铁溶于氢碘酸:Fe O + 6H+ + 2I-=2Fe2++ I + 3H O
2 3 2 2
C.加热石膏变为熟石膏:2(CaSO ·2H O) 2CaSO ·H O + 3H O
4 2 4 2 2
D.铬酸处理铝形成表面彩色氧化膜:2H CrO + 2Al=Cr O + Al O + 2H O
2 4 2 3 2 3 2
9.SmCo 作为第一代钐钴基稀土永磁材料,其优异的磁性性能源于独特的晶胞结构(如
5
图所示)。N 为阿伏加德罗常数的值。下列说法
A
不正确的是
A.Co位于元素周期表d区
B.该晶体的密度为 g·cm-3
C.A原子位于晶胞面上
D.向该材料中掺入其他元素可调控其性能
10.某实验小组用密封 W 形三口玻璃管制备少量氨气并探究其性质,装置如图所示。
下列说法不正确的是
A.固体a可为CaO或者NaOH
B.蘸碱石灰的脱脂棉团的作用是干燥氨气
C.若氧化铜粉末变红,说明NH 将其还原成了铜单质
3
D.实验结束,待装置冷却,需向三口玻璃管内注入适量稀硫酸后再拆卸装置
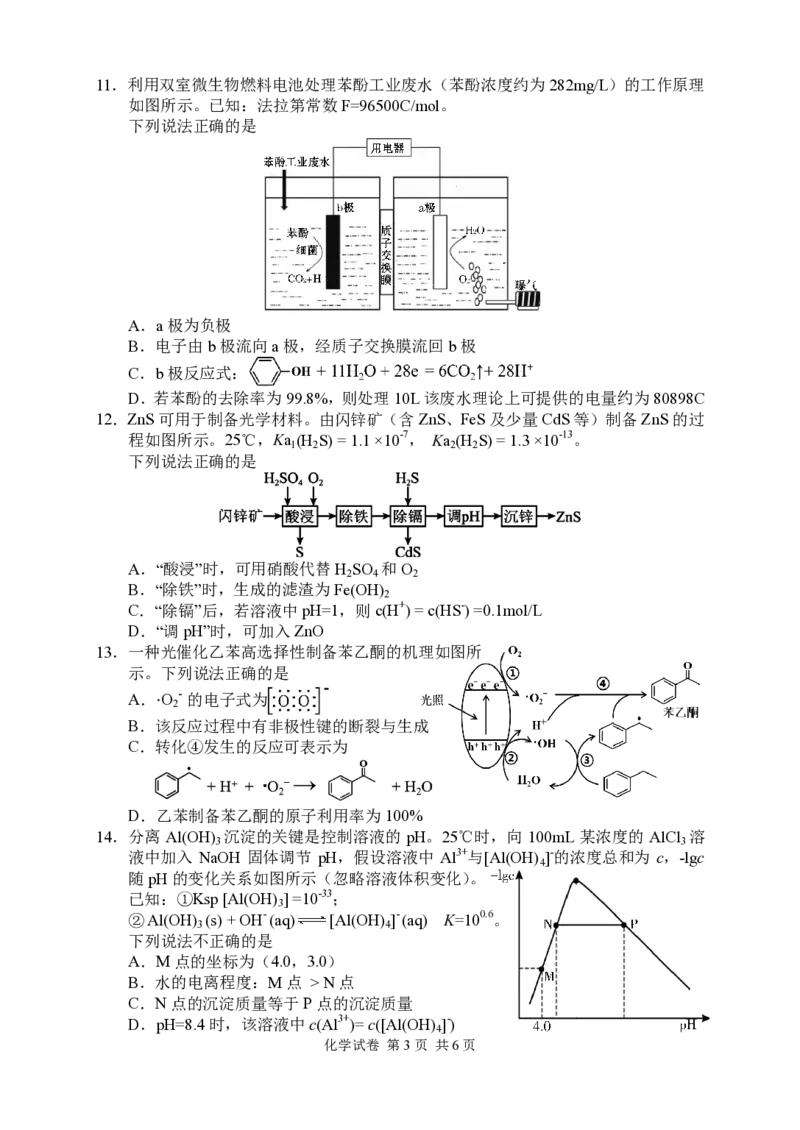
化学试卷 第2页 共6页11.利用双室微生物燃料电池处理苯酚工业废水(苯酚浓度约为282mg/L)的工作原理
如图所示。已知:法拉第常数F=96500C/mol。
下列说法正确的是
A.a极为负极
B.电子由b极流向a极,经质子交换膜流回b极
C.b极反应式:
D.若苯酚的去除率为99.8%,则处理10L该废水理论上可提供的电量约为80898C
12.ZnS可用于制备光学材料。由闪锌矿(含ZnS、FeS及少量CdS等)制备ZnS的过
程如图所示。25℃,Ka (H S) = 1.1 ×10-7, Ka (H S) = 1.3 ×10-13。
1 2 2 2
下列说法正确的是
A.“酸浸”时,可用硝酸代替H SO 和O
2 4 2
B.“除铁”时,生成的滤渣为Fe(OH)
2
C.“除镉”后,若溶液中pH=1,则c(H+) = c(HS-) =0.1mol/L
D.“调pH”时,可加入ZnO
13.一种光催化乙苯高选择性制备苯乙酮的机理如图所
示。下列说法正确的是
A.·O - 的电子式为
2
B.该反应过程中有非极性键的断裂与生成
C.转化④发生的反应可表示为
D.乙苯制备苯乙酮的原子利用率为100%
14.分离 Al(OH) 沉淀的关键是控制溶液的 pH。25℃时,向 100mL 某浓度的 AlCl 溶
3 3
液中加入 NaOH 固体调节 pH,假设溶液中 Al3+与[Al(OH) ]-的浓度总和为 c,-lgc
4
随pH的变化关系如图所示(忽略溶液体积变化)。
已知:①Ksp [Al(OH) ] =10-33;
3
② Al(OH) (s) + OH- (aq) [Al(OH) ]- (aq) K=100.6。
3 4
下列说法不正确的是
A.M点的坐标为(4.0,3.0)
B.水的电离程度:M点 > N点
C.N点的沉淀质量等于P点的沉淀质量
D.pH=8.4时,该溶液中c(Al3+)= c([Al(OH) ]-)
4
化学试卷 第3页 共6页二、非选择题:本部分共四题,共58分
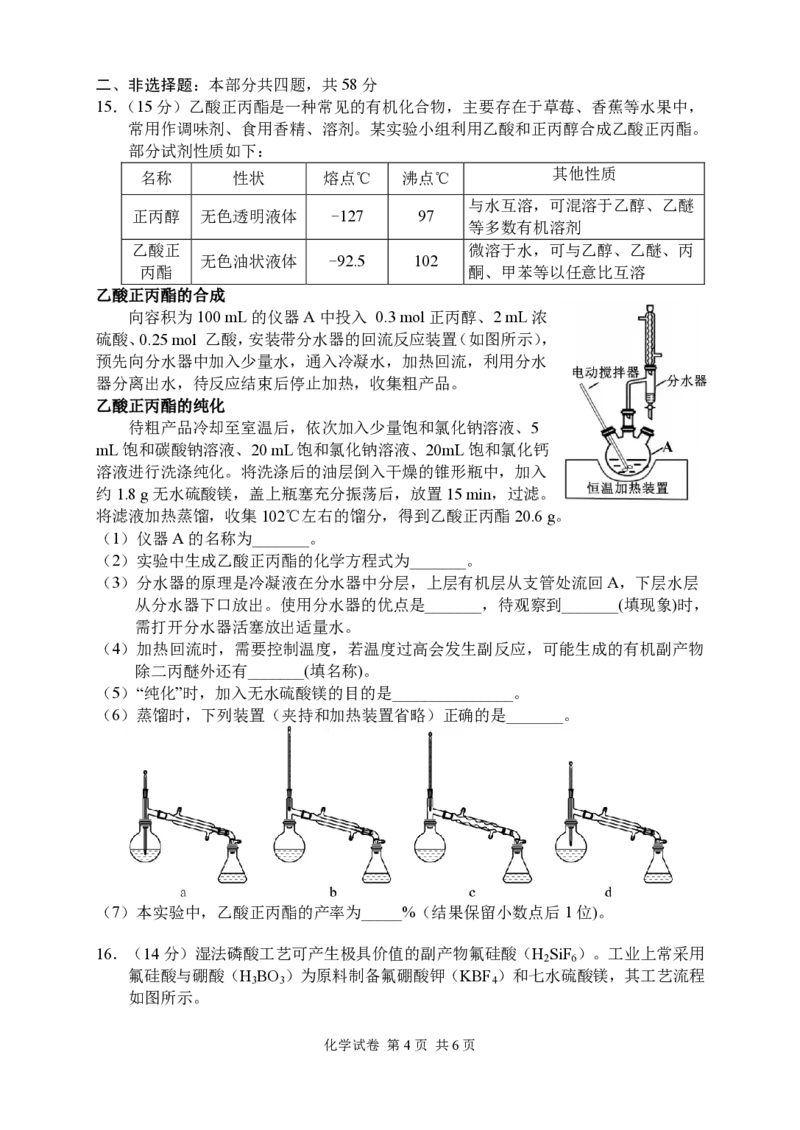
15.(15分)乙酸正丙酯是一种常见的有机化合物,主要存在于草莓、香蕉等水果中,
常用作调味剂、食用香精、溶剂。某实验小组利用乙酸和正丙醇合成乙酸正丙酯。
部分试剂性质如下:
名称 性状 熔点℃ 沸点℃ 其他性质
与水互溶,可混溶于乙醇、乙醚
正丙醇 无色透明液体 -127 97
等多数有机溶剂
乙酸正 微溶于水,可与乙醇、乙醚、丙
无色油状液体 -92.5 102
丙酯 酮、甲苯等以任意比互溶
乙酸正丙酯的合成
向容积为100 mL的仪器A中投入 0.3 mol正丙醇、2 mL浓
硫酸、0.25 mol 乙酸,安装带分水器的回流反应装置(如图所示),
预先向分水器中加入少量水,通入冷凝水,加热回流,利用分水
器分离出水,待反应结束后停止加热,收集粗产品。
乙酸正丙酯的纯化
待粗产品冷却至室温后,依次加入少量饱和氯化钠溶液、5
mL饱和碳酸钠溶液、20 mL饱和氯化钠溶液、20mL饱和氯化钙
溶液进行洗涤纯化。将洗涤后的油层倒入干燥的锥形瓶中,加入
约1.8 g无水硫酸镁,盖上瓶塞充分振荡后,放置15 min,过滤。
将滤液加热蒸馏,收集102℃左右的馏分,得到乙酸正丙酯20.6 g。
(1)仪器A的名称为_______。
(2)实验中生成乙酸正丙酯的化学方程式为_______。
(3)分水器的原理是冷凝液在分水器中分层,上层有机层从支管处流回A,下层水层
从分水器下口放出。使用分水器的优点是_______,待观察到_______(填现象)时,
需打开分水器活塞放出适量水。
(4)加热回流时,需要控制温度,若温度过高会发生副反应,可能生成的有机副产物
除二丙醚外还有_______(填名称)。
(5)“纯化”时,加入无水硫酸镁的目的是_______________。
(6)蒸馏时,下列装置(夹持和加热装置省略)正确的是_______。
(7)本实验中,乙酸正丙酯的产率为_____%(结果保留小数点后1位)。
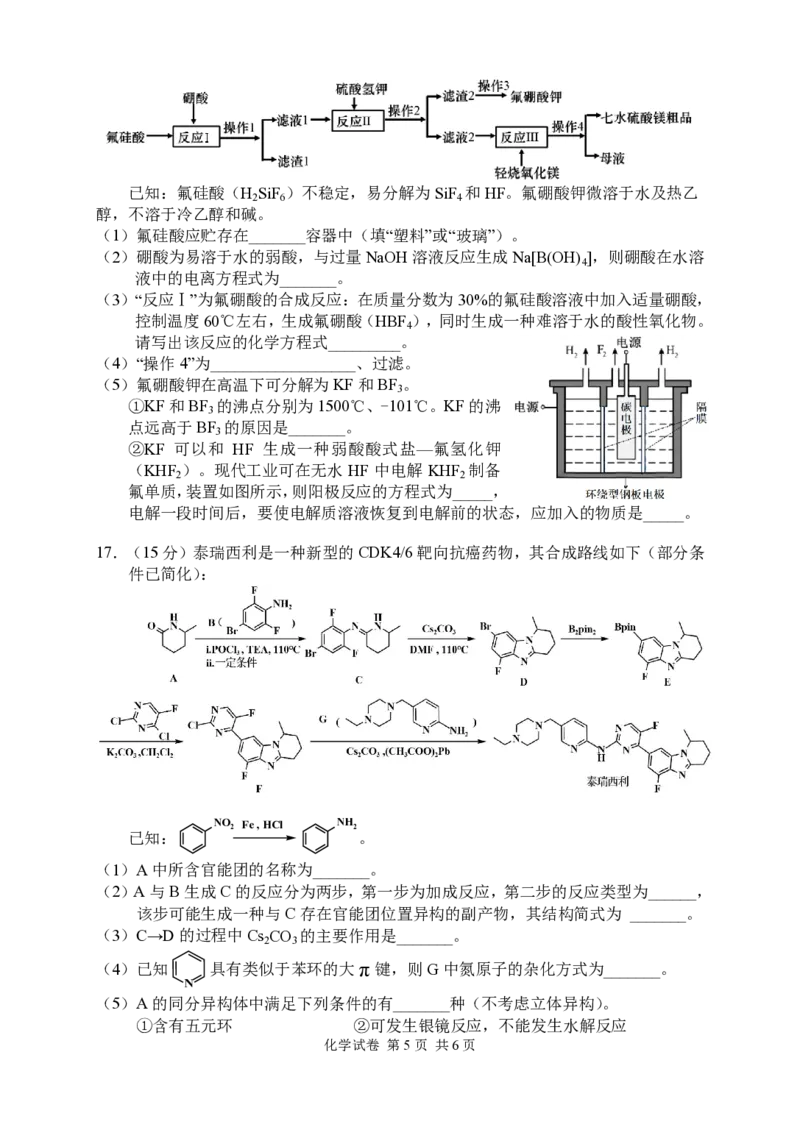
16.(14分)湿法磷酸工艺可产生极具价值的副产物氟硅酸(H SiF )。工业上常采用
2 6
氟硅酸与硼酸(H BO )为原料制备氟硼酸钾(KBF )和七水硫酸镁,其工艺流程
3 3 4
如图所示。
化学试卷 第4页 共6页已知:氟硅酸(H SiF )不稳定,易分解为SiF 和HF。氟硼酸钾微溶于水及热乙
2 6 4
醇,不溶于冷乙醇和碱。
(1)氟硅酸应贮存在_______容器中(填“塑料”或“玻璃”)。
(2)硼酸为易溶于水的弱酸,与过量NaOH溶液反应生成Na[B(OH) ],则硼酸在水溶
4
液中的电离方程式为_______。
(3)“反应Ⅰ”为氟硼酸的合成反应:在质量分数为30%的氟硅酸溶液中加入适量硼酸,
控制温度60℃左右,生成氟硼酸(HBF ),同时生成一种难溶于水的酸性氧化物。
4
请写出该反应的化学方程式_________。
(4)“操作4”为__________________、过滤。
(5)氟硼酸钾在高温下可分解为KF和BF 。
3
①KF和BF 的沸点分别为1500℃、-101℃。KF的沸
3
点远高于BF 的原因是_______。
3
②KF 可以和 HF 生成一种弱酸酸式盐—氟氢化钾
(KHF )。现代工业可在无水 HF 中电解 KHF 制备
2 2
氟单质,装置如图所示,则阳极反应的方程式为_____,
电解一段时间后,要使电解质溶液恢复到电解前的状态,应加入的物质是_____。
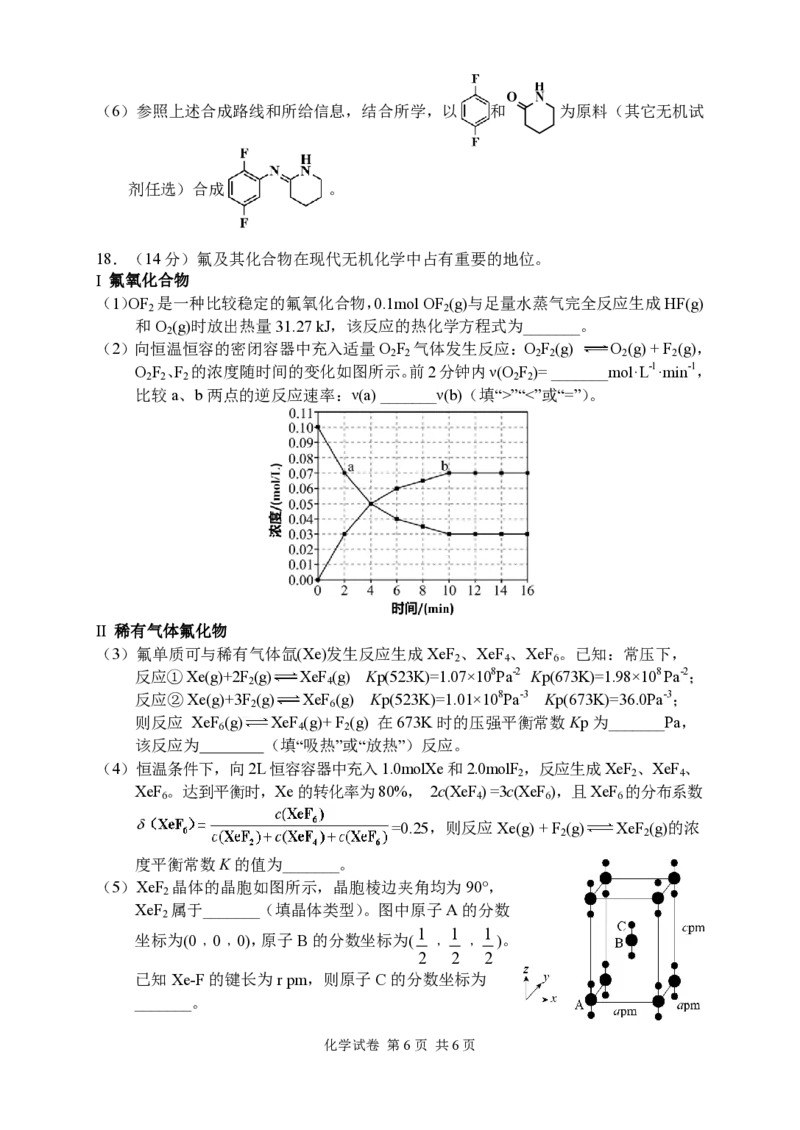
17.(15分)泰瑞西利是一种新型的CDK4/6靶向抗癌药物,其合成路线如下(部分条
件已简化):
NO 2 Fe , HCl NH 2
已知: 。
(1)A中所含官能团的名称为_______。
(2)A与B生成C的反应分为两步,第一步为加成反应,第二步的反应类型为______,
该步可能生成一种与C存在官能团位置异构的副产物,其结构简式为 _______。
(3)C→D的过程中Cs CO 的主要作用是_______。
2 3
(4)已知 具有类似于苯环的大π 键,则G中氮原子的杂化方式为_______。
N
(5)A的同分异构体中满足下列条件的有_______种(不考虑立体异构)。
①含有五元环 ②可发生银镜反应,不能发生水解反应
化学试卷 第5页 共6页H
O N
(6)参照上述合成路线和所给信息,结合所学,以 和 为原料(其它无机试
剂任选)合成 。
18.(14分)氟及其化合物在现代无机化学中占有重要的地位。
I 氟氧化合物
(1)OF 是一种比较稳定的氟氧化合物,0.1mol OF (g)与足量水蒸气完全反应生成HF(g)
2 2
和O (g)时放出热量31.27 kJ,该反应的热化学方程式为_______。
2
(2)向恒温恒容的密闭容器中充入适量O F 气体发生反应:O F (g) O (g) + F (g),
2 2 2 2 2 2
O F 、F 的浓度随时间的变化如图所示。前2分钟内ν(O F )= _______mol·L-1·min-1,
2 2 2 2 2
比较a、b两点的逆反应速率:ν(a) _______ν(b)(填“>”“<”或“=”)。
II 稀有气体氟化物
(3)氟单质可与稀有气体氙(Xe)发生反应生成XeF 、XeF 、XeF 。已知:常压下,
2 4 6
反应① Xe(g)+2F (g) XeF (g) Kp(523K)=1.07×108Pa-2 Kp(673K)=1.98×108 Pa-2;
2 4
反应② Xe(g)+3F (g) XeF (g) Kp(523K)=1.01×108Pa-3 Kp(673K)=36.0Pa-3;
2 6
则反应 XeF (g) XeF (g)+ F (g) 在673K时的压强平衡常数Kp为_______Pa,
6 4 2
该反应为 (填“吸热”或“放热”)反应。
(4)恒温条件下,向2L恒容容器中充入1.0molXe和2.0molF,反应生成XeF 、XeF、
2 2 4
XeF。达到平衡时,Xe的转化率为80%, 2c(XeF ) =3c(XeF),且XeF 的分布系数
6 4 6 6
=0.25,则反应Xe(g) + F (g) XeF (g)的浓
2 2
度平衡常数K的值为_______。
(5)XeF 晶体的晶胞如图所示,晶胞棱边夹角均为90°,
2
XeF 属于_______(填晶体类型)。图中原子A的分数
2
坐标为(0﹐0﹐0),原子B的分数坐标为( 1﹐1﹐1 )。
2 2 2
已知Xe-F的键长为r pm,则原子C的分数坐标为
_______。
化学试卷 第6页 共6页