文档内容
2025-2026 学年下期高 2026届二诊模拟测试
化学 试卷
可能用到的相对原子质量:H-1 C-12 O-16 Cl-35.5 S-32 K-39 Fe-56 Se-79 Bi-209
一、选择题:本题共 15小题,每小题 3分,共 45分。每小题只有一项符合题目要求。
1.科技发展与化学密切相关。下列说法错误的是
A.福建舰舰体材料无磁镍铬钛合金钢硬度高于纯铁
B.神舟十七号使用砷化镓(GaAs)太阳能电池,供电时的能量转化形式为化学能转化为电能
C.量子科技“墨子号”使用光纤作为地面传输材料,光纤的主要成分属于新型无机非金属材料
D.中国研制的先进微纳米光刻机,其原材料之一四甲基氢氧化铵[(CH ) NOH]可溶于水
3 4
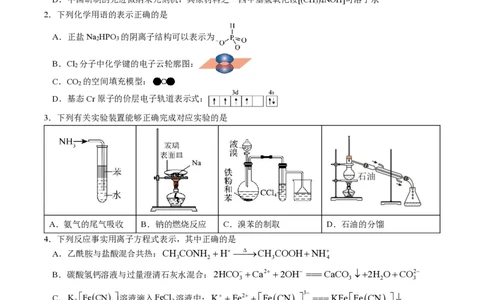
2.下列化学用语的表示正确的是
A.正盐Na HPO 的阴离子结构可以表示为
2 3
B.Cl 分子中化学键的电子云轮廓图:
2
C.CO 的空间填充模型:
2
D.基态Cr原子的价层电子轨道表示式:
3.下列有关实验装置能够正确完成对应实验的是
A.氨气的尾气吸收 B.钠的燃烧反应 C.溴苯的制取 D.石油的分馏
4.下列反应事实用离子方程式表示,其中正确的是
A.乙酰胺与盐酸混合共热:
1
C H
3
C O N H
2
+ H + ⎯ ⎯ → C H
3
C O O H + N H +4
B.碳酸氢钙溶液与过量澄清石灰水混合: 2 H C O −3 + C a 2 + + 2 O H − = = = C a C O
3
+ 2 H
2
O + C O 23 −
C. K
3
F e ( C N )
6
溶液滴入 F e C l
2
溶液中: K + + F e 2 + + F e ( C N )
6
3 − = = = K F e F e ( C N )
6
D. K
2
C r2 O
7
检测酒驾的反应原理: C
2
H
5
O H + 2 C r
2
O 27 − + 1 6 H + = = = 2 C O
2
+ 4 C r 3 + + 1 1 H
2
O
5.配位化合物广泛应用于物质分离、定量测定、医药、催化等方面。利用氧化法可制备某些配位化合
物,如 2 C o C l
2
+ 2 N H
4
C l + 8 N H
3
+ H
2
O
2
= = = 2 C o ( N H
3
)
5
C l C l
2
+ 2 H
2
O 。设N 为阿伏加德罗常数
A
的值,下列说法正确的是
A.1mol Co(NH ) ClCl 中含有键的数目为22 N
3 5 2 A
B.H-N-H的键角大小:NH < [Co(NH ) Cl]2+
3 3 5
C.0.1mol N 与足量H 在催化剂作用下合成氨,生成的NH 分子数为0.2 N
2 2 3 A
D.36 g 冰中所含的氢键的数目为2 N
A11.某温度下发生反应:2M(g) N(g),M和N的消耗速率与本身浓度的关系如图,已知:
3
v
消 耗
( M ) = k
1
c 2 ( M ) , v
消 耗
( N ) = k
2
c ( N ) , k
1
和 k
2
是速率常数,只与温度、催化剂有关。下列说法正确的是
A.曲线y代表的是 v
消 耗
( N )
B.其他条件不变,压缩容器体积,体系内活化分子百分数增大
C.此温度下,该反应的平衡常数 K =
k
2
2k
1
D.密闭容器中进行该反应,P点时反应逆向进行
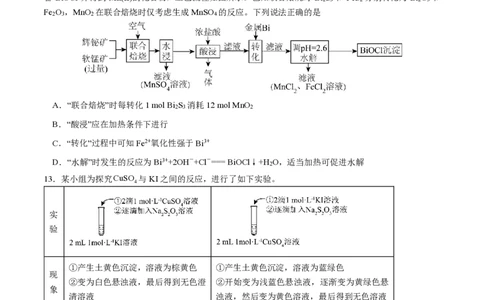
12.某工厂采用辉铋矿(主要成分为Bi S ,含有FeS 、SiO 杂质)与软锰矿(主要成分为MnO )联合焙烧法制
2 3 2 2 2
备 BiOCl 并得到 Mn(II)的化合物,工艺流程如图所示。已知联合焙烧时 Bi S 和 FeS 分别转化为 Bi O 和
2 3 2 2 3
Fe O ,MnO 在联合焙烧时仅考虑生成MnSO 的反应。下列说法正确的是
2 3 2 4
A.“联合焙烧”时每转化1 mol Bi S 消耗12 mol MnO
2 3 2
B.“酸浸”应在加热条件下进行
C.“转化”过程中可知Fe2+氧化性强于Bi3+
D.“水解”时发生的反应为Bi3++2OH-+Cl-=== BiOCl↓+H O,适当加热可促进水解
2
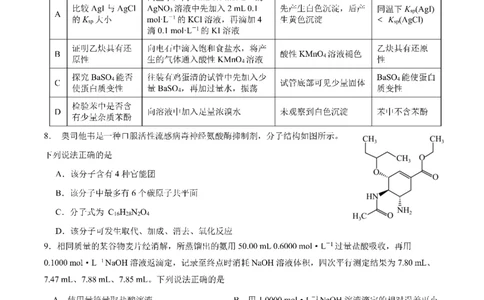
13.某小组为探究 C u S O
4
与KI之间的反应,进行了如下实验。
实
验
①产生土黄色沉淀,溶液为棕黄色 ①产生土黄色沉淀,溶液为蓝绿色
现
②变为白色悬浊液,最后得到无色澄 ②开始变为浅蓝色悬浊液,逐渐变为黄绿色悬
象
清溶液 浊液,然后变为黄色溶液,最后得到无色溶液
已知:2S O2−(无色)+I ===2I− +S O2−(无色);CuI为白色沉淀,可吸附
2 3 2 4 6
I
2
;CuI 在溶液中不存在;
2
Cu(S O ) 3−呈无色,Cu(S O ) 2−呈黄色。下列结论或推断错误的是
2 3 2 2 3 2
A.CuSO 与KI能发生反应:
4
2 C u 2 + + 4 I − = = = 2 C u I + I
2
B.CuI与Na S O 反应的速率慢于I 与Na S O 反应的速率
2 2 3 2 2 2 3
C.黄绿色悬浊液变为黄色溶液时,有Cu(S O ) 3−、Cu(S O ) 2−生成
2 3 2 2 3 2
D. Cu(Ⅱ)与S O2−生成配合物反应的限度大于二者发生氧化还原反应的限度
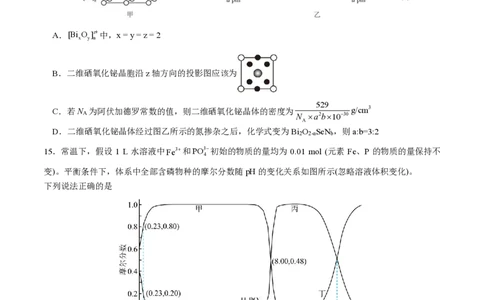
2 314.近年来,二维硒氧化铋因其稳定性好、载流子迁移率高等优点,被广泛应用于各种电子设备。研究人员
发现,与石墨烯等二维材料不同,二维硒氧化铋的
4
[ B i
x
O
y
] zn + 层与 S e 2
n
n - 层之间是通过弱静电力而非范德华
力维系。如图甲是二维硒氧化铋的结构示意图,图乙为其晶胞结构和氮掺杂后的结构。下列说法正确的是
A. [ B i
x
O
y
] z+n 中,x= y = z = 2
B.二维硒氧化铋晶胞沿z轴方向的投影图应该为
C.若N 为阿伏加德罗常数的值,则二维硒氧化铋晶体的密度为
A N
A
5
a
2
2 b
9
1 0 − 3 0
g / c m 3
D.二维硒氧化铋晶体经过图乙所示的氮掺杂之后,化学式变为Bi O SeN ,则a:b=3:2
2 2-a b
15.常温下,假设 1 L 水溶液中Fe3+和 P O 3−4 初始的物质的量均为 0.01 mol (元素 Fe、P 的物质的量保持不
变)。平衡条件下,体系中全部含磷物种的摩尔分数随pH的变化关系如图所示(忽略溶液体积变化)。
下列说法正确的是
已知 K
sp
( F e P O
4
) = 9 .9 1 0 − 1 6 , K
sp
F e ( O H )
3
= 1 0 − 3 8 。
A.丙线所示物种为 F e P O
4
B.H PO 的电离常数K 约为1.210−8
3 4 a2
C.pH=0.23时,c ( Fe3+) =0.002molL−1,不产生Fe(OH) 沉淀
3
D.pH=0.1时,c
( H+)
+3c
( Fe3+)
=3c
( PO3−)
+2c
( HPO2−)
+c
(
H
PO−)
+c
( OH−)
4 4 2 4二、非选择题:本题共 4小题,共 55分
16.二茂铁[Fe(C H ) ]是一种具有芳香族化合物性质的有机过渡金属化合物。二茂铁的熔点是173℃,在
5 5 2
100℃时开始升华,沸点是249℃,不溶于水,易溶于苯、乙醚、汽油、柴油等有机溶剂;化学性质稳定,
400℃以内不分解。
实验室制备二茂铁的装置示意图
环戊二烯和二茂铁的结构 提纯过程示意图
(夹持及加热装置略)
图1 图2 图3
实验步骤如下:
步骤1:在三颈烧瓶中加入25 g粉末状的KOH,并从仪器a中加入60 mL无水乙醚到三颈烧瓶中,充分
搅拌,同时通氮气约10 min;
步骤2:再从仪器a滴入5.5mL新蒸馏的环戊二烯 (密度0.95g/cm3),搅拌;
步骤3:将6.5 g无水FeCl 与(CH ) SO (二甲基亚砜,作溶剂)配成的溶液25 mL装入仪器a中,慢慢滴入
2 3 2
三颈烧瓶中,45 min滴完,继续搅拌45 min;
步骤4:再从仪器a加入25 mL无水乙醚搅拌,将液体经过“一系列操作”,得到二茂铁粗产品。
请回答下列问题:
(1)写出KOH、FeCl 、C H 反应生成二茂铁[Fe(C H ) ]的化学方程式: 。
2 5 6 5 5 2
(2)二茂铁[Fe(C H ) ]中,环戊二烯阴离子(C H -)以大π键电子参与配
5 5 2 5 5
位,二茂铁中配体提供给Fe2+形成配位键的电子有_______个。早期人们将
二茂铁的结构误认为右图,现代核磁共振法能够区分这两种结构,在核磁
共振氢谱中,正确的结构有___________组峰(选填序号,下同),错误的结构有___________组峰。
A.1 B.2 C.3 D.4 E.5
(3)仪器a的名称是 。
(4)步骤4中的“一系列操作”如下,请排序:
将液体转入分液漏斗→_______→_______→⑤→_______→_______
①用水洗涤2次并分液 ②过滤 ③用盐酸洗涤2次并分液 ④蒸出乙醚后得到产品 ⑤加入无水Na SO
2 4
(5)二茂铁粗产品提纯过程在图3所示装置中进行,其分离方法名称为 ,该操作中棉花的作用是
__________________________________________。
(6)若最终得到纯净的二茂铁4.8 g,则该实验的产率为 %(保留两位有效数字)。
517.锆(Zr)是一种稀有金属,广泛用在航空航天、军工、核反应、原子能领域。一种以锆英砂(主要含
ZrSiO ,还含有少量Cr、Fe、Hf等元素)为原料生产金属锆和副产物硅酸钙的工艺流程如下:
4
已知:①“酸溶”后各金属元素在溶液中的存在形式为
6
Z r O 2 + 、 H f O 2 + 、Fe3+、 C r 3 + 。
②25℃时, K
sp
F e ( O H )
3
= 1 0 − 3 8 , K
b
( N H
3
H
2
O ) = 1 .8 1 0 − 5 ;
③部分氯化物的沸点数据如表所示:
物质 ZrCl CrCl FeCl FeCl
4 3 3 2
沸点/℃ 331 1300 316 700
回答下列问题:
(1)Zr是 T i 的同族相邻元素,基态Zr原子的价电子排布式是
___________。
(2)“碱熔”时生成可以溶于水的钠盐的化学式
为: ,温度和时间对锆英砂碱熔分解率的影响如图
所示,应采取的条件为 。
(3)“萃取”时,锆元素与萃取剂形成多种络合物,写出生成 Z r ( N O
3
)
2
C l
2
2 T O P O 的离子方程式为:
_______________________,“萃取”操作除去的杂质元素为 。
(4)“氨沉”时产物为Zr(OH) 、Cr(OH) 和
4 3
F e ( O H )
3
,反应结束后溶液中
c (
c
N
(
H
N
3
H
+4
H
)
2
O )
= 1 .8 1 0 5 ,
则 c ( F e 3 + ) = molL−1,“滤液2”中主要成分是 (填名称)。
(5)“煅烧”时 Z r ( O H )
4
分解生成 Z r O
2
,“沸腾氯化”中反应①为“氯化反应”,请写出 Z r O
2
参与该反应
的化学方程式: ,氯化反应结束通入 H
2
,目的是 。
18.CO 的捕集、利用与封存(CCUS)被国际能源署列为实现全球净零排放的关键技术,包括从能源利用等
2
工业过程或大气中捕集分离CO 并加以资源化利用的过程。
2
(1)化学链燃烧是一种通过载氧体实现燃料与空气的无接触燃烧方式,可有效捕集含碳物质燃烧时产生的
CO 。基于CaSO 载氧体的CO化学链燃烧原理为反应I和反应II,同时体系中还存在副反应为反应III
2 4
反应I.CaSO (s)+4CO(g) CaS(s)+4CO (g) ΔH = -175.6kJmol-1。
4 2 1
反应II.CaS(s)+2O (g)===CaSO (s) ΔH = - 956.4kJmol-1。
2 4 2
反应III.CaSO (s)+CO(g) CaO(s)+SO (g)+CO (g) ΔH =+218.4kJmol-1
4 2 2 3①写出表示
7
C O 燃烧热的热化学方程式 。
②为减小平衡时
c
c
(( S
C
O
O
2
2
))
,可以采取的措施有 (填字母)。
a.在合适的温度区间内降低反应温度 b.在恒温恒容条件下提高 C O 的初始投料
c.在恒温恒压条件下往初始投料中添加适量Ar d.加入对反应I有利的催化剂
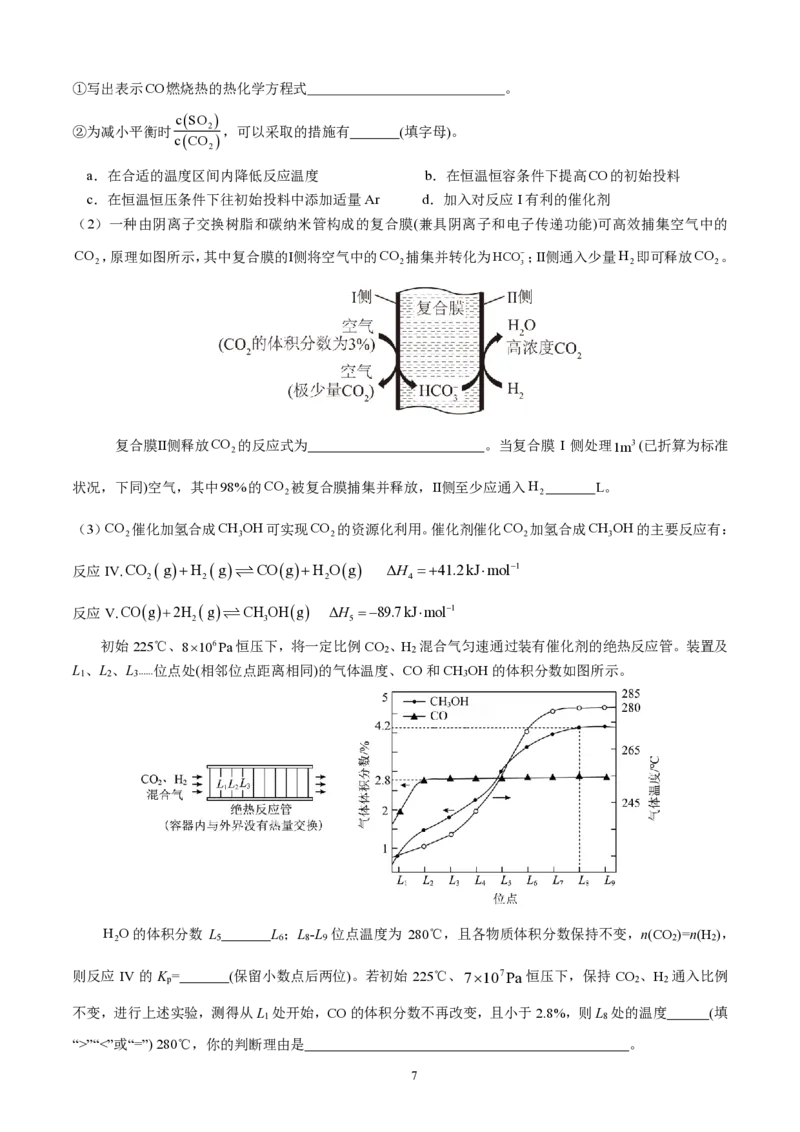
(2)一种由阴离子交换树脂和碳纳米管构成的复合膜(兼具阴离子和电子传递功能)可高效捕集空气中的
C O
2
,原理如图所示,其中复合膜的Ⅰ侧将空气中的 C O
2
捕集并转化为 H C O −3 ;Ⅱ侧通入少量H 即可释放CO 。
2 2
复合膜Ⅱ侧释放 C O
2
的反应式为 。当复合膜 I 侧处理1m3(已折算为标准
状况,下同)空气,其中 9 8 % 的 C O
2
被复合膜捕集并释放,Ⅱ侧至少应通入H L。
2
(3) C O
2
催化加氢合成 C H
3
O H 可实现 C O
2
的资源化利用。催化剂催化 C O
2
加氢合成 C H
3
O H 的主要反应有:
反应IV. C O
2
( g ) + H
2
( g ) C O ( g ) + H
2
O ( g ) Δ H
4
= + 4 1 .2 k J m o l − 1
反应V. C O ( g ) + 2 H
2
( g ) C H
3
O H ( g ) Δ H
5
= − 8 9 .7 k J m o l − 1
初始225℃、 8 1 0 6 P a 恒压下,将一定比例CO 、H 混合气匀速通过装有催化剂的绝热反应管。装置及 2 2
L 、L 、L 位点处(相邻位点距离相同)的气体温度、CO和CH OH的体积分数如图所示。
1 2 3…… 3
H
2
O 的体积分数 L L ;L -L 位点温度为 280℃,且各物质体积分数保持不变,n(CO )=n(H ),
5 6 8 9 2 2
则反应 IV 的 K = (保留小数点后两位)。若初始 225℃、7107Pa恒压下,保持 CO 、H 通入比例
p 2 2
不变,进行上述实验,测得从L 处开始,CO的体积分数不再改变,且小于2.8%,则L 处的温度 (填
1 8
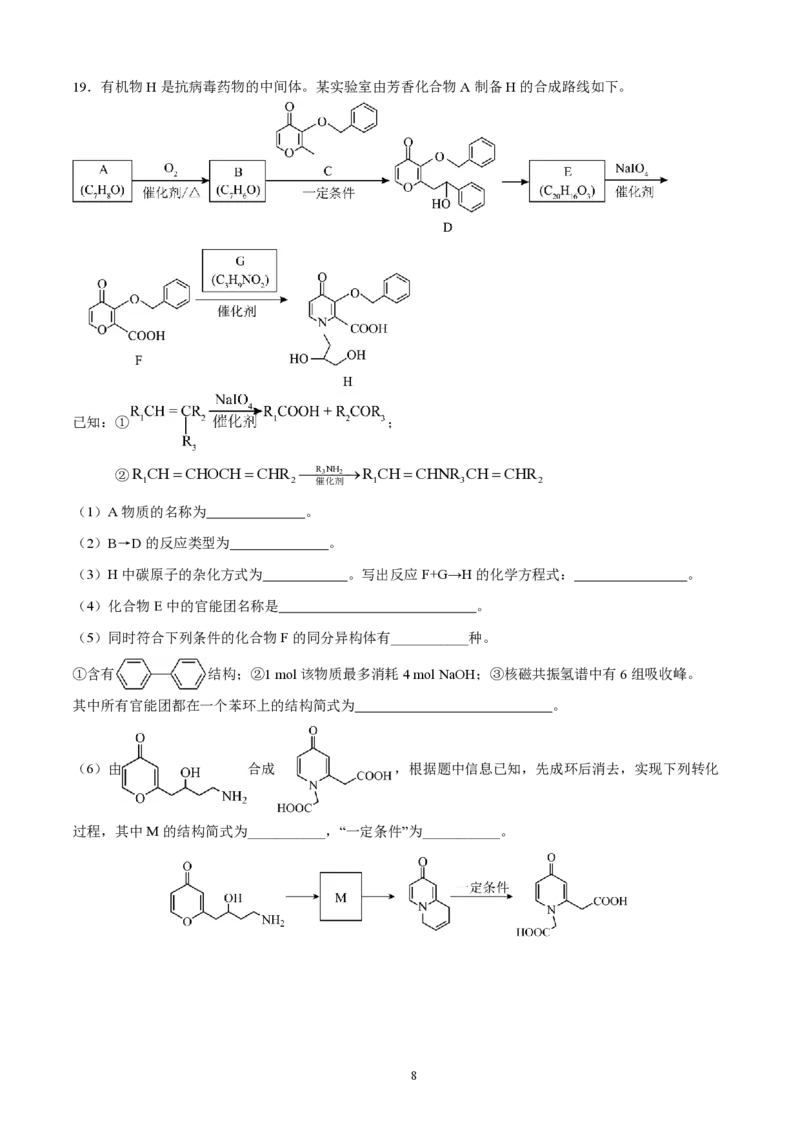
“>”“<”或“=”) 280℃,你的判断理由是 。19.有机物H是抗病毒药物的中间体。某实验室由芳香化合物A制备H的合成路线如下。
已知:① ;
②
8
R
1
C H = C H O C H = C H R
2
⎯ R⎯催 N3化 H⎯剂 2 → R
1
C H = C H N R
3
C H = C H R
2
(1)A物质的名称为 。
(2)B→D的反应类型为 。
(3)H中碳原子的杂化方式为 。写出反应F+G→H的化学方程式: 。
(4)化合物E中的官能团名称是 。
(5)同时符合下列条件的化合物F的同分异构体有___________种。
①含有 结构;②1 mol该物质最多消耗4 mol NaOH;③核磁共振氢谱中有6组吸收峰。
其中所有官能团都在一个苯环上的结构简式为 。
(6)由 合成 ,根据题中信息已知,先成环后消去,实现下列转化
过程,其中M的结构简式为___________,“一定条件”为___________。