文档内容
化学参考答案与解析
1.【答案】B
【解析】钢的含碳量一般为0.03%~2%,A正确;金属铝呈两性,所以不耐酸、碱腐蚀,B错误;涂层的主要成
分均属于合成有机高分子材料,C正确;聚偏二氟乙烯的结构简式为CH—CF,因此链节为
2 2
—CH—CF—,D正确。
2 2
2.【答案】D
【解析】转移NaCl溶液时,应将玻璃棒下端抵在刻度线以下,A错误;收集氯气装置无出气口,B错误;萃取操
作中放气方法应是将分液漏斗倒置,左手握住活塞部分,右手顶住塞子,打开活塞放气,C错误;氢氧化亚铁
易被氧气氧化,因此制备时,应用长胶头滴管将NaOH溶液滴入FeSO 溶液中,且用植物油液封,D正确。
4
3.【答案】B
【解析】石膏为电解质,可以使胶体发生聚沉,A正确;苯甲酸钠溶液呈碱性,B错误;硝酸铵受热或经撞击易
发生爆炸,因此硝酸铵必须经改性处理后才能施用,C正确;维生素 C具有还原性,可防止鲜榨果汁被氧化而
发生变色,D正确。
4.【答案】A
【解析】X分子中与苯环连接的碳原子为手性碳原子,A正确;Y既有羟基又有羧基,可以发生缩聚反应,而不
是加聚反应,B错误;M中的官能团名称为羟基和酰胺基,C错误;—CH 为推电子基,成键电子对间斥力大,
3
进一步压缩了H—N—H键角,所以CHNH 中键角C—N—H>H—N—H,D错误。
3 2
5.【答案】C
【解析】中子数为6的硼核素:11B,A错误;HBO 电离应用可逆号,B错误;根据信息,乙硼烷与 CO通过配位
5 3 3
键结合,且CO结构与N 相似,因此CO中C、O各有一个孤电子对,但是 C的电负性小,更易与 B形成配位
2
键,因此[COBH]中配位键可以表示为[HB←CO],C正确;NH 的VSEPR模型为 ,D错误。
3 3 3
6.【答案】B
【解析】BH 在B为+3价,H为-1价,其水解反应为归中反应,当1molBH 完全水解,转移电子总数为
2 6 2 6
6N,A错误;常温下pH=6的溶液,c(H+)=10-6mol·L-1,1L其溶液的 H+的数目一定为10-6N,B正确;
A A
未说明温度和压强,无法计算体积,C错误;1个NHBH 中σ键数目为7个,则3.1gNHBH 即物质的量为
3 3 3 3
0.1mol,σ键数目为0.7N,D错误。
A
7.【答案】C
【解析】离子液体难挥发因为离子液体的粒子全都是带电荷的离子,离子间作用力强于范德华力,所以难挥
发,C错误。
8.【答案】A
【解析】根据题意,元素X、Y、Z、M、W分别为F、O、N、C、S;电负性F最大,A正确;第一电离能:F>N>O,B错
误;M为碳,其氢化物有多种,沸点不确定,C错误;WY 中W的最外层不满足8电子稳定结构,D错误。
2
【化学答案 第1页(共5页)】
书书书9.【答案】D
【解析】应利用电解熔融氯化镁制取镁,A错误;乙烷与氯气在光照的条件下制备氯乙烷副反应多,B错误;硫
化亚铁与过量氧气生成二氧化硫,不能直接生成三氧化硫,C错误;石英砂与焦炭在高温条件下生成粗硅,与
氯化氢加热生成三氯硅烷,最后与氢气高温可制得高纯硅,D正确。
10.【答案】C
【解析】以上装置涉及太阳能和风能转化为电能、电能转化为化学能以及反应还原器中化学能与热能的转化
等,A错误;根据题意离子交换膜应为阴离子交换膜,左侧电极室产生的 OH-迁移至右侧电极室,因此当电
路转移2mol电子时,左侧电极室溶液质量减少 36g,B错误;根据整个装置工作原理,[Fe(CN)]3-/
6
[Fe(CN)]4-相当于反应的催化剂,实质是电解水的过程,因此无需外界补充 [Fe(CN)]3-/
6 6
[Fe(CN)]4-,C正确;反应还原器发生的反应为4[Fe(CN)]3-+4OH-4[Fe(CN)]4-+2HO+O
6 6 6 2 2
↑,反应未配平,D错误。
11.【答案】A
【解析】根据题干L—Pd—L中Pd的化合物价为0价,则含钯化合物ⅱ~ⅵ中钯除了与两个L成键,还与H、
Br、C等中两个原子成键,因此判断其中钯的化合价均为 +2,A正确;反应历程中碳碳双键先断裂发生加成
反应,后又消去,因此反应中既有非极性键的断裂,又有非极性键的形成,B错误;以上过程发生的总反应为
溴苯和丙烯酸甲酯发生反应生成目标产物,同时产生溴化氢,因此总反应的原子利用率小于100%,C错误;
因反应中产生HBr,弱碱性条件利于此反应正向进行,但强碱条件下目标产物中的酯基会发生水解反应,则
不利于此反应发生,D错误。
12.【答案】C
【解析】玻璃的主要成分中有NaSiO,灼烧时火焰呈黄色,不能证明待测液中存在Na+,A错误;加入的硝酸
2 3
铁溶液,在酸性条件下,硝酸根离子氧化性增强,也可以将铜粉溶解,不能证明 Fe3+>Cu2+,B错误;盐析是
蛋白质溶液中加入浓轻金属盐溶液,蛋白质因溶解度减小而析出,当再加水后蛋白质溶解,盐析是可逆的物
理变化,C正确;苯酚与碳酸钠溶液反应生成苯酚钠和碳酸氢钠,无二氧化碳产生,不能证明酸性:苯酚 >碳
酸,D错误。
13.【答案】D
3 1 1
【解析】CeO 晶胞中Ce4+周围等距且最近的O2-有8个,构成立方体,A正确;根据M的坐标为( , , ),
2 4 4 4
1 1 3
则N的坐标为( , , ),B正确;设CeO 中的Ce4+和Ce3+的个数分别为m和n,则m+n=1,由化合物
4 4 4 2-x
中各元素正、负化合价代数和为0可得4m+3n=4-2x,解得 m=1-2x,故一个 CeO 晶胞中 Ce4+和 Ce3+
2-x
1-2x
个数比为 ,C正确;利用均摊法计算,CeO 晶胞中,有4个 CeO,用含 a的代数式表示 CeO 晶胞密度
2x 2 2 2
6.88×1023
为 g·cm-3,D错误。
N ×a3
A
14.【答案】B
【解析】根据ⅰ~ⅳ反应,lgc(Pb2+)、lgc([PbOH]+)、lgc[Pb(OH)]及 lgc{[Pb(OH)]-}与 pH对应的直
2 3
线斜率依次为 -2、-1、0、+1,所以各离子依次对应的直线为 L、L、L、L。直线 L为 lgc([PbOH]+)随
4 3 2 1 3
【化学答案 第2页(共5页)】K
pH变化关系,A正确;利用ⅰ-ⅳ式,得出[Pb(OH)]-(aq)+3H+(aq)幑幐Pb2+(aq)+3HO(l) K= 1
3 2 K
4
=1028.2,当溶液中Pb2+(aq)与[Pb(OH)]-(aq)浓度相等时,计算出 c(H+)=10 -2 3 8.2 =10-9.4mol·L-1,即
3
pH=9.4,B错误;反应ⅳ-ⅲ得到:Pb(OH)(aq)+HO(l)幑幐Pb(OH)+(aq)+H+(aq),平衡常数 K=
2 2 3
K 10-15.5
4= =10-11.1,逆向平衡常数为1011.1,K越大,则进行趋势越大,C正确;根据图像当溶液酸性较强或
K 10-4.4
3
碱性较强区域内,溶液中Pb(Ⅱ)粒子的浓度会随着酸性增强或碱性增强而增大,因此可以判断 Pb(Ⅱ)的
氧化物具有两性的特征,D正确。
15.【答案】(15分,除标注分数外,其余每空2分)
(1) (1分)
(2)CO2-+HO幑幐HCO-+OH-
3 2 3
(3)抽滤瓶或吸滤瓶(1分) 过滤速率快,产品更干燥(1分)
(4)防止FeSO 结晶析出而损失 减少FeSO 溶解,且乙醇挥发时带走水分使产品迅速干燥
4 4
(5)MnO-+5Fe2++8H+Mn2++5Fe3++4HO 当加入最后半滴高锰酸钾溶液时,锥形瓶中溶液颜色
4 2
恰好变为浅紫色(或紫红色),且半分钟内不褪去 5.56V
【解析】(1)铁原子最外层有两个电子,因此Fe2+的离子结构示意图为 。
(2)碳酸钠溶液呈碱性,能去油污,用离子方程式表示为CO2-+HO幑幐HCO-+OH-。
3 2 3
(3)抽滤装置中仪器X为抽滤瓶或吸滤瓶;减压抽滤过滤速率快,产品更干燥。
(4)“在加热过程中添加少量水”及“趁热”减压抽滤的原因均是防止FeSO 结晶析出而损失,因为“趁热”减
4
压抽滤的目的是除去铁屑中不溶性杂质;用乙醇淋洗产品,可以 减少FeSO 溶解,且乙醇挥发时带走水分使
4
产品迅速干燥。
(5)高锰酸钾将亚铁离子氧化发生反应的离子方程式为 MnO-+5Fe2++8H+Mn2++5Fe3++4HO;当加
4 2
入最后半滴高锰酸钾溶液时,锥形瓶中溶液颜色恰好变为浅紫色(或紫红色),且半分钟内不褪去时为滴定
0.02×V×10-3×5×278
终点;计算FeSO·7HO含量为 ×100%=5.56V%。
4 2 0.500
16.【答案】(14分,除标注分数外,其余每空2分)
(1)1.00(1分) 当温度低于50℃时,温度升高,反应速率加快,浸取效率增大,当温度高于50℃时,氨水
大量挥发,使氨水浓度降低,浸取效率降低
50℃
(2)ZnS+SO2-+4NH·HO[Zn(NH)]2++2SO2-+4HO+S(不写温度不扣分)
2 8 3 2 3 4 4 2
(3)浸出液中剩余的过硫酸根(SO2-)需加热分解,避免其氧化后续加入的锌粉
2 8
(4)采用微压密闭加热方式可减少浸取液中大量水分的蒸发及氨的挥发
c(HS)×K ×K 0.1×1.0×10-7×1.0×10-13 1.6×10-24
(5)c(S2-)= 2 a1 a2= =10-13mol·L-1,c(Zn2+)= =
c2(H+) 10-8 10-13
【化学答案 第3页(共5页)】1.6×10-11mol·L-1,故Zn2+已沉淀完全
高温
(6)2ZnS+3O 2ZnO+2SO 作漂白剂或食品添加剂等(1分,合理即可给分)
2 2
【解析】(1)过硫酸铵的最佳浓度应使锌离子及铜离子萃取效率最高,因此选择1.00mol·L-1;当温度低于
50℃时,温度升高,反应速率加快,浸取效率增大,当温度高于50℃时,氨水大量挥发,使氨水浓度降低,浸
取效率降低。
50℃
(2)根据题意,含锌化合物生成[Zn(NH)]2+和 S,则离子方程式为 ZnS+SO2- +4NH·HO
3 4 2 8 3 2
[Zn(NH)]2++2SO2-+4HO+S。
3 4 4 2
(3)浸出液中剩余的过硫酸根(SO2-)需加热分解,避免其氧化后续加入的锌粉。
2 8
(4)根据题意,导致溶液pH下降的原因是水的蒸发及氨的挥发。
c(HS)×K ×K 0.1×1.0×10-7×1.0×10-13 1.6×10-24
(5)c(S2-)= 2 a1 a2= =10-13mol·L-1,c(Zn2+)= =
c2(H+) 10-8 10-13
1.6×10-11mol·L-1,故Zn2+已沉淀完全。
高温
(6)煅烧时,发生的化学反应方程式为2ZnS+3O 2ZnO+2SO。产生的气体为二氧化硫,二氧化硫在
2 2
生活中可用作漂白剂、食品添加剂等。
17.【答案】(15分,除标注分数外,其余每空2分)
(1)+123
(2)①AC ②1∶9(1分) 乙苯脱氢制备苯乙烯的反应气体体积增加,保持压强不变,充入水蒸气,相当于减
小反应气体的压强,反应正向进行,提高乙苯的转化率 ③<
(3)①Ⅰ和Ⅱ反应都是吸热反应,温度升高,使反应平衡正向移动,因此乙苯的转化率增大;温度升高时,副
0.646×0.646P
反应正向移动程度大于制备苯乙烯的反应,因此苯乙烯的选择性略下降 ②64.6% 或
0.32×5.68
0.646 0.646
P× P
5.68 5.68
(合理即可给分)
0.32
P
5.68
【解析】(1)ΔH =(2×413+348-615-436)=+123kJ·mol-1。
1
(2)①苯乙烯与氢气的物质的量始终保持1∶1,B不符合题意;消耗乙苯与生成苯乙烯及苯均为反应正向进
行,不能体现正、逆反应速率相等,D不符合题意。
②同温恒压条件下,初始乙苯与水蒸气的物质的量之比越低,乙苯分压越低,相当于减压,平衡朝气体分子
数增多的方向(正方向)移动,乙苯平衡转化率增大,所以 a曲线为乙苯与水蒸气之比最小的曲线,即
n(乙苯)∶n(HO)为1∶9。
2
1×(1-0.6)
③不妨设初始投入乙苯均为1mol,则 M点平衡时乙苯的分压为100kPa× =3.77kPa,
9+0.6+0.6+0.4
1×(1-0.45)
N点平衡时乙苯分压为100kPa× =10.09kPa,在同温(500K),都为平衡状态(正反
4+0.55+0.45+0.45
应速率等于逆反应速率)时分压越高,速率越快,所以v(M) <v(N) 。
正 逆
(3)①Ⅰ和Ⅱ反应都是吸热反应,温度升高,使反应平衡正向移动,因此乙苯的转化率增大;温度升高时,副
【化学答案 第4页(共5页)】反应正向移动程度大于制备苯乙烯的反应,因此苯乙烯的选择性略下降。
②苯乙烯的产率=乙苯转化率×苯乙烯的选择性=68%×95%×100%=64.6%。
若假设初始通入乙苯物质的量1mol,则水蒸气为4mol,转化率为68%,无论发生反应Ⅰ还是反应Ⅱ,增加
的物质的量相同,为 0.68mol,因此反应平衡后气体总物质的量为 5.68mol,反应生成苯乙烯的选择性
95%,因此苯乙烯的物质的量为0.646mol,同时生成氢气0.646mol,剩余乙苯为0.32mol。
CHCH(g)→CHCH(g)+H(g)
6 5 2 5 6 5 2 3 2
0.32 0.646 0.646
分压表示为/kPa P P P
5.68 5.68 5.68
0.646 0.646
P× P
5.68 5.68 0.646×0.646P
K = K =
p 0.32 p 0.32×5.68
P
5.68
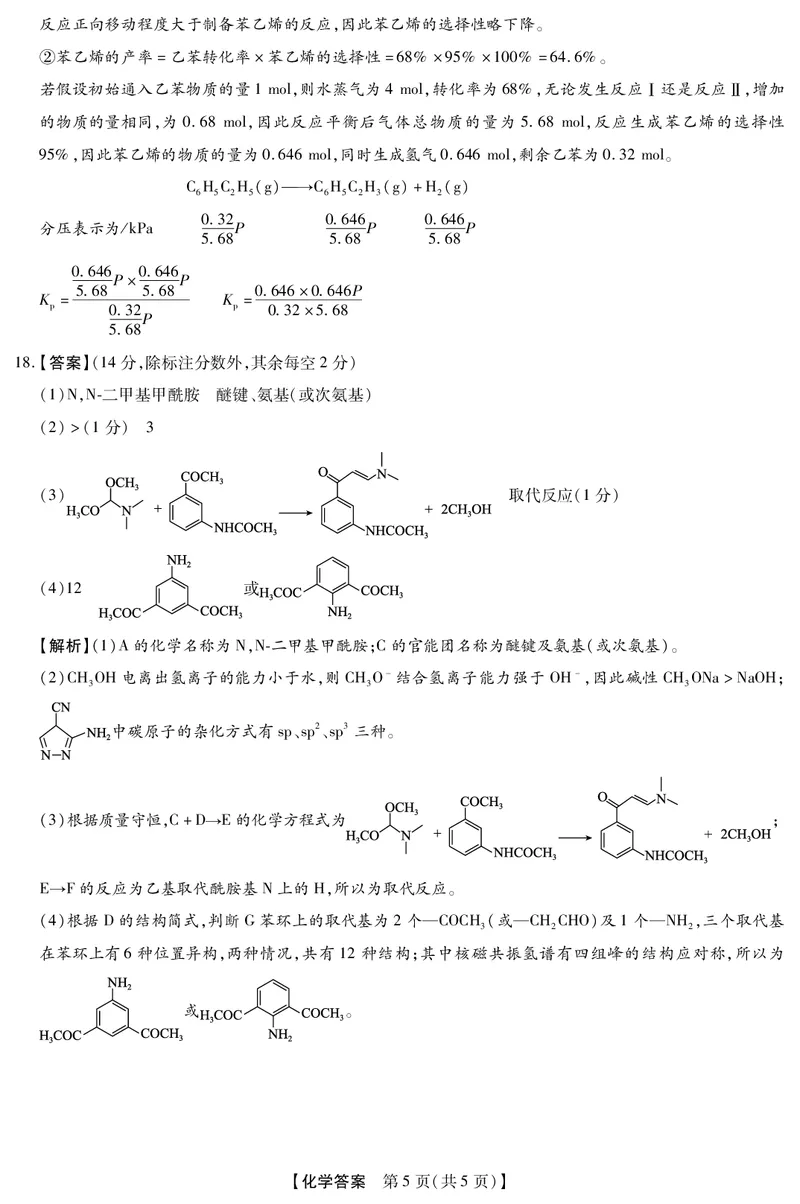
18.【答案】(14分,除标注分数外,其余每空2分)
(1)N,N二甲基甲酰胺 醚键、氨基(或次氨基)
(2)>(1分) 3
(3) 取代反应(1分)
(4)12 或
【解析】(1)A的化学名称为N,N二甲基甲酰胺;C的官能团名称为醚键及氨基(或次氨基)。
(2)CHOH电离出氢离子的能力小于水,则CHO-结合氢离子能力强于 OH-,因此碱性 CHONa>NaOH;
3 3 3
中碳原子的杂化方式有sp、sp2、sp3三种。
(3)根据质量守恒,C+D→E的化学方程式为 ;
E→F的反应为乙基取代酰胺基N上的H,所以为取代反应。
(4)根据D的结构简式,判断G苯环上的取代基为2个—COCH(或—CHCHO)及1个—NH,三个取代基
3 2 2
在苯环上有6种位置异构,两种情况,共有12种结构;其中核磁共振氢谱有四组峰的结构应对称,所以为
或 。
【化学答案 第5页(共5页)】